Ⅰ、在某温度时,在0.5L的恒容容器中发生气体M、N两种物质的相互转化,M、N的物质的量随时间变化的曲线如图所示,请根据图中数据分析,完成下列问题:
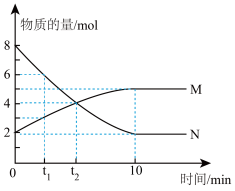
(1)该反应的化学方程式___________ 。
(2)反应开始的一瞬间进行的反应___________ (填“只有正反应发生”或者“只有逆反应发生”、“正、逆反应同时发生”),在t2时刻M的正反应速率___________ M的逆反应速率(填“大于”或者“小于”、“等于”),反应进行到10min时,N的平均反应速率为___________ 。
Ⅱ、被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪音、高效率的特点。如图为氢氧燃料电池的结构示意图,回答下列问题:
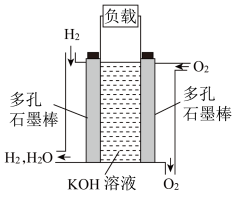
(3)O2进入的电极为___________ (填“正极”或“负极”)。
(4)电池工作时,溶液中的OH−向___________ (填“正极”或“负极”)迁移。
(5)若电池工作时转移0.04mol电子,理论上消耗标准状态下___________ mL O2。

(1)该反应的化学方程式
(2)反应开始的一瞬间进行的反应
Ⅱ、被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪音、高效率的特点。如图为氢氧燃料电池的结构示意图,回答下列问题:

(3)O2进入的电极为
(4)电池工作时,溶液中的OH−向
(5)若电池工作时转移0.04mol电子,理论上消耗标准状态下
更新时间:2023-06-03 07:30:24
|
相似题推荐
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐1】一定温度下,在体积为2.0L的恒容密闭容器中, 和
和 之间发生反应:
之间发生反应: (红棕色)
(红棕色)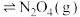 (无色),反应过程中各物质的物质的量与时间的关系如图所示,回答下列问题:
(无色),反应过程中各物质的物质的量与时间的关系如图所示,回答下列问题:
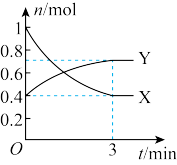
(1)曲线_______ (填“X”或“Y”)表示 的物质的量随时间的变化曲线。
的物质的量随时间的变化曲线。
(2)在0~3min内,用 表示的反应速率为
表示的反应速率为_______ 。
(3)下列叙述能说明该反应已达到化学平衡状态的是_______(填字母)。
(4)反应达到平衡后,若降低温度,混合气体的颜色变浅,相对于降温前v(正)_______ (填“增大”“减小”或“不变”,下同),v(逆)_______ 。
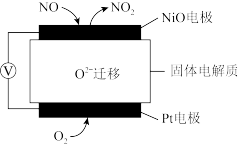
(5)氮氧化物是重要的大气污染物,如上图是监测NO含量的传感器工作原理示意图。NiO电极发生_______ (填“氧化”或“还原“)反应,Pt电极是电池_______ (填“正极”或“负极”)。
 和
和 之间发生反应:
之间发生反应: (红棕色)
(红棕色)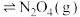 (无色),反应过程中各物质的物质的量与时间的关系如图所示,回答下列问题:
(无色),反应过程中各物质的物质的量与时间的关系如图所示,回答下列问题:
(1)曲线
 的物质的量随时间的变化曲线。
的物质的量随时间的变化曲线。(2)在0~3min内,用
 表示的反应速率为
表示的反应速率为(3)下列叙述能说明该反应已达到化学平衡状态的是_______(填字母)。
| A.容器内压强不再发生变化 |
B. 的颜色不再发生变化 的颜色不再发生变化 |
| C.容器内原子总数不再发生变化 |
D.相同时间内消耗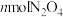 的同时生成 的同时生成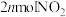 |

(5)氮氧化物是重要的大气污染物,如上图是监测NO含量的传感器工作原理示意图。NiO电极发生
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐2】乙烯(CH2=CH2)是非常重要的化工基础原料,由乙烯可以制备很多有机物。
I.在恒温1L的刚性密闭容器中,加入1mol乙烯和1mol水,发生CH2=CH2(g)+H2O(g) CH3-CH2-OH(g)。乙醇的物质的量与反应时间的关系如下图:
CH3-CH2-OH(g)。乙醇的物质的量与反应时间的关系如下图:
(1)计算在0-6min内的反应速率v(H2O)=___________ mol·L-1·min-1。
(2)8min时反应达到化学平衡状态,其理由是:___________ 。
Ⅱ.在恒温1L的刚性密闭容器中,加入1mol乙烯和1mol氢气,发生CH2=CH2(g)+H2(g) CH3CH3(g),容器内气体的压强与反应时间的关系如下图:
CH3CH3(g),容器内气体的压强与反应时间的关系如下图:
(3)下列措施能增大反应速率的是___________(填字母)。
(4)达到化学平衡状态时,下列数值与开始时相同的是___________(填序号)
(5)反应进行到10min时,乙烯(CH2=CH2)的转化率a%=___________ 。
I.在恒温1L的刚性密闭容器中,加入1mol乙烯和1mol水,发生CH2=CH2(g)+H2O(g)
 CH3-CH2-OH(g)。乙醇的物质的量与反应时间的关系如下图:
CH3-CH2-OH(g)。乙醇的物质的量与反应时间的关系如下图:| 时间(min) | 0 | 2 | 4 | 6 | 8 | 10 |
| 乙醇的物质的量(mol) | 0 | 0.3 | 0.5 | 0.6 | 0.65 | 0.65 |
(2)8min时反应达到化学平衡状态,其理由是:
Ⅱ.在恒温1L的刚性密闭容器中,加入1mol乙烯和1mol氢气,发生CH2=CH2(g)+H2(g)
 CH3CH3(g),容器内气体的压强与反应时间的关系如下图:
CH3CH3(g),容器内气体的压强与反应时间的关系如下图:| 时间(min) | 0 | 2 | 4 | 6 | 8 | 10 |
| 气体压强(MPa) | 100 | 80 | 70 | 65 | 60 | 60 |
| A.升高温度 |
| B.降低压强 |
| C.减小CH3CH3的浓度 |
| D.加入合适的催化剂 |
| A.容器内气体的压强 |
| B.容器内n(H2) |
| C.容器内c(CH2=CH2) |
| D.容器内气体的总质量 |
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐3】由γ-丁酸生成γ-丁内酯的反应如下:HOCH2CH2CH2COOH
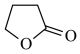 +H2O,在298K下,γ-羟基丁酸水溶液的初始浓度为0.180mol/L,测得γ-丁内酯的浓度随时间变化的数据如表所示。回答下列问题:
+H2O,在298K下,γ-羟基丁酸水溶液的初始浓度为0.180mol/L,测得γ-丁内酯的浓度随时间变化的数据如表所示。回答下列问题:
(1)该反应在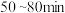 内的平均反应速率为
内的平均反应速率为_______  。
。
(2)该反应化学平衡常数K的表达式是_______ ,298K时该反应的平衡常数K=_______ 。
(3)求120min时γ-羟基丁酸的转化率为_______ (请写出计算过程,注意格式规范)
(4)为提高γ-羟基丁酸的平衡转化率,除适当控制反应温度外,还可采取的措施是_______

 +H2O,在298K下,γ-羟基丁酸水溶液的初始浓度为0.180mol/L,测得γ-丁内酯的浓度随时间变化的数据如表所示。回答下列问题:
+H2O,在298K下,γ-羟基丁酸水溶液的初始浓度为0.180mol/L,测得γ-丁内酯的浓度随时间变化的数据如表所示。回答下列问题: | 21 | 50 | 80 | 100 | 120 | 160 | 220 |  |
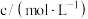 | 0.024 | 0.050 | 0.071 | 0.081 | 0.090 | 0.104 | 0.116 | 0.132 |
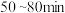 内的平均反应速率为
内的平均反应速率为 。
。(2)该反应化学平衡常数K的表达式是
(3)求120min时γ-羟基丁酸的转化率为
(4)为提高γ-羟基丁酸的平衡转化率,除适当控制反应温度外,还可采取的措施是
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐1】研究化学反应及其能量变化,对于社会发展、科技进步具有重要的意义。
(1)下列反应属于吸热反应的是___________。
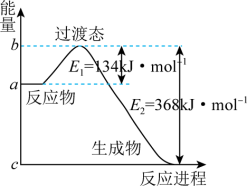
(2)如图是1molNO2和1molCO反应生成CO2和NO过程中能量变化的示意图,请写出NO2和CO反应的热化学方程式:_________ 。
(3)一定条件下CO2能与N2发生反应: 。某温度下,若向2L体积恒定的密闭容器中充入等物质的量的N2和CO2,其中N2、NO物质的量随时间变化的曲线如图所示:
。某温度下,若向2L体积恒定的密闭容器中充入等物质的量的N2和CO2,其中N2、NO物质的量随时间变化的曲线如图所示:
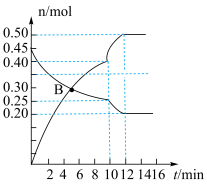
①图中B点v正_______ v逆(填“>”“<”或“=”);B点中CO2的转化率为_________ 。
②反应到10min时向容器中加入催化剂N2的消耗速率迅速增大,请用相关理论解释N2消耗速率增大的原因:_________ 。
③下列情况能说明该反应达到平衡状态的是_________ 。
A.2v(N2)=v(NO) B.混合气体的密度保持不变
C.t时刻,C(s)质量不再增加 D.混合气体的总物质的量不再改变
E.CO2、N2、NO的物质的量之比达到1:1:2
(1)下列反应属于吸热反应的是___________。
| A.碳酸氢钠溶液和盐酸的反应 | B.Ba(OH)2•8H2O与NH4Cl反应 |
| C.铝片与盐酸反应 | D.酒精在氧气中燃烧的反应 |
(2)如图是1molNO2和1molCO反应生成CO2和NO过程中能量变化的示意图,请写出NO2和CO反应的热化学方程式:

(3)一定条件下CO2能与N2发生反应:
 。某温度下,若向2L体积恒定的密闭容器中充入等物质的量的N2和CO2,其中N2、NO物质的量随时间变化的曲线如图所示:
。某温度下,若向2L体积恒定的密闭容器中充入等物质的量的N2和CO2,其中N2、NO物质的量随时间变化的曲线如图所示:
①图中B点v正
②反应到10min时向容器中加入催化剂N2的消耗速率迅速增大,请用相关理论解释N2消耗速率增大的原因:
③下列情况能说明该反应达到平衡状态的是
A.2v(N2)=v(NO) B.混合气体的密度保持不变
C.t时刻,C(s)质量不再增加 D.混合气体的总物质的量不再改变
E.CO2、N2、NO的物质的量之比达到1:1:2
您最近一年使用:0次
【推荐2】按要求回答下列问题:
(1)下列过程中,既属于氧化还原反应,又属于吸热反应的是_______ 。
①甲烷的燃烧 ②水煤气的制备 ③石灰石受热分解 ④碘升华 ⑤金属的锈蚀
(2)一定温度下,向容积为2 L的密闭容器中通入两种气体发生化学反应(产物均为气体),反应中各物质物质的量的变化如图所示。______________________ 。
②在0~6 s内,B的化学反应速率为________________ 。
③6s后容器内的压强与开始时压强之比为_____________ 。
(3)一定条件下,H2、CO在体积固定的绝热密闭容器中发生如下反应:2CO(g)+ 4H2(g)⇌ CH3OCH3(g)+H2O(g),
下列选项不能判断该反应达到平衡状态的依据的________________ 。
①密闭容器中CO的体积分数不变
②密闭容器中总压强不变
③密闭容器中混合气体的密度不变
④密闭容器中混合气体的平均相对分子质量不变
⑤体系内的温度不再变化
⑥单位时间内,断裂4mol H-H键,同时生成2mol H-O键
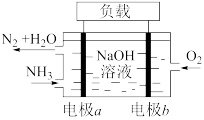
(4)潜艇中使用的液氨液氧燃料电池工作原理如图所示:_______ (填“正极”或“负极”),其电极反应为_____________________ 。
(1)下列过程中,既属于氧化还原反应,又属于吸热反应的是
①甲烷的燃烧 ②水煤气的制备 ③石灰石受热分解 ④碘升华 ⑤金属的锈蚀
(2)一定温度下,向容积为2 L的密闭容器中通入两种气体发生化学反应(产物均为气体),反应中各物质物质的量的变化如图所示。

②在0~6 s内,B的化学反应速率为
③6s后容器内的压强与开始时压强之比为
(3)一定条件下,H2、CO在体积固定的绝热密闭容器中发生如下反应:2CO(g)+ 4H2(g)⇌ CH3OCH3(g)+H2O(g),
下列选项不能判断该反应达到平衡状态的依据的
①密闭容器中CO的体积分数不变
②密闭容器中总压强不变
③密闭容器中混合气体的密度不变
④密闭容器中混合气体的平均相对分子质量不变
⑤体系内的温度不再变化
⑥单位时间内,断裂4mol H-H键,同时生成2mol H-O键
(4)潜艇中使用的液氨液氧燃料电池工作原理如图所示:
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐3】化学反应速率和限度与生产、生活密切相关。
(1)某学生为了探究锌与盐酸反应过程中的速率变化,在40mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
①哪一时间段反应速率最大___________ min(填“0~1”“1~2”“2~3”“3~4”或“4~5”),原因是___________ 。
②求3~4min时间段以盐酸的浓度变化来表示的该反应速率___________ (设溶液体积不变)。
(2)另一学生为控制反应速率防止反应过快难以测量氢气体积,他事先在盐酸中加入等体积的下列溶液以减慢反应速率,你认为不可行的是___________(填字母)。
(3)某温度下在4L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。
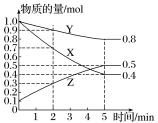
①该反应的化学方程式是___________ 。
②该反应达到平衡状态的标志是___________ (填字母)。
A.X、Y的反应速率比为3∶1
B.容器内气体压强保持不变
C.容器内气体的总质量保持不变
D.Y的体积分数在混合气体中保持不变
E.生成1molY的同时消耗2molZ
③2min内X的转化率为___________ 。
(1)某学生为了探究锌与盐酸反应过程中的速率变化,在40mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
| 时间/min | 1 | 2 | 3 | 4 | 5 |
| 氢气体积/mL(标准状况) | 100 | 240 | 464 | 576 | 620 |
②求3~4min时间段以盐酸的浓度变化来表示的该反应速率
(2)另一学生为控制反应速率防止反应过快难以测量氢气体积,他事先在盐酸中加入等体积的下列溶液以减慢反应速率,你认为不可行的是___________(填字母)。
| A.KNO3溶液 | B.KCl溶液 |
| C.蒸馏水 | D.CuSO4溶液 |

①该反应的化学方程式是
②该反应达到平衡状态的标志是
A.X、Y的反应速率比为3∶1
B.容器内气体压强保持不变
C.容器内气体的总质量保持不变
D.Y的体积分数在混合气体中保持不变
E.生成1molY的同时消耗2molZ
③2min内X的转化率为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】几种主族元素在元素周期表中的位置如下表所示:
回答下列问题:
(1)硅元素在周期表中的位置是___________ ,其氧化物的用途___________ (任写一种)。
(2)①②④三种元素的简单离子半径由大到小的顺序是___________ (填离子符号)。
(3)②③⑤三种元素最高价氧化物的水化物的碱性最强的是___________ (填化学式),该物质与元素③的最高价氧化物的水化物反应的离子方程式为___________ 。
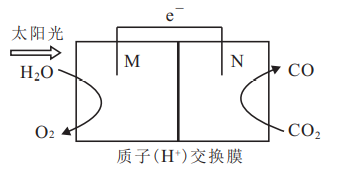
(4)科学家利用下图所示电池装置可以将 转化为气体燃料
转化为气体燃料 。该装置工作时,N电极为
。该装置工作时,N电极为___________ (填“正极”或“负极”),电子流向为___________ (填“M→N”或“N→M”)。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ⅢA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| 2 | ① | |||||||
| 3 | ② | ③ | ④ | |||||
| 4 | ⑤ |
(1)硅元素在周期表中的位置是
(2)①②④三种元素的简单离子半径由大到小的顺序是
(3)②③⑤三种元素最高价氧化物的水化物的碱性最强的是
(4)科学家利用下图所示电池装置可以将
 转化为气体燃料
转化为气体燃料 。该装置工作时,N电极为
。该装置工作时,N电极为
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐2】I.人们应用原电池原理制作了多种电池,以满足不同的需要,广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格。
(1)铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4=2PbSO4+2H2O。正极电极反应式为_________ 。电池工作一段时间后需要充电,充电过程中电池液中H2SO4的浓度_____ (填“增大”、“减小”或“不变”)。
⑵某学习小组依据氧化还原反应:2Ag++Cu===Cu2++2Ag设计成原电池,则负极发生的电极反应为___________ ;当反应进行到一段时间后取出电极材料,测得某一电极增重了 5.4g,则该原电池反应共转移了的电子数目是________________________ 。
⑶燃料电池是一种高效、环境友好的供电装置,如图是电解质为稀硫酸溶液的氢氧燃料电池原理示意图,回答下列问题:
①该电池的正极反应式_________________ 。
②若该电池的效率80%,当外电路通过0.2mol电子时,消耗O2的体积____ L(标准状况)
II.用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应4HCl+O2 2Cl2+2H2O,可实现氯的循环利用。已知上述反应中,4mol HCl被氧化,放出约116kJ的热量。
2Cl2+2H2O,可实现氯的循环利用。已知上述反应中,4mol HCl被氧化,放出约116kJ的热量。
计算断开1 mol H-O键与断开1 mol H-C1键断所吸收能量相差约为______ kJ。
(1)铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4=2PbSO4+2H2O。正极电极反应式为
⑵某学习小组依据氧化还原反应:2Ag++Cu===Cu2++2Ag设计成原电池,则负极发生的电极反应为
⑶燃料电池是一种高效、环境友好的供电装置,如图是电解质为稀硫酸溶液的氢氧燃料电池原理示意图,回答下列问题:

①该电池的正极反应式
②若该电池的效率80%,当外电路通过0.2mol电子时,消耗O2的体积
II.用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应4HCl+O2
 2Cl2+2H2O,可实现氯的循环利用。已知上述反应中,4mol HCl被氧化,放出约116kJ的热量。
2Cl2+2H2O,可实现氯的循环利用。已知上述反应中,4mol HCl被氧化,放出约116kJ的热量。
计算断开1 mol H-O键与断开1 mol H-C1键断所吸收能量相差约为
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
【推荐3】在一定温度下,对冰醋酸加水稀释的过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示。请回答下列问题:
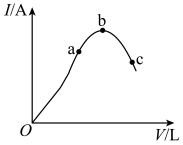
(1)a、b、c三点对应的溶液中, 由小到大的顺序为
由小到大的顺序为__________ 。
(2)a、b、c三点对应的溶液中, 的电离程度最大的是
的电离程度最大的是__________ 。
(3)若使c点对应的溶液中的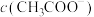 增大,则下列措施中,可行的是
增大,则下列措施中,可行的是__________ (填字母,下同)。
A.加热 B.加入NaOH固体 C.加入浓盐酸溶液
D.加水 E.加入 固体 F.加入锌粒
固体 F.加入锌粒
(4)在稀释过程中,随着醋酸浓度的减小,下列始终保持增大趋势的是__________。
(5)依反应 设计的原电池如图1所示。
设计的原电池如图1所示。
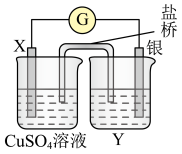
图1
请回答下列问题:
①电极X的材料是__________ ;电解质溶液Y是__________ 溶液。
②银电极为电池的__________ 极,发生的电极反应式为__________ 。

(1)a、b、c三点对应的溶液中,
 由小到大的顺序为
由小到大的顺序为(2)a、b、c三点对应的溶液中,
 的电离程度最大的是
的电离程度最大的是(3)若使c点对应的溶液中的
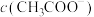 增大,则下列措施中,可行的是
增大,则下列措施中,可行的是A.加热 B.加入NaOH固体 C.加入浓盐酸溶液
D.加水 E.加入
 固体 F.加入锌粒
固体 F.加入锌粒(4)在稀释过程中,随着醋酸浓度的减小,下列始终保持增大趋势的是__________。
A. | B. |
C. 分子数 分子数 | D.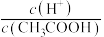 |
(5)依反应
 设计的原电池如图1所示。
设计的原电池如图1所示。
图1
请回答下列问题:
①电极X的材料是
②银电极为电池的
您最近一年使用:0次
【推荐1】Ⅰ.硅在元素周期表中,处于金属和非金属的交界处,是良好的半导体材料,单晶硅是生产芯片的重要材料。工业冶炼纯硅的原理是:① ;②
;② ;③
;③ 。化学反应与能量变化如图所示,回答下列问题:
。化学反应与能量变化如图所示,回答下列问题:
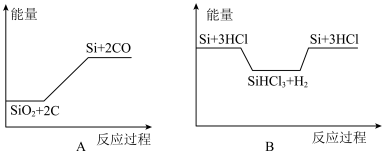
(1)反应①属于_______ 反应(填“吸热”或“放热”)。反应②破坏反应物中的化学键所吸收的能量_______ (填“>”或“<”)形成生成物中化学键所放出的能量。
Ⅱ.化学能与其他能量间的转换在生活中处处可见,比如某种氢氧燃料电池已经成功应用在城市公交汽车上,该电池用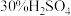 溶液作电解质溶液,其简易装置如图所示。
溶液作电解质溶液,其简易装置如图所示。
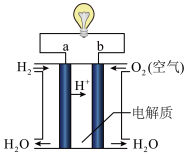
(2)在这个燃料电池中,正极的电极反应式为_______ 。若在标况下,消耗了33.6L的氢气,此时电路中转移的电子数目为_______ (用阿伏加德罗常数表示)。
Ⅲ.1868年狄肯和洪特发明用地康法制氯气,反应原理图示如图所示(反应温度为450℃):

(3)用地康法制备氯气时总反应的方程式为_______ ,其中氧化剂与还原剂的物质的量之比为_______ 。
(4)在该过程中,氧化铜的作用是_______ 。
 ;②
;② ;③
;③ 。化学反应与能量变化如图所示,回答下列问题:
。化学反应与能量变化如图所示,回答下列问题:
(1)反应①属于
Ⅱ.化学能与其他能量间的转换在生活中处处可见,比如某种氢氧燃料电池已经成功应用在城市公交汽车上,该电池用
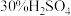 溶液作电解质溶液,其简易装置如图所示。
溶液作电解质溶液,其简易装置如图所示。
(2)在这个燃料电池中,正极的电极反应式为
Ⅲ.1868年狄肯和洪特发明用地康法制氯气,反应原理图示如图所示(反应温度为450℃):

(3)用地康法制备氯气时总反应的方程式为
(4)在该过程中,氧化铜的作用是
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐2】氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。请回答:
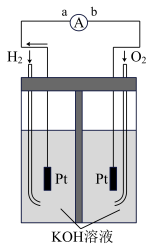
(1)氢氧燃料电池的在导线中电流的方向为由____ (用a、b表示)。
(2)负极反应式为___ 。
(3)该电池工作时,H2和O2连续由外部供给,电,池可连续不断提供电能。因此,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
Ⅰ. 2Li+H2=2LiH Ⅱ. LiH+H2O=LiOH+H2↑
①反应Ⅰ中的还原剂是___ ,反应Ⅱ中的氧化剂是___ 。
②已知LiH固体密度为0.82g·cm-3,用锂吸收224 L(标准状况)H2,生成的LiH体积与被吸收的H2体积比为______ 。
③由②生成的LiH与H2O作用,放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为___ mol。

(1)氢氧燃料电池的在导线中电流的方向为由
(2)负极反应式为
(3)该电池工作时,H2和O2连续由外部供给,电,池可连续不断提供电能。因此,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
Ⅰ. 2Li+H2=2LiH Ⅱ. LiH+H2O=LiOH+H2↑
①反应Ⅰ中的还原剂是
②已知LiH固体密度为0.82g·cm-3,用锂吸收224 L(标准状况)H2,生成的LiH体积与被吸收的H2体积比为
③由②生成的LiH与H2O作用,放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为
您最近一年使用:0次



