铝元素是地壳中含量最多的金属元素,常以化合态的形式存在于铝土矿中,其氧化物具有两性, 与
与 类似。
类似。
Ⅰ.工业上常常从铝土矿(主要成分为 ,含
,含 、
、 杂质)中提取
杂质)中提取 ,并通过电解法制备铝单质。请根据流程图,回答相关问题。
,并通过电解法制备铝单质。请根据流程图,回答相关问题。

已知: 属于两性氢氧化物,既能溶于稀盐酸又能溶于NaOH溶液。
属于两性氢氧化物,既能溶于稀盐酸又能溶于NaOH溶液。
(1)写出“滤渣A”的化学式:_______ ;过滤时,玻璃棒的作用为_______ ;“滤液B”中的溶质为 、
、_______ (写化学式)。
(2)上述流程中“过量氨水”能否改为“过量NaOH溶液”?_______ (填“能”或“不能”),请用离子方程式解释:_______ 。
Ⅱ.已知 能与NaOH溶液反应生成亚铬酸钠(
能与NaOH溶液反应生成亚铬酸钠( ),
), 可由
可由 和硫黄(S)混合后进行反应得到,发生反应的化学方程式为
和硫黄(S)混合后进行反应得到,发生反应的化学方程式为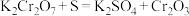 ,再经湿磨、热水洗涤、压滤、干燥、粉碎制得。回答下到问题:
,再经湿磨、热水洗涤、压滤、干燥、粉碎制得。回答下到问题:
(3)写出 与NaOH溶液反应的化学方程式:
与NaOH溶液反应的化学方程式:_______ 。
(4)由 和硫黄制取
和硫黄制取 的废水中含有一定量的
的废水中含有一定量的 ,Cr元素含量达标才能排放,可以加入
,Cr元素含量达标才能排放,可以加入 溶液去除酸性废水中的
溶液去除酸性废水中的 ,使
,使 转化为
转化为 而自身转化为三价铁,再放入沉淀池,达到指定标准后方可排放。上述过程
而自身转化为三价铁,再放入沉淀池,达到指定标准后方可排放。上述过程 溶液与
溶液与 发生的反应中氧化剂与还原剂的物质的量之比为
发生的反应中氧化剂与还原剂的物质的量之比为_______ 。
(5)某兴趣小组同学想根据上述反应原理测出该酸性废水中残留的 的物质的量浓度,采样后,经初步预算需要
的物质的量浓度,采样后,经初步预算需要 的
的 溶液240mL,配制该溶液时至少需称量
溶液240mL,配制该溶液时至少需称量_______ g 。
。
 与
与 类似。
类似。Ⅰ.工业上常常从铝土矿(主要成分为
 ,含
,含 、
、 杂质)中提取
杂质)中提取 ,并通过电解法制备铝单质。请根据流程图,回答相关问题。
,并通过电解法制备铝单质。请根据流程图,回答相关问题。
已知:
 属于两性氢氧化物,既能溶于稀盐酸又能溶于NaOH溶液。
属于两性氢氧化物,既能溶于稀盐酸又能溶于NaOH溶液。(1)写出“滤渣A”的化学式:
 、
、(2)上述流程中“过量氨水”能否改为“过量NaOH溶液”?
Ⅱ.已知
 能与NaOH溶液反应生成亚铬酸钠(
能与NaOH溶液反应生成亚铬酸钠( ),
), 可由
可由 和硫黄(S)混合后进行反应得到,发生反应的化学方程式为
和硫黄(S)混合后进行反应得到,发生反应的化学方程式为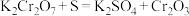 ,再经湿磨、热水洗涤、压滤、干燥、粉碎制得。回答下到问题:
,再经湿磨、热水洗涤、压滤、干燥、粉碎制得。回答下到问题:(3)写出
 与NaOH溶液反应的化学方程式:
与NaOH溶液反应的化学方程式:(4)由
 和硫黄制取
和硫黄制取 的废水中含有一定量的
的废水中含有一定量的 ,Cr元素含量达标才能排放,可以加入
,Cr元素含量达标才能排放,可以加入 溶液去除酸性废水中的
溶液去除酸性废水中的 ,使
,使 转化为
转化为 而自身转化为三价铁,再放入沉淀池,达到指定标准后方可排放。上述过程
而自身转化为三价铁,再放入沉淀池,达到指定标准后方可排放。上述过程 溶液与
溶液与 发生的反应中氧化剂与还原剂的物质的量之比为
发生的反应中氧化剂与还原剂的物质的量之比为(5)某兴趣小组同学想根据上述反应原理测出该酸性废水中残留的
 的物质的量浓度,采样后,经初步预算需要
的物质的量浓度,采样后,经初步预算需要 的
的 溶液240mL,配制该溶液时至少需称量
溶液240mL,配制该溶液时至少需称量 。
。
更新时间:2023-06-08 06:10:30
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】铝灰的回收利用方法很多,现用含有A12O3、SiO2和少量FeO•xFe2O3的铝灰制备A12(SO4)3•18H2O,工艺流程如图:

请回答下列问题:
(1)加入过量稀H2SO4溶解A12O3的离子方程式是_______ 。
(2)流程中加入的KMnO4也可用H2O2代替,若用H2O2发生反应的化学方程式为_______ 。
(3)已知:浓度均为0.1mol/L的金属阳离子,生成氢氧化物沉淀的pH如表:
步骤③的目的是_______ ;若在该浓度下除去铁的化合物,调节pH的最大范围是_______ 。
(4)已知Ksp[Fe(OH)3]=c(Fe3+)•c3(OH-)=4.0×10-38,常温下,当pH=2时,Fe3+开始沉淀的浓度为_______ 。
(5)操作④发生反应的离子方程式为_______ 。
(6)操作⑤“一系列操作”,下列仪器中用不到的是_______ (填序号).
A.蒸发皿 B.坩埚 C.玻璃棒 D.酒精灯 E.漏斗

请回答下列问题:
(1)加入过量稀H2SO4溶解A12O3的离子方程式是
(2)流程中加入的KMnO4也可用H2O2代替,若用H2O2发生反应的化学方程式为
(3)已知:浓度均为0.1mol/L的金属阳离子,生成氢氧化物沉淀的pH如表:
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
(4)已知Ksp[Fe(OH)3]=c(Fe3+)•c3(OH-)=4.0×10-38,常温下,当pH=2时,Fe3+开始沉淀的浓度为
(5)操作④发生反应的离子方程式为
(6)操作⑤“一系列操作”,下列仪器中用不到的是
A.蒸发皿 B.坩埚 C.玻璃棒 D.酒精灯 E.漏斗
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】铝灰的回收利用方法很多,现用含有A12O3、SiO2和少量FeO·xFe2O3的铝灰制备A12(SO4)3·18H2O,工艺流程如图:

请回答下列问题:
(1)加入过量稀H2SO4溶解Al2O3的离子方程式是___________ 。
(2)步骤③中加入KMnO4发生反应的离子方式为___________ 。
(3)已知:浓度均为0.1mol/L的金属阳离子,生成氢氧化物沉淀的pH如表:步骤③的目的是___________ ;若在该浓度下除去铁的化合物,调节pH的最大范围是___________ 。
(4)已知Ksp[Fe(OH)3]=c(Fe3+)×c3(OH−)=4.0×10−38,常温下,当pH=2时,Fe3+开始沉淀的浓度为___________ 。
(5)步骤④中加MnSO4的作用___________ 。
(6)操作⑤“一系列操作”,下列仪器中用不到的是___________ (填序号)。
A.蒸发皿B.坩埚C.玻璃棒D.酒精灯E.漏斗

请回答下列问题:
(1)加入过量稀H2SO4溶解Al2O3的离子方程式是
(2)步骤③中加入KMnO4发生反应的离子方式为
(3)已知:浓度均为0.1mol/L的金属阳离子,生成氢氧化物沉淀的pH如表:步骤③的目的是
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
(4)已知Ksp[Fe(OH)3]=c(Fe3+)×c3(OH−)=4.0×10−38,常温下,当pH=2时,Fe3+开始沉淀的浓度为
(5)步骤④中加MnSO4的作用
(6)操作⑤“一系列操作”,下列仪器中用不到的是
A.蒸发皿B.坩埚C.玻璃棒D.酒精灯E.漏斗
您最近一年使用:0次
【推荐3】无铁硫酸铝是制造高档纸张和高级织物的重要原材料,制取无铁硫酸铝的工艺流程如下图所示。铝土矿酸溶后得到含铁(Fe2+和Fe3+)的硫酸铝溶液,再经过后续加工,最终得到成品无铁硫酸铝(溶液中各种金属离子开始沉淀和沉淀完全时的pH见表)。
| 开始 | 完全 | |
| Fe2+ | 7.6 | 9.7 |
| Fe3+ | 2.7 | 3.7 |
| Al3+ | 3.3 | 5.0 |
| Mn2+ | 8.3 | 9.8 |
a.铝土矿粉 b.氢氧化钠 c.氧化钙
(2)生产中控制pH为3而不大于3的原因是
(3)除铁时,必须先加入高锰酸钾溶液,目的是
(4)滤渣的含铁成分是
(5)活性二氧化锰能和Fe(OH)3发生吸附共沉作用,用化学平衡理论解释活性二氧化锰的作用
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】用湿法制磷酸的副产品氟硅酸(H2SiF6)生成无水氟化氢的工艺如图所示:
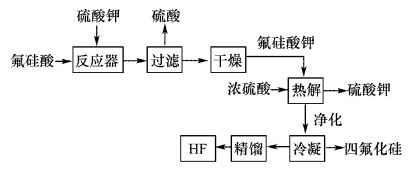
已知氟硅酸钾(K2SiF6)微酸性,有吸湿性,微溶于水,不溶于酒精。
(1)写出反应器中的化学方程式:________________ 。
(2)在实验室过滤操作中所用的玻璃仪器有_____________ ,在洗涤氟硅酸钾(K2SiF6)时常用酒精洗涤,其目的是:____________ 。
(3)该流程中哪些物质可以循环使用:_____________ 。(用化学式表达)
(4)氟化氢可以腐蚀刻画玻璃,在刻蚀玻璃过程中也会生成H2SiF6,试写出该反应的化学方程式:__________________ 。

已知氟硅酸钾(K2SiF6)微酸性,有吸湿性,微溶于水,不溶于酒精。
(1)写出反应器中的化学方程式:
(2)在实验室过滤操作中所用的玻璃仪器有
(3)该流程中哪些物质可以循环使用:
(4)氟化氢可以腐蚀刻画玻璃,在刻蚀玻璃过程中也会生成H2SiF6,试写出该反应的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】工业上用粗制的氧化铜粉末(含杂质Fe和SiO2)来制取无水CuCl2的工艺流程如图所示:

(1)“酸浸”时发生的复分解反应化学方程式为:____ 。为加快酸浸速率可以采取的措施是:____ (任举一条)。
(2)“氧化”时发生的离子方程式为:_____ 。
(3)下表列出了相关金属离子生成氢氧化物沉淀的pH。“调pH”时应控制溶液pH范围为_____ 。
当pH=4时,溶液中c(Fe3+)=____ 。已知:Ksp[Fe(OH)3]=2.6×10―39
(4)“加热脱水”需要提供的条件为:_____ 。

(1)“酸浸”时发生的复分解反应化学方程式为:
(2)“氧化”时发生的离子方程式为:
(3)下表列出了相关金属离子生成氢氧化物沉淀的pH。“调pH”时应控制溶液pH范围为
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1. 5 | 3. 7 |
| Cu2+ | 4.2 | 6. 4 |
| Fe2+ | 6.5 | 9.7 |
当pH=4时,溶液中c(Fe3+)=
(4)“加热脱水”需要提供的条件为:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】高锰酸钾是常用的氧化剂。工业上以软锰矿(主要成分是MnO2)为原料制备高锰酸钾晶体。中间产物为锰酸钾。下图是实验室模拟制备KMnO4晶体的操作流程:
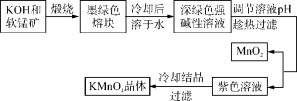
已知:锰酸钾(K2MnO4)是墨绿色晶体,其水溶液呈深绿色,这是锰酸根离子(MnO42-)在水溶液中的特征颜色,在强碱性溶液中能稳定存在;在酸性、中性和弱碱性环境下,MnO42-会发生自身氧化还原反应,生成MnO4-和MnO2。
回答下列问题:
(1)KOH的电子式为____________ ,煅烧时KOH和软锰矿的混合物应放在________ 中加热(填标号)。
A 烧杯 B 瓷坩埚
C 蒸发皿 D 铁坩埚
(2)调节溶液pH过程中,所得氧化产物与还原产物的物质的量之比为____________ 。
(3)趁热过滤的目的是_____________________________________________ 。
(4)已知20 ℃时K2SO4、KCl、CH3COOK的溶解度分别为11.1 g、34 g、217 g,则从理论上分析,选用下列酸中________ (填标号),得到的高锰酸钾晶体纯度更高。
A 稀硫酸 B 浓盐酸
C 醋酸 D 稀盐酸
(5)产品中KMnO4的定量分析:
①配制浓度为0.1250 mg· mL-1的KMnO4标准溶液100 mL。
②将上述溶液稀释为浓度分别为2.5、5.0、7.5、10.0、12.5、15.0(单位:mg·L-1)的溶液,分别测定不同浓度溶液对光的吸收程度,并将测定结果绘制成曲线如下。
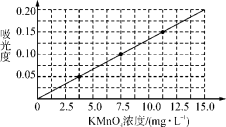
③称取KMnO4样品(不含K2MnO4)0.1250 g按步骤①配得产品溶液1000 mL,取10 mL稀释至100 mL,然后按步骤②的方法进行测定,两次测定所得的吸光度分别为0.149、0.151,则样品中KMnO4的质量分数为________ 。
(6)酸性KMnO4溶液与FeSO4溶液反应的离子方程式为____________ 。

已知:锰酸钾(K2MnO4)是墨绿色晶体,其水溶液呈深绿色,这是锰酸根离子(MnO42-)在水溶液中的特征颜色,在强碱性溶液中能稳定存在;在酸性、中性和弱碱性环境下,MnO42-会发生自身氧化还原反应,生成MnO4-和MnO2。
回答下列问题:
(1)KOH的电子式为
A 烧杯 B 瓷坩埚
C 蒸发皿 D 铁坩埚
(2)调节溶液pH过程中,所得氧化产物与还原产物的物质的量之比为
(3)趁热过滤的目的是
(4)已知20 ℃时K2SO4、KCl、CH3COOK的溶解度分别为11.1 g、34 g、217 g,则从理论上分析,选用下列酸中
A 稀硫酸 B 浓盐酸
C 醋酸 D 稀盐酸
(5)产品中KMnO4的定量分析:
①配制浓度为0.1250 mg· mL-1的KMnO4标准溶液100 mL。
②将上述溶液稀释为浓度分别为2.5、5.0、7.5、10.0、12.5、15.0(单位:mg·L-1)的溶液,分别测定不同浓度溶液对光的吸收程度,并将测定结果绘制成曲线如下。

③称取KMnO4样品(不含K2MnO4)0.1250 g按步骤①配得产品溶液1000 mL,取10 mL稀释至100 mL,然后按步骤②的方法进行测定,两次测定所得的吸光度分别为0.149、0.151,则样品中KMnO4的质量分数为
(6)酸性KMnO4溶液与FeSO4溶液反应的离子方程式为
您最近一年使用:0次



