某小组同学设计如图所示装置(夹持仪器略去)制备硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O]。
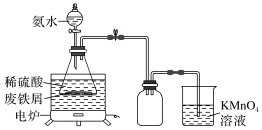
称取一定量的废铁屑于锥形瓶中,加入适量的稀硫酸,在通风橱中置于50~60 ℃热水浴中加热,充分反应。待锥形瓶中溶液冷却后加入氨水,搅拌使其反应完全,制得浅绿色悬浊液。在实验中选择50~60 ℃热水浴的原因是___________

称取一定量的废铁屑于锥形瓶中,加入适量的稀硫酸,在通风橱中置于50~60 ℃热水浴中加热,充分反应。待锥形瓶中溶液冷却后加入氨水,搅拌使其反应完全,制得浅绿色悬浊液。在实验中选择50~60 ℃热水浴的原因是
2023高三·全国·专题练习 查看更多[1]
(已下线)题型32 原因描述型实验
更新时间:2023/06/08 16:57:07
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】我国古代就已经开始研究金属,《抱朴子内篇》记载:“曾青涂铁,铁赤色如铜” 描述了古代炼铜的原理。现对其中的原理作出进一步研究。
【实验探究】
【实验结论】铁可以置换出铜,铜不可以置换出铁。
(1)写出步骤一对应的实验现象___________ 。
(2)写出步骤一发生反应的离子方程式,并用单线桥标出电子转移___________ 。
(3)金属活动性顺序表反应了金属性质的递变规律,根据金属活动性顺序表判断,下列金属还原性最强的是___________ (填标号),其对应的金属离子氧化性最强的是___________ (填标号)。
A.Ag B.K C.Mg D.Cu
(4)经实验测得 Hg2+的氧化性与 Fe3+的氧化性近似相同,请你预测Fe与Fe3+___________ (填“能”或“不能”)发生氧化还原反应,如果能,请分别写出该反应的氧化产物和还原产物的离子符号:氧化产物___________ ,还原产物 ___________ ;如果不能,请说明理由_________ 。
(5)向含有 AgNO3和Cu(NO3)2的溶液中同时加入 ag 铁粉和镁粉的混合物,充分反应后过滤,得到滤渣 M 和滤液N。向滤液N中滴入NaCl溶液,有白色沉淀产生。则下列判断中,错误的是_______ (填标号)
【实验探究】
| 实验操作 | 实验现象 |
| 步骤一:向 CuSO4溶液中加入足量的铁片 | |
| 步骤二:向 FeSO4溶液中加入足量的铜片 | 实验无明显现象 |
(1)写出步骤一对应的实验现象
(2)写出步骤一发生反应的离子方程式,并用单线桥标出电子转移
(3)金属活动性顺序表反应了金属性质的递变规律,根据金属活动性顺序表判断,下列金属还原性最强的是
A.Ag B.K C.Mg D.Cu
(4)经实验测得 Hg2+的氧化性与 Fe3+的氧化性近似相同,请你预测Fe与Fe3+
(5)向含有 AgNO3和Cu(NO3)2的溶液中同时加入 ag 铁粉和镁粉的混合物,充分反应后过滤,得到滤渣 M 和滤液N。向滤液N中滴入NaCl溶液,有白色沉淀产生。则下列判断中,错误的是_______ (填标号)
A.滤液 N 中一定含有 和 Cu2+ 和 Cu2+ | B.滤渣 M 的质量一定小于ag |
| C.滤液 N 中一定含有Fe2+和Mg2+ | D.滤渣 M 中一定是混合物 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】学习化学应该明确“从生活中来,到生活中去”道理。在生产生活中,我们会遇到各种各样的化学物质和化学反应。请按要求填空
(1)计算机芯片的主要成分是___ (填名称),节日的烟花是利用___ 。
(2)请你写出工业上用氯气和消石灰反应制取漂白粉的化学反应方程式:___ 。
(3)玉石的主要成分基本都属于硅酸盐,如某种翡翠的主要成分为NaAlSi2O6,将其表示为氧化物形式可写为___ 。
(4)沾有水的铁质器皿在加热时会发黑,该反应的化学方程式是___ 。
(5)补铁剂中的Fe2+易被氧化成Fe3+,服用时医生常建议同时服用维生素C,这是利用维生素C的___ 。
(1)计算机芯片的主要成分是
(2)请你写出工业上用氯气和消石灰反应制取漂白粉的化学反应方程式:
(3)玉石的主要成分基本都属于硅酸盐,如某种翡翠的主要成分为NaAlSi2O6,将其表示为氧化物形式可写为
(4)沾有水的铁质器皿在加热时会发黑,该反应的化学方程式是
(5)补铁剂中的Fe2+易被氧化成Fe3+,服用时医生常建议同时服用维生素C,这是利用维生素C的
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】以下关于化学实验中“先与后”的说法中正确的是____________________
①加热试管时,先均匀加热,后局部加热
②加热氯酸钾和二氧化锰的混合物制备氧气,用排水法收集气体后,先移出导管后撤酒精灯
③使用托盘天平称量物体质量时,先放质量较小的砝码,后放质量较大的砝码
④点燃可燃性气体如H2、CO等时,先检验气体纯度后点燃
⑤做H2还原CuO实验时,先通H2后加热CuO,反应完毕后,先撒酒精灯待试管冷却后停止通H2
⑥制取气体时,先检查装置气密性后装药品
⑦配制稀硫酸时,先量取一定体积的浓硫酸倒入烧杯中,后加适量的蒸馏水稀释
①加热试管时,先均匀加热,后局部加热
②加热氯酸钾和二氧化锰的混合物制备氧气,用排水法收集气体后,先移出导管后撤酒精灯
③使用托盘天平称量物体质量时,先放质量较小的砝码,后放质量较大的砝码
④点燃可燃性气体如H2、CO等时,先检验气体纯度后点燃
⑤做H2还原CuO实验时,先通H2后加热CuO,反应完毕后,先撒酒精灯待试管冷却后停止通H2
⑥制取气体时,先检查装置气密性后装药品
⑦配制稀硫酸时,先量取一定体积的浓硫酸倒入烧杯中,后加适量的蒸馏水稀释
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】海洋资源的利用具有广阔前景。
(1)无需经过化学变化就能从海水中获得的物质是( ) (填序号)
A.Cl2 B.淡水 C.烧碱 D.食盐
(2)下图是从海水中提取镁的简单流程。
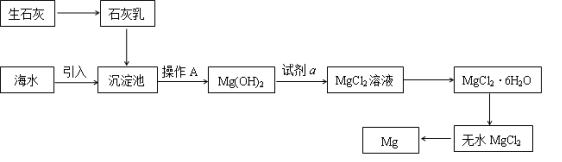
①操作A是_______________________ 。
②无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为____________________________ 。
③海水提镁的过程,为什么要将海水中的氯化镁转变为氢氧化镁,再转变为氯化镁?_____________________________________________ 。
(3)海带灰中富含以I-形式存在的碘元素。实验室提取I2的途径如下所示:

①灼烧海带至灰烬时所用的主要仪器名称是( ) (填序号)
a.坩埚 b.试管 c.蒸发皿 d.烧杯
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式________________________________ 。
③用CCl4提取碘时除了用CCl4还可以选用的试剂是( ) (填字母序号)
a.苯 b.乙醇 c.乙酸
④为检验用CCl4提取碘后的水溶液中是否还含有碘单质。请写出该实验的实验步骤、现象及结论:________ 。
(4)利用海底的“可燃冰”制作的燃料电池的总反应式为CH4+2O2+2KOH = K2CO3+3H2O,则该燃料电池的负极的电极反应为__________________ 。
(5)海底的煤经综合利用开发的副产物CO2能生产甲醇燃料,其反应的方程式为:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。某科学实验将6 mol CO2和8 mol H2充入2 L的密闭容器中,测得H2的物质的量随时间变化如图实线所示。a,b,c,d括号内数据表示坐标。
CH3OH(g)+H2O(g)。某科学实验将6 mol CO2和8 mol H2充入2 L的密闭容器中,测得H2的物质的量随时间变化如图实线所示。a,b,c,d括号内数据表示坐标。
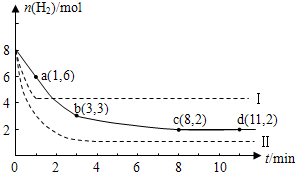
①a点正反应速率_________ (填“大于、等于或小于”)a点逆反应速率。
②平衡时CO2的物质的量浓度是___________ mol/L。
③能够说明该反应达到化学平衡状态的标志是_______ (双选)。
A.单位时间内消耗1molCO2,同时生成3mol H2 B.混合气体的密度不随时间变化
C.CH3OH、H2的浓度不再随时间变化 D.CH3OH和H2O浓度相等
(1)无需经过化学变化就能从海水中获得的物质是
A.Cl2 B.淡水 C.烧碱 D.食盐
(2)下图是从海水中提取镁的简单流程。

①操作A是
②无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为
③海水提镁的过程,为什么要将海水中的氯化镁转变为氢氧化镁,再转变为氯化镁?
(3)海带灰中富含以I-形式存在的碘元素。实验室提取I2的途径如下所示:

①灼烧海带至灰烬时所用的主要仪器名称是
a.坩埚 b.试管 c.蒸发皿 d.烧杯
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式
③用CCl4提取碘时除了用CCl4还可以选用的试剂是
a.苯 b.乙醇 c.乙酸
④为检验用CCl4提取碘后的水溶液中是否还含有碘单质。请写出该实验的实验步骤、现象及结论:
(4)利用海底的“可燃冰”制作的燃料电池的总反应式为CH4+2O2+2KOH = K2CO3+3H2O,则该燃料电池的负极的电极反应为
(5)海底的煤经综合利用开发的副产物CO2能生产甲醇燃料,其反应的方程式为:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。某科学实验将6 mol CO2和8 mol H2充入2 L的密闭容器中,测得H2的物质的量随时间变化如图实线所示。a,b,c,d括号内数据表示坐标。
CH3OH(g)+H2O(g)。某科学实验将6 mol CO2和8 mol H2充入2 L的密闭容器中,测得H2的物质的量随时间变化如图实线所示。a,b,c,d括号内数据表示坐标。
①a点正反应速率
②平衡时CO2的物质的量浓度是
③能够说明该反应达到化学平衡状态的标志是
A.单位时间内消耗1molCO2,同时生成3mol H2 B.混合气体的密度不随时间变化
C.CH3OH、H2的浓度不再随时间变化 D.CH3OH和H2O浓度相等
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】1-溴丁烷可用于合成抗胆碱药物、制备压敏色素、热敏色素等功能性色素,是一种重要的化工原料。可通过如图方法制备: CH3CH2CH2CH2Br+H2O
CH3CH2CH2CH2Br+H2O
NaBr+H2SO4 HBr↑+NaHSO4
HBr↑+NaHSO4
实验装置如图所示(夹持、加热装置已略去),步骤如下:
Ⅰ.在圆底烧瓶中加入15mL水,滴入20mL浓硫酸,混合冷却至室温后,加入7.5mL正丁醇,混合均匀。
Ⅱ.加入15g研细的NaBr,充分摇动,加入沸石,加热回流40min。
Ⅲ冷却,改用蒸馏装置,蒸出1-溴丁烷粗品。
Ⅳ.粗品倒入分液漏斗中,经水洗、浓硫酸洗、水洗、Na2CO3溶液洗、水洗后,分液,加入无水CaCl2干燥。
Ⅴ.蒸馏,得到8.0g产品。
已知相关物质信息:
回答下列问题:
(1)仪器A的名称是_______ ,B的作用是_______ ,其中导管不能伸入液面以下的原因是_______ 。
(2)实验装置中应选用的圆底烧瓶规格为_______
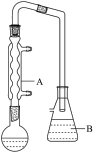
 CH3CH2CH2CH2Br+H2O
CH3CH2CH2CH2Br+H2ONaBr+H2SO4
 HBr↑+NaHSO4
HBr↑+NaHSO4实验装置如图所示(夹持、加热装置已略去),步骤如下:
Ⅰ.在圆底烧瓶中加入15mL水,滴入20mL浓硫酸,混合冷却至室温后,加入7.5mL正丁醇,混合均匀。
Ⅱ.加入15g研细的NaBr,充分摇动,加入沸石,加热回流40min。
Ⅲ冷却,改用蒸馏装置,蒸出1-溴丁烷粗品。
Ⅳ.粗品倒入分液漏斗中,经水洗、浓硫酸洗、水洗、Na2CO3溶液洗、水洗后,分液,加入无水CaCl2干燥。
Ⅴ.蒸馏,得到8.0g产品。
已知相关物质信息:
| 物质 | 性状 | 密度/(g•cm3) | 沸点/℃ | 溶解性 |
| 1-溴丁烷 | 无色液体 | 1.28 | 101.6 | 不溶于水,易溶于醇、醚 |
| 正丁醇 | 无色液体 | 0.80 | 117.6 | 微溶于水,溶于醇、醚 |
| ※醇、醚易溶于浓硫酸。 | ||||
(1)仪器A的名称是
(2)实验装置中应选用的圆底烧瓶规格为_______
| A.25mL | B.50mL | C.100mL | D.250mL |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】以红土镍矿(主要成分为NiO、FeO、Fe2O3、MgO和SiO2等)为原料制备Ni(OH)2的工艺流程如图:
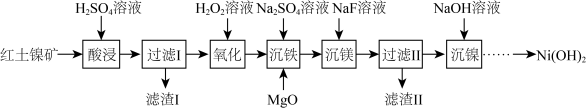
(1)“酸浸”时,加快化学反应速率的措施______ (写一条即可),滤渣Ⅰ的成分为____ (填化学式)。
(2)“氧化”时,Fe2+发生反应的离子方程式为_____ ,若用NaClO代替H2O2溶液,使0.1molFe2+转化为Fe3+,则需NaClO至少为____ mol。
(3)MgO的作用是调节溶液pH使Fe3+沉淀,根据下表的数据,则调节溶液pH的范围是_____ 。
(4)“沉镁”是生成MgF2沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原因是_____ 。
(5)“沉镍”后需过滤、洗涤,证明沉淀已洗涤干净的方法是_____ 。

(1)“酸浸”时,加快化学反应速率的措施
(2)“氧化”时,Fe2+发生反应的离子方程式为
(3)MgO的作用是调节溶液pH使Fe3+沉淀,根据下表的数据,则调节溶液pH的范围是
| 金属离子 | Fe2+ | Fe3+ | Mg2+ | Ni2+ |
| 开始沉淀的pH | 6.3 | 1.5 | 8.9 | 6.9 |
| 沉淀完全的pH | 8.3 | 2.8 | 10.9 | 8.9 |
(5)“沉镍”后需过滤、洗涤,证明沉淀已洗涤干净的方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】焦亚硫酸钠(Na2S2O5)在医药、橡胶、印染、食品等方面应用广泛。回答下列问题:
(1)生产Na2S2O5,通常是由NaHSO3过饱和溶液经结晶脱水制得。写出该过程的化学方程式:_______________________________________________________ 。
(2)利用烟道气中的SO2生产Na2S2O5的工艺为:
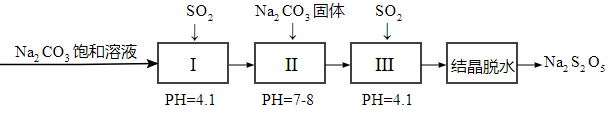
①pH=4.1时,Ⅰ中为________ 溶液(写化学式)。
②工艺中加入Na2CO3固体、并再次充入SO2的目的是__________________ 。
(3)Na2S2O5可用作食品的抗氧化剂。在测定某葡萄酒中Na2S2O5残留量时,取50.00 mL葡萄酒样品,用0.010 00 mol·L-1的碘标准液滴定至终点,消耗10.00 mL。滴定反应的离子方程式为___________________________________________ ,该样品中Na2S2O5的残留量为____ g·L-1(以SO2计)。
(1)生产Na2S2O5,通常是由NaHSO3过饱和溶液经结晶脱水制得。写出该过程的化学方程式:
(2)利用烟道气中的SO2生产Na2S2O5的工艺为:

①pH=4.1时,Ⅰ中为
②工艺中加入Na2CO3固体、并再次充入SO2的目的是
(3)Na2S2O5可用作食品的抗氧化剂。在测定某葡萄酒中Na2S2O5残留量时,取50.00 mL葡萄酒样品,用0.010 00 mol·L-1的碘标准液滴定至终点,消耗10.00 mL。滴定反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】二草酸合铜(Ⅱ)酸钾( )可用于无机合成、功能材料制备。实验室制备二草酸合铜(Ⅱ)酸钾可采用如下步骤:
)可用于无机合成、功能材料制备。实验室制备二草酸合铜(Ⅱ)酸钾可采用如下步骤:
Ⅰ.取已知浓度的 溶液,搅拌下滴加足量
溶液,搅拌下滴加足量 溶液,产生浅蓝色沉淀。加热,沉淀转变成黑色,过滤。
溶液,产生浅蓝色沉淀。加热,沉淀转变成黑色,过滤。
Ⅱ.向草酸( )溶液中加入适量
)溶液中加入适量 固体,制得
固体,制得 和
和 混合溶液。
混合溶液。
Ⅲ.将Ⅱ的混合溶液加热至80-85℃,加入Ⅰ中的黑色沉淀。全部溶解后,趁热过滤。
Ⅳ.将Ⅲ的滤液用蒸汽浴加热浓缩,经一系列操作后,干燥,得到二草酸合铜(Ⅱ)酸钾晶体,进行表征和分析。
回答下列问题:
(1)长期存放的 中,会出现少量白色固体,原因是
中,会出现少量白色固体,原因是_______ 。
 )可用于无机合成、功能材料制备。实验室制备二草酸合铜(Ⅱ)酸钾可采用如下步骤:
)可用于无机合成、功能材料制备。实验室制备二草酸合铜(Ⅱ)酸钾可采用如下步骤:Ⅰ.取已知浓度的
 溶液,搅拌下滴加足量
溶液,搅拌下滴加足量 溶液,产生浅蓝色沉淀。加热,沉淀转变成黑色,过滤。
溶液,产生浅蓝色沉淀。加热,沉淀转变成黑色,过滤。Ⅱ.向草酸(
 )溶液中加入适量
)溶液中加入适量 固体,制得
固体,制得 和
和 混合溶液。
混合溶液。Ⅲ.将Ⅱ的混合溶液加热至80-85℃,加入Ⅰ中的黑色沉淀。全部溶解后,趁热过滤。
Ⅳ.将Ⅲ的滤液用蒸汽浴加热浓缩,经一系列操作后,干燥,得到二草酸合铜(Ⅱ)酸钾晶体,进行表征和分析。
回答下列问题:
(1)长期存放的
 中,会出现少量白色固体,原因是
中,会出现少量白色固体,原因是
您最近一年使用:0次

 的形式存在。回答下列问题:
的形式存在。回答下列问题:


