回答下列问题:
(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是_______ (填字母)。
A.Fe B.Fe2+ C.Fe3+
(2)已知Fe(CrO2)2中铬元素是+3价,则其中铁元素是_______ 价。 是一种酸根离子,则Fe(CrO2)2属于
是一种酸根离子,则Fe(CrO2)2属于_______ (填“酸”、“碱”、“盐”或“氧化物”)。
(3)工业盐的主要成分是NaNO2,曾多次发生过因误食NaNO2而中毒的事件,其原因是NaNO2把人体内的Fe2+转化为Fe3+而失去与O2结合的能力,工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有_______ 性。
(4)在Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了_______ 性和_______ 性,则56 gFe参加反应时,被还原的HNO3为_______ g。
(5) Ca(Cl O)2+4HCl(浓)=2Cl2↑+CaCl2+2H2O 用双线桥表示反应电子转移方向和数目_______ 。
(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是
A.Fe B.Fe2+ C.Fe3+
(2)已知Fe(CrO2)2中铬元素是+3价,则其中铁元素是
 是一种酸根离子,则Fe(CrO2)2属于
是一种酸根离子,则Fe(CrO2)2属于(3)工业盐的主要成分是NaNO2,曾多次发生过因误食NaNO2而中毒的事件,其原因是NaNO2把人体内的Fe2+转化为Fe3+而失去与O2结合的能力,工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有
(4)在Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了
(5) Ca(Cl O)2+4HCl(浓)=2Cl2↑+CaCl2+2H2O 用双线桥表示反应电子转移方向和数目
更新时间:2023-05-12 15:49:19
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】同学们吃的零食的包装袋中经常有一个小纸袋,上面写着“干燥剂”,其主要成分是生石灰(CaO)。
(1)生石灰属于_______ (填字母,下同)。
A.酸 B.碱 C.盐 D.纯净物 E.化合物 F.金属氧化物 G.非金属氧化物 H.碱性氧化物 I.酸性氧化物
(2)某同学将浓硫酸、NaOH固体、生石灰等物质划分为一类。该同学的分类依据为_______ 。
A.酸类 B.碱类 C.氧化物 D.干燥剂
氢氧化钠中的化学键类型_______ 。
(3)生石灰还可以跟哪些类别的物质发生化学反应?请列举三例并填表。
(4)小纸袋中的物质是否能长期持续地作干燥剂?_______ (填“是”或“否”)。请说明理由:_______ 。
(1)生石灰属于
A.酸 B.碱 C.盐 D.纯净物 E.化合物 F.金属氧化物 G.非金属氧化物 H.碱性氧化物 I.酸性氧化物
(2)某同学将浓硫酸、NaOH固体、生石灰等物质划分为一类。该同学的分类依据为
A.酸类 B.碱类 C.氧化物 D.干燥剂
氢氧化钠中的化学键类型
(3)生石灰还可以跟哪些类别的物质发生化学反应?请列举三例并填表。
| 物质类别 | 化学方程式 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】某校化学实验室由于长时间未使用,很多试剂药品摆放杂乱无章,现需要对其进行分类整理,现有药品:①硫酸钠固体 ②蔗糖溶液 ③铜 ④CH3CH2OH ⑤石墨 ⑥液氨 ⑦NaHCO3溶液 ⑧稀硫酸 ⑨碳酸钠粉末 ⑩氢氧化铁胶体 ⑪Ba(OH)2固体
(1)其中属于混合物的是_______ (填标号,下同);属于盐的是_______ 。
(2)上述物质状态下(除⑩外)能导电的是_______ ;属于电解质的是_______ 。
(3)将少量的⑪加入⑧中发生反应的离子方程式为_______ 。
(1)其中属于混合物的是
(2)上述物质状态下(除⑩外)能导电的是
(3)将少量的⑪加入⑧中发生反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】央视《每周质量报告》曝光了河北省一些明胶企业将皮革废料熬制成工业明胶,出售给浙江绍兴某些制药企业,最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属铬,会对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
(1)已知 中铬元素是+3价,则其中铁元素是
中铬元素是+3价,则其中铁元素是__________ 价。 是一种酸根离子,则
是一种酸根离子,则 属于
属于__________ (填“酸”、“碱”、“盐”或“氧化物”)。
(2)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的装置是下列中的__________ (填序号)。
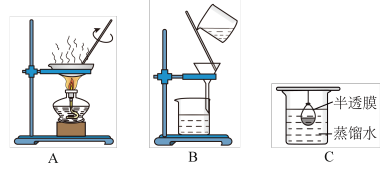
(3)现有10mL明胶的水溶液与5mLK2SO4溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明 能够透过半透膜:
能够透过半透膜:_____________________ ;该检验过程中发生的离子方程式为____________________ 。
(1)已知
 中铬元素是+3价,则其中铁元素是
中铬元素是+3价,则其中铁元素是 是一种酸根离子,则
是一种酸根离子,则 属于
属于(2)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的装置是下列中的

(3)现有10mL明胶的水溶液与5mLK2SO4溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明
 能够透过半透膜:
能够透过半透膜:
您最近一年使用:0次
【推荐1】KClO3和浓盐酸在一定温度下发生如(1)的反应:
(1)请配平方程式,并用双线桥表示得失电子情况:
_____ KClO3+______ HCl(浓)=______ KCl+______ ClO2↑+Cl2↑+______ H2O
_______________________________________________________________
(2)氧化剂是_________ ,还原产物是_________ (写化学式)。
(3)产生0.1molCl2时,转移电子的物质的量为__________ mol。
(1)请配平方程式,并用双线桥表示得失电子情况:
(2)氧化剂是
(3)产生0.1molCl2时,转移电子的物质的量为
您最近一年使用:0次
【推荐2】按要求填空。
(1)反应 在化学上被称为“铝热反应”,人们可利用该反应来焊接铁轨。该反应中,
在化学上被称为“铝热反应”,人们可利用该反应来焊接铁轨。该反应中,___________ (填分子式,下同)是氧化剂,___________ 是还原产物。
(2)适量服用维生素C有利于铁元素的吸收,原因是维生素C可以将 转变为
转变为 。这说明维生素C具有:
。这说明维生素C具有:___________ (填“氧化性”或“还原性”)。
(3)已知有 ,
,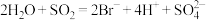 ,根据上述反应可判断
,根据上述反应可判断 、
、 、
、 的还原性由强到弱的顺序为
的还原性由强到弱的顺序为___________ 。
(4)含氮废水不仅会引起水体富营养化而导致黑臭,而且对人群及其他生物产生毒害作用。现采用铝还原法来将 还原为
还原为 。请配平该化学反应方程式并在该反应方程式上用单线桥表示该反应中电子转移情况:
。请配平该化学反应方程式并在该反应方程式上用单线桥表示该反应中电子转移情况:________
___________ ___________Al+___________
___________Al+___________ ___________
___________ ___________
___________ ___________KOH
___________KOH
(5)元素G的一种含氧酸化学式为 ,属于二元酸,则
,属于二元酸,则 与过量氢氧化钠溶液反应生成的产物
与过量氢氧化钠溶液反应生成的产物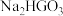 为
为___________ (填“酸式盐”或“正盐”)。
(1)反应
 在化学上被称为“铝热反应”,人们可利用该反应来焊接铁轨。该反应中,
在化学上被称为“铝热反应”,人们可利用该反应来焊接铁轨。该反应中,(2)适量服用维生素C有利于铁元素的吸收,原因是维生素C可以将
 转变为
转变为 。这说明维生素C具有:
。这说明维生素C具有:(3)已知有
 ,
,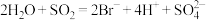 ,根据上述反应可判断
,根据上述反应可判断 、
、 、
、 的还原性由强到弱的顺序为
的还原性由强到弱的顺序为(4)含氮废水不仅会引起水体富营养化而导致黑臭,而且对人群及其他生物产生毒害作用。现采用铝还原法来将
 还原为
还原为 。请配平该化学反应方程式并在该反应方程式上用单线桥表示该反应中电子转移情况:
。请配平该化学反应方程式并在该反应方程式上用单线桥表示该反应中电子转移情况:___________
 ___________Al+___________
___________Al+___________ ___________
___________ ___________
___________ ___________KOH
___________KOH(5)元素G的一种含氧酸化学式为
 ,属于二元酸,则
,属于二元酸,则 与过量氢氧化钠溶液反应生成的产物
与过量氢氧化钠溶液反应生成的产物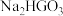 为
为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下:3Cu + 8HNO3 (稀)=3Cu(NO3)2 + 2NO↑+ 4H2O。
(1)被氧化的元素是_______ ,被还原的元素是__________ ,发生氧化反应的物质是________ ,发生还原反应的物质是______________ 。
(2)用双线桥法表示反应电子得失的方向和数目:__________________________________ 。
(3)用单线桥法表示反应电子得失的方向和数目:__________________________________ 。
(1)被氧化的元素是
(2)用双线桥法表示反应电子得失的方向和数目:
(3)用单线桥法表示反应电子得失的方向和数目:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生过程:H2O2→O2。
(1)该反应中的还原剂是___ 。
(2)该反应中,发生还原反应的过程是:___ →___ 。
(3)H2O2常用作氧化剂、漂白剂和消毒剂。为了便于贮存、运输和使用,工业上将过氧化氢转化为固态的过碳酸钠晶体(2Na2CO3·3H2O2),该晶体具有Na2CO3和H2O2的双重性质。接触下列物质不会使过碳酸钠失效的是___ 。
A.MnO2 B.Ca(OH)2 C.HCl D.NaCl
(1)该反应中的还原剂是
(2)该反应中,发生还原反应的过程是:
(3)H2O2常用作氧化剂、漂白剂和消毒剂。为了便于贮存、运输和使用,工业上将过氧化氢转化为固态的过碳酸钠晶体(2Na2CO3·3H2O2),该晶体具有Na2CO3和H2O2的双重性质。接触下列物质不会使过碳酸钠失效的是
A.MnO2 B.Ca(OH)2 C.HCl D.NaCl
您最近一年使用:0次
【推荐2】实验室里迅速制备少量氯气可利用如下反应:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,此反应不需加热,常温下就可以迅速进行,而且对盐酸的浓度要求不高。
(1)该反应中,氧化剂是________ ,还原剂是________ 。
(2)当参加反应的氧化剂的物质的量是1mol时,被氧化的还原剂的物质的量是________ ,产生的氯气在标准状况下的体积为________ ,电子转移数目为________ 。
(3)氯化氢在该反应过程中表现出的化学性质有________ 。
A 酸性B 还原性C 氧化性D 挥发性
(1)该反应中,氧化剂是
(2)当参加反应的氧化剂的物质的量是1mol时,被氧化的还原剂的物质的量是
(3)氯化氢在该反应过程中表现出的化学性质有
A 酸性B 还原性C 氧化性D 挥发性
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】铁元素存在多种价态,且不同价态的铁元素在一定条件下可以相互转化。
(1)向2 mL 1 mol/L的Fe(NO3)2溶液中加入2 mol/L的H2SO4溶液至Fe2+恰好转化为Fe3+为止,写出反应的离子方程式___________ 。
(2) 是一种新型水处理剂,将
是一种新型水处理剂,将 溶液、
溶液、 溶液与
溶液与 溶液混合可得到
溶液混合可得到 。
。
① 中铁元素的化合价为
中铁元素的化合价为___________ ,当有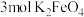 生成时,反应中转移的电子数目为
生成时,反应中转移的电子数目为___________  。
。
②发生相应反应的离子方程式为___________ 。
(3)某同学设计如图装置制备一定量的 ,并使其能在较长时间内存在。
,并使其能在较长时间内存在。

①X不能是硝酸,原因是___________ ,装置4的作用是___________ 。
②实验开始时,开关 应
应___________ (填“打开”成“关闭”);这样操作的目的是___________ 。
(1)向2 mL 1 mol/L的Fe(NO3)2溶液中加入2 mol/L的H2SO4溶液至Fe2+恰好转化为Fe3+为止,写出反应的离子方程式
(2)
 是一种新型水处理剂,将
是一种新型水处理剂,将 溶液、
溶液、 溶液与
溶液与 溶液混合可得到
溶液混合可得到 。
。①
 中铁元素的化合价为
中铁元素的化合价为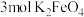 生成时,反应中转移的电子数目为
生成时,反应中转移的电子数目为 。
。②发生相应反应的离子方程式为
(3)某同学设计如图装置制备一定量的
 ,并使其能在较长时间内存在。
,并使其能在较长时间内存在。
①X不能是硝酸,原因是
②实验开始时,开关
 应
应
您最近一年使用:0次
【推荐1】请将5种物质:N2O、FeCl2、Fe (NO3)3、HNO3和FeCl3分别填入下面对应的横线上,组成一个未配平的化学方程式。
(1)___ +___ →___ +___ +___ +H2O(不需配平)
(2)反应过程中,N2O与FeCl2的物质的量之比为____ 。
(1)
(2)反应过程中,N2O与FeCl2的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】防治环境污染,改善生态环境已成为全球共识。回答下列问题:
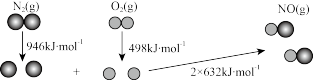
(1)汽车尾气中NO生成过程中的能量变化如图所示。生成1 mol
___________ (填“吸收”或“放出”)___________ kJ的热量。
(2)汽车尾气(含CO、 和
和 等)是城市空气的污染源之一,三元催化可以将汽车尾气中的CO和
等)是城市空气的污染源之一,三元催化可以将汽车尾气中的CO和 进行净化处理,写出NO和CO反应转化为无害气体的化学方程式
进行净化处理,写出NO和CO反应转化为无害气体的化学方程式___________ 。
(3)硝酸工业废气中有氮氧化物( ),利用尿素消除
),利用尿素消除 污染的转化反应为:
污染的转化反应为:
ⅰ.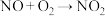 ,ⅱ.
,ⅱ.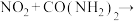 无污染气体。
无污染气体。
尿素中C元素的化合价___________ ,反应ⅱ的化学方程式为___________ 。
(4)用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。

①在酸性NaClO溶液中,HClO氧化NO生成 和
和 ,其离子方程式为
,其离子方程式为___________ 。
②NaClO溶液的初始pH越小,NO转化率越高。其原因是___________ 。
(5)加入过量次氯酸钠可使废水中 完全转化为
完全转化为 ,而本身被还原为NaCl。
,而本身被还原为NaCl。
①检验废水中是否存在 的方法是
的方法是___________ 。
②若处理废水产生了0.448 L (标准状况),则需消耗浓度为2 mol/L的次氯酸钠的体积为
(标准状况),则需消耗浓度为2 mol/L的次氯酸钠的体积为___________ mL。
(1)汽车尾气中NO生成过程中的能量变化如图所示。生成1 mol


(2)汽车尾气(含CO、
 和
和 等)是城市空气的污染源之一,三元催化可以将汽车尾气中的CO和
等)是城市空气的污染源之一,三元催化可以将汽车尾气中的CO和 进行净化处理,写出NO和CO反应转化为无害气体的化学方程式
进行净化处理,写出NO和CO反应转化为无害气体的化学方程式(3)硝酸工业废气中有氮氧化物(
 ),利用尿素消除
),利用尿素消除 污染的转化反应为:
污染的转化反应为:ⅰ.
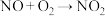 ,ⅱ.
,ⅱ.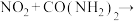 无污染气体。
无污染气体。尿素中C元素的化合价
(4)用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为
 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
①在酸性NaClO溶液中,HClO氧化NO生成
 和
和 ,其离子方程式为
,其离子方程式为②NaClO溶液的初始pH越小,NO转化率越高。其原因是
(5)加入过量次氯酸钠可使废水中
 完全转化为
完全转化为 ,而本身被还原为NaCl。
,而本身被还原为NaCl。①检验废水中是否存在
 的方法是
的方法是②若处理废水产生了0.448 L
 (标准状况),则需消耗浓度为2 mol/L的次氯酸钠的体积为
(标准状况),则需消耗浓度为2 mol/L的次氯酸钠的体积为
您最近一年使用:0次

 CO2↑+2SO2↑+2H2O反应中:
CO2↑+2SO2↑+2H2O反应中: 

