某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生过程:H2O2→O2。
(1)该反应中的还原剂是___ 。
(2)该反应中,发生还原反应的过程是:___ →___ 。
(3)H2O2常用作氧化剂、漂白剂和消毒剂。为了便于贮存、运输和使用,工业上将过氧化氢转化为固态的过碳酸钠晶体(2Na2CO3·3H2O2),该晶体具有Na2CO3和H2O2的双重性质。接触下列物质不会使过碳酸钠失效的是___ 。
A.MnO2 B.Ca(OH)2 C.HCl D.NaCl
(1)该反应中的还原剂是
(2)该反应中,发生还原反应的过程是:
(3)H2O2常用作氧化剂、漂白剂和消毒剂。为了便于贮存、运输和使用,工业上将过氧化氢转化为固态的过碳酸钠晶体(2Na2CO3·3H2O2),该晶体具有Na2CO3和H2O2的双重性质。接触下列物质不会使过碳酸钠失效的是
A.MnO2 B.Ca(OH)2 C.HCl D.NaCl
更新时间:2020-12-30 20:06:37
|
相似题推荐
【推荐1】氧化还原反应在生产、生活中具有广泛的用途。
(1)下列生产、生活中的事例中没有发生氧化还原反应的是______ (填字母)。
(2)过氧化氢的水溶液俗称双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称,如消除采矿业胶液中的氰化物(如KCN),经以下反应实现:KCN+H2O2+H2O===A+NH3↑,则生成物A的化学式为____________________ 。
(3)“四种基本反应类型与氧化还原反应的关系”可用下图表达。
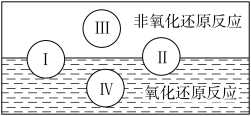
下列化学反应(部分化学反应未配平)符合反应类型Ⅳ的是________ (填序号)。
①P4+CuSO4+H2O→Cu3P+H3PO4+H2SO4
②P4(白磷)===P4(红磷)
③10C+P4O10===P4↑+10CO↑
④2Ca3(PO4)2+6SiO2===6CaSiO3+P4O10
反应①中,氧化剂为______ ,上述反应①中反应物还可以发生如下反应P4+CuSO4+H2O→Cu+H3PO4+H2SO4,则两个化学反应中被氧化的P4的物质的量相等时,消耗的CuSO4的物质的量之比为________ 。
(4)氯化铵常用作焊接。如在焊接铜器时用氯化铵除去铜器表面的氧化铜以便焊接,其反应为CuO+NH4Cl Cu+CuCl2+N2↑+H2O。该反应中,被氧化的元素是
Cu+CuCl2+N2↑+H2O。该反应中,被氧化的元素是______ (填元素名称),反应中若产生0.2mol气体,则_____ mol电子发生转移。
(1)下列生产、生活中的事例中没有发生氧化还原反应的是

(2)过氧化氢的水溶液俗称双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称,如消除采矿业胶液中的氰化物(如KCN),经以下反应实现:KCN+H2O2+H2O===A+NH3↑,则生成物A的化学式为
(3)“四种基本反应类型与氧化还原反应的关系”可用下图表达。

下列化学反应(部分化学反应未配平)符合反应类型Ⅳ的是
①P4+CuSO4+H2O→Cu3P+H3PO4+H2SO4
②P4(白磷)===P4(红磷)
③10C+P4O10===P4↑+10CO↑
④2Ca3(PO4)2+6SiO2===6CaSiO3+P4O10
反应①中,氧化剂为
(4)氯化铵常用作焊接。如在焊接铜器时用氯化铵除去铜器表面的氧化铜以便焊接,其反应为CuO+NH4Cl
 Cu+CuCl2+N2↑+H2O。该反应中,被氧化的元素是
Cu+CuCl2+N2↑+H2O。该反应中,被氧化的元素是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】三氟化氮(NF3)是一种无色、无味的气体,它是微电子工业技术的关键原料之一。
(1)三氟化氮可由氨气和氟气反应得到:4NH3+3F2=NF3+3NH4F。NH3的电子式为_______ ,反应中氨气显示的化学性质有_____________ ,当有17.0g氨气发生反应时,转移电子的物质的量为_______ 。
(2)在潮湿的空气中,NF3能与水蒸气发生反应,产物有HF、NO和一种酸,则被氧化与被还原元素原子的物质的量之比为___________ ,NF3、F2、NO三种气体氧化性由弱到强的顺序为____________ 。
(3)三氟化氮在空气中泄漏时,很容易被发现,依据的现象是_______________________ 。
(4)NCl3的结构类似NF3,但NCl3中N元素显-3价,NCl3遇水发生反应,且反应为非氧化还原反应,该反应的化学方程式为______________________________ 。
(1)三氟化氮可由氨气和氟气反应得到:4NH3+3F2=NF3+3NH4F。NH3的电子式为
(2)在潮湿的空气中,NF3能与水蒸气发生反应,产物有HF、NO和一种酸,则被氧化与被还原元素原子的物质的量之比为
(3)三氟化氮在空气中泄漏时,很容易被发现,依据的现象是
(4)NCl3的结构类似NF3,但NCl3中N元素显-3价,NCl3遇水发生反应,且反应为非氧化还原反应,该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】阅读下列材料后回答有关问题。
一个体重50 kg的健康人,体内含铁元素2 g,这2 g铁元素以Fe2+和Fe3+的形式存在。Fe2+易被吸收,所以给贫血者补充铁时,应补充含Fe2+的亚铁盐(如FeSO4),服用维生素C可使食物中的Fe3+转化成Fe2+,有利于人体对铁的吸收。
(1)人体中经常进行Fe2+与Fe3+的转化,在此转化过程中,Fe2+作___________ (填“氧化”或“还原”,下同)剂,被___________ 。
(2)“服用维生素C可使食物中的Fe3+转化为Fe2+”这句话说明,维生素C在这个反应中作___________ (填“氧化”或“还原”,下同)剂,具有___________ 性。
(3)补血剂的主要成分是FeSO4,请写出产物有FeSO4的符合要求的化学方程式:
①置换反应:___________ 。
②复分解反应:___________ 。
(4)有人在研究硫酸亚铁(FeSO4)热稳定性时,假设它按CaCO3受热分解的方式分解,反应的化学方程式为___________ 。
一个体重50 kg的健康人,体内含铁元素2 g,这2 g铁元素以Fe2+和Fe3+的形式存在。Fe2+易被吸收,所以给贫血者补充铁时,应补充含Fe2+的亚铁盐(如FeSO4),服用维生素C可使食物中的Fe3+转化成Fe2+,有利于人体对铁的吸收。
(1)人体中经常进行Fe2+与Fe3+的转化,在此转化过程中,Fe2+作
(2)“服用维生素C可使食物中的Fe3+转化为Fe2+”这句话说明,维生素C在这个反应中作
(3)补血剂的主要成分是FeSO4,请写出产物有FeSO4的符合要求的化学方程式:
①置换反应:
②复分解反应:
(4)有人在研究硫酸亚铁(FeSO4)热稳定性时,假设它按CaCO3受热分解的方式分解,反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1)已知反应:K2Cr2O7 + 14HCl=2KCl + 2CrCl3 + 3Cl2↑+ 7H2O,用“单线桥”表示电子转移的方向和数目,并指出氧化产物和还原产物_____________ 。
(2)Cl2是一种有毒气体,如果泄漏会造成严重的环境污染。化工厂可用浓氨水来检验Cl2是否泄漏,有关反应的化学方程式为:3Cl2(气)+8NH3(气)=6NH4Cl(固)+N2(气),若反应中消耗Cl2 1.5 mol,求被氧化的NH3在标准状况下的体积_________________ 。
(2)Cl2是一种有毒气体,如果泄漏会造成严重的环境污染。化工厂可用浓氨水来检验Cl2是否泄漏,有关反应的化学方程式为:3Cl2(气)+8NH3(气)=6NH4Cl(固)+N2(气),若反应中消耗Cl2 1.5 mol,求被氧化的NH3在标准状况下的体积
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)芒硝的化学式是_________________ 。
(2)以氯化钠、石灰石、水为原料制取漂白粉,写出有关反应的化学方程式。
①______________________________ ;②_________________________________ ;
③______________________________ ;④_________________________________ 。
(3)元素铬(Cr)在溶液中主要以Cr3+、Cr2O72—(橙红色)、CrO42—(黄色)CrO2—等形式存在。回答下列问题:
① 与
与 的化学性质相似。写出向
的化学性质相似。写出向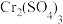 溶液中加入过量
溶液中加入过量 溶液反应的离子方程式
溶液反应的离子方程式_____________________________________________ 。
② 价铬的化合物毒性较大,常用
价铬的化合物毒性较大,常用 将废液中的
将废液中的 还原成
还原成 ,该反应的离子方程式为
,该反应的离子方程式为 ______________________________________________________ 。
(2)以氯化钠、石灰石、水为原料制取漂白粉,写出有关反应的化学方程式。
①
③
(3)元素铬(Cr)在溶液中主要以Cr3+、Cr2O72—(橙红色)、CrO42—(黄色)CrO2—等形式存在。回答下列问题:
①
 与
与 的化学性质相似。写出向
的化学性质相似。写出向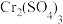 溶液中加入过量
溶液中加入过量 溶液反应的离子方程式
溶液反应的离子方程式②
 价铬的化合物毒性较大,常用
价铬的化合物毒性较大,常用 将废液中的
将废液中的 还原成
还原成 ,该反应的离子方程式为
,该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】有10mLNaOH溶液,问其中逐渐通入一定量的CO2,然后向该溶液中逐滴加入1mol·L-1盐酸,所加入盐酸的体积与产生二氧化碳的体积(标准状况)关系如图所示。
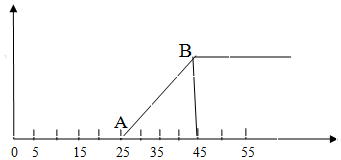
(1)NaOH在吸收CO2气体后,所得溶液中存在的溶质是_______ ,其物质的量之比是_______ 。
(2)当加入35mL盐酸时,所产生的二氧化碳的体积(标准状况)是_______ 。
(3)计算原NaOH溶液的物质的量浓度是_______ 。

(1)NaOH在吸收CO2气体后,所得溶液中存在的溶质是
(2)当加入35mL盐酸时,所产生的二氧化碳的体积(标准状况)是
(3)计算原NaOH溶液的物质的量浓度是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】依据图像特点判断溶液溶质成分


若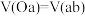 (即 (即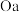 段与 段与 段消耗盐酸的体积相同) 段消耗盐酸的体积相同) | 溶液中的溶质为 | 涉及离子方程式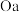 : : : : |
若 (即 (即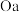 段消耗盐酸的体积大于 段消耗盐酸的体积大于 段消耗盐酸的体积) 段消耗盐酸的体积) | 溶液中的溶质为 | 涉及离子方程式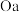 : : : : |
若 (即 (即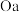 段消耗盐酸的体积小于 段消耗盐酸的体积小于 段消耗盐酸的体积) 段消耗盐酸的体积) | 溶液中的溶质为 | 涉及离子方程式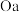 : : : : |
若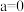 (即图像从原点开始) (即图像从原点开始) | 溶液中的溶质为 | 涉及离子方程式: |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)相同质量的氢气和二氧化碳的物质的量较多的是______ ,同温同压下体积较大的是______ 。
(2)相同物质的量的碳酸钠和碳酸氢钠与足量的盐酸反应,消耗盐酸较多的是______ 。相同质量的碳酸钠和碳酸氢钠与足量的盐酸反应,生成二氧化碳较多的是______ 。
(3)10.6g无水碳酸钠的物质的量为______ mol;将它溶于水制成500mL溶液,溶液中Na+的浓度为______ mol/L。
(4)实验室用二氧化锰与浓盐酸制取并收集干燥的氯气时,氢氧化钠的作用是______ ,浓硫酸的作用是______ 。
(5)在反应2H2S+SO2=3S↓+2H2O中,氧化产物和还原产物的质量比为______ ,SO2做______ 剂。
(2)相同物质的量的碳酸钠和碳酸氢钠与足量的盐酸反应,消耗盐酸较多的是
(3)10.6g无水碳酸钠的物质的量为
(4)实验室用二氧化锰与浓盐酸制取并收集干燥的氯气时,氢氧化钠的作用是
(5)在反应2H2S+SO2=3S↓+2H2O中,氧化产物和还原产物的质量比为
您最近一年使用:0次

 ,而铁钉在盐酸中生成浅绿色的
,而铁钉在盐酸中生成浅绿色的 溶液。则在
溶液。则在 、
、 、
、 中,具有氧化性的是
中,具有氧化性的是 在不同的反应中,可以分别表现出酸性、氧化性和还原性。现有如下反应,请写出
在不同的反应中,可以分别表现出酸性、氧化性和还原性。现有如下反应,请写出 :
: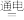 H2+Cl2:
H2+Cl2:

