阅读下列材料后回答有关问题。
一个体重50 kg的健康人,体内含铁元素2 g,这2 g铁元素以Fe2+和Fe3+的形式存在。Fe2+易被吸收,所以给贫血者补充铁时,应补充含Fe2+的亚铁盐(如FeSO4),服用维生素C可使食物中的Fe3+转化成Fe2+,有利于人体对铁的吸收。
(1)人体中经常进行Fe2+与Fe3+的转化,在此转化过程中,Fe2+作___________ (填“氧化”或“还原”,下同)剂,被___________ 。
(2)“服用维生素C可使食物中的Fe3+转化为Fe2+”这句话说明,维生素C在这个反应中作___________ (填“氧化”或“还原”,下同)剂,具有___________ 性。
(3)补血剂的主要成分是FeSO4,请写出产物有FeSO4的符合要求的化学方程式:
①置换反应:___________ 。
②复分解反应:___________ 。
(4)有人在研究硫酸亚铁(FeSO4)热稳定性时,假设它按CaCO3受热分解的方式分解,反应的化学方程式为___________ 。
一个体重50 kg的健康人,体内含铁元素2 g,这2 g铁元素以Fe2+和Fe3+的形式存在。Fe2+易被吸收,所以给贫血者补充铁时,应补充含Fe2+的亚铁盐(如FeSO4),服用维生素C可使食物中的Fe3+转化成Fe2+,有利于人体对铁的吸收。
(1)人体中经常进行Fe2+与Fe3+的转化,在此转化过程中,Fe2+作
(2)“服用维生素C可使食物中的Fe3+转化为Fe2+”这句话说明,维生素C在这个反应中作
(3)补血剂的主要成分是FeSO4,请写出产物有FeSO4的符合要求的化学方程式:
①置换反应:
②复分解反应:
(4)有人在研究硫酸亚铁(FeSO4)热稳定性时,假设它按CaCO3受热分解的方式分解,反应的化学方程式为
23-24高一下·全国·课时练习 查看更多[1]
更新时间:2023-12-20 09:52:26
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】双氧水、84消毒液、高铁酸钠是生活中常用的消毒剂,请回答下列问题:
(1)某同学设计如表实验研究H2O2的性质
已知:I2遇淀粉溶液变蓝
①从化合价改变上看H2O2,既有氧化性又有还原性,具有还原性的原因是_______ 。
②能证明H2O2具有氧化性的实验是________ (填序号“i”或“ii”)。
(2)2016年巴西奥运会期间,由于工作人员将84消毒液(有效成分为NaClO)与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是NaClO与H2O2反应产生O2促进藻类快速生长。
已知:NaClO具有强氧化性,易被还原为NaCl
①该反应说明氧化性:NaClO________ O2(填“>”或“<”)。
②当有3个氧气分子生成时,转移________ 个电子。
(3)湿法制备Na2FeO4,反应为:2Fe(OH)3+3NaClO+4NaOH=2Na2FeO4+3NaCl+5H2O。
①该反应的氧化产物是________ 。
②用双线桥法标出该反应电子转移的方向和数目______ 。
(1)某同学设计如表实验研究H2O2的性质
| 序号 | 实验 | 实验现象 |
| i | 向5%H2O2溶液中滴加酸性KMnO4溶液 | a.溶液紫色褪去 b.有大量气泡产生 |
| ii | 向5%H2O2溶液中滴加淀粉碘化钾溶液 | c.溶液变蓝 |
①从化合价改变上看H2O2,既有氧化性又有还原性,具有还原性的原因是
②能证明H2O2具有氧化性的实验是
(2)2016年巴西奥运会期间,由于工作人员将84消毒液(有效成分为NaClO)与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是NaClO与H2O2反应产生O2促进藻类快速生长。
已知:NaClO具有强氧化性,易被还原为NaCl
①该反应说明氧化性:NaClO
②当有3个氧气分子生成时,转移
(3)湿法制备Na2FeO4,反应为:2Fe(OH)3+3NaClO+4NaOH=2Na2FeO4+3NaCl+5H2O。
①该反应的氧化产物是
②用双线桥法标出该反应电子转移的方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有以下化学方程式,按要求回答下列问题:
A.
B.
C.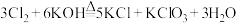
D.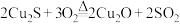
E.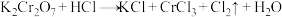 (未配平)
(未配平)
(1)A反应中被氧化的元素是_____ (填元素符号),还原产物是_____ (填化学式)。
(2)B反应中氧化产物与还原产物的质量比为_____ 。
(3)C反应中有3个氯气分子发生反应时,转移电子的数目是_____ 。
(4)用单线桥标出D反应中电子转移的方向和数目_____ 。
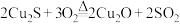
(5)配平E并用双线桥法标出下列反应的电子转移情况:_____ 。

A.

B.

C.
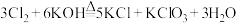
D.
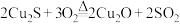
E.
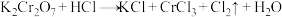 (未配平)
(未配平)(1)A反应中被氧化的元素是
(2)B反应中氧化产物与还原产物的质量比为
(3)C反应中有3个氯气分子发生反应时,转移电子的数目是
(4)用单线桥标出D反应中电子转移的方向和数目
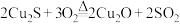
(5)配平E并用双线桥法标出下列反应的电子转移情况:

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题
(1)平常我们食用的水果中含有丰富的维生素C,维生素C又被称为“抗坏血酸”,在人体内有重要的功能,例如,能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有___________ (填“氧化性”或“还原性”)。
(2)工业废水中含有的重铬酸根离子(Cr2O )有毒,必需处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)做处理剂,反应的离子方程式如下:6Fe2+ + Cr2O
)有毒,必需处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)做处理剂,反应的离子方程式如下:6Fe2+ + Cr2O + 14H+ = 6Fe3+ + 2Cr3+ + 7H2O,在该反应中,还原剂是
+ 14H+ = 6Fe3+ + 2Cr3+ + 7H2O,在该反应中,还原剂是___________ (填离子符号,下同),氧化剂是___________ 。
(3)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为:S + 2KNO3 + 3C = K2S + N2↑+ 3CO2↑,在该反应中,还原剂是___________ (填化学式,下同),氧化剂是___________ 。
(4)在明代宋应星所著的《天工开物》中,有关火法炼锌的工艺记载:“每炉甘石十斤,装载入一泥罐内,……然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,罐中炉甘石烙化成团。冷定毁罐取出。……即倭铅也。……以其似铅而性猛,故名之曰‘倭’云。”(注:炉甘石的主要成分是碳酸锌。)
①请完成上述火法炼锌反应的化学方程式:________
ZnCO3 +___________ = ___________ +___________ CO↑。
②在该反应中,还原剂是___________ (填化学式,下同),被还原的是___________ 。
(1)平常我们食用的水果中含有丰富的维生素C,维生素C又被称为“抗坏血酸”,在人体内有重要的功能,例如,能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有
(2)工业废水中含有的重铬酸根离子(Cr2O
 )有毒,必需处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)做处理剂,反应的离子方程式如下:6Fe2+ + Cr2O
)有毒,必需处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)做处理剂,反应的离子方程式如下:6Fe2+ + Cr2O + 14H+ = 6Fe3+ + 2Cr3+ + 7H2O,在该反应中,还原剂是
+ 14H+ = 6Fe3+ + 2Cr3+ + 7H2O,在该反应中,还原剂是(3)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为:S + 2KNO3 + 3C = K2S + N2↑+ 3CO2↑,在该反应中,还原剂是
(4)在明代宋应星所著的《天工开物》中,有关火法炼锌的工艺记载:“每炉甘石十斤,装载入一泥罐内,……然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,罐中炉甘石烙化成团。冷定毁罐取出。……即倭铅也。……以其似铅而性猛,故名之曰‘倭’云。”(注:炉甘石的主要成分是碳酸锌。)
①请完成上述火法炼锌反应的化学方程式:
ZnCO3 +___________ = ___________ +___________ CO↑。
②在该反应中,还原剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】氧化还原反应是一类非常重要的反应。回答下列问题:
(1)按如图所示操作,充分反应后:

①I中反应的离子方程式 为_______ ;
②II中充分反应后溶液的质量_______ (选填“增加”、“不变”或者“减少”);
③结合I、II验现象可知Fe2+、Cu2+、Ag+的氧化性由强到弱的顺序为_______ 。
(2)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲。黑火药在发生爆炸时,发生如下反应:2KNO3+3C+S=K2S+N2↑+3CO2↑。该反应的氧化产物是_______ ;
(3)高锰酸钾固体常温下即可与浓盐酸反应,此反应也可用于实验室制取氯气:KMnO4+HCl(浓)=Cl2↑+MnCl2+KCl+_____,请补充完整短线上的物质并配平该方程式______ 。
(1)按如图所示操作,充分反应后:

①I中反应的
②II中充分反应后溶液的质量
③结合I、II验现象可知Fe2+、Cu2+、Ag+的氧化性由强到弱的顺序为
(2)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲。黑火药在发生爆炸时,发生如下反应:2KNO3+3C+S=K2S+N2↑+3CO2↑。该反应的氧化产物是
(3)高锰酸钾固体常温下即可与浓盐酸反应,此反应也可用于实验室制取氯气:KMnO4+HCl(浓)=Cl2↑+MnCl2+KCl+_____,请补充完整短线上的物质并配平该方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)X、Y、Z三种物质存在如图所示转化关系。
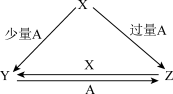
回答下列问题:
①若X为黑色固体单质,A为O2,写出Z→Y的化学方程式:___ 。
②若X为NaOH溶液,则写出Y→Z的离子方程式:___ 。
(2)已知常温下在溶液中可发生如下两个反应:
Ce4++Fe2+=Fe3++Ce3+
Sn2++2Fe3+=2Fe2++Sn4+
由此可以确定Ce4+、Sn4+、Fe3+三种离子的氧化性由强到弱的顺序是___ 。
(3)Mn2+、Bi3+、BiO 、MnO
、MnO 、H+、H2O组成的一个氧化还原反应体系中,发生BiO
、H+、H2O组成的一个氧化还原反应体系中,发生BiO →Bi3+的反应过程。
→Bi3+的反应过程。
①该反应中,被氧化的元素是___ (填元素符号),氧化剂是___ (填化学式)。
②将以上物质分别填入下面对应的横线上,组成一个未配平的化学方程式:______+______+______→______+______+H2O。___
(4)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图所示。
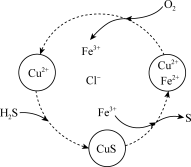
①写出CuCl2与H2S反应的离子方程式:___ 。
②通过上述流程图的分析,整个流程的总反应为___ 。
(1)X、Y、Z三种物质存在如图所示转化关系。

回答下列问题:
①若X为黑色固体单质,A为O2,写出Z→Y的化学方程式:
②若X为NaOH溶液,则写出Y→Z的离子方程式:
(2)已知常温下在溶液中可发生如下两个反应:
Ce4++Fe2+=Fe3++Ce3+
Sn2++2Fe3+=2Fe2++Sn4+
由此可以确定Ce4+、Sn4+、Fe3+三种离子的氧化性由强到弱的顺序是
(3)Mn2+、Bi3+、BiO
 、MnO
、MnO 、H+、H2O组成的一个氧化还原反应体系中,发生BiO
、H+、H2O组成的一个氧化还原反应体系中,发生BiO →Bi3+的反应过程。
→Bi3+的反应过程。①该反应中,被氧化的元素是
②将以上物质分别填入下面对应的横线上,组成一个未配平的化学方程式:______+______+______→______+______+H2O。
(4)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图所示。

①写出CuCl2与H2S反应的离子方程式:
②通过上述流程图的分析,整个流程的总反应为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】I.自门捷列夫发现元素周期律以来,人类对自然的认识程度逐步加深,元素周期表中的成员数目不断增加。回答下列问题:
(1)2016年IUPAC确认了四种新元素,其中一种为 ,中文为“镆”。元素
,中文为“镆”。元素 可由反应
可由反应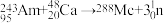 得到。该元素的质子数为
得到。该元素的质子数为_____ ,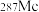 与
与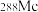 互为
互为_____ 。
II.如图是元素周期表的一部分,其中每个字母代表对应的一种元素。
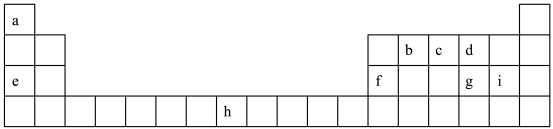
请按要求回答下列问题:
(2)写出d与e按1∶1的原子个数比形成的化合物与水反应的离子方程式:_______ ,g的离子结构示意图为_______ 。 的性质与
的性质与 相似,
相似, 与e的最高价氧化物水化物的水溶液反应的离子方程式为
与e的最高价氧化物水化物的水溶液反应的离子方程式为________ 。
(3)h在周期表中的位置为________ ,与e同主族第六周期的元素的某一核素中子数为82,该核素符号是_________ ,
(4)由以上某些元素构成A→G八种物质,常见金属单质A可发生如图所示转化(部分反应物、产物和反应条件已略去)。F是一种温室气体;气体G的水溶液显弱碱性;H是一种具有磁性的黑色氧化物;B、C、D、E四种化合物中含有一种相同的元素。
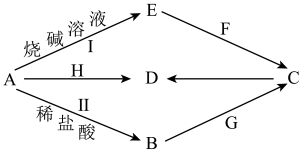
请回答下列问题:
①B与过量G的水溶液反应的化学方程式为___________ 。
②写出反应I的离子方程式___________ 。该反应中的氧化剂是___________ 。
③资料显示H可用于除去地下水中的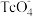 (
(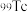 具有放射性)。在酸性条件下,H将
具有放射性)。在酸性条件下,H将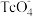 转化为难溶于水的
转化为难溶于水的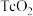 ,同时得到一种难溶于水的弱碱,该反应的离子方程式为
,同时得到一种难溶于水的弱碱,该反应的离子方程式为___________ 。
(1)2016年IUPAC确认了四种新元素,其中一种为
 ,中文为“镆”。元素
,中文为“镆”。元素 可由反应
可由反应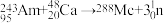 得到。该元素的质子数为
得到。该元素的质子数为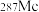 与
与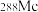 互为
互为II.如图是元素周期表的一部分,其中每个字母代表对应的一种元素。

请按要求回答下列问题:
(2)写出d与e按1∶1的原子个数比形成的化合物与水反应的离子方程式:
 的性质与
的性质与 相似,
相似, 与e的最高价氧化物水化物的水溶液反应的离子方程式为
与e的最高价氧化物水化物的水溶液反应的离子方程式为(3)h在周期表中的位置为
(4)由以上某些元素构成A→G八种物质,常见金属单质A可发生如图所示转化(部分反应物、产物和反应条件已略去)。F是一种温室气体;气体G的水溶液显弱碱性;H是一种具有磁性的黑色氧化物;B、C、D、E四种化合物中含有一种相同的元素。

请回答下列问题:
①B与过量G的水溶液反应的化学方程式为
②写出反应I的离子方程式
③资料显示H可用于除去地下水中的
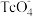 (
(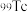 具有放射性)。在酸性条件下,H将
具有放射性)。在酸性条件下,H将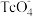 转化为难溶于水的
转化为难溶于水的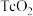 ,同时得到一种难溶于水的弱碱,该反应的离子方程式为
,同时得到一种难溶于水的弱碱,该反应的离子方程式为
您最近一年使用:0次
【推荐1】I、氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:NO3-+4H++3e→NO+2H2O
KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)写出并配平该氧化还原反应的方程式:_____________________________________________________
(2)反应中若产生0.2mol气体,则转移电子的物质的量是____________ mol。
(3)若1mol甲与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是:________________________________________________________ 。
Ⅱ、某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2;已知该反应中H2O2只发生如下过程:H2O2→ O2
(1)该反应中的还原剂是_____________ 。
(2)写出该反应的化学方程式________________________________________________________________________ 。
(3)如反应转移了0.3mol电子,则产生的气体在标准状况下体积为________________ 。
KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)写出并配平该氧化还原反应的方程式:
(2)反应中若产生0.2mol气体,则转移电子的物质的量是
(3)若1mol甲与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是:
Ⅱ、某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2;已知该反应中H2O2只发生如下过程:H2O2→ O2
(1)该反应中的还原剂是
(2)写出该反应的化学方程式
(3)如反应转移了0.3mol电子,则产生的气体在标准状况下体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】海水是人类重要的资源宝库。海水综合开发利用的部分过程如下:

回答下列问题:
(1)从海水中提取粗盐的操作名称为______ 。
(2)向苦卤中通入 是为了提取溴,发生反应的离子方程式为
是为了提取溴,发生反应的离子方程式为____________ ,富集溴一般先用热空气和水蒸气吹出单质溴,这是利用单质溴的______ (填“挥发性”或“密度比空气大”),再用纯减溶液吸收溴,主要反应是 (未配平),若吸收
(未配平),若吸收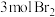 时,该反应中转移的电子的物质的量为
时,该反应中转移的电子的物质的量为____________ 。
(3)工业生产中沉淀 所用沉淀剂为
所用沉淀剂为______ (填化学式),电解熔融 制备Mg的化学方程式为
制备Mg的化学方程式为____________ 。

回答下列问题:
(1)从海水中提取粗盐的操作名称为
(2)向苦卤中通入
 是为了提取溴,发生反应的离子方程式为
是为了提取溴,发生反应的离子方程式为 (未配平),若吸收
(未配平),若吸收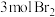 时,该反应中转移的电子的物质的量为
时,该反应中转移的电子的物质的量为(3)工业生产中沉淀
 所用沉淀剂为
所用沉淀剂为 制备Mg的化学方程式为
制备Mg的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】FeSO4可用于制备一种新型、高效、多功能绿色水处理剂高铁酸钾(K2FeO4),氧化性比Cl2、O2、ClO2、KMnO4更强,主要反应:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑。
(1)该反应中的还原剂是__ 。
(2)人体正常的血红蛋白含有Fe2+,若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是___ (填字母)。
A.亚硝酸盐被氧化
B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+
D.亚硝酸盐是还原剂
(1)该反应中的还原剂是
(2)人体正常的血红蛋白含有Fe2+,若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是
A.亚硝酸盐被氧化
B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+
D.亚硝酸盐是还原剂
您最近一年使用:0次



