双氧水、84消毒液、高铁酸钠是生活中常用的消毒剂,请回答下列问题:
(1)某同学设计如表实验研究H2O2的性质
已知:I2遇淀粉溶液变蓝
①从化合价改变上看H2O2,既有氧化性又有还原性,具有还原性的原因是_______ 。
②能证明H2O2具有氧化性的实验是________ (填序号“i”或“ii”)。
(2)2016年巴西奥运会期间,由于工作人员将84消毒液(有效成分为NaClO)与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是NaClO与H2O2反应产生O2促进藻类快速生长。
已知:NaClO具有强氧化性,易被还原为NaCl
①该反应说明氧化性:NaClO________ O2(填“>”或“<”)。
②当有3个氧气分子生成时,转移________ 个电子。
(3)湿法制备Na2FeO4,反应为:2Fe(OH)3+3NaClO+4NaOH=2Na2FeO4+3NaCl+5H2O。
①该反应的氧化产物是________ 。
②用双线桥法标出该反应电子转移的方向和数目______ 。
(1)某同学设计如表实验研究H2O2的性质
| 序号 | 实验 | 实验现象 |
| i | 向5%H2O2溶液中滴加酸性KMnO4溶液 | a.溶液紫色褪去 b.有大量气泡产生 |
| ii | 向5%H2O2溶液中滴加淀粉碘化钾溶液 | c.溶液变蓝 |
①从化合价改变上看H2O2,既有氧化性又有还原性,具有还原性的原因是
②能证明H2O2具有氧化性的实验是
(2)2016年巴西奥运会期间,由于工作人员将84消毒液(有效成分为NaClO)与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是NaClO与H2O2反应产生O2促进藻类快速生长。
已知:NaClO具有强氧化性,易被还原为NaCl
①该反应说明氧化性:NaClO
②当有3个氧气分子生成时,转移
(3)湿法制备Na2FeO4,反应为:2Fe(OH)3+3NaClO+4NaOH=2Na2FeO4+3NaCl+5H2O。
①该反应的氧化产物是
②用双线桥法标出该反应电子转移的方向和数目
更新时间:2023-10-05 00:27:04
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】氮及其化合物与生产生活关系密切。请完成下列填空:
(1)肼由N、H 两种元素组成,它常用作火箭推进剂。肼的相对分子质量为32,分子中N、H原子的个数比为1:2。肼的分子式为_____________ 。1mol 的肼分子中含有的电子总数为______ NA(NA为阿伏伽德罗常数的值)。16g 肼分子中所含的氮原子数与标准状况下_______ LN2中所含的氮原子数相等。
(2)在相同温度和压强下,体积相同的两个容器中分别盛有N2和O2。下列说法不正确的是____ (填序号)。
A. N2和O2的密度之比为7:8 B.两容器内的气体具有相同的分子数
C.两容器内的气体具有相同的原子数 D.两容器内的气体具有相同的质子数
(3)工业上用N2和O2在一定条件下合成NH3。该反应的化学方程式为N2(g)+3H2(g) 2NH3(g)。下列关于该反应的说法正确的是
2NH3(g)。下列关于该反应的说法正确的是____________ 。(填序号)。
A.1mol NH3中含有10mole-
B.反应中每消耗1molN2失去6 mole-
C.反应中消耗N2和生成NH3的物质的量之比为14 :17
D.相同温度和压强下,消耗N2、消耗H2、生成NH3的体积比为1: 3 :2
(1)肼由N、H 两种元素组成,它常用作火箭推进剂。肼的相对分子质量为32,分子中N、H原子的个数比为1:2。肼的分子式为
(2)在相同温度和压强下,体积相同的两个容器中分别盛有N2和O2。下列说法不正确的是
A. N2和O2的密度之比为7:8 B.两容器内的气体具有相同的分子数
C.两容器内的气体具有相同的原子数 D.两容器内的气体具有相同的质子数
(3)工业上用N2和O2在一定条件下合成NH3。该反应的化学方程式为N2(g)+3H2(g)
 2NH3(g)。下列关于该反应的说法正确的是
2NH3(g)。下列关于该反应的说法正确的是A.1mol NH3中含有10mole-
B.反应中每消耗1molN2失去6 mole-
C.反应中消耗N2和生成NH3的物质的量之比为14 :17
D.相同温度和压强下,消耗N2、消耗H2、生成NH3的体积比为1: 3 :2
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】高铁酸钾是一种非氯高效消毒剂,主要用于饮用水处理。高铁酸钾( )在强碱性条件下能够稳定存在。工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入饱和的KOH溶液,使高铁酸钾析出。
)在强碱性条件下能够稳定存在。工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入饱和的KOH溶液,使高铁酸钾析出。
(1)方法一:可利用固体反应物反应: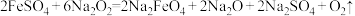 ,该反应中的氧化剂是
,该反应中的氧化剂是___________ ,消耗117 g  转移
转移___________ mol电子。
(2)方法二:反应: (未配平)
(未配平)
①配平离子反应方程式:_______ ____ _____
_____ ______
______ _____
_____ _______
_______ ______
______
②若反应过程中转移了1.5 mol电子,则还原产物的物质的量为______ mol。
(3)向 溶液中加入适量饱和的KOH溶液,有
溶液中加入适量饱和的KOH溶液,有 析出,请写出该反应的离子方程式:
析出,请写出该反应的离子方程式:___________ 。
 )在强碱性条件下能够稳定存在。工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入饱和的KOH溶液,使高铁酸钾析出。
)在强碱性条件下能够稳定存在。工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入饱和的KOH溶液,使高铁酸钾析出。(1)方法一:可利用固体反应物反应:
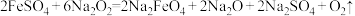 ,该反应中的氧化剂是
,该反应中的氧化剂是 转移
转移(2)方法二:反应:
 (未配平)
(未配平)①配平离子反应方程式:
 _____
_____ ______
______ _____
_____ _______
_______ ______
______
②若反应过程中转移了1.5 mol电子,则还原产物的物质的量为
(3)向
 溶液中加入适量饱和的KOH溶液,有
溶液中加入适量饱和的KOH溶液,有 析出,请写出该反应的离子方程式:
析出,请写出该反应的离子方程式:
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)已知2KMnO4+16HCl==2KCl+2MnCl2+5Cl2↑+8H2O,该反应中,氧化剂是_______ ,氧化产物是_____ 。若生成氯气11.2L(标准状况),则转移电子的物质的量为_____ mol。
(2)配置0.2mol/L的NaCl溶液450mL, 需要用到的仪器有托盘天平(含砝码)、药匙、烧杯、玻璃棒、_____________ 和_________ ,需要用托盘天平称取NaCl__________ g。
(3)漂白粉的有效成分是_______________
(4)已知每1 克氢气完全燃烧生成水蒸气时将放出121kJ热量,写出该反应的热化学方程式___________________________________________
(2)配置0.2mol/L的NaCl溶液450mL, 需要用到的仪器有托盘天平(含砝码)、药匙、烧杯、玻璃棒、
(3)漂白粉的有效成分是
(4)已知每1 克氢气完全燃烧生成水蒸气时将放出121kJ热量,写出该反应的热化学方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】阅读下列科普短文并填空:
海洋约占地球表面积的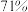 ,其中水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如
,其中水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如 、
、 等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和
等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和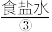 用以生产
用以生产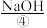 、
、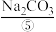 、
、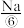 、
、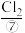 、
、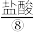 等,苦卤经过氯气氧化,热空气吹出、
等,苦卤经过氯气氧化,热空气吹出、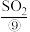 吸收等一系列操作可获得
吸收等一系列操作可获得 。海水淡化与化工生产、能源开发等相结合已经成为海水综合利用的重要方向。
。海水淡化与化工生产、能源开发等相结合已经成为海水综合利用的重要方向。
(1)上述标有序号的物质中属于电解质的是___________ (填序号,下同);属于非电解质的是___________ ;能导电的物质是___________ 。
(2)写出⑤溶于水的电离方程式:___________ 。将少量的⑤溶于装有 蒸馏水的烧杯中后,逐滴加入⑧观察到刚开始并没有出现气泡,一段时间后出现气泡,则出现该现象的原因是
蒸馏水的烧杯中后,逐滴加入⑧观察到刚开始并没有出现气泡,一段时间后出现气泡,则出现该现象的原因是___________ ,写出对应反应的离子方程式:______ ,______ 。
(3)海水提溴的过程中涉及的反应有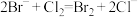 ,
, ,根据上述反应可判断
,根据上述反应可判断 、
、 、
、 的还原性由强到弱的顺序为
的还原性由强到弱的顺序为___________ 。
海洋约占地球表面积的
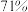 ,其中水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如
,其中水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如 、
、 等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和
等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和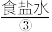 用以生产
用以生产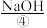 、
、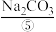 、
、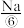 、
、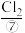 、
、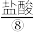 等,苦卤经过氯气氧化,热空气吹出、
等,苦卤经过氯气氧化,热空气吹出、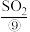 吸收等一系列操作可获得
吸收等一系列操作可获得 。海水淡化与化工生产、能源开发等相结合已经成为海水综合利用的重要方向。
。海水淡化与化工生产、能源开发等相结合已经成为海水综合利用的重要方向。(1)上述标有序号的物质中属于电解质的是
(2)写出⑤溶于水的电离方程式:
 蒸馏水的烧杯中后,逐滴加入⑧观察到刚开始并没有出现气泡,一段时间后出现气泡,则出现该现象的原因是
蒸馏水的烧杯中后,逐滴加入⑧观察到刚开始并没有出现气泡,一段时间后出现气泡,则出现该现象的原因是(3)海水提溴的过程中涉及的反应有
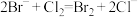 ,
, ,根据上述反应可判断
,根据上述反应可判断 、
、 、
、 的还原性由强到弱的顺序为
的还原性由强到弱的顺序为
您最近半年使用:0次
【推荐2】某一反应体系中的物质有:HCl、SnCl2、H2SnCl6、As、H3AsO3、H2O,
已知:As是产物之一。
(1)写出并配平该反应的化学方程式______________
(2)在反应中,每转移1 mol电子,消耗(或生成)HCl_______ mol;
(3)下列叙述正确的是_____________ (填写序号)。
a.在相同条件下,第VIIA族元素的阴离子的还原性从上到下逐渐增强
b.Sn和Pb位于同一主族,其+4价的化合物均很稳定
c.在相同条件下,还原性顺序:S2->I->Fe2+>Br->Cl-
d.在上述反应中,氧化性:SnCl2 >As,还原性:H3AsO3>H2SnCl6
已知:As是产物之一。
(1)写出并配平该反应的化学方程式
(2)在反应中,每转移1 mol电子,消耗(或生成)HCl
(3)下列叙述正确的是
a.在相同条件下,第VIIA族元素的阴离子的还原性从上到下逐渐增强
b.Sn和Pb位于同一主族,其+4价的化合物均很稳定
c.在相同条件下,还原性顺序:S2->I->Fe2+>Br->Cl-
d.在上述反应中,氧化性:SnCl2 >As,还原性:H3AsO3>H2SnCl6
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】氧化还原反应在生产、生活和生命活动中起着十分重要的作用.例如,饮用水处理和污水净化问题中就广泛应用了氧化还原反应的原理.
Ⅰ.高铁酸钠 是一种新型绿色消毒剂,主要用于饮用水处理.工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用化学方程式表示为:
是一种新型绿色消毒剂,主要用于饮用水处理.工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用化学方程式表示为:
(1)在 中,
中, 的化合价为
的化合价为___________ 价;上述反应中,每生成 ,有
,有___________  电子转移.
电子转移.
(2)制备 的另外一种方法是在碱性条件下用
的另外一种方法是在碱性条件下用 和
和 反应,请配平下列离子方程式:
反应,请配平下列离子方程式:_____
__ ____
____ _____
_____ ____
____ _____
_____ _____
_____
Ⅱ.含氯消毒剂在自来水净化过程中也起到了重要作用.
(3)很多自来水厂用氯气来杀菌、消毒,实验室不能用自来水配制硝酸银溶液,用离子方程式表示其原因___________ .实验室常用浓盐酸与二氧化锰反应来制取 ,请写出反应的化学方程式
,请写出反应的化学方程式___________ .
(4)亚氯酸钠 是一种高效的漂白剂和氧化剂,其制备方法如下:
是一种高效的漂白剂和氧化剂,其制备方法如下: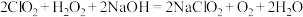
根据氧化剂的氧化性强于氧化产物这一规律,从上述反应中可知氧化性_________ >__________;
(5)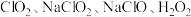 都常被用作消毒剂,上述物质消毒效率最高的是___________(填序号).(已知:消毒效率是以单位物质的量的物质得电子的数目多少表示,得电子越多效率越高)
都常被用作消毒剂,上述物质消毒效率最高的是___________(填序号).(已知:消毒效率是以单位物质的量的物质得电子的数目多少表示,得电子越多效率越高)
Ⅰ.高铁酸钠
 是一种新型绿色消毒剂,主要用于饮用水处理.工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用化学方程式表示为:
是一种新型绿色消毒剂,主要用于饮用水处理.工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用化学方程式表示为:
(1)在
 中,
中, 的化合价为
的化合价为 ,有
,有 电子转移.
电子转移.(2)制备
 的另外一种方法是在碱性条件下用
的另外一种方法是在碱性条件下用 和
和 反应,请配平下列离子方程式:
反应,请配平下列离子方程式:__
 ____
____ _____
_____ ____
____ _____
_____ _____
_____
Ⅱ.含氯消毒剂在自来水净化过程中也起到了重要作用.
(3)很多自来水厂用氯气来杀菌、消毒,实验室不能用自来水配制硝酸银溶液,用离子方程式表示其原因
 ,请写出反应的化学方程式
,请写出反应的化学方程式(4)亚氯酸钠
 是一种高效的漂白剂和氧化剂,其制备方法如下:
是一种高效的漂白剂和氧化剂,其制备方法如下: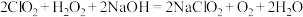
根据氧化剂的氧化性强于氧化产物这一规律,从上述反应中可知氧化性
(5)
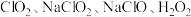 都常被用作消毒剂,上述物质消毒效率最高的是___________(填序号).(已知:消毒效率是以单位物质的量的物质得电子的数目多少表示,得电子越多效率越高)
都常被用作消毒剂,上述物质消毒效率最高的是___________(填序号).(已知:消毒效率是以单位物质的量的物质得电子的数目多少表示,得电子越多效率越高)A. | B. | C. | D. |
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】高铁酸钠( )(铁元素为+6价)是一种新型的净水剂,可以通过下述反应制取:
)(铁元素为+6价)是一种新型的净水剂,可以通过下述反应制取:
(1)配平下列化学方程式,并用单线桥法标明电子转移的方向与数目:___________ 。
 ______
______ ______
______ ______
______ ______
______ _______
_______
(2)该反应中氧化剂是___________ ,___________ 元素被氧化,还原产物为___________ 。
(3)当反应中有1mol高铁酸钠生成,转移的电子数为___________ 。
(4)欲配制250mL0.1 NaOH溶液,需用电子天平称取
NaOH溶液,需用电子天平称取___________ gNaOH固体,所需的玻璃仪器有___________ 、___________ 、___________ 、___________ 。
 )(铁元素为+6价)是一种新型的净水剂,可以通过下述反应制取:
)(铁元素为+6价)是一种新型的净水剂,可以通过下述反应制取:(1)配平下列化学方程式,并用单线桥法标明电子转移的方向与数目:
 ______
______ ______
______ ______
______ ______
______ _______
_______
(2)该反应中氧化剂是
(3)当反应中有1mol高铁酸钠生成,转移的电子数为
(4)欲配制250mL0.1
 NaOH溶液,需用电子天平称取
NaOH溶液,需用电子天平称取
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】黄铁矿[主要成分为二硫化亚铁(FeS2)]、焦炭和适量空气混合加热发生如下反应:
i.3FeS2+2C+3O2=3S2+Fe3O4+2CO
(1)反应i生成1molS2时,转移电子的物质的量为___________ mol。
(2)反应i所得气体经冷凝回收S2后,尾气中还含有CO和SO2.将尾气通过催化剂进行处理,发生反应ii,同时发生副反应iii。
ii.2SO2(g)+4CO(g) S2(g)+4CO2(g) ΔH<0
S2(g)+4CO2(g) ΔH<0
iii.SO2(g)+3CO(g) COS(g)+2CO2(g) ΔH<0
COS(g)+2CO2(g) ΔH<0
理论分析及实验结果表明,600~1000K范围内,SO2平衡转化率接近100%。其他条件相同,不同温度下,S2、COS平衡产率和10min时S2实际产率如图。___________ 。
②随温度升高,S2平衡产率上升,推测其原因是___________ 。
③900K,在10min后继续反应足够长时间,推测S2实际产率的变化趋势可能为___________ 。
i.3FeS2+2C+3O2=3S2+Fe3O4+2CO
(1)反应i生成1molS2时,转移电子的物质的量为
(2)反应i所得气体经冷凝回收S2后,尾气中还含有CO和SO2.将尾气通过催化剂进行处理,发生反应ii,同时发生副反应iii。
ii.2SO2(g)+4CO(g)
 S2(g)+4CO2(g) ΔH<0
S2(g)+4CO2(g) ΔH<0iii.SO2(g)+3CO(g)
 COS(g)+2CO2(g) ΔH<0
COS(g)+2CO2(g) ΔH<0理论分析及实验结果表明,600~1000K范围内,SO2平衡转化率接近100%。其他条件相同,不同温度下,S2、COS平衡产率和10min时S2实际产率如图。
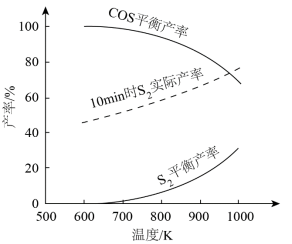
②随温度升高,S2平衡产率上升,推测其原因是
③900K,在10min后继续反应足够长时间,推测S2实际产率的变化趋势可能为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】铁及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为:
3FeS2+8O2 6SO2+Fe3O4,若3 mol FeS2参加反应转移
6SO2+Fe3O4,若3 mol FeS2参加反应转移_______ mol电子。
(2)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为____________________________ ;腐蚀废液回收得到金属铜还需要的试剂为____________ 。
(3)与明矾相似,硫酸铁也可用作絮凝剂,在使用时发现硫酸铁并不能使酸性废水中的悬浮物沉降除去,其原因是_____________________________________ 。
(4)下表中,对陈述I、Ⅱ及其有无因果关系的判断,都正确的是_____ (填字母)
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为:
3FeS2+8O2
 6SO2+Fe3O4,若3 mol FeS2参加反应转移
6SO2+Fe3O4,若3 mol FeS2参加反应转移(2)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为
(3)与明矾相似,硫酸铁也可用作絮凝剂,在使用时发现硫酸铁并不能使酸性废水中的悬浮物沉降除去,其原因是
(4)下表中,对陈述I、Ⅱ及其有无因果关系的判断,都正确的是
| 选项 | 陈述I | 陈述Ⅱ | 判断 |
| A | 铁是地壳中含量最高的金属元素 | 铁是人类最早使用的金属材料 | I对;Ⅱ对;有 |
| B | 常温下铁与稀硫酸反应生成氢气 | 高温下氢气能还原氧化铁生成铁 | I对;Ⅱ对;无 |
| C | 铁属于过渡金属元素 | 铁和铁的某些化合物可以用作催化剂 | I错;Ⅱ对;无 |
| D | 铁在空气中表面生成致密氧化膜 | 可用铁罐储存运输浓硫酸、浓硝酸 | I对;Ⅱ对;有 |
您最近半年使用:0次



