铁及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为:
3FeS2+8O2 6SO2+Fe3O4,若3 mol FeS2参加反应转移
6SO2+Fe3O4,若3 mol FeS2参加反应转移_______ mol电子。
(2)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为____________________________ ;腐蚀废液回收得到金属铜还需要的试剂为____________ 。
(3)与明矾相似,硫酸铁也可用作絮凝剂,在使用时发现硫酸铁并不能使酸性废水中的悬浮物沉降除去,其原因是_____________________________________ 。
(4)下表中,对陈述I、Ⅱ及其有无因果关系的判断,都正确的是_____ (填字母)
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为:
3FeS2+8O2
 6SO2+Fe3O4,若3 mol FeS2参加反应转移
6SO2+Fe3O4,若3 mol FeS2参加反应转移(2)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为
(3)与明矾相似,硫酸铁也可用作絮凝剂,在使用时发现硫酸铁并不能使酸性废水中的悬浮物沉降除去,其原因是
(4)下表中,对陈述I、Ⅱ及其有无因果关系的判断,都正确的是
| 选项 | 陈述I | 陈述Ⅱ | 判断 |
| A | 铁是地壳中含量最高的金属元素 | 铁是人类最早使用的金属材料 | I对;Ⅱ对;有 |
| B | 常温下铁与稀硫酸反应生成氢气 | 高温下氢气能还原氧化铁生成铁 | I对;Ⅱ对;无 |
| C | 铁属于过渡金属元素 | 铁和铁的某些化合物可以用作催化剂 | I错;Ⅱ对;无 |
| D | 铁在空气中表面生成致密氧化膜 | 可用铁罐储存运输浓硫酸、浓硝酸 | I对;Ⅱ对;有 |
更新时间:2016-12-09 07:18:45
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】化学实验室产生的废液中含有大量会污染环境的物质,为了保护环境,这些废液必须经处理后才能排放。某化学实验室产生的废液中含有两种金属离子:Fe3+、Cu2+,化学小组设计了如下图所示的方案对废液进行处理,以回收金属,保护环境。

(1)操作①的名称是_______ 。
(2)沉淀A中含有的金属单质有_______ 。
(3)操作②中观察到的实验现象是_______ 。
(4)操作③中发生反应的离子方程式为_______ 。

(1)操作①的名称是
(2)沉淀A中含有的金属单质有
(3)操作②中观察到的实验现象是
(4)操作③中发生反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】“佛立苏”是一种常见补血剂,主要成分为FeSO4;FeSO4·7H2O俗称“绿矾”,在工业生产和日常生活中都有广泛的用途,回答下列问题:
(1)人体正常的血红蛋白含有Fe2+,若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是______ (填字母)。
A.亚硝酸盐被还原B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+D.亚硝酸盐是还原剂
(2)已知Fe(OH)2是一种白色沉淀,极易被空气中的氧气氧化,反应的化学方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3(红褐色沉淀),用双线桥法表示转移电子数和氧化还原反应______ 。
向FeSO4溶液中加入一小块金属钠,发现开始有气体和白色沉淀产生,过一段时间,白色沉淀变为红褐色,写出上述反应中涉及到的离子方程式________________________________ 。
(3)FeSO4可用于制备一种新型、高效、多功能绿色水处理剂高铁酸钾(K2FeO4),氧化性比Cl2、O2、ClO2、KMnO4更强,主要反应:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑。
①上述反应中作还原剂的是______ (填化学式)。
②简要说明K2FeO4作为水处理剂时所起的作用____________ (写出一点即可)。
(4)将Na2O2固体加入酚酞溶液中产生的现象是_______ 。写出该反应的离子方程式______ 。
(1)人体正常的血红蛋白含有Fe2+,若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是
A.亚硝酸盐被还原B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+D.亚硝酸盐是还原剂
(2)已知Fe(OH)2是一种白色沉淀,极易被空气中的氧气氧化,反应的化学方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3(红褐色沉淀),用双线桥法表示转移电子数和氧化还原反应
向FeSO4溶液中加入一小块金属钠,发现开始有气体和白色沉淀产生,过一段时间,白色沉淀变为红褐色,写出上述反应中涉及到的离子方程式
(3)FeSO4可用于制备一种新型、高效、多功能绿色水处理剂高铁酸钾(K2FeO4),氧化性比Cl2、O2、ClO2、KMnO4更强,主要反应:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑。
①上述反应中作还原剂的是
②简要说明K2FeO4作为水处理剂时所起的作用
(4)将Na2O2固体加入酚酞溶液中产生的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】有人认为,向 溶液中加入少量冰醋酸,冰醋酸会与
溶液中加入少量冰醋酸,冰醋酸会与 溶液水解产生的
溶液水解产生的 反应,使平衡向水解方向移动,这种说法对吗?为什么
反应,使平衡向水解方向移动,这种说法对吗?为什么_______ 。
 溶液中加入少量冰醋酸,冰醋酸会与
溶液中加入少量冰醋酸,冰醋酸会与 溶液水解产生的
溶液水解产生的 反应,使平衡向水解方向移动,这种说法对吗?为什么
反应,使平衡向水解方向移动,这种说法对吗?为什么
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
请回答:
(1)从①组情况分析,HA是强酸还是弱酸?____________ (填“强酸”或“弱酸”)。
(2)②组情况表明,c____________ 0.2mol/L(选填“大于”、“小于”或“等于”)。混合液中离子浓度c(A-)与c(Na+)的大小关系是____________ 。
(3)从③组实验结果分析,说明HA的电离程度____________ NaA的水解程度(选填“大于”、“小于”或“等于”),该混合溶液中离子浓度由大到小的顺序是____________ 。
(4)①组实验所得混合溶液中由水电离出的c(OH-)=____________ mol/L。
| 实验编号 | HA物质的量浓度(mol/L) | NaOH物质的量浓度(mol/L) | 混合溶液的pH |
| ① | 0.1 | 0.1 | pH=9 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.2 | 0.1 | pH<7 |
(1)从①组情况分析,HA是强酸还是弱酸?
(2)②组情况表明,c
(3)从③组实验结果分析,说明HA的电离程度
(4)①组实验所得混合溶液中由水电离出的c(OH-)=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】去除水体中砷的技术主要有物理吸附法及化学氧化法。
(1)物理吸附法
用活性炭负载纳米二氧化钛吸附水中的砷,纳米二氧化钛投加量对活性炭去除砷效果如图1所示:

①纳米二氧化钛投加量为____ 时,砷的吸附量可达最大。
②未加二氧化钛时就有一定的吸附砷的能力,可能的原因是____ 。
③若要提高废水中As(III)的去除率,可采取的措施___ 。
(2)化学氧化法
该方法须将废水中的As(III)用空气或铁离子氧化为As(V),然后再去除,为了探究As(III)被哪种氧化剂氧化,设计如下实验:取含As(III)废水,在pH分别为1~10条件下反应1h后,过滤,测定滤液中三价铁和二价铁的含量,得出不同pH下三价铁和二价铁的浓度随pH变化如图2所示:

①pH在3~4时Fe3+浓度变化的主要原因为____ 。
②由实验可知废水中的As(III)主要被___ 氧化为As(V),理由为___ 。
(1)物理吸附法
用活性炭负载纳米二氧化钛吸附水中的砷,纳米二氧化钛投加量对活性炭去除砷效果如图1所示:

①纳米二氧化钛投加量为
②未加二氧化钛时就有一定的吸附砷的能力,可能的原因是
③若要提高废水中As(III)的去除率,可采取的措施
(2)化学氧化法
该方法须将废水中的As(III)用空气或铁离子氧化为As(V),然后再去除,为了探究As(III)被哪种氧化剂氧化,设计如下实验:取含As(III)废水,在pH分别为1~10条件下反应1h后,过滤,测定滤液中三价铁和二价铁的含量,得出不同pH下三价铁和二价铁的浓度随pH变化如图2所示:

①pH在3~4时Fe3+浓度变化的主要原因为
②由实验可知废水中的As(III)主要被
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】研究物质性质及物质转化具有重要的价值,根据所学知识回答下列问题:
(1)我国四大发明之一的火药是由硫磺粉、硝酸钾、木炭粉按一定比例混合而成的,爆炸时的反应为 ,在该反应的生成物中,属于非电解质的物质是
,在该反应的生成物中,属于非电解质的物质是___________ (填化学式,下同),属于电解质的物质是___________ ,还原产物是___________ ;当3.2gS参与反应时,生成的气体质量为___________ g。
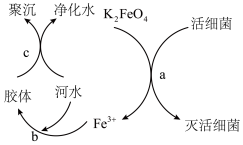
(2) 是高效、绿色的水处理剂,其原理如图所示。
是高效、绿色的水处理剂,其原理如图所示。
①从物质的类别来看,高铁酸钾( )属于
)属于___________ (“酸”“碱”“盐”或“氧化物”)。
②从元素的化合价角度来看, 中铁的化合价为
中铁的化合价为___________ 价,则过程a中 体现了
体现了___________ (填“氧化”或“还原”)性,活细菌发生了___________ (填“氧化”或“还原”)反应,该过程中消耗2个 时,转移的电子数目为
时,转移的电子数目为___________ 。
(3)纯碱和小苏打是日常家庭厨房中的常见用品,从物质的类别来看,均属于盐类。若取适量小苏打加水溶解,配制成溶液,再向其中加入少量澄清石灰水,发生反应的离子方程式是___________ 。
(1)我国四大发明之一的火药是由硫磺粉、硝酸钾、木炭粉按一定比例混合而成的,爆炸时的反应为
 ,在该反应的生成物中,属于非电解质的物质是
,在该反应的生成物中,属于非电解质的物质是(2)
 是高效、绿色的水处理剂,其原理如图所示。
是高效、绿色的水处理剂,其原理如图所示。
①从物质的类别来看,高铁酸钾(
 )属于
)属于②从元素的化合价角度来看,
 中铁的化合价为
中铁的化合价为 体现了
体现了 时,转移的电子数目为
时,转移的电子数目为(3)纯碱和小苏打是日常家庭厨房中的常见用品,从物质的类别来看,均属于盐类。若取适量小苏打加水溶解,配制成溶液,再向其中加入少量澄清石灰水,发生反应的离子方程式是
您最近一年使用:0次
【推荐2】二氧化氯消毒剂是国际上公认的高效消毒灭菌剂,可以杀灭一切微生物。二氧化氮常温下为黄绿色或桔黄色气体,以下是二氧化氮的几种工业制备方法。
(1)H2C2O4还原法:
2NaClO3+H2C2O4+2H2SO4=2ClO2↑+2CO2↑+2H2O+2NaHSO4。请用双线桥表示该反应电子转移的方向和数目_______ 。
(2) 还原法:
还原法:
①配平该反应的离子方程式:_______ 。





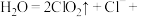




②还原产物为_______ 。
(3)盐酸法:
2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O;该反应中做还原剂的HCl与做酸性介质的HCl物质的量之比为_______ ,0.1mol NaClO3参加反应,做酸性介质的HCl的物质的量为_______ mol。
(4)NaClO2自氧化法:
5NaClO2+4HCl=4ClO2↑+5NaCl+2H2O;该反应中,氧化剂与还原剂的物质的量之比为_______ ,0.2mol HCl参加反应,转移的电子数为_______ 。
(5)Solvey法:
NaClO3在酸性条件下将CH3OH氧化为HCHO,该反应的离子方程式为:_______ 。
(1)H2C2O4还原法:
2NaClO3+H2C2O4+2H2SO4=2ClO2↑+2CO2↑+2H2O+2NaHSO4。请用双线桥表示该反应电子转移的方向和数目
(2)
 还原法:
还原法:①配平该反应的离子方程式:





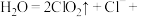




②还原产物为
(3)盐酸法:
2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O;该反应中做还原剂的HCl与做酸性介质的HCl物质的量之比为
(4)NaClO2自氧化法:
5NaClO2+4HCl=4ClO2↑+5NaCl+2H2O;该反应中,氧化剂与还原剂的物质的量之比为
(5)Solvey法:
NaClO3在酸性条件下将CH3OH氧化为HCHO,该反应的离子方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】I.人们对酸碱的认识,已有几百年的历史。1923年丹麦化学家布朗斯特和英国化学家劳莱提出了质子论。凡是能够释放质子(氢离子)的任何含氢原子的分子或离子都是酸;凡是能与质子(氢离子)结合的分子或离子都是碱。按质子理论,下列水溶液既可看作酸又可看作碱的是__________ (填字母序号)。
A.H2O B. NH4+ C. OH- D. HCO3- E. CH3COOO- F. Cl-
Ⅱ.建筑工地常用的NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生如下反应:
□NaNO2+□HI→□NO↑+□I2+□NaI+□H2O
(1)配平上面方程式______________ 。
(2)上述反应的氧化剂是__________ ;若有1mol的还原剂被氧化,则反应中转移电子的数目是_______________ 。
(3)某厂废液中,含有2%~5%的NaNO2,直接排放会造成污染,能使NaNO2转化为不引起二次污染的N2,反应的化学方程式为_________________ 。
A.H2O B. NH4+ C. OH- D. HCO3- E. CH3COOO- F. Cl-
Ⅱ.建筑工地常用的NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生如下反应:
□NaNO2+□HI→□NO↑+□I2+□NaI+□H2O
(1)配平上面方程式
(2)上述反应的氧化剂是
(3)某厂废液中,含有2%~5%的NaNO2,直接排放会造成污染,能使NaNO2转化为不引起二次污染的N2,反应的化学方程式为
您最近一年使用:0次



