研究物质性质及物质转化具有重要的价值,根据所学知识回答下列问题:
(1)我国四大发明之一的火药是由硫磺粉、硝酸钾、木炭粉按一定比例混合而成的,爆炸时的反应为 ,在该反应的生成物中,属于非电解质的物质是
,在该反应的生成物中,属于非电解质的物质是___________ (填化学式,下同),属于电解质的物质是___________ ,还原产物是___________ ;当3.2gS参与反应时,生成的气体质量为___________ g。
(2) 是高效、绿色的水处理剂,其原理如图所示。
是高效、绿色的水处理剂,其原理如图所示。
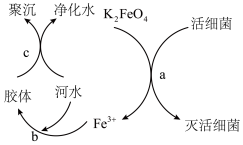
①从物质的类别来看,高铁酸钾( )属于
)属于___________ (“酸”“碱”“盐”或“氧化物”)。
②从元素的化合价角度来看, 中铁的化合价为
中铁的化合价为___________ 价,则过程a中 体现了
体现了___________ (填“氧化”或“还原”)性,活细菌发生了___________ (填“氧化”或“还原”)反应,该过程中消耗2个 时,转移的电子数目为
时,转移的电子数目为___________ 。
(3)纯碱和小苏打是日常家庭厨房中的常见用品,从物质的类别来看,均属于盐类。若取适量小苏打加水溶解,配制成溶液,再向其中加入少量澄清石灰水,发生反应的离子方程式是___________ 。
(1)我国四大发明之一的火药是由硫磺粉、硝酸钾、木炭粉按一定比例混合而成的,爆炸时的反应为
 ,在该反应的生成物中,属于非电解质的物质是
,在该反应的生成物中,属于非电解质的物质是(2)
 是高效、绿色的水处理剂,其原理如图所示。
是高效、绿色的水处理剂,其原理如图所示。
①从物质的类别来看,高铁酸钾(
 )属于
)属于②从元素的化合价角度来看,
 中铁的化合价为
中铁的化合价为 体现了
体现了 时,转移的电子数目为
时,转移的电子数目为(3)纯碱和小苏打是日常家庭厨房中的常见用品,从物质的类别来看,均属于盐类。若取适量小苏打加水溶解,配制成溶液,再向其中加入少量澄清石灰水,发生反应的离子方程式是
更新时间:2023-12-31 08:04:25
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】离子反应广泛用于化学研究、化工生产、医疗诊断和环境保护等各个领域。
(1)实验室中可利用Na2SO3粉末与质量分数为70%的硫酸反应制取少量SO2,反应的化学方程式为___________ 。
(2)酸性高锰酸钾溶液可吸收SO2,反应的化学方程式为2KMnO4+5SO2+2H2O=K2SO4+2MnSO4+2H2SO4,改写成离子方程式为___________ 。该反应中被还原的元素是___________ (填元素符号)。
(3)某硫酸厂每天排放1.12×104m3(标准状况)尾气,其中含0.2%(体积分数)的SO2,则其中所含SO2的物质的量为___________ 。现用含NaOH浓度为0.5mol·L-1的废碱液(假设其他成分不参与反应)进行处理,每天至少需要这种废碱液的体积为___________ L。
(4)某同学向BaCl2溶液中通入SO2,未观察到白色沉淀生成,由此可知酸性强弱:H2SO3___________ HCl(填“>”或“<”)。取上述所得溶液进行下列操作,能观察到白色沉淀生成的___________ (填字母)。
A.通入Cl2 B.滴加H2O2溶液 C.滴加稀盐酸 D.滴加NaOH溶液
(1)实验室中可利用Na2SO3粉末与质量分数为70%的硫酸反应制取少量SO2,反应的化学方程式为
(2)酸性高锰酸钾溶液可吸收SO2,反应的化学方程式为2KMnO4+5SO2+2H2O=K2SO4+2MnSO4+2H2SO4,改写成离子方程式为
(3)某硫酸厂每天排放1.12×104m3(标准状况)尾气,其中含0.2%(体积分数)的SO2,则其中所含SO2的物质的量为
(4)某同学向BaCl2溶液中通入SO2,未观察到白色沉淀生成,由此可知酸性强弱:H2SO3
A.通入Cl2 B.滴加H2O2溶液 C.滴加稀盐酸 D.滴加NaOH溶液
您最近一年使用:0次
【推荐2】生活污水中氮是造成水体富营养化的主要原因。若某污水中NH4Cl含量为180mg/L。
(1)写出NH4Cl电子式:___ 。
(2)氮原子的电子排布式是:___ ,写出与氯同周期,有2个未成对电子的原子的元素符号为___ 、___ 。
(3)为除去废水中的NH4+,向103L该污水中加入0.1mol/LNaOH溶液,理论上需要NaOH溶液的体积为___ L(计算结果保留两位小数)。
(4)可先在酸性污水中加入铁屑将NO3-转化为NH4+后再除去,请配平下列离子方程式并标出电子转移的方向和数目___ 。
___ Fe+___ NO3-+___ H+→___ Fe2++___ NH4++___ H2O
(1)写出NH4Cl电子式:
(2)氮原子的电子排布式是:
(3)为除去废水中的NH4+,向103L该污水中加入0.1mol/LNaOH溶液,理论上需要NaOH溶液的体积为
(4)可先在酸性污水中加入铁屑将NO3-转化为NH4+后再除去,请配平下列离子方程式并标出电子转移的方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)有BaCl2和KCl的混合溶液V L,将它分成两等份。一份滴加稀硫酸,使Ba2+完全沉淀,消耗a mol H2SO4;另一份滴加AgNO3溶液,消耗b mol AgNO3使Cl-完全沉淀。原混合溶液中的K+的物质的量浓度为___ mol·L-1。
(2)一定条件下,PbO2与Cr3+反应,产物是 和Pb2+,则与1 mol Cr3+反应所需PbO2的物质的量为
和Pb2+,则与1 mol Cr3+反应所需PbO2的物质的量为____ mol;
(3)在一定条件下,实验室分别以过氧化氢、高锰酸钾、氯酸钾、过氧化钠为原料制取氧气,当制得同温同压下相同体积的氧气时,四个反应中转移的电子数之比为___________ 。
(4)自来水中的NO3-对人类健康产生危害。为了降低自来水中NO3-的浓度,某研究人员提出在碱性条件下用Al粉还原NO3-,产物是N2。发生的反应可表示如下,请完成方程式的配平 。Al+NO3-+ —AlO2-+N2↑+H2O,_____________
(5)某化学反应的反应物和产物:KMnO4+KI+H2SO4→MnSO4+I2+KIO3+K2SO4+H2O
①该反应的氧化产物是__________ 。
②若该反应方程式中I2和KIO3的计量数分别是是6和3,请在下边的化学式上用单线桥标出电子转移的方向和数目:KMnO4+KI+H2SO4→__________ 。
(2)一定条件下,PbO2与Cr3+反应,产物是
 和Pb2+,则与1 mol Cr3+反应所需PbO2的物质的量为
和Pb2+,则与1 mol Cr3+反应所需PbO2的物质的量为(3)在一定条件下,实验室分别以过氧化氢、高锰酸钾、氯酸钾、过氧化钠为原料制取氧气,当制得同温同压下相同体积的氧气时,四个反应中转移的电子数之比为
(4)自来水中的NO3-对人类健康产生危害。为了降低自来水中NO3-的浓度,某研究人员提出在碱性条件下用Al粉还原NO3-,产物是N2。发生的反应可表示如下,请完成方程式的
(5)某化学反应的反应物和产物:KMnO4+KI+H2SO4→MnSO4+I2+KIO3+K2SO4+H2O
①该反应的氧化产物是
②若该反应方程式中I2和KIO3的计量数分别是是6和3,请在下边的化学式上用单线桥标出电子转移的方向和数目:KMnO4+KI+H2SO4→
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题
(1)有以下六种物质:
①乙醇;②Na2CO3溶液;③ 固体;④液态氯化氢;⑤冰醋酸;⑥石墨。
固体;④液态氯化氢;⑤冰醋酸;⑥石墨。
上述状态下的物质中,能导电的有___________ (填序号,下同),属于电解质的有___________ 。
(2)已知H3PO2是一元弱酸,NaH2PO2属于___________ (填:酸式盐、正盐或者碱式盐)。写出H3PO2与足量NaOH溶液反应的离子方程式:___________
(3)某种飞船以联氨 和
和 为动力源,发生反应:
为动力源,发生反应: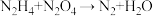 ,反应温度可高达
,反应温度可高达 ,回答下列问题。
,回答下列问题。
①配平该方程式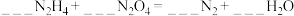 。
。___________
②该反应中,氧化产物与还原产物的质量之比为___________ 。
(4)补全并配平下列方程式
①_______ _______HCl=______KCl+______
_______HCl=______KCl+______ ______
______ ______
______
___________
②______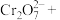 _______
_______ _______H+=______
_______H+=______ _______
_______ ________
________ ___________
(1)有以下六种物质:
①乙醇;②Na2CO3溶液;③
 固体;④液态氯化氢;⑤冰醋酸;⑥石墨。
固体;④液态氯化氢;⑤冰醋酸;⑥石墨。上述状态下的物质中,能导电的有
(2)已知H3PO2是一元弱酸,NaH2PO2属于
(3)某种飞船以联氨
 和
和 为动力源,发生反应:
为动力源,发生反应: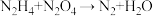 ,反应温度可高达
,反应温度可高达 ,回答下列问题。
,回答下列问题。①配平该方程式
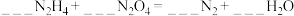 。
。②该反应中,氧化产物与还原产物的质量之比为
(4)补全并配平下列方程式
①_______
 _______HCl=______KCl+______
_______HCl=______KCl+______ ______
______ ______
______
②______
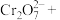 _______
_______ _______H+=______
_______H+=______ _______
_______ ________
________
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】利用所学知识进行填空(用NA表示阿伏加德罗常数的值)。
(1)0.4mol氨气中含有NH3分子数是___________ ,其质量是___________ g。
(2)标准状况下,44.8LCH4对应的物质的量是___________ ,其电子数为___________ 。
(3)现有物质:①NaOH溶液;②铜;③熔融KHSO4;④BaCO3固体;⑤液态HCl;⑥CO2,以上物质中属于混合物的是___________  填序号
填序号 ,以上物质中属于电解质的
,以上物质中属于电解质的___________  填序号
填序号 ;以上物质中能导电的是
;以上物质中能导电的是___________  填序号
填序号 。
。
(4)现有CO与O2两种气态物质,试回答下列问题:
①同温同压下,CO与O2的密度之比为___________ 。
②相同温度和压强下,等质量的CO和O2.二者体积比为___________ 。
(5)将4gNaOH溶于水配成1L溶液,然后取出10mL,这10mL溶液的物质的量浓度为___________ 。
(6)18.6gNa2X含有0.6molNa+,则Na2X的物质的量是___________ ,Na2X的摩尔质量是___________ 。
(7)已知O2和CO2的混合气体,在标准状况下体积为11.2L,质量为18g,则混合气体的平均相对分子质量是___________ ,混合气体中O2和CO2物质的量之比为___________ 。
(1)0.4mol氨气中含有NH3分子数是
(2)标准状况下,44.8LCH4对应的物质的量是
(3)现有物质:①NaOH溶液;②铜;③熔融KHSO4;④BaCO3固体;⑤液态HCl;⑥CO2,以上物质中属于混合物的是
 填序号
填序号 ,以上物质中属于电解质的
,以上物质中属于电解质的 填序号
填序号 ;以上物质中能导电的是
;以上物质中能导电的是 填序号
填序号 。
。(4)现有CO与O2两种气态物质,试回答下列问题:
①同温同压下,CO与O2的密度之比为
②相同温度和压强下,等质量的CO和O2.二者体积比为
(5)将4gNaOH溶于水配成1L溶液,然后取出10mL,这10mL溶液的物质的量浓度为
(6)18.6gNa2X含有0.6molNa+,则Na2X的物质的量是
(7)已知O2和CO2的混合气体,在标准状况下体积为11.2L,质量为18g,则混合气体的平均相对分子质量是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】完成下列填空:
(1)现有下列9种物质,① ②淀粉溶液 ③
②淀粉溶液 ③ ④
④ ⑤
⑤ ⑥
⑥ ⑦纯醋酸 ⑧
⑦纯醋酸 ⑧ 溶液 ⑨
溶液 ⑨ ,根据所学知识回答下列问题:属于强电解质的是
,根据所学知识回答下列问题:属于强电解质的是_______ (填写序号)。
(2)标准状况下,若④和⑤混合气体相对于氢气的密度为14.5,则④和⑤物质的量之比为_______ 。标准状况下,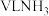 溶入
溶入 中,溶液密度为
中,溶液密度为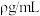 ,则氨水物质的量浓度表达式为
,则氨水物质的量浓度表达式为_______ mol/L。
(3)现取一定量的硫酸酸化的硫酸锰( )溶液,向其中依次滴加下列溶液,对应的现象如下表所示:
)溶液,向其中依次滴加下列溶液,对应的现象如下表所示:
已知:①金属铋(Bi)价态为+3时较稳定, 无色;②铋酸钠(
无色;②铋酸钠( )无色,难溶于水;③淀粉溶液遇到
)无色,难溶于水;③淀粉溶液遇到 变成蓝色。
变成蓝色。
Ⅰ.请配平步骤②发生反应的化学方程式:

_______ 。
Ⅱ.由上述现象可得 、
、 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为_______ 。
根据上述结论,请写出 与KI溶液在酸性条件下反应的离子方程式
与KI溶液在酸性条件下反应的离子方程式_______ 。
(1)现有下列9种物质,①
 ②淀粉溶液 ③
②淀粉溶液 ③ ④
④ ⑤
⑤ ⑥
⑥ ⑦纯醋酸 ⑧
⑦纯醋酸 ⑧ 溶液 ⑨
溶液 ⑨ ,根据所学知识回答下列问题:属于强电解质的是
,根据所学知识回答下列问题:属于强电解质的是(2)标准状况下,若④和⑤混合气体相对于氢气的密度为14.5,则④和⑤物质的量之比为
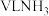 溶入
溶入 中,溶液密度为
中,溶液密度为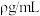 ,则氨水物质的量浓度表达式为
,则氨水物质的量浓度表达式为(3)现取一定量的硫酸酸化的硫酸锰(
 )溶液,向其中依次滴加下列溶液,对应的现象如下表所示:
)溶液,向其中依次滴加下列溶液,对应的现象如下表所示:| 加入溶液 | ①适量铋酸钠溶液 | ②过量的双氧水 | ③适量KI-淀粉溶液 |
| 实验现象 | 溶液呈紫红色 | 紫红色消失,产生气泡 | 溶液变成蓝色 |
 无色;②铋酸钠(
无色;②铋酸钠( )无色,难溶于水;③淀粉溶液遇到
)无色,难溶于水;③淀粉溶液遇到 变成蓝色。
变成蓝色。Ⅰ.请配平步骤②发生反应的化学方程式:

Ⅱ.由上述现象可得
 、
、 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为根据上述结论,请写出
 与KI溶液在酸性条件下反应的离子方程式
与KI溶液在酸性条件下反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】按要求回答问题
(1)辉铜矿(Cu2S)可发生反应:2Cu2S+2H2SO4+5O2=4CuSO4+2H2O,该反应的还原剂是_______ 。当1mol O2发生反应时,还原剂所失电子的物质的量为_______ mol。
(2)焙烧明矾的化学方程式为4KAl(SO4)2·12H2O+3S 2K2SO4+2Al2O3+9SO2↑+48H2O,在该反应中,还原剂是
2K2SO4+2Al2O3+9SO2↑+48H2O,在该反应中,还原剂是_______ 。
(3)KClO3可用于实验室制O2,若不加催化剂,400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴、阳离子个数比为1∶1.写出该反应的化学方程式:_______ 。
(4)NaBH4是一种重要的储氢载体,能与水反应得到NaBO2,且反应前后B的化合价不变,该反应的化学方程式_______ ,反应消耗1 mol NaBH4时转移的电子数目为_______ 。
(1)辉铜矿(Cu2S)可发生反应:2Cu2S+2H2SO4+5O2=4CuSO4+2H2O,该反应的还原剂是
(2)焙烧明矾的化学方程式为4KAl(SO4)2·12H2O+3S
 2K2SO4+2Al2O3+9SO2↑+48H2O,在该反应中,还原剂是
2K2SO4+2Al2O3+9SO2↑+48H2O,在该反应中,还原剂是(3)KClO3可用于实验室制O2,若不加催化剂,400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴、阳离子个数比为1∶1.写出该反应的化学方程式:
(4)NaBH4是一种重要的储氢载体,能与水反应得到NaBO2,且反应前后B的化合价不变,该反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】铁及其化合物在日常生产生活中应用广泛,研究铁及其化合物的应用意义重大。
(1)高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂。湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒: 、
、 、
、 、
、 、
、 、H2O。写出并配平湿法制高铁酸钾的离子反应方程式:
、H2O。写出并配平湿法制高铁酸钾的离子反应方程式:_____ ,____ +___
+___ +___=___
+___=___ +___
+___ +___。
+___。
(2)电子工业中,常用 溶液腐蚀绝缘板上的铜箔,制造印刷电路板,请写出反应的离子方程式
溶液腐蚀绝缘板上的铜箔,制造印刷电路板,请写出反应的离子方程式________ ,反应后铜箔质量减少12.8g,此过程中消耗 的质量为
的质量为________ 。
(3)已知常温下在溶液中可发生如下两个反应: 、
、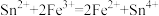 ,由此可以确定
,由此可以确定 、
、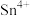 、
、 三种离子的氧化性由强到弱的顺序是
三种离子的氧化性由强到弱的顺序是_________ 。
(4) 、
、 、
、 、
、 、
、 、
、 组成的一个氧化还原反应体系中,发生
组成的一个氧化还原反应体系中,发生 →
→ 的反应过程。
的反应过程。
①该反应中,被氧化的元素是_______ (填元素符号),氧化剂是______ (填化学式)。
②将以上物质分别填入下面对应的横线上,组成一个配平的离子方程式:___________ ;____+_____+____ = ______+______+ 。
。
(1)高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂。湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:
 、
、 、
、 、
、 、
、 、H2O。写出并配平湿法制高铁酸钾的离子反应方程式:
、H2O。写出并配平湿法制高铁酸钾的离子反应方程式: +___
+___ +___=___
+___=___ +___
+___ +___。
+___。(2)电子工业中,常用
 溶液腐蚀绝缘板上的铜箔,制造印刷电路板,请写出反应的离子方程式
溶液腐蚀绝缘板上的铜箔,制造印刷电路板,请写出反应的离子方程式 的质量为
的质量为(3)已知常温下在溶液中可发生如下两个反应:
 、
、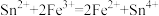 ,由此可以确定
,由此可以确定 、
、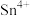 、
、 三种离子的氧化性由强到弱的顺序是
三种离子的氧化性由强到弱的顺序是(4)
 、
、 、
、 、
、 、
、 、
、 组成的一个氧化还原反应体系中,发生
组成的一个氧化还原反应体系中,发生 →
→ 的反应过程。
的反应过程。①该反应中,被氧化的元素是
②将以上物质分别填入下面对应的横线上,组成一个配平的离子方程式:
 。
。
您最近一年使用:0次
【推荐3】二氧化氯消毒剂是国际上公认的高效消毒灭菌剂,可以杀灭一切微生物。二氧化氮常温下为黄绿色或桔黄色气体,以下是二氧化氮的几种工业制备方法。
(1)H2C2O4还原法:
2NaClO3+H2C2O4+2H2SO4=2ClO2↑+2CO2↑+2H2O+2NaHSO4。请用双线桥表示该反应电子转移的方向和数目_______ 。
(2) 还原法:
还原法:
①配平该反应的离子方程式:_______ 。





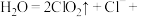




②还原产物为_______ 。
(3)盐酸法:
2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O;该反应中做还原剂的HCl与做酸性介质的HCl物质的量之比为_______ ,0.1mol NaClO3参加反应,做酸性介质的HCl的物质的量为_______ mol。
(4)NaClO2自氧化法:
5NaClO2+4HCl=4ClO2↑+5NaCl+2H2O;该反应中,氧化剂与还原剂的物质的量之比为_______ ,0.2mol HCl参加反应,转移的电子数为_______ 。
(5)Solvey法:
NaClO3在酸性条件下将CH3OH氧化为HCHO,该反应的离子方程式为:_______ 。
(1)H2C2O4还原法:
2NaClO3+H2C2O4+2H2SO4=2ClO2↑+2CO2↑+2H2O+2NaHSO4。请用双线桥表示该反应电子转移的方向和数目
(2)
 还原法:
还原法:①配平该反应的离子方程式:





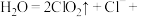




②还原产物为
(3)盐酸法:
2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O;该反应中做还原剂的HCl与做酸性介质的HCl物质的量之比为
(4)NaClO2自氧化法:
5NaClO2+4HCl=4ClO2↑+5NaCl+2H2O;该反应中,氧化剂与还原剂的物质的量之比为
(5)Solvey法:
NaClO3在酸性条件下将CH3OH氧化为HCHO,该反应的离子方程式为:
您最近一年使用:0次
【推荐1】二氧化氯(ClO2)是一种黄绿色到橙黄色的气体,是国际上公认的安全、无毒的绿色消毒剂。已知:工业上制备二氧化氯的方法之一是用甲醇在酸性介质中与氯酸钠反应。完成下列填空:
(1)请配平下列反应的化学方程式(CH3OH中H为+1价,O为-2价):_____ 。
_______CH3OH +______NaClO3 +_______ →______CO2↑+_______ClO2↑+________ Na2SO4 +___________H2O
→______CO2↑+_______ClO2↑+________ Na2SO4 +___________H2O
该反应中,被氧化的元素是___________ ,还原产物与氧化产物的物质的量之比是___________ 。
(2)根据上述反应可推知___________
a.氧化性:C1O2>NaClO3 b.氧化性:NaClO3>CH3OH
c.还原性:CH3OH>ClO2 d.还原性:CH3OH>Na2SO4
(3)若转移的电子数目为0.3NA(NA为阿伏加德罗常数),则反应产生气体(标准状况)为___________ 升。
(1)请配平下列反应的化学方程式(CH3OH中H为+1价,O为-2价):
_______CH3OH +______NaClO3 +_______
 →______CO2↑+_______ClO2↑+________ Na2SO4 +___________H2O
→______CO2↑+_______ClO2↑+________ Na2SO4 +___________H2O该反应中,被氧化的元素是
(2)根据上述反应可推知
a.氧化性:C1O2>NaClO3 b.氧化性:NaClO3>CH3OH
c.还原性:CH3OH>ClO2 d.还原性:CH3OH>Na2SO4
(3)若转移的电子数目为0.3NA(NA为阿伏加德罗常数),则反应产生气体(标准状况)为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】汽车安全气囊内含 、
、 、
、 、
、 等物质,当汽车发生碰撞时,
等物质,当汽车发生碰撞时, 迅速分解产生
迅速分解产生 和
和 ,同时放出大量的热,使气囊迅速膨胀,从而起到保护作用。
,同时放出大量的热,使气囊迅速膨胀,从而起到保护作用。
(1) 的俗名是
的俗名是__________ ; 是由
是由 和
和__________ (填离子符号)构成。
(2) 可与
可与 发生反应生成
发生反应生成 和
和 。
。
①该反应属于__________ (填基本反应类型)。
②反应中, 是
是__________ (填“氧化剂”或“还原剂”),发生__________ (填“氧化”或“还原”)反应。
(3) 是冷却剂,可以吸收产气过程释放的热量。
是冷却剂,可以吸收产气过程释放的热量。
① 属于
属于__________ (填字母)。
a.混合物 b.酸 c.碱 d.盐 e.氧化物 f.强电解质 g.弱电解质 h.非电解质 i.单质
② 起冷却作用时发生反应的化学方程式为
起冷却作用时发生反应的化学方程式为__________ 。
(4)若一个安全气囊里装有65g ,且在碰撞时完全分解。
,且在碰撞时完全分解。
①反应过程中转移__________  电子。
电子。
②所释放的 在标准状况下的体积为
在标准状况下的体积为__________ L。
 、
、 、
、 、
、 等物质,当汽车发生碰撞时,
等物质,当汽车发生碰撞时, 迅速分解产生
迅速分解产生 和
和 ,同时放出大量的热,使气囊迅速膨胀,从而起到保护作用。
,同时放出大量的热,使气囊迅速膨胀,从而起到保护作用。(1)
 的俗名是
的俗名是 是由
是由 和
和(2)
 可与
可与 发生反应生成
发生反应生成 和
和 。
。①该反应属于
②反应中,
 是
是(3)
 是冷却剂,可以吸收产气过程释放的热量。
是冷却剂,可以吸收产气过程释放的热量。①
 属于
属于a.混合物 b.酸 c.碱 d.盐 e.氧化物 f.强电解质 g.弱电解质 h.非电解质 i.单质
②
 起冷却作用时发生反应的化学方程式为
起冷却作用时发生反应的化学方程式为(4)若一个安全气囊里装有65g
 ,且在碰撞时完全分解。
,且在碰撞时完全分解。①反应过程中转移
 电子。
电子。②所释放的
 在标准状况下的体积为
在标准状况下的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】一些物质的分类如图,根据所学知识填空。

(1)A组物质中属于碱性氧化物的电解质是________ 。A组物质中Na2O2具有强氧化性,和A组中CO2一样SO2也为非电解质,但SO2有还原性,写出Na2O2和SO2反应的化学方程式________ 。
(2)B组中两种金属均可在氯气中燃烧,l个Cl2与足量金属铁粉充分反应生成+3价的三氯化铁,理论上转移电子数为_______ 个。
(3)D组中两种单质均能与H2O反应,写出熔点低的那种金属与H2O反应的方程式________ (属于离子反应的写离子方程式)。
(4)写出A组物质中属于酸式盐的物质在熔融状态下的电离方程式___________ 。
(5)向少量的Ba(OH)2溶液中逐滴加入稀硫酸可生成硫酸钡,其反应的离子方程式为:Ba2++2OH-+2H++ =BaSO4↓+2H2O。下列三种情况下,离子方程式与题干中相同的是___________(填序号)。
=BaSO4↓+2H2O。下列三种情况下,离子方程式与题干中相同的是___________(填序号)。
(6)磷元素的含氧酸有H3PO4、H3PO3(亚磷酸)、H3PO2(次磷酸)等多种。其中已知:H3PO2+NaOH(过量)=NaH2PO2+H2O。则NaH2PO2属于___________ (填“正盐”或“酸式盐”)。

(1)A组物质中属于碱性氧化物的电解质是
(2)B组中两种金属均可在氯气中燃烧,l个Cl2与足量金属铁粉充分反应生成+3价的三氯化铁,理论上转移电子数为
(3)D组中两种单质均能与H2O反应,写出熔点低的那种金属与H2O反应的方程式
(4)写出A组物质中属于酸式盐的物质在熔融状态下的电离方程式
(5)向少量的Ba(OH)2溶液中逐滴加入稀硫酸可生成硫酸钡,其反应的离子方程式为:Ba2++2OH-+2H++
 =BaSO4↓+2H2O。下列三种情况下,离子方程式与题干中相同的是___________(填序号)。
=BaSO4↓+2H2O。下列三种情况下,离子方程式与题干中相同的是___________(填序号)。| A.向NaHSO4溶液中逐滴加入Ba(OH)2溶液至溶液显中性 |
B.向NaHSO4溶液中逐滴加入Ba(OH)2溶液至 恰好完全沉淀 恰好完全沉淀 |
| C.向NaHSO4溶液中逐滴加入Ba(OH)2溶液至过量 |
| D.向少量的稀硫酸溶液中逐滴加入Ba(OH)2至溶液显中性 |
您最近一年使用:0次



