高铁酸钾是一种非氯高效消毒剂,主要用于饮用水处理。高铁酸钾( )在强碱性条件下能够稳定存在。工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入饱和的KOH溶液,使高铁酸钾析出。
)在强碱性条件下能够稳定存在。工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入饱和的KOH溶液,使高铁酸钾析出。
(1)方法一:可利用固体反应物反应: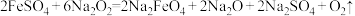 ,该反应中的氧化剂是
,该反应中的氧化剂是___________ ,消耗117 g  转移
转移___________ mol电子。
(2)方法二:反应: (未配平)
(未配平)
①配平离子反应方程式:_______ ____ _____
_____ ______
______ _____
_____ _______
_______ ______
______
②若反应过程中转移了1.5 mol电子,则还原产物的物质的量为______ mol。
(3)向 溶液中加入适量饱和的KOH溶液,有
溶液中加入适量饱和的KOH溶液,有 析出,请写出该反应的离子方程式:
析出,请写出该反应的离子方程式:___________ 。
 )在强碱性条件下能够稳定存在。工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入饱和的KOH溶液,使高铁酸钾析出。
)在强碱性条件下能够稳定存在。工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入饱和的KOH溶液,使高铁酸钾析出。(1)方法一:可利用固体反应物反应:
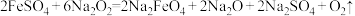 ,该反应中的氧化剂是
,该反应中的氧化剂是 转移
转移(2)方法二:反应:
 (未配平)
(未配平)①配平离子反应方程式:
 _____
_____ ______
______ _____
_____ _______
_______ ______
______
②若反应过程中转移了1.5 mol电子,则还原产物的物质的量为
(3)向
 溶液中加入适量饱和的KOH溶液,有
溶液中加入适量饱和的KOH溶液,有 析出,请写出该反应的离子方程式:
析出,请写出该反应的离子方程式:
更新时间:2022-01-08 14:33:26
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】氧化还原反应在日常生活和工业生产中有重要应用。
I.K2Cr2O7是火柴工业用作制造火柴头的原料之一
已知反应:
(1)用“双线桥”标明该反应中电子转移的方向和数目。__________

(2)该反应中被氧化的元素是___________ ,还原产物是___________ 。
(3)该反应中氧化剂与还原剂的微粒个数比为___________ 。
Ⅱ.阅读下面一段材料并回答问题。
【性状】暗紫色具有金属光泽的粉末,无臭无味
【产品特点】干燥品在室温下稳定,在强碱溶液中稳定,随着pH减小,稳定性下降,与水反应放出氧气。K2FeO4通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。K2FeO4与水反应还能产生具有强吸附性的Fe(OH)3胶体,可除去水中细微的悬浮物,有净水作用
【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理
【用量】消毒净化1L水投放5mgK2FeO4即可达到卫生标准
……
(4) K2FeO4中铁元素的化合价为___________ 。
(5)下列关于K2FeO4的说法中,不正确的是___________ 。
a.是强氧化性的盐 b.固体保存需要防潮
b.固体保存需要防潮
c.其消毒和净化水的原理相同 d.其净水优点有:作用快、安全性好、无异味
(6)工业制备K2FeO4需要在碱性环境下进行,现提供反应体系中7种物质,Fe(NO3)3、Cl2、H2O、KOH、K2FeO4、KCl、KNO3请写出制备K2FeO4的化学反应方程式___________ 。
(7)将K2FeO4与水反应的化学方程式补充完整并配平:____________
___________ +___________
+___________ =___________
=___________ (胶体)+___________+___________
(胶体)+___________+___________
该反应消耗1个K2FeO4时,转移的电子数为___________ 个
(8)消毒净化198L水,按照卫生标准投入K2FeO4,则K2FeO4与水充分反应后产生的KOH质量为___________ g。
I.K2Cr2O7是火柴工业用作制造火柴头的原料之一
已知反应:

(1)用“双线桥”标明该反应中电子转移的方向和数目。

(2)该反应中被氧化的元素是
(3)该反应中氧化剂与还原剂的微粒个数比为
Ⅱ.阅读下面一段材料并回答问题。
高铁酸钾使用说明书
【化学式】K2FeO4【性状】暗紫色具有金属光泽的粉末,无臭无味
【产品特点】干燥品在室温下稳定,在强碱溶液中稳定,随着pH减小,稳定性下降,与水反应放出氧气。K2FeO4通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。K2FeO4与水反应还能产生具有强吸附性的Fe(OH)3胶体,可除去水中细微的悬浮物,有净水作用
【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理
【用量】消毒净化1L水投放5mgK2FeO4即可达到卫生标准
……
(4) K2FeO4中铁元素的化合价为
(5)下列关于K2FeO4的说法中,不正确的是
a.是强氧化性的盐
 b.固体保存需要防潮
b.固体保存需要防潮c.其消毒和净化水的原理相同 d.其净水优点有:作用快、安全性好、无异味
(6)工业制备K2FeO4需要在碱性环境下进行,现提供反应体系中7种物质,Fe(NO3)3、Cl2、H2O、KOH、K2FeO4、KCl、KNO3请写出制备K2FeO4的化学反应方程式
(7)将K2FeO4与水反应的化学方程式补充完整并配平:
___________
 +___________
+___________ =___________
=___________ (胶体)+___________+___________
(胶体)+___________+___________
该反应消耗1个K2FeO4时,转移的电子数为
(8)消毒净化198L水,按照卫生标准投入K2FeO4,则K2FeO4与水充分反应后产生的KOH质量为
您最近一年使用:0次
【推荐2】按要求填空。
(1)在Fe、Fe2+、Fe3+、H+中,
①只有氧化性的是______________________________ ;
②只有还原性的是______________________________ ;
③既有氧化性又有还原性的是____________________ 。
(2)已知Rx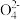 +
+ +H+―→RO2+Mn2++H2O变化过程中,0.2 mol Rx
+H+―→RO2+Mn2++H2O变化过程中,0.2 mol Rx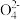 参加反应,共转移0.4 mol电子。
参加反应,共转移0.4 mol电子。
①反应中的被还原的微粒是________ 。
②x=________ 。
③参加反应的氢离子的物质的量为________ 。
(1)在Fe、Fe2+、Fe3+、H+中,
①只有氧化性的是
②只有还原性的是
③既有氧化性又有还原性的是
(2)已知Rx
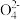 +
+ +H+―→RO2+Mn2++H2O变化过程中,0.2 mol Rx
+H+―→RO2+Mn2++H2O变化过程中,0.2 mol Rx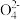 参加反应,共转移0.4 mol电子。
参加反应,共转移0.4 mol电子。①反应中的被还原的微粒是
②x=
③参加反应的氢离子的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】已知实验室制取氯气的反应原理:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,据此回答下列问题:
MnCl2+Cl2↑+2H2O,据此回答下列问题:
(1)该反应中氧化剂是___________ (填化学式),HCl在反应中体现的性质为___________ (填序号)
A、氧化性B、还原性C、酸性
(2)MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,用单线桥法表示电子转移的方向和数目:
MnCl2+Cl2↑+2H2O,用单线桥法表示电子转移的方向和数目:___________ 。
(3)有一种“地康法”制取氯气的反应原理如下所示:
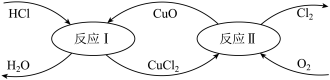
【提示:箭头进去的为反应物,出来的为生成物】
①反应Ⅰ的离子方程式为___________ 。
②反应Ⅱ属于___________ 反应(填四种基本反应类型之一),整个过程的总反应的化学方程式为___________ 。
③工业生产中常用氨气检查输送氯气的管道是否有Cl2泄漏。若Cl2有泄漏,可以观察到有大量的白烟生成(为NH4Cl固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式:___________ 。
 MnCl2+Cl2↑+2H2O,据此回答下列问题:
MnCl2+Cl2↑+2H2O,据此回答下列问题:(1)该反应中氧化剂是
A、氧化性B、还原性C、酸性
(2)MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O,用单线桥法表示电子转移的方向和数目:
MnCl2+Cl2↑+2H2O,用单线桥法表示电子转移的方向和数目:(3)有一种“地康法”制取氯气的反应原理如下所示:

【提示:箭头进去的为反应物,出来的为生成物】
①反应Ⅰ的离子方程式为
②反应Ⅱ属于
③工业生产中常用氨气检查输送氯气的管道是否有Cl2泄漏。若Cl2有泄漏,可以观察到有大量的白烟生成(为NH4Cl固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】在肉制品加工中,常使用来硝酸钠作发色剂,但必须严格控制亚硝酸钠的用量,以确保使用安全。亚硝酸钠也是一种常见的水污染物,在工业废水中亚硝酸盐的含量较高,如不做处理排放在环境中,对人体、水生物有毒害作用。
Ⅰ.某一反应体系中反应物和生成物共六种:NaNO2 、H2O、NO 、I2、NaI、HI。已知该反应中 NaNO2只发生还原反应。
(1)该反应的还原剂__________ 。
(2)写出该反应的化学方程式_____________________________________ ,该反应中,氧化剂和氧化产物的微粒数之比为_____________ ,当有n个氧化产物生成时,转移电子数为____ e-。
(3)HI在上述反应中表现出的性质是____________________ 。
(4)误食 NaNO2 会导致血红蛋白中 Fe2+转化 Fe3+而中毒,服用维生素 C 可以解除 NaNO2
引起的中毒。下列关于上述中毒、解毒过程的说法中正确的是_________ 。
A.中毒过程NaNO2 是还原剂 B.解毒过程维生素 C 是还原剂
C.解毒过程,维生素 C 能把 Fe2+氧化 Fe3+ D.中毒时亚硝酸盐发生还原反应
Ⅱ.工业废水中亚硝酸盐的处理这一研究已有很久的历史了,传统常见的方法有离子交换法、反渗透法、电渗析法、生物及反硝化法、化学还原法和化学催化硝化法,其中化学还原法是利用加NH4Cl进行处理含亚硝酸盐的废水,转化为无污染的物质进行排放。
(5)写出该处理方法的离子方程式________________________________________ 。
Ⅰ.某一反应体系中反应物和生成物共六种:NaNO2 、H2O、NO 、I2、NaI、HI。已知该反应中 NaNO2只发生还原反应。
(1)该反应的还原剂
(2)写出该反应的化学方程式
(3)HI在上述反应中表现出的性质是
(4)误食 NaNO2 会导致血红蛋白中 Fe2+转化 Fe3+而中毒,服用维生素 C 可以解除 NaNO2
引起的中毒。下列关于上述中毒、解毒过程的说法中正确的是
A.中毒过程NaNO2 是还原剂 B.解毒过程维生素 C 是还原剂
C.解毒过程,维生素 C 能把 Fe2+氧化 Fe3+ D.中毒时亚硝酸盐发生还原反应
Ⅱ.工业废水中亚硝酸盐的处理这一研究已有很久的历史了,传统常见的方法有离子交换法、反渗透法、电渗析法、生物及反硝化法、化学还原法和化学催化硝化法,其中化学还原法是利用加NH4Cl进行处理含亚硝酸盐的废水,转化为无污染的物质进行排放。
(5)写出该处理方法的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)X、Y、Z三种物质存在如图所示转化关系。
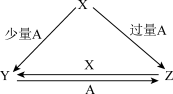
回答下列问题:
①若X为黑色固体单质,A为O2,写出Z→Y的化学方程式:___ 。
②若X为NaOH溶液,则写出Y→Z的离子方程式:___ 。
(2)已知常温下在溶液中可发生如下两个反应:
Ce4++Fe2+=Fe3++Ce3+
Sn2++2Fe3+=2Fe2++Sn4+
由此可以确定Ce4+、Sn4+、Fe3+三种离子的氧化性由强到弱的顺序是___ 。
(3)Mn2+、Bi3+、BiO 、MnO
、MnO 、H+、H2O组成的一个氧化还原反应体系中,发生BiO
、H+、H2O组成的一个氧化还原反应体系中,发生BiO →Bi3+的反应过程。
→Bi3+的反应过程。
①该反应中,被氧化的元素是___ (填元素符号),氧化剂是___ (填化学式)。
②将以上物质分别填入下面对应的横线上,组成一个未配平的化学方程式:______+______+______→______+______+H2O。___
(4)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图所示。
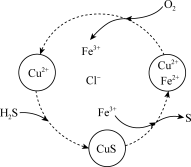
①写出CuCl2与H2S反应的离子方程式:___ 。
②通过上述流程图的分析,整个流程的总反应为___ 。
(1)X、Y、Z三种物质存在如图所示转化关系。

回答下列问题:
①若X为黑色固体单质,A为O2,写出Z→Y的化学方程式:
②若X为NaOH溶液,则写出Y→Z的离子方程式:
(2)已知常温下在溶液中可发生如下两个反应:
Ce4++Fe2+=Fe3++Ce3+
Sn2++2Fe3+=2Fe2++Sn4+
由此可以确定Ce4+、Sn4+、Fe3+三种离子的氧化性由强到弱的顺序是
(3)Mn2+、Bi3+、BiO
 、MnO
、MnO 、H+、H2O组成的一个氧化还原反应体系中,发生BiO
、H+、H2O组成的一个氧化还原反应体系中,发生BiO →Bi3+的反应过程。
→Bi3+的反应过程。①该反应中,被氧化的元素是
②将以上物质分别填入下面对应的横线上,组成一个未配平的化学方程式:______+______+______→______+______+H2O。
(4)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图所示。

①写出CuCl2与H2S反应的离子方程式:
②通过上述流程图的分析,整个流程的总反应为
您最近一年使用:0次
【推荐3】为防止在大灾之后疫病流行,全国各地向灾区运送了大量的各种消毒剂、漂白剂等。
(1) 过碳酸钠是一种有多用途的新型氧系固态漂白剂,化学式可表示为Na2CO3·3H2O2,它具有Na2CO3和H2O2的双重性质。过碳酸钠与下列物质均会发生化学反应而失效,其中过碳酸钠有发生了还原反应的是_______
A.MnO2 B.KMnO4溶液 C.Na2SO3溶液 D.稀硫酸
(2) 漂白剂亚氯酸钠(NaClO2)在常温与黑暗处可保存一年,亚氯酸不稳定可分解,反应的离子方程式为HClO2→ClO2↑+H++Cl-+H2O(未配平)。当生成1molClO2时转移的电子数是_______
(3) 二氧化氯是目前国际上公认的第四代高效、无毒的广谱消毒剂,它可由KClO3在H2SO4存在下与SO2反应制得。请写出反应的离子方程式:_______
(4)有Fe2+、NO 、Fe3+、NH
、Fe3+、NH 、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,则该反应中还原剂与氧化剂的物质的量之比为
、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,则该反应中还原剂与氧化剂的物质的量之比为_______
(1) 过碳酸钠是一种有多用途的新型氧系固态漂白剂,化学式可表示为Na2CO3·3H2O2,它具有Na2CO3和H2O2的双重性质。过碳酸钠与下列物质均会发生化学反应而失效,其中过碳酸钠有发生了还原反应的是
A.MnO2 B.KMnO4溶液 C.Na2SO3溶液 D.稀硫酸
(2) 漂白剂亚氯酸钠(NaClO2)在常温与黑暗处可保存一年,亚氯酸不稳定可分解,反应的离子方程式为HClO2→ClO2↑+H++Cl-+H2O(未配平)。当生成1molClO2时转移的电子数是
(3) 二氧化氯是目前国际上公认的第四代高效、无毒的广谱消毒剂,它可由KClO3在H2SO4存在下与SO2反应制得。请写出反应的离子方程式:
(4)有Fe2+、NO
 、Fe3+、NH
、Fe3+、NH 、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,则该反应中还原剂与氧化剂的物质的量之比为
、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,则该反应中还原剂与氧化剂的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】氯气可用于制备多种消毒剂,消毒泡腾片。如“84”消毒液。漂白粉等。其中 是最新一代安全环保型高效杀菌消毒剂。含氯消毒剂可用于对生活用水受到污染的地区的饮用水或环境进行清毒。回答下列问题:
是最新一代安全环保型高效杀菌消毒剂。含氯消毒剂可用于对生活用水受到污染的地区的饮用水或环境进行清毒。回答下列问题:
(1)若将 通入紫色石蕊试液中。观察到的现象为
通入紫色石蕊试液中。观察到的现象为___________
(2) 中氯的化合价为
中氯的化合价为___________ 价。我国广泛采用经干燥空气稀释的氯气通入填有固体亚氯酸钠( )的柱内的方法制得
)的柱内的方法制得 ,发生反应的化学方程式为
,发生反应的化学方程式为___________ ,从氧化还原反应角度分析。在该反应中 的作用是
的作用是___________ ;每生成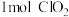 转移的电子数为
转移的电子数为___________  。
。
(3)工业上制取漂白粉的化学方程式为___________ 。若制取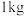 漂白粉(有效成分含量为
漂白粉(有效成分含量为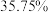 )。则至少需要标准状况下
)。则至少需要标准状况下 的体积为
的体积为___________ L。
 是最新一代安全环保型高效杀菌消毒剂。含氯消毒剂可用于对生活用水受到污染的地区的饮用水或环境进行清毒。回答下列问题:
是最新一代安全环保型高效杀菌消毒剂。含氯消毒剂可用于对生活用水受到污染的地区的饮用水或环境进行清毒。回答下列问题:(1)若将
 通入紫色石蕊试液中。观察到的现象为
通入紫色石蕊试液中。观察到的现象为(2)
 中氯的化合价为
中氯的化合价为 )的柱内的方法制得
)的柱内的方法制得 ,发生反应的化学方程式为
,发生反应的化学方程式为 的作用是
的作用是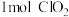 转移的电子数为
转移的电子数为 。
。(3)工业上制取漂白粉的化学方程式为
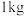 漂白粉(有效成分含量为
漂白粉(有效成分含量为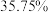 )。则至少需要标准状况下
)。则至少需要标准状况下 的体积为
的体积为
您最近一年使用:0次
【推荐2】有下列三个反应:
a.2FeCl3 + 2KI=2FeC12+ 2KCl +I2
b.2FeC12+ Cl2=2FeCl3
c.2KMnO4+ 16HCl(浓)= 2KC1 + 2MnC12+ 5Cl2↑+8H2O
(1)上述三个反应中氧化剂氧化性强弱关系为___________ 。
(2)在反应c中,若被氧化的HCl为1.5mol,则转移的电子数是___________ 个。
a.2FeCl3 + 2KI=2FeC12+ 2KCl +I2
b.2FeC12+ Cl2=2FeCl3
c.2KMnO4+ 16HCl(浓)= 2KC1 + 2MnC12+ 5Cl2↑+8H2O
(1)上述三个反应中氧化剂氧化性强弱关系为
(2)在反应c中,若被氧化的HCl为1.5mol,则转移的电子数是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】钠及其化合物在生活生产中应用广泛,下面是一些它们的具体应用及反应原理。
①碳酸氢钠作食品膨松剂: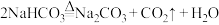
②氢化钠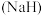 可用作野外生氢剂:
可用作野外生氢剂: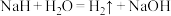
③钠单质组成“可呼吸”的 充电电池:
充电电池: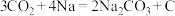
④饱和食盐水作侯氏制碱原料: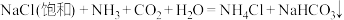
⑤电解饱和食盐水制备氯气和氢氧化钠(氯碱工业):
⑥高铁酸钠 可同时消毒和净水:
可同时消毒和净水: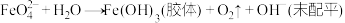
回答下列问题:
(1)以上反应中不属于氧化还原反应的是___________ (填标号)。
(2)钠是一种很活泼的金属,可用石蜡封存,实验室少量 保存于
保存于___________ 中(填字母)。
A.细沙 B.水 C.煤油
(3)野外生氢剂 中氢元素的化合价为
中氢元素的化合价为___________ 价,常用作___________ (填“氧化剂”或“还原剂”)。
(4)“可呼吸” 充电电池消耗
充电电池消耗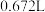 (标准状况)
(标准状况) 气体时,转移电子数为
气体时,转移电子数为_____  。
。
(5)氯碱工业生产中会使用阳离子交换膜,目的之一是将 溶液和
溶液和 分隔开,若未分隔开,两者会发生反应,该反应的化学反应方程式为
分隔开,若未分隔开,两者会发生反应,该反应的化学反应方程式为___________ 。
(6)请配平高铁酸钠 (
( 为
为 价)在水中发生反应的离子反应方程式:
价)在水中发生反应的离子反应方程式:___________ 。
并比较氧化性强弱:
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
①碳酸氢钠作食品膨松剂:
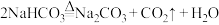
②氢化钠
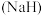 可用作野外生氢剂:
可用作野外生氢剂: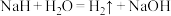
③钠单质组成“可呼吸”的
 充电电池:
充电电池: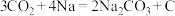
④饱和食盐水作侯氏制碱原料:
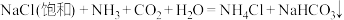
⑤电解饱和食盐水制备氯气和氢氧化钠(氯碱工业):

⑥高铁酸钠
 可同时消毒和净水:
可同时消毒和净水: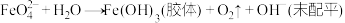
回答下列问题:
(1)以上反应中不属于氧化还原反应的是
(2)钠是一种很活泼的金属,可用石蜡封存,实验室少量
 保存于
保存于A.细沙 B.水 C.煤油
(3)野外生氢剂
 中氢元素的化合价为
中氢元素的化合价为(4)“可呼吸”
 充电电池消耗
充电电池消耗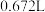 (标准状况)
(标准状况) 气体时,转移电子数为
气体时,转移电子数为 。
。(5)氯碱工业生产中会使用阳离子交换膜,目的之一是将
 溶液和
溶液和 分隔开,若未分隔开,两者会发生反应,该反应的化学反应方程式为
分隔开,若未分隔开,两者会发生反应,该反应的化学反应方程式为(6)请配平高铁酸钠
 (
( 为
为 价)在水中发生反应的离子反应方程式:
价)在水中发生反应的离子反应方程式:
并比较氧化性强弱:

 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
您最近一年使用:0次



