硝酸是一种具有强氧化性、腐蚀性的强酸,其还原产物因硝酸浓度的不同而有变化,从总体上说,硝酸浓度越高,平均每分子硝酸得到的电子数越少,浓硝酸的还原产物主要为 、稀硝酸的还原产物为
、稀硝酸的还原产物为 。实验室中,常用
。实验室中,常用 与浓
与浓 反应制取
反应制取 ,用
,用 与稀
与稀 反应制取
反应制取 。
。
(1)浓硝酸具有以下性质:①强氧化性②酸性③还原性④不稳定性⑤挥发性,下列反应或者现象主要体现了硝酸的什么性质:
①久置浓硝酸显黄色___________ (填序号,下同),请写出反应的化学方程式___________ 。
②用稀硝酸清洗试管壁上的银___________ 。
(2) 与适量的浓
与适量的浓 反应,铜全部作用后,共收集到
反应,铜全部作用后,共收集到 气体(标准状况下),反应中消耗的
气体(标准状况下),反应中消耗的 的物质的量是___________(填字母代号)。
的物质的量是___________(填字母代号)。
(3)硝酸的还原产物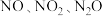 等对环境均有副作用,为了可持续发展,当今社会提出的一个新概念:“绿色化学”,它要求从经济、环保和技术上设计可行的化学反应,则下列由单质钢制取硝酸铜的方法可行且符合“绿色化学”的是_______ (填字母代号)。
等对环境均有副作用,为了可持续发展,当今社会提出的一个新概念:“绿色化学”,它要求从经济、环保和技术上设计可行的化学反应,则下列由单质钢制取硝酸铜的方法可行且符合“绿色化学”的是_______ (填字母代号)。
(4)实际上硝酸不仅可被还原为 或
或 ,浓度更稀时硝酸还可以被还原为
,浓度更稀时硝酸还可以被还原为 等,锌与很稀的硝酸反应生成硝酸锌、硝酸铵和水,写出该反应的化学方程式
等,锌与很稀的硝酸反应生成硝酸锌、硝酸铵和水,写出该反应的化学方程式___________ ,当生成 硝酸锌时,被还原的硝酸的物质的量为
硝酸锌时,被还原的硝酸的物质的量为___________ 。
(5)汽车彻底改变了我们生活,成为我们的不可成缺的交通工具之一,汽车尾气系统中的催化转化器,可有效降低尾气中的 和
和 等向大气的排放,在催化转化器的前半部发生的反应为
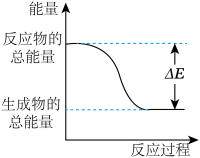
等向大气的排放,在催化转化器的前半部发生的反应为 ,已知汽车尾气处理反应能量过程如下图,下列说法正确的是___________。
,已知汽车尾气处理反应能量过程如下图,下列说法正确的是___________。
 、稀硝酸的还原产物为
、稀硝酸的还原产物为 。实验室中,常用
。实验室中,常用 与浓
与浓 反应制取
反应制取 ,用
,用 与稀
与稀 反应制取
反应制取 。
。(1)浓硝酸具有以下性质:①强氧化性②酸性③还原性④不稳定性⑤挥发性,下列反应或者现象主要体现了硝酸的什么性质:
①久置浓硝酸显黄色
②用稀硝酸清洗试管壁上的银
(2)
 与适量的浓
与适量的浓 反应,铜全部作用后,共收集到
反应,铜全部作用后,共收集到 气体(标准状况下),反应中消耗的
气体(标准状况下),反应中消耗的 的物质的量是___________(填字母代号)。
的物质的量是___________(填字母代号)。A. | B. | C. | D. |
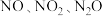 等对环境均有副作用,为了可持续发展,当今社会提出的一个新概念:“绿色化学”,它要求从经济、环保和技术上设计可行的化学反应,则下列由单质钢制取硝酸铜的方法可行且符合“绿色化学”的是_______ (填字母代号)。
等对环境均有副作用,为了可持续发展,当今社会提出的一个新概念:“绿色化学”,它要求从经济、环保和技术上设计可行的化学反应,则下列由单质钢制取硝酸铜的方法可行且符合“绿色化学”的是_______ (填字母代号)。A.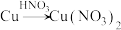 |
B. |
C.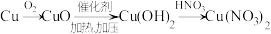 |
D.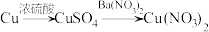 |
 或
或 ,浓度更稀时硝酸还可以被还原为
,浓度更稀时硝酸还可以被还原为 等,锌与很稀的硝酸反应生成硝酸锌、硝酸铵和水,写出该反应的化学方程式
等,锌与很稀的硝酸反应生成硝酸锌、硝酸铵和水,写出该反应的化学方程式 硝酸锌时,被还原的硝酸的物质的量为
硝酸锌时,被还原的硝酸的物质的量为(5)汽车彻底改变了我们生活,成为我们的不可成缺的交通工具之一,汽车尾气系统中的催化转化器,可有效降低尾气中的
 和
和 等向大气的排放,在催化转化器的前半部发生的反应为
等向大气的排放,在催化转化器的前半部发生的反应为 ,已知汽车尾气处理反应能量过程如下图,下列说法正确的是___________。
,已知汽车尾气处理反应能量过程如下图,下列说法正确的是___________。
| A.该反应为放热反应 | B.该反应为吸热反应 |
C.形成 化学键需要吸收热量 化学键需要吸收热量 | D.反应物的总能量小于生成物的总能量 |
更新时间:2023-05-17 09:01:09
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】完成并配平下列化学方程式__ FeO +__ HNO3——___ Fe(NO3)3 +___ NO↑+__ ____ ,该反应中氧化剂是________ ,当生成2mol NO时,转移的电子数为________ NA。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】氮化镓(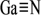 )材料具有低的热产生率和高的击穿电场,是制造大功率和高频微波电子器件的理想半导体材料。
)材料具有低的热产生率和高的击穿电场,是制造大功率和高频微波电子器件的理想半导体材料。
已知:①Ga和Al同主族且相邻,化学性质与铝相似;②在室温下,氮化镓不溶于水,硬度高,熔点高,能与热的碱溶液缓慢反应。
(1)配平氮化镓制备的化学方程式:□Ga(l)+□NH3(g)⇌□GaN(s)+□H2(g)+QkJ(Q>0)_____________
(2)上述反应的平衡常数表达式K=_____________ ;在恒温恒容密闭容器中制备氮化镓,下列有关说法正确的是_____________
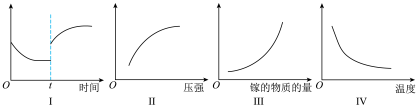
A.Ⅰ图像中如果纵坐标为正反应速率,则t时刻改变的条件可能是加压
B.Ⅱ图像中纵坐标可以为镓的转化率
C.Ⅲ图像中纵坐标可以为化学反应速率
D.Ⅳ图像中纵坐标可以为平衡常数
(3)Ga最外层电子的核外电子排布式___________________ ,N核外能量最高的电子亚层上电子云空间伸展方向有_____________ 种;
(4)氮化镓的晶体类型_____________ ,氮化铝和氮化镓晶体类型相同,且结构相似,比较两者熔点的高低并解释原因_____________________________________________________________ ;
(5)写出氮化镓溶于热的NaOH溶液的离子方程式____________________________________ 。
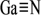 )材料具有低的热产生率和高的击穿电场,是制造大功率和高频微波电子器件的理想半导体材料。
)材料具有低的热产生率和高的击穿电场,是制造大功率和高频微波电子器件的理想半导体材料。已知:①Ga和Al同主族且相邻,化学性质与铝相似;②在室温下,氮化镓不溶于水,硬度高,熔点高,能与热的碱溶液缓慢反应。
(1)配平氮化镓制备的化学方程式:□Ga(l)+□NH3(g)⇌□GaN(s)+□H2(g)+QkJ(Q>0)
(2)上述反应的平衡常数表达式K=

A.Ⅰ图像中如果纵坐标为正反应速率,则t时刻改变的条件可能是加压
B.Ⅱ图像中纵坐标可以为镓的转化率
C.Ⅲ图像中纵坐标可以为化学反应速率
D.Ⅳ图像中纵坐标可以为平衡常数
(3)Ga最外层电子的核外电子排布式
(4)氮化镓的晶体类型
(5)写出氮化镓溶于热的NaOH溶液的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】某班同学用如下实验探究 、
、 的性质。请回答下列问题:
的性质。请回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1 的溶液。在FeCl2溶液中需加入少量铁屑,其目的是
的溶液。在FeCl2溶液中需加入少量铁屑,其目的是___________ ;
(2)甲组同学在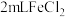 溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和1滴
溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和1滴 溶液,溶液变红,发生反应的离子方程式为
溶液,溶液变红,发生反应的离子方程式为___________ ;
(3)乙组同学向盛有H2O2溶液的试管和加入几滴酸化的 溶液,溶液变成棕黄色,发生反应的离子方程式为
溶液,溶液变成棕黄色,发生反应的离子方程式为___________ ;一段时间后,溶液中有气泡出现,并放热,随后有红褐色沉淀生成。产生气泡的原因是___________ ;生成沉淀的原因是(用平衡移动原理解)___________ 。
(4)丙组同学模拟工业上用 和废液制备
和废液制备 溶液。
溶液。
①若酸性 废液中:
废液中: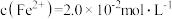 ,
,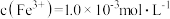 ,
,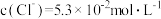 ,则该溶液的pH约为
,则该溶液的pH约为___________ 。
②完成 氧化
氧化 的离子方程式:
的离子方程式:____________
___________ +___________Fe2++___________→___________Cl-+___________
+___________Fe2++___________→___________Cl-+___________ +___________。
+___________。
③若该组同学在处理废水时消耗浓度为0.15 的
的 500mL,则该反应转移的电子数目为
500mL,则该反应转移的电子数目为___________ 。
 、
、 的性质。请回答下列问题:
的性质。请回答下列问题:(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1
 的溶液。在FeCl2溶液中需加入少量铁屑,其目的是
的溶液。在FeCl2溶液中需加入少量铁屑,其目的是(2)甲组同学在
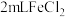 溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和1滴
溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和1滴 溶液,溶液变红,发生反应的离子方程式为
溶液,溶液变红,发生反应的离子方程式为(3)乙组同学向盛有H2O2溶液的试管和加入几滴酸化的
 溶液,溶液变成棕黄色,发生反应的离子方程式为
溶液,溶液变成棕黄色,发生反应的离子方程式为(4)丙组同学模拟工业上用
 和废液制备
和废液制备 溶液。
溶液。①若酸性
 废液中:
废液中: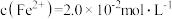 ,
,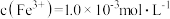 ,
,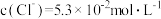 ,则该溶液的pH约为
,则该溶液的pH约为②完成
 氧化
氧化 的离子方程式:
的离子方程式:___________
 +___________Fe2++___________→___________Cl-+___________
+___________Fe2++___________→___________Cl-+___________ +___________。
+___________。③若该组同学在处理废水时消耗浓度为0.15
 的
的 500mL,则该反应转移的电子数目为
500mL,则该反应转移的电子数目为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下面三个方法都可以用来制氯气:
①4HCl(浓)+MnO2 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
②KClO3+6HCl(浓)=3Cl2↑+KCl+3H2O
③KMnO4+HCl(浓)——KCl+MnCl2+Cl2↑+H2O(未配平)
根据以上三个反应,回答下列有关问题:
(1)反应②中,氧化产物与还原产物的质量比为_______ 。
(2)若要制得相同质量的氯气,①②③反应中电子转移的数目之比为_______ 。
(3)请用双线桥表示反应②的电子转移情况_______ 。
KClO3+6HCl(浓)=3Cl2↑+KCl+3H2O
(4)请将反应③配平:_______ 。
_______KMnO4+_______HCl(浓)=_______KCl+_______MnCl2+_______Cl2↑+_______H2O。
(5)将离子方程式补充完成并配平:_______ 。
_______Ag++_______H3PO2+_______H2O=_______Ag↓+_______H3PO4+_______ _______。
(6)工业废水中的Cr2O 有毒,常在酸性条件下用Fe2+做处理剂,将Cr2O
有毒,常在酸性条件下用Fe2+做处理剂,将Cr2O 转化为Cr3+,反应的离子方程式
转化为Cr3+,反应的离子方程式_______ 。
(7)在碱性条件下,Cl2可将废水中的CN-氧化为无毒的CO2、N2,该过程中反应的离子方程式为_______ 。
①4HCl(浓)+MnO2
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O②KClO3+6HCl(浓)=3Cl2↑+KCl+3H2O
③KMnO4+HCl(浓)——KCl+MnCl2+Cl2↑+H2O(未配平)
根据以上三个反应,回答下列有关问题:
(1)反应②中,氧化产物与还原产物的质量比为
(2)若要制得相同质量的氯气,①②③反应中电子转移的数目之比为
(3)请用双线桥表示反应②的电子转移情况
KClO3+6HCl(浓)=3Cl2↑+KCl+3H2O
(4)请将反应③配平:
_______KMnO4+_______HCl(浓)=_______KCl+_______MnCl2+_______Cl2↑+_______H2O。
(5)将离子方程式补充完成并配平:
_______Ag++_______H3PO2+_______H2O=_______Ag↓+_______H3PO4+_______ _______。
(6)工业废水中的Cr2O
 有毒,常在酸性条件下用Fe2+做处理剂,将Cr2O
有毒,常在酸性条件下用Fe2+做处理剂,将Cr2O 转化为Cr3+,反应的离子方程式
转化为Cr3+,反应的离子方程式(7)在碱性条件下,Cl2可将废水中的CN-氧化为无毒的CO2、N2,该过程中反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某一反应体系中有反应物和生成物共八种物质:KMnO4、SO2、CuS、H2SO4、CuSO4、K2SO4、MnSO4、H2O。反应中氧化过程如下:CuS→SO2。
(1)该反应中被还原的元素是___________ ,CuS发生氧化反应的实质是__________ 。
(2)若反应过程中转移了3 mol电子,则参加反应的CuS的物质的量为________ mol。
(3)写出并配平该反应的化学方程式________________________________________ 。
(4)当KMnO4过量时,KMnO4会继续与SO2发生如下反应:
2KMnO4+5SO2+2H2O=2H2SO4+K2SO4+2MnSO4
该反应中氧化产物与还原产物的物质的量之比为_______ 。
(1)该反应中被还原的元素是
(2)若反应过程中转移了3 mol电子,则参加反应的CuS的物质的量为
(3)写出并配平该反应的化学方程式
(4)当KMnO4过量时,KMnO4会继续与SO2发生如下反应:
2KMnO4+5SO2+2H2O=2H2SO4+K2SO4+2MnSO4
该反应中氧化产物与还原产物的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】大气污染越来越成为人们关注的问题,烟气中的NOx必须脱除(即脱硝)后才能排放,脱硝的方法有多种。
完成下列填空:
Ⅰ直接脱硝
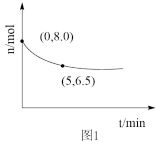
(1)NO在催化剂作用下分解为氮气和氧气。在10L密闭容器中,NO经直接脱硝反应时,其物质的量变化如图1所示。则0~5min内氧气的平均反应速率为___ mol/(L•min)。
Ⅱ臭氧脱硝
(2)O3氧化NO结合水洗可完全转化为HNO3,此时O3与NO的物质的量之比为___ 。
Ⅲ氨气脱硝
(3)实验室制取纯净的氨气,除了氯化铵外,还需要___ 、___ (填写试剂名称)。不使用碳酸铵的原因是___ (用化学方程式表示)。
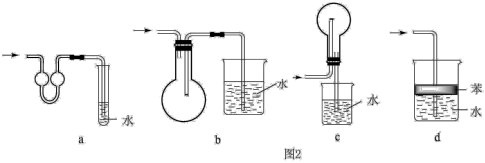
(4)吸收氨气时,常使用防倒吸装置,图2装置不能达到此目的是___ 。
NH3脱除烟气中NO的原理如图3:
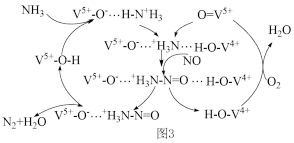
(5)该脱硝原理中,NO最终转化为___ (填化学式)和H2O。当消耗1molNH3和0.25molO2时,除去的NO在标准状况下的体积为___ L。
完成下列填空:
Ⅰ直接脱硝
(1)NO在催化剂作用下分解为氮气和氧气。在10L密闭容器中,NO经直接脱硝反应时,其物质的量变化如图1所示。则0~5min内氧气的平均反应速率为

Ⅱ臭氧脱硝
(2)O3氧化NO结合水洗可完全转化为HNO3,此时O3与NO的物质的量之比为
Ⅲ氨气脱硝
(3)实验室制取纯净的氨气,除了氯化铵外,还需要
(4)吸收氨气时,常使用防倒吸装置,图2装置不能达到此目的是

NH3脱除烟气中NO的原理如图3:

(5)该脱硝原理中,NO最终转化为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】如图是氨元素的几种价态与物质类别的对应关系:

回答下列问题:
(1)写出氮元素在元素周期表的位置_______ 。
(2)从氢元素化合价分析, 具有氧化性和还原性。写出
具有氧化性和还原性。写出 生成A的化学反应方程式:
生成A的化学反应方程式:_______ ,这个反应 体现了
体现了_______ 性。
(3) 与图中的物质C常用于检验
与图中的物质C常用于检验 的存在,则C的化学式为
的存在,则C的化学式为_______ 。写出用C检验 的存在的离子方程式
的存在的离子方程式_______ 。
(4)物质B为氮元素的气态氢化物,B的化学式为_______ ;实验室制取B的化学方程式为_______ 。
(5)浓硝酸与木炭在加热条件下反应的化学方程式为_______ 。

回答下列问题:
(1)写出氮元素在元素周期表的位置
(2)从氢元素化合价分析,
 具有氧化性和还原性。写出
具有氧化性和还原性。写出 生成A的化学反应方程式:
生成A的化学反应方程式: 体现了
体现了(3)
 与图中的物质C常用于检验
与图中的物质C常用于检验 的存在,则C的化学式为
的存在,则C的化学式为 的存在的离子方程式
的存在的离子方程式(4)物质B为氮元素的气态氢化物,B的化学式为
(5)浓硝酸与木炭在加热条件下反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】含氨污染物治理及其回收利用是重要课题。
(1)用碱液脱硝是目前研究的课题之一。将 通入石灰乳中可制备重要的工业原料
通入石灰乳中可制备重要的工业原料 。该工艺需控制
。该工艺需控制 和
和 物质的量之比接近
物质的量之比接近 。若
。若 ,则会导致
,则会导致___________ 。若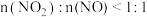 ,则会导致
,则会导致___________ 。
(2)用尿素 (N元素为
(N元素为 价)吸收氮氧化物是一种可行的方法。尿素在高温条存下与
价)吸收氮氧化物是一种可行的方法。尿素在高温条存下与 反应转化成无毒气体,该反应的化学方程式:
反应转化成无毒气体,该反应的化学方程式:___________ 。
(3)工业上在催化剂作用下用 还原工业废气中所含少量
还原工业废气中所含少量 生成
生成 和
和 达到脱除目的,但当温度高于
达到脱除目的,但当温度高于 时,
时, 脱除率下降,原因可能是
脱除率下降,原因可能是___________ 。
(4)用纳米铁粉处理废水中的 :
:
①酸性条件下,纳米铁粉与废水中 反应生成
反应生成 与
与 ,其反应的离子方程式是
,其反应的离子方程式是___________ 。
②研究发现,废水中溶解氧会对 的去除产生一定影响。在初始
的去除产生一定影响。在初始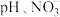 初始浓度、纳米铁粉与硝酸盐质量比均一定的条件下,有氧与无氧条作下
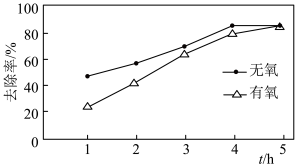
初始浓度、纳米铁粉与硝酸盐质量比均一定的条件下,有氧与无氧条作下 的去除率随反应时间的变化如图所示。
的去除率随反应时间的变化如图所示。 时,有氧条件下
时,有氧条件下 去除率低于无氧条件下,其可能的原因是
去除率低于无氧条件下,其可能的原因是___________ 。
(5)将 铜与
铜与 一定浓度的硝酸反应,铜完全溶解,产生的气体为
一定浓度的硝酸反应,铜完全溶解,产生的气体为 和
和 混合气体,其在标准状况下的体积为
混合气体,其在标准状况下的体积为 ,则混合气体中
,则混合气体中 的体积为
的体积为___________ 。(写出计算过程)
(1)用碱液脱硝是目前研究的课题之一。将
 通入石灰乳中可制备重要的工业原料
通入石灰乳中可制备重要的工业原料 。该工艺需控制
。该工艺需控制 和
和 物质的量之比接近
物质的量之比接近 。若
。若 ,则会导致
,则会导致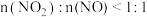 ,则会导致
,则会导致(2)用尿素
 (N元素为
(N元素为 价)吸收氮氧化物是一种可行的方法。尿素在高温条存下与
价)吸收氮氧化物是一种可行的方法。尿素在高温条存下与 反应转化成无毒气体,该反应的化学方程式:
反应转化成无毒气体,该反应的化学方程式:(3)工业上在催化剂作用下用
 还原工业废气中所含少量
还原工业废气中所含少量 生成
生成 和
和 达到脱除目的,但当温度高于
达到脱除目的,但当温度高于 时,
时, 脱除率下降,原因可能是
脱除率下降,原因可能是(4)用纳米铁粉处理废水中的
 :
:①酸性条件下,纳米铁粉与废水中
 反应生成
反应生成 与
与 ,其反应的离子方程式是
,其反应的离子方程式是②研究发现,废水中溶解氧会对
 的去除产生一定影响。在初始
的去除产生一定影响。在初始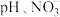 初始浓度、纳米铁粉与硝酸盐质量比均一定的条件下,有氧与无氧条作下
初始浓度、纳米铁粉与硝酸盐质量比均一定的条件下,有氧与无氧条作下 的去除率随反应时间的变化如图所示。
的去除率随反应时间的变化如图所示。 时,有氧条件下
时,有氧条件下 去除率低于无氧条件下,其可能的原因是
去除率低于无氧条件下,其可能的原因是
(5)将
 铜与
铜与 一定浓度的硝酸反应,铜完全溶解,产生的气体为
一定浓度的硝酸反应,铜完全溶解,产生的气体为 和
和 混合气体,其在标准状况下的体积为
混合气体,其在标准状况下的体积为 ,则混合气体中
,则混合气体中 的体积为
的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】化学反应中伴随着能量的变化。
(1)下列变化中属于吸热反应的是_______(填字母)。
①液态水汽化 ②将胆矾加热变为白色粉末 ③苛性钠固体溶于水 ④氯酸钾分解制氧气 ⑤生石灰跟水反应生成熟石灰 ⑥干冰升华
(2)断开 键、
键、 键、
键、 键分别需要吸收的能量为436kJ、391 kJ、946 kJ,则
键分别需要吸收的能量为436kJ、391 kJ、946 kJ,则 生成
生成 理论上能
理论上能_______ (填“吸收”或“放出”)能量_______ kJ。
(1)下列变化中属于吸热反应的是_______(填字母)。
①液态水汽化 ②将胆矾加热变为白色粉末 ③苛性钠固体溶于水 ④氯酸钾分解制氧气 ⑤生石灰跟水反应生成熟石灰 ⑥干冰升华
| A.①② | B.②④ | C.③ | D.①⑥ |
 键、
键、 键、
键、 键分别需要吸收的能量为436kJ、391 kJ、946 kJ,则
键分别需要吸收的能量为436kJ、391 kJ、946 kJ,则 生成
生成 理论上能
理论上能
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】2022年11月29日,神舟十五号载人飞船在酒泉卫星发射中心成功发射。11月30日,与神舟十四号航天员乘组在空间站胜利会师。
(1)搭载神舟十五号载人飞船的长征二号F遥十五运载火箭所用的燃料为偏二甲肼和四氧化二氮。
已知: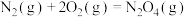


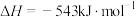
 和
和 反应的热化学方程式为:
反应的热化学方程式为:___________ 。
(2)可通过制备氨来进一步制取 。拆开
。拆开 共价键所需吸收的能量如下表:
共价键所需吸收的能量如下表:
① 和
和 完全反应为
完全反应为
_______ (填“吸收”或“放出”)________  能量。
能量。
②事实上,将 和
和 放入反应容器中,使它们充分反应,反应的热量变化总小于计算值,原因是
放入反应容器中,使它们充分反应,反应的热量变化总小于计算值,原因是___________ 。
(3)目前,大部分的载人航天器通过萨巴蒂尔循环实现元素的循环和能量的充分利用,其流程图为:

已知:25℃和 时,①
时,① 的燃烧热
的燃烧热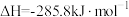 ;
;
② 的燃烧热
的燃烧热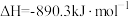 ;
;
③
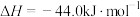 。
。
则萨巴蒂尔反应: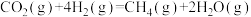 的
的
___________  。
。
(1)搭载神舟十五号载人飞船的长征二号F遥十五运载火箭所用的燃料为偏二甲肼和四氧化二氮。
已知:
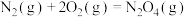


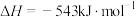
 和
和 反应的热化学方程式为:
反应的热化学方程式为:(2)可通过制备氨来进一步制取
 。拆开
。拆开 共价键所需吸收的能量如下表:
共价键所需吸收的能量如下表:| 共价键 |  |  |  |
吸收的能量 | 436 | 946 | 391 |
 和
和 完全反应为
完全反应为
 能量。
能量。②事实上,将
 和
和 放入反应容器中,使它们充分反应,反应的热量变化总小于计算值,原因是
放入反应容器中,使它们充分反应,反应的热量变化总小于计算值,原因是(3)目前,大部分的载人航天器通过萨巴蒂尔循环实现元素的循环和能量的充分利用,其流程图为:

已知:25℃和
 时,①
时,① 的燃烧热
的燃烧热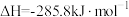 ;
;②
 的燃烧热
的燃烧热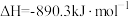 ;
;③

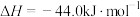 。
。则萨巴蒂尔反应:
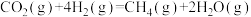 的
的
 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】能源是现代社会发展的支柱之一。请回答下列问题:
(1)化学反应中的能量变化,通常主要表现为热量的变化。
①下列反应中,属于放热反应的是___________ (填字母)。
a.Ba(OH)2·8H2O与NH4Cl混合搅拌
b.高温煅烧石灰石
c.铝与盐酸反应
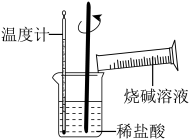
②某同学进行如图所示实验,测量稀盐酸与烧碱溶液中和反应的能量变化。实验表明:反应温度升高,由此判断该反应是__________ (填“吸热”或“放热”)反应,其离子方程式是____________ 。
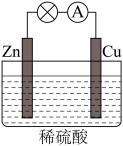
(2)电能是现代社会应用最广泛的能源之一。如图所示的原电池装置中,其负极是___________ ,正极上 能够观察到的现象是____________________ ,正极的电极反应式是___________________ 。原电池工作一段时间后,若消耗锌6.5 g,则放出标准状况下气体__________ L。
(1)化学反应中的能量变化,通常主要表现为热量的变化。
①下列反应中,属于放热反应的是
a.Ba(OH)2·8H2O与NH4Cl混合搅拌
b.高温煅烧石灰石
c.铝与盐酸反应
②某同学进行如图所示实验,测量稀盐酸与烧碱溶液中和反应的能量变化。实验表明:反应温度升高,由此判断该反应是

(2)电能是现代社会应用最广泛的能源之一。如图所示的原电池装置中,其负极是

您最近一年使用:0次



