现有下列物质:①稀硫酸 ②NaHCO3固体 ③氨水 ④二氧化碳气体 ⑤FeCl3固体 ⑥NaOH溶液 ⑦硫酸亚铁溶液。
(1)能导电的物质序号为_______ 。
(2)属于电解质的物质序号为_______ 。
(3)既能与稀硫酸、又能与NaOH溶液发生化学反应的物质序号为_______ 。
(4)一定量的④与⑥充分反应后,向所得溶液中逐滴加入①,立刻有气体生成,生成气体的离子反应方程式为_______ 。
(5)实验室用⑤制备胶体的化学方程式为_______ 。胶体制备过程中不能搅拌,目的是防止_______ ,如果将1molFeCl3全部制成胶体,胶粒数目_______ NA(选填“大于”“等于”“小于”)。
(1)能导电的物质序号为
(2)属于电解质的物质序号为
(3)既能与稀硫酸、又能与NaOH溶液发生化学反应的物质序号为
(4)一定量的④与⑥充分反应后,向所得溶液中逐滴加入①,立刻有气体生成,生成气体的离子反应方程式为
(5)实验室用⑤制备胶体的化学方程式为
更新时间:2023-06-26 21:15:41
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】现有中学化学中常见的九种物质:
①氯酸钾固体 ②铜丝 ③Fe(OH)3胶体 ④纯醋酸 ⑤二氧化碳气体 ⑥碳酸氢钾固体 ⑦稀盐酸 ⑧蔗糖晶体 ⑨熔融氢氧化钡,请用上述序号填空:
(1)上述状态下可导电的是__________________ ,属于非电解质的是_______________________ 。
(2)写出⑥在水溶液中的电离方程式:________________________________________ 。
(3)制备③Fe(OH)3胶体的化学方程式:________________________________________ 。
(4)已知①和⑦的浓溶液可以反应:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O,当有10个电子发生转移后,被氧化的氯原子与被还原的氯原子的个数之比是__________________ 。
(5)少量⑥的溶液与大量⑨的溶液混合的离子方程式_______________________ 。
①氯酸钾固体 ②铜丝 ③Fe(OH)3胶体 ④纯醋酸 ⑤二氧化碳气体 ⑥碳酸氢钾固体 ⑦稀盐酸 ⑧蔗糖晶体 ⑨熔融氢氧化钡,请用上述序号填空:
(1)上述状态下可导电的是
(2)写出⑥在水溶液中的电离方程式:
(3)制备③Fe(OH)3胶体的化学方程式:
(4)已知①和⑦的浓溶液可以反应:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O,当有10个电子发生转移后,被氧化的氯原子与被还原的氯原子的个数之比是
(5)少量⑥的溶液与大量⑨的溶液混合的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题
(1)现有以下物质①NaCl溶液;②二氧化碳;③纯净的醋酸;④铜;⑤NaOH固体;⑥蔗糖;⑦硫酸钡;⑧水,属于电解质的是:_______ 。(填写序号)
(2)实验室常用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入某种物质M的饱和水溶液,继续煮沸可制得一种红褐色液体。
①物质M的化学式为_______ 。
②证明红褐色液体是胶体的实验操作是_______ 。
③物质M和红褐色液体的本质区别是_______ 。
(3)在实验室制氯气的反应中:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,氧化剂为
MnCl2+Cl2↑+2H2O,氧化剂为_______ ;氧化产物为_______ ;氧化剂与还原剂的分子个数比值为_______ 。
(4)目前,汽车尾气系统中安装了催化转化器。在催化转化器中汽车尾气中的CO和NO在催化剂的作用下发生反应,生成两种大气中常见的无污染气体。请写出反应的化学方程式:_______ 。
(1)现有以下物质①NaCl溶液;②二氧化碳;③纯净的醋酸;④铜;⑤NaOH固体;⑥蔗糖;⑦硫酸钡;⑧水,属于电解质的是:
(2)实验室常用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入某种物质M的饱和水溶液,继续煮沸可制得一种红褐色液体。
①物质M的化学式为
②证明红褐色液体是胶体的实验操作是
③物质M和红褐色液体的本质区别是
(3)在实验室制氯气的反应中:MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O,氧化剂为
MnCl2+Cl2↑+2H2O,氧化剂为(4)目前,汽车尾气系统中安装了催化转化器。在催化转化器中汽车尾气中的CO和NO在催化剂的作用下发生反应,生成两种大气中常见的无污染气体。请写出反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】按要求填空:
(1)现有下列物质,请用序号填空:
①硫酸钡②固体氢氧化钠③熔融氯化钠④稀盐酸⑤氨水⑥蔗糖⑦二氧化硫
上述状态下可导电的是___________ 。属于电解质的是___________ 。属于非电解质的是___________ 。
(2)向 沸水中加入
沸水中加入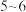 滴饱和
滴饱和 溶液,加热至产生红褐色液体,停止加热,利用
溶液,加热至产生红褐色液体,停止加热,利用___________ 来证明得到的分散系是氢氧化铁胶体,生成胶体的化学方程式为___________ 。
(3)已知:Ⅰ. ;
;
Ⅱ. ;
;
Ⅲ. 。
。
可推知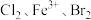 氧化性由强到弱为
氧化性由强到弱为___________ 。若反应Ⅰ中共转移 电子,则消耗标准状况下
电子,则消耗标准状况下 的体积为
的体积为___________ 。
(1)现有下列物质,请用序号填空:
①硫酸钡②固体氢氧化钠③熔融氯化钠④稀盐酸⑤氨水⑥蔗糖⑦二氧化硫
上述状态下可导电的是
(2)向
 沸水中加入
沸水中加入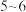 滴饱和
滴饱和 溶液,加热至产生红褐色液体,停止加热,利用
溶液,加热至产生红褐色液体,停止加热,利用(3)已知:Ⅰ.
 ;
;Ⅱ.
 ;
;Ⅲ.
 。
。可推知
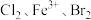 氧化性由强到弱为
氧化性由强到弱为 电子,则消耗标准状况下
电子,则消耗标准状况下 的体积为
的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】Ⅰ.如图是一种“纳米药物分子运输车”,该技术可提高肿瘤的治疗效果。回答下列问题:
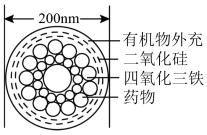
(1)“纳米药物分子车”分散于水中所得的分散系_______ (填“属于”或“不属于”)胶体。
(2)“纳米药物分子车”的外壳属于有机物。酒精、蔗糖、冰醋酸这三种有机物中,属于电解质的是_______ 。
(3)从元素组成的角度分析, 和
和 可归为同一类物质,其类别属于化合物中的
可归为同一类物质,其类别属于化合物中的_______ 。
(4)纳米级的 是一种非常重要的磁性材料。
是一种非常重要的磁性材料。 溶于稀盐酸生成
溶于稀盐酸生成 、
、_______ 和 。
。
Ⅱ.1L海水在逐渐浓缩过程中析出盐的种类和质量(单位:g)的关系如表所示:
注:画“-”的数据少于 ,可以忽略不计。
,可以忽略不计。
(5)从海水中获得粗盐,一般采用的方法是_______ 。
(6)根据表中数据,要获得杂质较少的食盐,应控制海水的最佳密度为 (填字母)。
(填字母)。
(7)粗盐中常含有 、
、 、
、 等杂质,要除去这些杂质,按顺序加入的试剂依次为
等杂质,要除去这些杂质,按顺序加入的试剂依次为 、
、 、
、_______ 、_______ 等(填化学式)。

(1)“纳米药物分子车”分散于水中所得的分散系
(2)“纳米药物分子车”的外壳属于有机物。酒精、蔗糖、冰醋酸这三种有机物中,属于电解质的是
(3)从元素组成的角度分析,
 和
和 可归为同一类物质,其类别属于化合物中的
可归为同一类物质,其类别属于化合物中的(4)纳米级的
 是一种非常重要的磁性材料。
是一种非常重要的磁性材料。 溶于稀盐酸生成
溶于稀盐酸生成 、
、 。
。Ⅱ.1L海水在逐渐浓缩过程中析出盐的种类和质量(单位:g)的关系如表所示:
海水密度( ) ) |  |  |  |  |  |
| 1.21 | 0.05 | 3.26 | 0.004 | 0.008 | - |
| 1.22 | 0.015 | 9.65 | 0.01 | 0.012 | - |
| 1.26 | 0.01 | 2.64 | 0.02 | 0.02 | 0.04 |
| 1.31 | - | 1.40 | 0.54 | 0.03 | 0.06 |
注:画“-”的数据少于
 ,可以忽略不计。
,可以忽略不计。(5)从海水中获得粗盐,一般采用的方法是
(6)根据表中数据,要获得杂质较少的食盐,应控制海水的最佳密度为
 (填字母)。
(填字母)。| A.1.21 | B.1.22 | C.1.26 | D.1.31 |
 、
、 、
、 等杂质,要除去这些杂质,按顺序加入的试剂依次为
等杂质,要除去这些杂质,按顺序加入的试剂依次为 、
、 、
、
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有下列九种物质:①乙醇②铝③CaO④CO2⑤氯化氢⑥澄清的石灰水⑦液氨⑧稀硝酸⑨熔融态的Fe2(SO4)3
(1)上述九种物质中,属于电解质的是___ (填序号),能导电的是___ (填序号)
(2)上述九种物质中有两种物质之间可发生离子反应:H++OH-=H2O,该离子反应对应的化学方程式为___ 。
(3)⑨在水中的电离方程式为___ ,20g⑨溶于水配成250mL溶液,所含阴离子的粒子数为___ ,阳离子的物质的量浓度为___ 。
(4)少量的④通入⑥的溶液中反应的离子方程式为___ 。
(1)上述九种物质中,属于电解质的是
(2)上述九种物质中有两种物质之间可发生离子反应:H++OH-=H2O,该离子反应对应的化学方程式为
(3)⑨在水中的电离方程式为
(4)少量的④通入⑥的溶液中反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】有下列物质:①石墨;②银;③氢氧化钠固体;④稀硫酸;⑤熔融氯化钾;⑥醋酸;⑦液态氯化氢;⑧硫酸钡;⑨氨气;⑩蔗糖。
其中能导电的有_____ ;属于电解质的有________ ;属于非电解质的有_______ .
其中能导电的有
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】现有几组物质的熔点(℃)数据:
据此回答下列问题:
(1)A组属于___________ 晶体,其熔化时克服的微粒间的作用力是___________ 。
(2)B组晶体属于___________ 晶体。
(3)C组晶体属于___________ 晶体,晶体含有的作用力有___________ 。
(4)D组晶体可能具有的性质是___________ (填序号)。
①硬度小②水溶液能导电③固体能导电④熔融状态能导电
| A组 | B组 | C组 | D组 |
| 金刚石:>3550 | Li:181 | HF:-84 | NaCl:801 |
| 硅晶体:1410 | Na:98 | HCl:-114 | KCl:776 |
| 硼晶体:2300 | K:64 | HBr:-87 | RbCl:718 |
| 二氧化硅:1723 | Rb:39 | HI:-51 | CsCl:645 |
据此回答下列问题:
(1)A组属于
(2)B组晶体属于
(3)C组晶体属于
(4)D组晶体可能具有的性质是
①硬度小②水溶液能导电③固体能导电④熔融状态能导电
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】①石墨、②氯化钠、③蔗糖、④稀硫酸、⑤NH4HSO4溶液、⑥碳酸氢钠、⑦氢氧化钡溶液、⑧冰醋酸、⑨氯化氢、⑩铜
(1)其中能导电的是___________ (填写序号,下同);属于电解质的是___________ ;属于非电解质的是___________ 。
(2)写出少量⑥和过量⑦在水中发生反应的离子方程式:___________ 。
(3)某兴趣小组的同学向一定体积的Ba(OH)2溶液中逐滴加入稀盐酸,并测得混合溶液的导电能力随时间变化的曲线如图所示,回答下列问题。
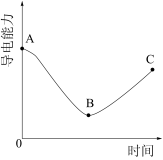
①AB段发生的反应的离子方程式为___________ 。
②B处Ba(OH)2溶液与稀盐酸恰好完全中和,此时溶液中主要存在的离子有___________ (填离子符号)。
③下列化学反应的实质与Ba(OH)2溶液与稀盐酸反应的实质相同的是___________ (填字母)。
A.Ba(OH)2和H2SO4 B.NaOH和H2SO4 C.KOH与HNO3
(1)其中能导电的是
(2)写出少量⑥和过量⑦在水中发生反应的离子方程式:
(3)某兴趣小组的同学向一定体积的Ba(OH)2溶液中逐滴加入稀盐酸,并测得混合溶液的导电能力随时间变化的曲线如图所示,回答下列问题。

①AB段发生的反应的离子方程式为
②B处Ba(OH)2溶液与稀盐酸恰好完全中和,此时溶液中主要存在的离子有
③下列化学反应的实质与Ba(OH)2溶液与稀盐酸反应的实质相同的是
A.Ba(OH)2和H2SO4 B.NaOH和H2SO4 C.KOH与HNO3
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】白居易《暮江吟》,“一道残阳铺水中,半江瑟瑟半江红。”诗句中“瑟瑟”指像绿松石似的碧绿色,绿松石的化学式为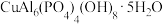 ,另含少量埃洛石(
,另含少量埃洛石(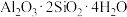 ),石英(
),石英( )、褐铁矿[
)、褐铁矿[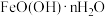 ]等杂质。回答下列问题:
]等杂质。回答下列问题:
(1) 在周期表中的位置为
在周期表中的位置为___________ ,离子半径
___________ (填“>”或“<”) 。
。
(2)检验绿松石含铜的较简单的方法是___________ ;若将绿松石写成氧化物形式(参照埃洛石),则理论上 的质量分数为
的质量分数为___________ %(结果保留三位有效数字)。
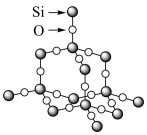
(3)已知 的结构如图所示。
的结构如图所示。 石英中含
石英中含 键的数目为
键的数目为___________ 。
(4)褐铁矿溶于稀硫酸的离子方程式为___________ 。
(5) 固态时是一种离子化合物,阳离子比阴离子少36个电子,阳离子中各原子均达到八电子稳定结构,该离子化合物的化学式为
固态时是一种离子化合物,阳离子比阴离子少36个电子,阳离子中各原子均达到八电子稳定结构,该离子化合物的化学式为___________ 。
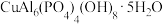 ,另含少量埃洛石(
,另含少量埃洛石(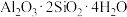 ),石英(
),石英( )、褐铁矿[
)、褐铁矿[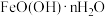 ]等杂质。回答下列问题:
]等杂质。回答下列问题:(1)
 在周期表中的位置为
在周期表中的位置为
 。
。(2)检验绿松石含铜的较简单的方法是
 的质量分数为
的质量分数为(3)已知
 的结构如图所示。
的结构如图所示。 石英中含
石英中含 键的数目为
键的数目为
(4)褐铁矿溶于稀硫酸的离子方程式为
(5)
 固态时是一种离子化合物,阳离子比阴离子少36个电子,阳离子中各原子均达到八电子稳定结构,该离子化合物的化学式为
固态时是一种离子化合物,阳离子比阴离子少36个电子,阳离子中各原子均达到八电子稳定结构,该离子化合物的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】下表是元素周期表的一部分,除标出的元素外,表中的每个编号代表一种元素,请根据要求回答问题:
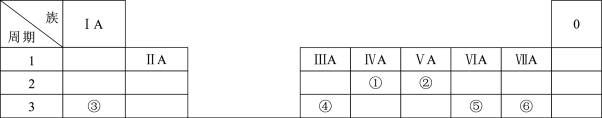
(1)②的原子结构示意图是_______ 。
(2)写出①的最高价氧化物的电子式:_______ 。
(3)⑤和⑥分别形成的最简单氢化物更稳定的是_______ (填化学式)。
(4)③对应的最高价氧化物形成的水化物与④形成的氧化物反应的离子方程式为_______ 。

(1)②的原子结构示意图是
(2)写出①的最高价氧化物的电子式:
(3)⑤和⑥分别形成的最简单氢化物更稳定的是
(4)③对应的最高价氧化物形成的水化物与④形成的氧化物反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐3】我国规定饮用水质量标准必须符合下列要求:
以下是源水处理成自来水的工艺流程示意图:

(1)源水中含Ca2+ 、Mg2+、HCO3-、Cl-等,加入石灰后生成Ca(OH)2,进而发生若干复分解反应,写出其中一个离子方程式 。
(2)凝聚剂除去悬浮固体颗粒的过程 (填写编号,多选倒扣分)
①只是物理过程 ②只是化学过程 ③是物理和化学过程
FeSO4.7H2O是常用的凝聚剂,它在水中最终生成 沉淀。
(3)通入二氧化碳的目的是 和 。
(4)气体A的作用是 。这种作用是基于气体A和水反应的产物具有 性
(5)下列物质中, 可以作为气体A的代用品。(填写编号,多选倒扣分)
①Ca(ClO)2 ②NH3 (液) ③K2FeO4 ④SO2
| pH | 6.5~6.8 |
| Ca2+、Mg2+总浓度 | <0.0045mol/L |
| 细菌总数 | <100个/L |
以下是源水处理成自来水的工艺流程示意图:

(1)源水中含Ca2+ 、Mg2+、HCO3-、Cl-等,加入石灰后生成Ca(OH)2,进而发生若干复分解反应,写出其中一个离子方程式 。
(2)凝聚剂除去悬浮固体颗粒的过程 (填写编号,多选倒扣分)
①只是物理过程 ②只是化学过程 ③是物理和化学过程
FeSO4.7H2O是常用的凝聚剂,它在水中最终生成 沉淀。
(3)通入二氧化碳的目的是 和 。
(4)气体A的作用是 。这种作用是基于气体A和水反应的产物具有 性
(5)下列物质中, 可以作为气体A的代用品。(填写编号,多选倒扣分)
①Ca(ClO)2 ②NH3 (液) ③K2FeO4 ④SO2
您最近一年使用:0次



