用0.1mol•L-1稀盐酸与锌反应制取氢气,不能使氢气生成速率增大的是
| A.对该反应体系加热 | B.不用锌片,改用锌粉 |
| C.加入少量NaCl溶液 | D.加入少量2mol•L-1硫酸 |
更新时间:2023-05-25 19:53:59
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】一定条件下将0.1 mol N2和0.3 mol H2置于密闭容器中发生反应:N2+3H2 2NH3。下列关于该反应的说法正确的是
2NH3。下列关于该反应的说法正确的是
 2NH3。下列关于该反应的说法正确的是
2NH3。下列关于该反应的说法正确的是| A.最终可生成0.2 mol NH3 |
| B.压缩体积,增大压强能使反应速率减小 |
| C.降低反应体系的温度能加快反应速率 |
| D.容器体积不变,向容器中再加入N2,能加快反应速率 |
您最近一年使用:0次
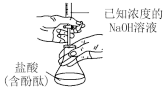
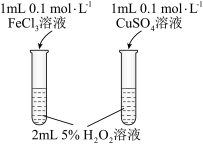
【推荐2】下列实验及相关叙述正确的是
 ① ① | 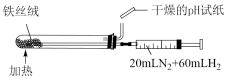 ② ② |
 ③ ③ | 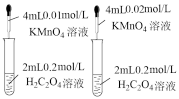 ④ ④ |
| A.滴定法用装置①测定盐酸的浓度 |
| B.可用装置②来合成氨并检验氨气的生成 |
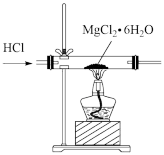
| C.用装置③能制取无水MgCl2 |
| D.装置④依据单位时间内颜色变化来比较浓度对反应速率的影响 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】一定量的稀盐酸与过量铁粉反应时,为了减缓反应速率,且又不影响生成氢气的总量,可向稀盐酸中加入
| A.NaOH固体 | B.CH3COONa固体 | C.NaCl固体 | D.CuCl2固体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某实验小组用0.1 mol/L Na2S2O3溶液和0.1 mol/L H2SO4溶液为反应物,探究外界条件对化学反应速率的影响,实验记录如下表。
已知:Na2S2O3 + H2SO4 = Na2SO4 + SO2 + S ↓+ H2O
实验结果:t1>t2>t3。下列说法不正确的是
已知:Na2S2O3 + H2SO4 = Na2SO4 + SO2 + S ↓+ H2O
| 实验序号 | 温度/℃ | Na2S2O3溶液体积/mL | H2SO4溶液体积/mL | H2O体积/mL | 出现沉淀所需的时间/s |
| Ⅰ | 20 | 5 | 5 | 10 | t1 |
| Ⅱ | 20 | 5 | 10 | a | t2 |
| Ⅲ | 60 | 5 | 5 | 10 | t3 |
| A.研究H2SO4浓度对该反应速率的影响,a = 5 |
| B.对比实验Ⅰ、Ⅱ可知,c (H2SO4) 越大,反应速率越快 |
| C.对比实验Ⅱ、Ⅲ可知,升高温度能加快该反应速率 |
| D.进行实验Ⅰ、Ⅱ时,依次向试管中加入Na2S2O3溶液、H2SO4溶液、H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列方案设计、现象和结论都正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 比较镁、铝元素的金属性强弱 | 分别将相同浓度的氢氧化钠溶液逐滴加入一定浓度的氯化镁、氯化铝溶液中,直至过量 | 均出现白色沉淀,氯化镁溶液中沉淀不溶解,氯化铝溶液中沉淀逐渐溶解。说明金属性镁比铝强 |
| B | 检验未知溶液中是否含有铵盐 | 取一定量未知液于试管中,滴入氢氧化钠溶液并加热,试管口放置湿润红色石蕊试纸 | 试纸变蓝。说明溶液中含有铵盐 |
| C | 探究浓度对反应速率的影响 | 两支试管中均装有2 mL 0.01 mol·L 酸性高锰酸钾溶液,向第一支加入2 mL 0.01 mol·L 酸性高锰酸钾溶液,向第一支加入2 mL 0.01 mol·L 草酸溶液、3 mL蒸馏水,第二支加入5 mL 0.01 mol/L)草酸溶液 草酸溶液、3 mL蒸馏水,第二支加入5 mL 0.01 mol/L)草酸溶液 | 第一支试管褪色时间比第二支试管长。说明其他条件相同时,反应物浓度越大,反应速率越快 |
| D | 检验丙烯醛中含有碳碳双键 | 取少量丙烯醛于试管中,先向其中加入足量新制氢氧化铜悬浊液并加热,静置后取上层清液,加入溴水 | 溴水褪色。说明丙烯醛中含碳碳双键 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】工业上主要利用碳热还原重晶石制得硫化钡,进而生产各种钡化合物。下图为不同反应温度下,实验中碳热还原硫酸钡反应体系的平衡组成随反应温度的变化关系。下列说法正确的是
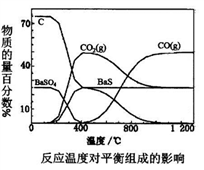

| A.约150℃,体系中开始出现BaS,说明温度越高反应速率越快 |
B.400℃时发生的化学反应方程式: BaSO4+2C BaS+2CO2 BaS+2CO2 |
| C.CO—定无法还原重晶石 |
| D.温度高于400℃后,硫酸钡才能转化为BaS |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】科学家结合实验与计算机模拟结果,研究出了均相催化的思维模型。总反应: (
( 为催化剂)①
为催化剂)①
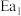 ,②
,②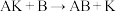
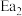
 (
( 为催化剂)①
为催化剂)①
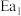 ,②
,②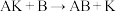
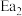
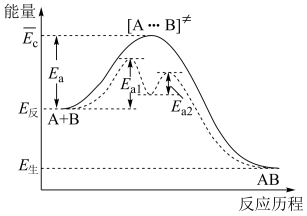
| A.第①步为决速步骤 |
| B.升高温度,该反应的速率加快 |
C.该反应的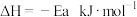 |
| D.加入催化剂,不能改变该化学反应的反应热 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】100mL 6mol.L-1的硫酸溶液与过量锌粉反应,在一定温度下为了减缓反应速率但又不影响生成氢气的总质量,可向反应物中加入适量的
| A.硝酸 | B.水 | C.硫酸氢钾 | D.氯化氢气体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】当其他条件不变时,下列说法正确的是
| A.加水稀释能减慢双氧水分解的反应速率 |
| B.用块状锌代替粉末状锌与稀硫酸反应能加快反应速率 |
| C.当反应物与生成物浓度相等时,反应达到限度 |
| D.在合成氨反应中,增大N2浓度一定可以使H2的转化率达到100% |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】H2O2分解速率受多种因素影响。实验测得 70 ℃时不同条件下H2O2浓度随时间的变化如图所示。下列说法不正确的是
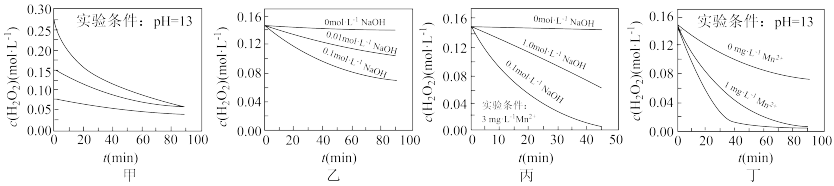

| A.图甲表明,其他条件相同时,H2O2浓度越大,其分解速率越快 |
| B.图乙表明,其他条件相同时,NaOH溶液浓度越小,H2O2分解速率越慢 |
| C.图丙表明,少量Mn2+存在时,溶液碱性越强,H2O2分解速率越快 |
| D.图丙和图丁表明,碱性溶液中,Mn2+对H2O2分解速率的影响大 |
您最近一年使用:0次




 溶液和稀硫酸各
溶液和稀硫酸各 ,加水
,加水 ,反应温度
,反应温度
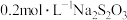 溶液和稀硫酸各
溶液和稀硫酸各



