如图为元素周期表的一部分。请回答下列问题:
(1)N的原子序数是___________ 。
(2)C、N和O三种元素中,非金属性最强的是___________ 。
(3)O和S的原子半径大小:O___________ S(填“>”或“<”)。
(4)S在空气中燃烧的化学方程式为___________ 。
| C | N | O |
| S |
(2)C、N和O三种元素中,非金属性最强的是
(3)O和S的原子半径大小:O
(4)S在空气中燃烧的化学方程式为
2023高一·湖南·学业考试 查看更多[3]
更新时间:2023-06-28 10:12:54
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】下表是元素周期表的一部分。
回答下列问题:
(1)元素①的名称是____ ,元素⑧的符号是____ 。
(2)在这些元素中,___ (用元素符号或化学式填写,下同)是最活泼的非金属元素,____ 是最不活泼的元素。
(3)这些元素的最高价氧化物对应的水化物中,____ 酸性最强,____ 碱性最强,具有两性的氢氧化物是____ 。
(4)比较⑤与⑥的化学性质,____ 更活泼,试用实验证明此结论(简述操作、现象和结论):________________________ 。
(5)⑦的最高价氧化物与⑤的最高价氧化物对应的水化物反应的离子方程式是______________________________________________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
回答下列问题:
(1)元素①的名称是
(2)在这些元素中,
(3)这些元素的最高价氧化物对应的水化物中,
(4)比较⑤与⑥的化学性质,
(5)⑦的最高价氧化物与⑤的最高价氧化物对应的水化物反应的离子方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】元素在周期表中的位置,反映了元素的原子结构和元素的性质。如图是元素周期表的一部分。
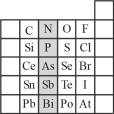
(1)阴影部分元素N在元素周期表中的位置为_____ 。根据元素周期律,预测酸性强弱:H3AsO4______ H3PO4(填“>”或“<”)。
(2)在一定条件下,S与H2反应有一定限度(可理解为反应进行的程度),请判断:在相同条件下Se与H2反应的程度比S与H2反应程度___ (填“更大”“更小”或“相同”)。
(3)下列说法错误的是______ (填序号)。
①C、N、O、F的原子半径随着原子序数的增大而减小
②Si、P、S、Cl元素的非金属性随着核电荷数的增加而增强
③干冰升华、液态水转变为气态水都要克服分子内的共价键
④HF、HCl、HBr、HI的热稳定性依次减弱

(1)阴影部分元素N在元素周期表中的位置为
(2)在一定条件下,S与H2反应有一定限度(可理解为反应进行的程度),请判断:在相同条件下Se与H2反应的程度比S与H2反应程度
(3)下列说法错误的是
①C、N、O、F的原子半径随着原子序数的增大而减小
②Si、P、S、Cl元素的非金属性随着核电荷数的增加而增强
③干冰升华、液态水转变为气态水都要克服分子内的共价键
④HF、HCl、HBr、HI的热稳定性依次减弱
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】1828年,德国化学家维勒在制备无机盐氰酸铵( )时得到尿素
)时得到尿素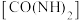 。尿素的人工合成,揭开了人工合成有机物的序幕。完成下列填空:
。尿素的人工合成,揭开了人工合成有机物的序幕。完成下列填空:
(1)将上述元素按原子半径由小到大的顺序排列________ 。(用元素符号表示)
(2)已知氰酸分子内含有叁键,且所有原子最外层均已达到稳定结构,试写出其结构式________ 。
(3) 性质与
性质与 相似,也可与硫酸反应生成
相似,也可与硫酸反应生成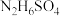 ,则
,则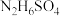 中存在的作用力为
中存在的作用力为________ ,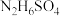 与强碱溶液反应的离子方程式为
与强碱溶液反应的离子方程式为________
(4)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸( )。
)。
①写出反应的化学方程式,并用单线桥标出电子转移方向与数目________ 。
②还原产物是________ ,若反应中有 个电子发生转移,参与反应的氨的质量为
个电子发生转移,参与反应的氨的质量为________ g。
 )时得到尿素
)时得到尿素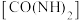 。尿素的人工合成,揭开了人工合成有机物的序幕。完成下列填空:
。尿素的人工合成,揭开了人工合成有机物的序幕。完成下列填空:(1)将上述元素按原子半径由小到大的顺序排列
(2)已知氰酸分子内含有叁键,且所有原子最外层均已达到稳定结构,试写出其结构式
(3)
 性质与
性质与 相似,也可与硫酸反应生成
相似,也可与硫酸反应生成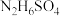 ,则
,则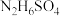 中存在的作用力为
中存在的作用力为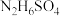 与强碱溶液反应的离子方程式为
与强碱溶液反应的离子方程式为(4)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(
 )。
)。①写出反应的化学方程式,并用单线桥标出电子转移方向与数目
②还原产物是
 个电子发生转移,参与反应的氨的质量为
个电子发生转移,参与反应的氨的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】元素周期表中第ⅦA族元素的单质及其化合物的用途广泛。工业上,通过如下转化可制得KClO3晶体:
(1) 与氯元素同族的短周期元素的原子核外电子排布式为______________________ 。
(2)上述转化过程中所涉及的短周期元素中,原子半径由大到小的顺序是______________ 。
(3)硫与氯同周期,写出一个能比较硫和氯非金属性强弱的化学反应方程式____________ 。硫单质不溶于水,易溶于CS2,则CS2分子的结构式为___________ 。
(4)电解氯化钠溶液可以得到NaClO3与H2。写出该反应的化学方程式,并标出电子转移的方向和数目_________________________________________________________________ 。
(5) II中不断加入细粒状KCl,搅拌,发生复分解反应,析出KClO3晶体。该反应能够发生的原因是__________________________________________________________________ 。

(1) 与氯元素同族的短周期元素的原子核外电子排布式为
(2)上述转化过程中所涉及的短周期元素中,原子半径由大到小的顺序是
(3)硫与氯同周期,写出一个能比较硫和氯非金属性强弱的化学反应方程式
(4)电解氯化钠溶液可以得到NaClO3与H2。写出该反应的化学方程式,并标出电子转移的方向和数目
(5) II中不断加入细粒状KCl,搅拌,发生复分解反应,析出KClO3晶体。该反应能够发生的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】下表是元素周期表的一部分,针对①~⑩元素在表中的位置,回答下列问题:
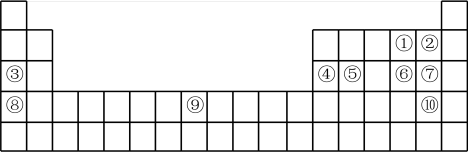
(1)⑨元素在元素周期表中的位置为___________ 。
(2)在①、②、③、④四种元素中,其离子半径按由大到小的顺序排列为___________ (用离子符号比较大小)。
(3)②、⑥、⑦元素所形成简单氢化物的稳定性由强到弱的顺序是___________ (用化学式比较强弱)。
(4)请写出⑥的最高价氧化物对应水化物和4的单质之间发生的化学方程式___________ 。
(5)写出⑩的单质与SO2水溶液反应的方程式:___________ 。
(6)写出工业制单质⑤的化学方程式___________ 。
(7)⑤的最高价氧化物与⑧的最高价氧化物对应的水化物反应的离子方程式___________ 。

(1)⑨元素在元素周期表中的位置为
(2)在①、②、③、④四种元素中,其离子半径按由大到小的顺序排列为
(3)②、⑥、⑦元素所形成简单氢化物的稳定性由强到弱的顺序是
(4)请写出⑥的最高价氧化物对应水化物和4的单质之间发生的化学方程式
(5)写出⑩的单质与SO2水溶液反应的方程式:
(6)写出工业制单质⑤的化学方程式
(7)⑤的最高价氧化物与⑧的最高价氧化物对应的水化物反应的离子方程式
您最近一年使用:0次



