元素周期表中第ⅦA族元素的单质及其化合物的用途广泛。工业上,通过如下转化可制得KClO3晶体:
(1) 与氯元素同族的短周期元素的原子核外电子排布式为______________________ 。
(2)上述转化过程中所涉及的短周期元素中,原子半径由大到小的顺序是______________ 。
(3)硫与氯同周期,写出一个能比较硫和氯非金属性强弱的化学反应方程式____________ 。硫单质不溶于水,易溶于CS2,则CS2分子的结构式为___________ 。
(4)电解氯化钠溶液可以得到NaClO3与H2。写出该反应的化学方程式,并标出电子转移的方向和数目_________________________________________________________________ 。
(5) II中不断加入细粒状KCl,搅拌,发生复分解反应,析出KClO3晶体。该反应能够发生的原因是__________________________________________________________________ 。

(1) 与氯元素同族的短周期元素的原子核外电子排布式为
(2)上述转化过程中所涉及的短周期元素中,原子半径由大到小的顺序是
(3)硫与氯同周期,写出一个能比较硫和氯非金属性强弱的化学反应方程式
(4)电解氯化钠溶液可以得到NaClO3与H2。写出该反应的化学方程式,并标出电子转移的方向和数目
(5) II中不断加入细粒状KCl,搅拌,发生复分解反应,析出KClO3晶体。该反应能够发生的原因是
更新时间:2019-10-27 09:43:21
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)请写出下列微粒的电子式:Na2S_____________ ,CO2_________________ ;
(2)请写出下列微粒的结构式:O2_______________ ,NH3_________________ ;
(3)请写出下列微粒的结构示意图:Al3+______________ ,Cl_________________ 。
(2)请写出下列微粒的结构式:O2
(3)请写出下列微粒的结构示意图:Al3+
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】填空
(1)请用化学用语填空:
①氯离子的结构示意图_____ 。
②NaOH溶液的电离方程式_____ 。
③稀H2SO4的电离方程式_____ 。
(2)已知: (过量)
(过量)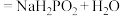 。据此回答下列问题:
。据此回答下列问题:
①该反应属于四种基本反应类型中的_____ 反应(选填“化合”、“分解”、“置换”或“复分解”)。该反应_____ (选填“属于”或“不属于”)氧化还原反应。
②H3PO2属于_____ (选填“一”、“二”或“三”)元酸。NaH2PO2属于_____ (选填“正盐”或“酸式盐”)。
(1)请用化学用语填空:
①氯离子的结构示意图
②NaOH溶液的电离方程式
③稀H2SO4的电离方程式
(2)已知:
 (过量)
(过量)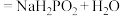 。据此回答下列问题:
。据此回答下列问题:①该反应属于四种基本反应类型中的
②H3PO2属于
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】H、C、N、O、Mg、Al、Si 、Cl、Fe是中学化学中的常见元素。
(1)Si元素在周期表中的位置是_____ ;C元素的一种同位素可测定文物年代,这种同位素的符号是_____ ;MgCl2中包含的化学键类型为____ 。
(2)用“>”、“<”或“= ”填空:
(3)一定温度下在一容积不变的密闭容器中发生可逆反应 N2(g)+3H2(g) 2NH3(g),以下能说明该反应达到化学平衡状态的是
2NH3(g),以下能说明该反应达到化学平衡状态的是_____ 。
A.混合气体的密度不再变化
B.体系的压强不再改变
C.单位时间内3mol H-H键断裂,同时6mol N-H 键也断裂
D.c(N2)∶c(H2)∶c(NH3)=1∶3∶2
(4)印刷电路板是由高分子材料和铜箔复合而成,刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”,生成CuCl2和FeCl2。写出化学方程式并用单线桥标出电子转移的方向和数目:________ 。
(1)Si元素在周期表中的位置是
(2)用“>”、“<”或“= ”填空:
| 酸性 | 金属性 | 离子半径 |
| H2CO3 | Fe | O2- |
(3)一定温度下在一容积不变的密闭容器中发生可逆反应 N2(g)+3H2(g)
 2NH3(g),以下能说明该反应达到化学平衡状态的是
2NH3(g),以下能说明该反应达到化学平衡状态的是A.混合气体的密度不再变化
B.体系的压强不再改变
C.单位时间内3mol H-H键断裂,同时6mol N-H 键也断裂
D.c(N2)∶c(H2)∶c(NH3)=1∶3∶2
(4)印刷电路板是由高分子材料和铜箔复合而成,刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”,生成CuCl2和FeCl2。写出化学方程式并用单线桥标出电子转移的方向和数目:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】I、配平下列方程式:
____ MnO +
+____ H++____ Cl- === ____ Mn2++____ Cl2↑+____ H2O
____ H2S+____ HNO3 ===____ S↓+____ NO↑+____ H2O
II、KClO3 和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯,其化学方程式为:
2KClO3 +4HCl(浓)=== 2KCl+2ClO2↑+Cl2↑+2H2O
(1)浓盐酸在反应中表现出来的性质是____ (填写编号)
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(2)产生 0.1molCl2,则转移电子的物质的量为____ mol。
(3)用单线桥法标出该反应的电子转移的方向和数目。____
 +
+II、KClO3 和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯,其化学方程式为:
2KClO3 +4HCl(浓)=== 2KCl+2ClO2↑+Cl2↑+2H2O
(1)浓盐酸在反应中表现出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(2)产生 0.1molCl2,则转移电子的物质的量为
(3)用单线桥法标出该反应的电子转移的方向和数目。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】铁的重要化合物高铁酸钠 Na2FeO4 是一种新型净水剂,具有消毒能力强、安全性好等优点。
(1)高铁酸钠生产方法之一是 Fe+2NaOH+2H2O Na2FeO4+3H2↑,该反应中还原剂是
Na2FeO4+3H2↑,该反应中还原剂是 ____________ (填化学式,下同),还原产物是___________ 。
(2)高铁酸钠生产方法之二是2Fe(OH)3+3NaClO+4NaOH=2Na2FeO4+3NaCl+5H2O,用双线桥表示该反应的电子转移的方向和数目:___________ 。
(3)高铁酸钠在水中可以发生如下反应 4FeO +10H2O = 4Fe(OH)3(胶体)+8OH–+3O2 ↑。 由此看来,高铁酸钠能够杀菌消毒是因为它具有
+10H2O = 4Fe(OH)3(胶体)+8OH–+3O2 ↑。 由此看来,高铁酸钠能够杀菌消毒是因为它具有________________ 性,而能够除去水中悬浮物是因为____________________ 。
(1)高铁酸钠生产方法之一是 Fe+2NaOH+2H2O
 Na2FeO4+3H2↑,该反应中还原剂是
Na2FeO4+3H2↑,该反应中还原剂是 (2)高铁酸钠生产方法之二是2Fe(OH)3+3NaClO+4NaOH=2Na2FeO4+3NaCl+5H2O,用双线桥表示该反应的电子转移的方向和数目:
(3)高铁酸钠在水中可以发生如下反应 4FeO
 +10H2O = 4Fe(OH)3(胶体)+8OH–+3O2 ↑。 由此看来,高铁酸钠能够杀菌消毒是因为它具有
+10H2O = 4Fe(OH)3(胶体)+8OH–+3O2 ↑。 由此看来,高铁酸钠能够杀菌消毒是因为它具有
您最近一年使用:0次
【推荐1】(1)NA表示阿伏伽德罗常数的数值.46g NO2和N2O4的混合气体中含有_____ NA个氧原子;2L0.6 mol·L−1 Fe(NO3)3溶液中含_____ NA个NO3—离子.
(2)三氟化氮(NF3)是一种气体,它是微电子工业技术的关键原料之一,三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3。
①写出该反应的化学方程式_________________________________
②三氟化氮可由氨气和氟气反应得到:4NH3+3F2NF3+3NH4F;据题意推测NF3,F2,NO三种气体中,氧化性由强到弱的顺序为________________________
(3)H2C2O4溶液和KMnO4酸性溶液可发生反应:___ H2C2O4+___ MnO4﹣+___ H+→___ CO2↑+___ Mn2++___ H2O,反应中每生成标况下4.48L CO2气体,外电路中通过的电子的物质的量为___________ mol.
(4)氨和联氨(N2H4)是氮的两种常见化合物,制备联氨可用丙酮为催化剂,将次氯酸钠与氨气反应,该反应中还原剂与氧化剂的物质的量之比为2∶1,写出该反应的化学方程式_______ 。
(2)三氟化氮(NF3)是一种气体,它是微电子工业技术的关键原料之一,三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3。
①写出该反应的化学方程式
②三氟化氮可由氨气和氟气反应得到:4NH3+3F2NF3+3NH4F;据题意推测NF3,F2,NO三种气体中,氧化性由强到弱的顺序为
(3)H2C2O4溶液和KMnO4酸性溶液可发生反应:
(4)氨和联氨(N2H4)是氮的两种常见化合物,制备联氨可用丙酮为催化剂,将次氯酸钠与氨气反应,该反应中还原剂与氧化剂的物质的量之比为2∶1,写出该反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】实验室迅速制备少量氯气可利用如下反应:KMnO4+HCl(浓)→KCl+MnCl2+Cl2↑+H2O(未配平),此反应常温下就可以迅速进行。结合信息,回答下列问题:
(1)上述反应中被氧化的元素为________ ,还原产物是________ 。
(2)Fe2+也能与MnO4-反应生成Mn2+,反应后Fe2+转化为________ 。反应中Fe2+表现________ (填“氧化”或“还原”,下同)性,发生________ 反应。
(3)如果上述化学方程式中KMnO4和 MnCl2的化学计量数都是2,则HCl的化学计量数是___ 。
(4)实验室通常利用MnO2与浓盐酸共热反应制得氯气,据此可知KMnO4、Cl2、MnO2三种物质的氧化性由强到弱的顺序为________________________________ 。
(1)上述反应中被氧化的元素为
(2)Fe2+也能与MnO4-反应生成Mn2+,反应后Fe2+转化为
(3)如果上述化学方程式中KMnO4和 MnCl2的化学计量数都是2,则HCl的化学计量数是
(4)实验室通常利用MnO2与浓盐酸共热反应制得氯气,据此可知KMnO4、Cl2、MnO2三种物质的氧化性由强到弱的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】原电池是化学对人类的一项重大贡献。
(1)某兴趣小组为研究原电池原理,设计如图装置。

①a和b不连接时,烧杯中发生反应的离子方程式是_______ 。
②a和b用导线连接,Cu极为原电池_______ 极(填“正”或“负”),该电极反应式是_______ ,溶液中的H+移向_______ (填“Cu”或“Zn”)极。
③无论a和b是否连接,Zn片均被腐蚀,若转移了0.2 mol电子,则理论上Zn片质量减轻_______ g。
(2)如图是甲烷燃料电池原理示意图,回答下列问题:

①电池的负极是_______ (填“a”或“b”)电极,该极的电极反应式为:_______ 。
②电池工作一段时间后电解质溶液的pH_______ (填“增大”“减小”或“不变”)。
(3)现有下列三个氧化还原反应:
A.2FeCl3+2KI=2FeCl2+2KCl+I2
B.2FeCl2+Cl2=2FeCl3
C.2KMnO4+16HCl(浓)=2KCl+2MnCl2+8H2O+5Cl2↑
Fe3+、I2、Cl2、MnO 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为_______
(1)某兴趣小组为研究原电池原理,设计如图装置。

①a和b不连接时,烧杯中发生反应的离子方程式是
②a和b用导线连接,Cu极为原电池
③无论a和b是否连接,Zn片均被腐蚀,若转移了0.2 mol电子,则理论上Zn片质量减轻
(2)如图是甲烷燃料电池原理示意图,回答下列问题:

①电池的负极是
②电池工作一段时间后电解质溶液的pH
(3)现有下列三个氧化还原反应:
A.2FeCl3+2KI=2FeCl2+2KCl+I2
B.2FeCl2+Cl2=2FeCl3
C.2KMnO4+16HCl(浓)=2KCl+2MnCl2+8H2O+5Cl2↑
Fe3+、I2、Cl2、MnO
 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】硫及其化合物在人类生产生活中起着重要作用。回答下列问题:
(1)S在元素周期表中位于第______ 族,属于______ 区。
(2)基态S原子的价层电子轨道表示式为______ ,其原子核外电子共有______ 种空间运动状态。
(3)完成下列比较(填“>”、“<”或“=”)。
第一电离能:S______ P;电负性:S______ O;半径:
______ Na+。
(4)已知:25℃时 的电离常数:
的电离常数:
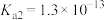 ,则NaHS的水解常数
,则NaHS的水解常数
______ ,NaHS溶液的pH______ 7(填“>”“<”或“=”)。
(5)锅炉水垢既会降低燃料的利用率,又会影响锅炉的使用寿命。为了除去水垢中的 可先用
可先用 溶液处理,写出该反应的离子方程式:
溶液处理,写出该反应的离子方程式:__________________ 。
(6)0.1 mol/L 溶液中各种离子浓度由大到小的顺序是
溶液中各种离子浓度由大到小的顺序是______ 。
(1)S在元素周期表中位于第
(2)基态S原子的价层电子轨道表示式为
(3)完成下列比较(填“>”、“<”或“=”)。
第一电离能:S

(4)已知:25℃时
 的电离常数:
的电离常数:
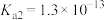 ,则NaHS的水解常数
,则NaHS的水解常数
(5)锅炉水垢既会降低燃料的利用率,又会影响锅炉的使用寿命。为了除去水垢中的
 可先用
可先用 溶液处理,写出该反应的离子方程式:
溶液处理,写出该反应的离子方程式:(6)0.1 mol/L
 溶液中各种离子浓度由大到小的顺序是
溶液中各种离子浓度由大到小的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下表是元素周期表的一部分,表中的每个编号表示一种元素,请根据要求回答问题

(1)⑤和⑥两种元素的原子半径大小是⑤____ ⑥(填“<"或“>”);
(2)由①和②两种元素组成的最简单化合物的化学式是________ ;
(3)⑥的单质与⑤的最高价氧化物的水化物的水溶液反应的化学方程式为____________ 。

(1)⑤和⑥两种元素的原子半径大小是⑤
(2)由①和②两种元素组成的最简单化合物的化学式是
(3)⑥的单质与⑤的最高价氧化物的水化物的水溶液反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】下表是元素周期表的一部分,表中所列的数字分别代表某一种元素。
针对元素①~⑩回答下列问题。
(1)元素①和②的单质化合形成的化合物NaH中H元素的化合价为_______ ;NaH能与水反应生成氢气,在反应后的溶液中滴入酚酞,溶液变红,其化学方程式为_______ 。
(2)元素④是人体必不可缺少的一种元素,缺乏会出现骨质疏松、易骨折等症状,请写出其原子结构示意图_______ 。
(3)由元素①和⑥形成的一种物质是天然气的主要成分,其电子式为_______ ;元素⑥还可以和⑦形成一种三原子直线型分子,其结构式为_______ ;元素②的单质在元素⑦的单质中点燃生成的淡黄色固体将其投入硫酸亚铁溶液中,预测主要的反应现象是_______ 。
(4)元素③、⑧、⑨的简单离子中半径最大是_______ (填离子符号),元素②和⑤的最高价氧化物对应的水化物之间可以发生反应,其反应的离子方程式为_______ 。
(5)表中元素⑨和⑩的气态氢化物中更稳定的是_______ (填化学式)。
| 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ⑥ | ⑦ | ||||||
| 3 | ② | ⑤ | ⑧ | ⑨ | ||||
| 4 | ③ | ④ | ⑩ |
(1)元素①和②的单质化合形成的化合物NaH中H元素的化合价为
(2)元素④是人体必不可缺少的一种元素,缺乏会出现骨质疏松、易骨折等症状,请写出其原子结构示意图
(3)由元素①和⑥形成的一种物质是天然气的主要成分,其电子式为
(4)元素③、⑧、⑨的简单离子中半径最大是
(5)表中元素⑨和⑩的气态氢化物中更稳定的是
您最近一年使用:0次

 结构示意图:
结构示意图: );④熔融的
);④熔融的 ;⑤
;⑤ 固体;⑥液氨;⑦冰醋酸;⑧石墨。其中,属于电解质且能导电的是
固体;⑥液氨;⑦冰醋酸;⑧石墨。其中,属于电解质且能导电的是 的化学性质和卤素(
的化学性质和卤素( ,如
,如 )很相似,化学上称为拟卤素,试写出
)很相似,化学上称为拟卤素,试写出

