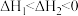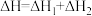下列事实得出的相应结论正确的是
| 选项 | 事实 | 结论 |
| A | 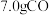 在足量 在足量 中完全燃烧放出70.8kJ的热量 中完全燃烧放出70.8kJ的热量 | 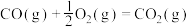 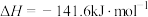 |
| B |   | 向密闭容器中通入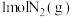 、 、 ,反应达到平衡时放出92.4kJ热量 ,反应达到平衡时放出92.4kJ热量 |
| C | 将铜片插入 溶液中,铜片逐渐变小,直至消失 溶液中,铜片逐渐变小,直至消失 | 以Cu、石墨棒为电极,以 溶液为电解质溶液可设计原电池 溶液为电解质溶液可设计原电池 |
| D | 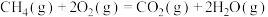    | 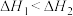 |
| A.A | B.B | C.C | D.D |
更新时间:2023-07-05 22:30:40
|
相似题推荐
【推荐1】已知:C(s)+ H2O(g) = CO(g) +H2(g) ΔH= -131.3 kJ/mol下列说法正确的是( )
| A.加入催化剂,可以减小该反应的反应热 |
| B.通入水蒸气可增大该反应的反应热 |
| C.该反应中反应物的总能量低于生成物的总能量 |
| D.反应 CO(g) +H2(g) = C(s)+ H2O(g) 的ΔH=+131.3 kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列关于右图所示转化关系(X代表卤素)的说法错误的是
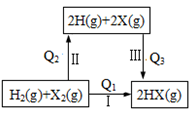

| A.Q3>0 | B.Q1=Q2 + Q3 |
| C.按Cl、Br、I的顺序,Q2依次增大 | D.Q1越大,HX越稳定 |
您最近一年使用:0次
【推荐1】已知 ,如图是
,如图是 燃烧的反应过程中能量变化示意图。
燃烧的反应过程中能量变化示意图。
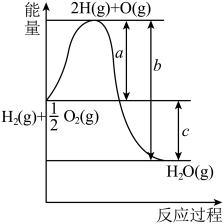
氢气在氧气中燃烧,破坏 键吸收
键吸收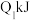 的能量,破坏
的能量,破坏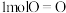 键吸收
键吸收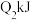 的能量,形成
的能量,形成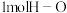 键释放
键释放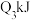 的能题,则下列关系式正确的是
的能题,则下列关系式正确的是
 ,如图是
,如图是 燃烧的反应过程中能量变化示意图。
燃烧的反应过程中能量变化示意图。
氢气在氧气中燃烧,破坏
 键吸收
键吸收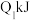 的能量,破坏
的能量,破坏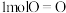 键吸收
键吸收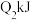 的能量,形成
的能量,形成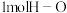 键释放
键释放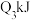 的能题,则下列关系式正确的是
的能题,则下列关系式正确的是A.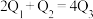 | B. | C.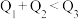 | D.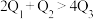 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列依据热化学方程式得出的结论正确的是
| A.已知Ni(CO)4(s)=Ni(s)+4CO(g) ΔH=Q kJ·mol-1,则:Ni(s)+4CO(g)= Ni(CO)4(s) ΔH=-Q kJ·mol-1 |
B.在一定温度和压强下,将1 mol N2和3 mol H2置于密闭容器中充分反应生成NH3(g),放出热量19.3 kJ,则其热化学方程式为N2(g)+3H2(g) 2NH3(g) ΔH=-19.3 kJ·mol-1 2NH3(g) ΔH=-19.3 kJ·mol-1 |
| C.已知2H2(g)+O2(g)=2H2O(l) ΔH1,2H2(g)+O2(g)=2H2O(g) ΔH2,则ΔH1>ΔH2 |
| D.已知C(石墨,s)= C(金刚石,s) ΔH>0,则金刚石比石墨稳定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】用H2O2和H2SO4的混合溶液可溶出印刷电路板中的铜,其热化学方程式为Cu(s)+H2O2(1)+2H+(aq)=Cu2+(aq)+2H2O(l) △H。已知:
①Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) △H1=+64 kJ/mol
②2H2O2(l)=2H2O(l)+O2(g) △H2=-196 kJ/mol
③H2(g)+ O2(g)=H2O(l) △H3=-286 kJ/mol
O2(g)=H2O(l) △H3=-286 kJ/mol
下列说法不正确的是
①Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) △H1=+64 kJ/mol
②2H2O2(l)=2H2O(l)+O2(g) △H2=-196 kJ/mol
③H2(g)+
 O2(g)=H2O(l) △H3=-286 kJ/mol
O2(g)=H2O(l) △H3=-286 kJ/mol下列说法不正确的是
| A.反应②若加入少量FeCl3可加快化学反应速率 |
| B.反应②在任何条件下都能自发进行 |
C.若H2(g)+ O2(g)=H2O(g) △H4,则△H4<△H3 O2(g)=H2O(g) △H4,则△H4<△H3 |
| D.△H= -320 kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】实验室中,用 浓度为
浓度为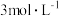 的稀硫酸与过量的锌粒在一定温度下发生反应制取氢气,为了降低反应速率,但又不影响生成氢气的总量,下列措施能达到目的的是
的稀硫酸与过量的锌粒在一定温度下发生反应制取氢气,为了降低反应速率,但又不影响生成氢气的总量,下列措施能达到目的的是
 浓度为
浓度为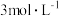 的稀硫酸与过量的锌粒在一定温度下发生反应制取氢气,为了降低反应速率,但又不影响生成氢气的总量,下列措施能达到目的的是
的稀硫酸与过量的锌粒在一定温度下发生反应制取氢气,为了降低反应速率,但又不影响生成氢气的总量,下列措施能达到目的的是A.向稀硫酸中加 溶液 溶液 | B.将锌粒制成薄锌片 |
C.向稀硫酸中加 固体 固体 | D.向稀硫酸中加 固体 固体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法中,错误的是
| A.实验室用铁片和稀硫酸制备H2时,滴入几滴CuSO4溶液,能加快反应速率 |
| B.镀锡铁皮表面有破损时,铁的腐蚀速率会加快 |
| C.硫粉分别在纯氧和空气中燃烧,前者反应更剧烈 |
| D.酶作为催化剂,在任何温度下均能极大地提高反应速率 |
您最近一年使用:0次

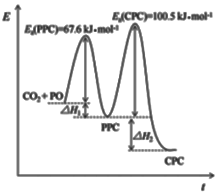
 和PO(环氧丙烷)共聚生成主产物PPC(聚碳酸丙烯酯)和副产物CPC(环状碳酸丙烯酯),其能量与时间变化如图所示,已知反应的活化能越大,则该反应的速率越慢。下列说法正确的是
和PO(环氧丙烷)共聚生成主产物PPC(聚碳酸丙烯酯)和副产物CPC(环状碳酸丙烯酯),其能量与时间变化如图所示,已知反应的活化能越大,则该反应的速率越慢。下列说法正确的是