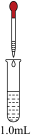
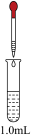
在化学研究中,往往可以通过观察现象认识物质变化的情况。请分析以下一组有现象变化的化学反应。
(1)用离子方程式解释现象I中出现胶状沉淀的原因: ______ 。
(2)II中加碱时出现的现象是____________________ ,此现象说明溶液中发生反应的离子方程式是__________________________ 。
(3)III中加碱时出现的现象是_____ 。
(4)IV中加酸时出现的现象是_____________ ,用离子方程式解释产生此现象的原因:___________________ 。
(5)滴加试剂顺序的变化会影响溶液中的现象和发生的反应。请继续分析以下实验。
①探究加酸时Fe(NO3)2溶液中是否发生了反应:向1.0 mL 0.1 mol·L-1 Fe(NO3)2溶液中_______ ,如果溶液变红色,说明溶液中含Fe3+,证明加酸时溶液中发生了反应。(请将上述操作补充完整)
②推测溶液中产生Fe3+的可能原因有两种:a._________ ;b._________ 。
| 实验 | 试剂及操作 | 现象 | |
| 试管 | 滴管 | ||
| 饱和Na2SiO3溶液(含2滴酚酞) | 先滴加1.0 mL0.5 mol·L-1NaOH溶液;再滴加1.5 mL 1.0 mol·L-1H2SO4溶液 | Ⅰ.红色溶液中出现胶状沉淀 |
| 0.1 mol·L-1AlCl3溶液 | Ⅱ.加碱时____;加酸时产生白色沉淀,又逐渐溶解至消失 | ||
| 0.1 mol·L-1Fe(NO3)2溶液 | Ⅲ.加碱时____;加酸后得棕黄色溶液 | ||
| 新制饱和氯水 | Ⅳ.加碱时溶液变为无色;加酸后____ | ||
(2)II中加碱时出现的现象是
(3)III中加碱时出现的现象是
(4)IV中加酸时出现的现象是
(5)滴加试剂顺序的变化会影响溶液中的现象和发生的反应。请继续分析以下实验。
| 实验 | 试剂及操作 | 现象 | |
| 试管 | 滴管 | ||
| 0.1 mol·L-1 Fe(NO3)2溶液 | 先滴加1.5 mL 1.0 mol·L-1 H2SO4溶液;再滴加1.0 mL 0.5 mol·L-1NaOH溶液 | Ⅴ.加酸时溶液无明显现象;加碱后溶液依然没有明显变化 |
②推测溶液中产生Fe3+的可能原因有两种:a.
2023高三·全国·专题练习 查看更多[2]
更新时间:2023-07-06 13:06:42
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】I.将铁丝插入硫酸铜溶液中,充分反应后:
(1)铁丝上观察到的现象是_______ ;
(2)发生反应的离子方程式为_______ ;
II.将铜丝插入到硝酸银溶液中:
(3)发生反应的离子方程式为_______ ;
(4)结合I、II实验现象可知,Fe、Cu、Ag的还原性顺序为_______ 。
(1)铁丝上观察到的现象是
(2)发生反应的离子方程式为
II.将铜丝插入到硝酸银溶液中:
(3)发生反应的离子方程式为
(4)结合I、II实验现象可知,Fe、Cu、Ag的还原性顺序为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】磺酰氯(SO2Cl2)是一种重要的有机合成试剂,实验室可利用SO2与Cl2在活性炭作用下反应制取少量的SO2Cl2,装置如图所示(部分夹持装置省略)。已知SO2Cl2的熔点为-54.1℃,沸点为69.1℃,遇水能发生剧烈的水解反应,并产生白雾。
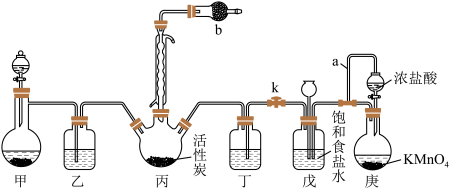
回答下列问题。
(1)甲装置可以用于实验室制SO2,则下列试剂组合中合适的是_____ 。
A.18.4mol·L-1的硫酸和Cu
B.10mol·L-1的硝酸和Na2SO3固体
C.70%的硫酸和Na2SO3固体
装置庚中发生反应的离子方程式为:_____ 。
(2)导管a的作用是_____ 。仪器b盛放的试剂为_____ 。装置乙和丁中可以使用同一种试剂,该试剂为_____ 。
(3)控制反应过程中装置丙中进气速率的方法是_____ ,实验结束时,关闭分液漏斗活塞和止水夹k,此时装置戊的作用是_____ 。
(4)氯磺酸(ClSO3H)加热分解,也能制得磺酰氯与另外一种物质,该反应的化学方程式为_____ 。
(5)若反应中消耗的氯气体积为896mL(已转化为标准状况,SO2足量),最后得到纯净的磺酰氯3.3g,则磺酰氯的产率为_____ (保留三位有效数字)。

回答下列问题。
(1)甲装置可以用于实验室制SO2,则下列试剂组合中合适的是
A.18.4mol·L-1的硫酸和Cu
B.10mol·L-1的硝酸和Na2SO3固体
C.70%的硫酸和Na2SO3固体
装置庚中发生反应的离子方程式为:
(2)导管a的作用是
(3)控制反应过程中装置丙中进气速率的方法是
(4)氯磺酸(ClSO3H)加热分解,也能制得磺酰氯与另外一种物质,该反应的化学方程式为
(5)若反应中消耗的氯气体积为896mL(已转化为标准状况,SO2足量),最后得到纯净的磺酰氯3.3g,则磺酰氯的产率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】草酸(HOOC-COOH,弱酸)及其化合物在工业中有重要作用。某实验小组同学在实验室利用两种方法制备草酸。回答下列问题:
(1)利用CO与亚硝酸甲酯(CH3ONO)先合成草酸二甲酯(CH3OOCCOOCH3),然后草酸二甲酯水解生成草酸。草酸二甲酯水解的化学方程式为_______ ;其中制备亚硝酸甲酯的反应为 ,实验室制备NO常用的试剂为
,实验室制备NO常用的试剂为_______ 。
(2)在浓硫酸催化作用下,用硝酸氧化葡萄糖可制取草酸,实验装置(夹持仪器已省略)如图所示。
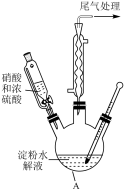
①仪器A的名称为_______ 。
②葡萄糖溶液可由反应 (淀粉)
(淀粉) (葡萄糖)得到。该实验中证明淀粉已经完全水解的实验操作及现象是
(葡萄糖)得到。该实验中证明淀粉已经完全水解的实验操作及现象是_______ 。
③反应在55℃~60℃进行,仪器A中除生成 外,同时也生成NO。要将16.2g淀粉完全水解后的淀粉水解液完全转化为草酸,理论上消耗
外,同时也生成NO。要将16.2g淀粉完全水解后的淀粉水解液完全转化为草酸,理论上消耗 的硝酸溶液的体积为
的硝酸溶液的体积为_______ mL。
④该实验中催化剂浓硫酸用量不宜过多,否则会导致草酸产率减少,其原因是_______ 。
(3)草酸具有较强的还原性,与氧化剂作用易被氧化成二氧化碳和水,故实验室可利用草酸测定次氯酸钠溶液的浓度。实验步骤如下:取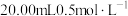 草酸溶液于锥形瓶中,用次氯酸钠溶液滴定,至终点时消耗次氯酸钠溶液为25.00mL。
草酸溶液于锥形瓶中,用次氯酸钠溶液滴定,至终点时消耗次氯酸钠溶液为25.00mL。
①次氯酸钠与草酸反应的离子方程式为_______ 。
②次氯酸钠溶液物质的量浓度为_______  。
。
(1)利用CO与亚硝酸甲酯(CH3ONO)先合成草酸二甲酯(CH3OOCCOOCH3),然后草酸二甲酯水解生成草酸。草酸二甲酯水解的化学方程式为
 ,实验室制备NO常用的试剂为
,实验室制备NO常用的试剂为(2)在浓硫酸催化作用下,用硝酸氧化葡萄糖可制取草酸,实验装置(夹持仪器已省略)如图所示。

①仪器A的名称为
②葡萄糖溶液可由反应
 (淀粉)
(淀粉) (葡萄糖)得到。该实验中证明淀粉已经完全水解的实验操作及现象是
(葡萄糖)得到。该实验中证明淀粉已经完全水解的实验操作及现象是③反应在55℃~60℃进行,仪器A中除生成
 外,同时也生成NO。要将16.2g淀粉完全水解后的淀粉水解液完全转化为草酸,理论上消耗
外,同时也生成NO。要将16.2g淀粉完全水解后的淀粉水解液完全转化为草酸,理论上消耗 的硝酸溶液的体积为
的硝酸溶液的体积为④该实验中催化剂浓硫酸用量不宜过多,否则会导致草酸产率减少,其原因是
(3)草酸具有较强的还原性,与氧化剂作用易被氧化成二氧化碳和水,故实验室可利用草酸测定次氯酸钠溶液的浓度。实验步骤如下:取
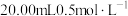 草酸溶液于锥形瓶中,用次氯酸钠溶液滴定,至终点时消耗次氯酸钠溶液为25.00mL。
草酸溶液于锥形瓶中,用次氯酸钠溶液滴定,至终点时消耗次氯酸钠溶液为25.00mL。①次氯酸钠与草酸反应的离子方程式为
②次氯酸钠溶液物质的量浓度为
 。
。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】铁是人类较早使用的金属之一、运用铁及其化合物的知识,完成下列问题。
Ⅰ.印刷电路板(PCB)是用腐蚀液( 溶液)将覆铜板上的部分铜腐蚀掉而制得。一种制作PCB并将腐蚀后废液(其中金属阳离子主要含
溶液)将覆铜板上的部分铜腐蚀掉而制得。一种制作PCB并将腐蚀后废液(其中金属阳离子主要含 、
、 、
、 )回收再生的流程如下。
)回收再生的流程如下。
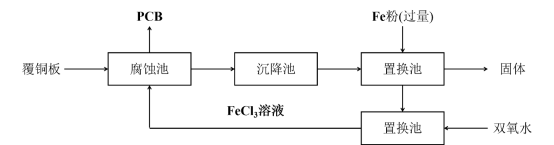
请回答:
(1)腐蚀池中发生反应的化学方程式是______ 。
(2)上述各池中,没有发生化学变化的是______ 池
(3)由置换池中得到固体的操作名称是______ 。
(4)向再生池中通入 也可以使废液再生,相比
也可以使废液再生,相比 ,用双氧水的优点是
,用双氧水的优点是______ 。
(5)若取少量循环使用的氯化铁溶液于烧杯中,同时加入铁粉和铜粉。反应结束后,下列结果不可能出现的是______ (填写编号)
A.有铜无铁 B.有铁无铜 C.铁、铜都有 D.铁、铜都无
Ⅱ.高铁酸钾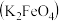 是一种新型、高效、多功能绿色水处理剂,比
是一种新型、高效、多功能绿色水处理剂,比 、
、 、
、 、
、 氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(6)干法制备高铁酸钠的主要反应为: , 该反应中
, 该反应中 是
是______ (填“氧化剂”、“还原剂”)。
(7)湿法制备高铁酸钾的反应体系中有六种微粒: 、
、 、
、 、
、 、
、 、
、 。
。
①碱性条件下,氧化剂和还原剂的物质的量的比为 发生反应,写出并配平湿法制高铁酸钾的离子反应方程式:
发生反应,写出并配平湿法制高铁酸钾的离子反应方程式:______ 。
②若反应过程中转移了0.3mol电子,则还原产物的物质的量为______ mol。
Ⅰ.印刷电路板(PCB)是用腐蚀液(
 溶液)将覆铜板上的部分铜腐蚀掉而制得。一种制作PCB并将腐蚀后废液(其中金属阳离子主要含
溶液)将覆铜板上的部分铜腐蚀掉而制得。一种制作PCB并将腐蚀后废液(其中金属阳离子主要含 、
、 、
、 )回收再生的流程如下。
)回收再生的流程如下。
请回答:
(1)腐蚀池中发生反应的化学方程式是
(2)上述各池中,没有发生化学变化的是
(3)由置换池中得到固体的操作名称是
(4)向再生池中通入
 也可以使废液再生,相比
也可以使废液再生,相比 ,用双氧水的优点是
,用双氧水的优点是(5)若取少量循环使用的氯化铁溶液于烧杯中,同时加入铁粉和铜粉。反应结束后,下列结果不可能出现的是
A.有铜无铁 B.有铁无铜 C.铁、铜都有 D.铁、铜都无
Ⅱ.高铁酸钾
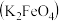 是一种新型、高效、多功能绿色水处理剂,比
是一种新型、高效、多功能绿色水处理剂,比 、
、 、
、 、
、 氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。(6)干法制备高铁酸钠的主要反应为:
 , 该反应中
, 该反应中 是
是(7)湿法制备高铁酸钾的反应体系中有六种微粒:
 、
、 、
、 、
、 、
、 、
、 。
。①碱性条件下,氧化剂和还原剂的物质的量的比为
 发生反应,写出并配平湿法制高铁酸钾的离子反应方程式:
发生反应,写出并配平湿法制高铁酸钾的离子反应方程式:②若反应过程中转移了0.3mol电子,则还原产物的物质的量为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】(1)已知25℃:
写出H2S与钾盐KA溶液 ( A-表示酸根 ) 反应的化学方程式:______________________ 。
(2)次磷酸(H3PO2)是一种化工产品,具有较强的还原性。
①H3PO2是一元弱酸,写出其电离方程式____________________ 。
②H3PO2和NaH2PO2均可将溶液中的Ag+还原为Ag,从而可用于化学镀银。NaH2PO2为________ (填 “正盐”或“酸式盐”),其溶液显______ (填“弱酸性”、“中性”或“弱碱性”)。利用H3PO2进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4:1,则氧化产物为_______ (填化学式)。
(3)向NH4Al(SO4)2溶液中滴加1mol・L—1NaOH溶液,沉淀的物质的量随加入NaOH溶液体积的变化如图所示。(滴加过程无气体放出)
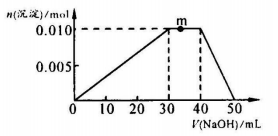
①写出m点发生反应的离子方程式_____________________________________ 。
②往NH4Al(SO4)2溶液中改加20mL1.2mol/L Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为_____________ mol 。
| H2S | 一元酸HA |
| Ka1=9.1×10—8,Ka2=1.1×10—12, | Ka=9.1×10—10 |
写出H2S与钾盐KA溶液 ( A-表示酸根 ) 反应的化学方程式:
(2)次磷酸(H3PO2)是一种化工产品,具有较强的还原性。
①H3PO2是一元弱酸,写出其电离方程式
②H3PO2和NaH2PO2均可将溶液中的Ag+还原为Ag,从而可用于化学镀银。NaH2PO2为
(3)向NH4Al(SO4)2溶液中滴加1mol・L—1NaOH溶液,沉淀的物质的量随加入NaOH溶液体积的变化如图所示。(滴加过程无气体放出)

①写出m点发生反应的离子方程式
②往NH4Al(SO4)2溶液中改加20mL1.2mol/L Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为
您最近一年使用:0次
【推荐3】回答下列问题:
(1)复旦大学、北京大学和上海电力大学等的研究团队共同报道了一种新型NASICON相铁基磷酸盐负极材料Na3Fe2(PO4)P2O7,Na3Fe2(PO4)P2O7放电后生成Na2Fe2(PO4)P2O7。回答下列问题:
①基态Fe2+的价电子排布式为________ 。
②Na2Fe2(PO4)P2O7中n(Fe2+):n(Fe3+)=________ 。
(2)一组同学对铁和稀硝酸的反应进行探究。他们用amolFe和含有bmolHNO3的稀硝酸进行实验,若HNO3只被还原成NO,且反应结束后溶液中含有Fe3+和Fe2+。若反应结束后的溶液中n(Fe3+):n(Fe2+)=1:2,则 的值为
的值为________ 。
(3)硫酸铁铵可用作媒染剂和制药,其晶体化学式为(NH4)aFeb(SO4)c•dH2O。硫酸铁铵晶体组成的测定过程如下:通过计算确定a:b:c________ 。
步骤1:准确称取质量为9.640g固体在酸性条件下溶于水配成100.00mL溶液A;
步骤2:取25.00mL溶液A,加入足量的BaCl2溶液,过滤得2.330g沉淀;
步骤3:取25.00mL溶液A,加入足量氢氧化钠溶液,过滤、洗涤并灼烧得0.4g红棕色固体。
(4)制备黄血盐K4[Fe(CN)6]可以由FeSO4与KCN直接在溶液中作用而合成,但制备赤血盐K3[Fe(CN)6],却不能直接用Fe3+离子与CN-直接作用而得,而是采用氧化剂Cl2或H2O2将黄血盐氧化为赤血盐。已知CN-在性质上与卤离子相似,而(CN)2则似卤素单质,故(CN)2称为拟卤素。
①1mol[Fe(CN)6]3-中含有的σ键数目为________ 。(用NA表示,假设NA为阿伏加德罗常数的值)
②用离子方程式表示不能用Fe2(SO4)3与KCN直接反应制备赤血盐的原因是________ 。
③写出在稀硫酸中用H2O2氧化黄血盐制备赤血盐的化学方程式:________ 。
(1)复旦大学、北京大学和上海电力大学等的研究团队共同报道了一种新型NASICON相铁基磷酸盐负极材料Na3Fe2(PO4)P2O7,Na3Fe2(PO4)P2O7放电后生成Na2Fe2(PO4)P2O7。回答下列问题:
①基态Fe2+的价电子排布式为
②Na2Fe2(PO4)P2O7中n(Fe2+):n(Fe3+)=
(2)一组同学对铁和稀硝酸的反应进行探究。他们用amolFe和含有bmolHNO3的稀硝酸进行实验,若HNO3只被还原成NO,且反应结束后溶液中含有Fe3+和Fe2+。若反应结束后的溶液中n(Fe3+):n(Fe2+)=1:2,则
 的值为
的值为(3)硫酸铁铵可用作媒染剂和制药,其晶体化学式为(NH4)aFeb(SO4)c•dH2O。硫酸铁铵晶体组成的测定过程如下:通过计算确定a:b:c
步骤1:准确称取质量为9.640g固体在酸性条件下溶于水配成100.00mL溶液A;
步骤2:取25.00mL溶液A,加入足量的BaCl2溶液,过滤得2.330g沉淀;
步骤3:取25.00mL溶液A,加入足量氢氧化钠溶液,过滤、洗涤并灼烧得0.4g红棕色固体。
(4)制备黄血盐K4[Fe(CN)6]可以由FeSO4与KCN直接在溶液中作用而合成,但制备赤血盐K3[Fe(CN)6],却不能直接用Fe3+离子与CN-直接作用而得,而是采用氧化剂Cl2或H2O2将黄血盐氧化为赤血盐。已知CN-在性质上与卤离子相似,而(CN)2则似卤素单质,故(CN)2称为拟卤素。
①1mol[Fe(CN)6]3-中含有的σ键数目为
②用离子方程式表示不能用Fe2(SO4)3与KCN直接反应制备赤血盐的原因是
③写出在稀硫酸中用H2O2氧化黄血盐制备赤血盐的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某实验小组为探究 和
和 的氧化能力设计如下实验.
的氧化能力设计如下实验.
Ⅰ.探究 和
和 氧化
氧化 的速率向体积均为
的速率向体积均为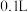 、浓度均为
、浓度均为 的
的 溶液和
溶液和 溶液中加入表面积相同、质量相等的铜片,反应一段时间后,经检验,
溶液中加入表面积相同、质量相等的铜片,反应一段时间后,经检验, 已完全消耗,
已完全消耗, 还有剩余.该小组同学猜测
还有剩余.该小组同学猜测 和
和 的氧化能力:
的氧化能力: .
.
(1)检验溶液中还有 剩余的试剂为
剩余的试剂为___________ 。
(2)相较于 溶液,
溶液, 溶液和铜反应速率较快的原因为
溶液和铜反应速率较快的原因为______________________________ 。
Ⅱ.探究反应 为可逆反应 将浓度均为
为可逆反应 将浓度均为 的
的 溶液和
溶液和 溶液等体积混合,一段时间后,溶液变为黄色,且有灰黑色沉淀生成.
溶液等体积混合,一段时间后,溶液变为黄色,且有灰黑色沉淀生成.
(3)若要证明该反应为可逆反应,只需用 溶液检测出有
溶液检测出有 的存在即可,写出该检测反应的离子方程式
的存在即可,写出该检测反应的离子方程式_________________________ 。
Ⅲ.测定反应 的平衡常数
的平衡常数
取 中上层清液,用
中上层清液,用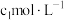 酸性
酸性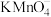 溶液滴定上层清液中剩余的
溶液滴定上层清液中剩余的 ,并记录滴定终点所消耗的酸性
,并记录滴定终点所消耗的酸性 溶液的体积;重复滴定3次,平均消耗酸性
溶液的体积;重复滴定3次,平均消耗酸性 溶液的体积为
溶液的体积为 .
.
(4)滴定至接近终点时,控制标准溶液半滴滴入,其操作是用锥形瓶口内壁轻靠滴定管尖嘴悬挂的液滴.要使这半滴液体流入锥形瓶内的操作是___________ ;滴定终点时的现象为___________ 。
(5)平衡时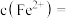
___________ (用含V、 、
、 的代数式表示),由此可计算出反应的平衡常数K.若盛装酸性
的代数式表示),由此可计算出反应的平衡常数K.若盛装酸性 溶液的滴定管未润洗,则计算得到的K值
溶液的滴定管未润洗,则计算得到的K值___________ (填“偏大”“偏小”或“不影响”)。
 和
和 的氧化能力设计如下实验.
的氧化能力设计如下实验.Ⅰ.探究
 和
和 氧化
氧化 的速率向体积均为
的速率向体积均为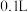 、浓度均为
、浓度均为 的
的 溶液和
溶液和 溶液中加入表面积相同、质量相等的铜片,反应一段时间后,经检验,
溶液中加入表面积相同、质量相等的铜片,反应一段时间后,经检验, 已完全消耗,
已完全消耗, 还有剩余.该小组同学猜测
还有剩余.该小组同学猜测 和
和 的氧化能力:
的氧化能力: .
.(1)检验溶液中还有
 剩余的试剂为
剩余的试剂为(2)相较于
 溶液,
溶液, 溶液和铜反应速率较快的原因为
溶液和铜反应速率较快的原因为Ⅱ.探究反应
 为可逆反应 将浓度均为
为可逆反应 将浓度均为 的
的 溶液和
溶液和 溶液等体积混合,一段时间后,溶液变为黄色,且有灰黑色沉淀生成.
溶液等体积混合,一段时间后,溶液变为黄色,且有灰黑色沉淀生成.(3)若要证明该反应为可逆反应,只需用
 溶液检测出有
溶液检测出有 的存在即可,写出该检测反应的离子方程式
的存在即可,写出该检测反应的离子方程式Ⅲ.测定反应
 的平衡常数
的平衡常数 取
 中上层清液,用
中上层清液,用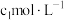 酸性
酸性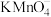 溶液滴定上层清液中剩余的
溶液滴定上层清液中剩余的 ,并记录滴定终点所消耗的酸性
,并记录滴定终点所消耗的酸性 溶液的体积;重复滴定3次,平均消耗酸性
溶液的体积;重复滴定3次,平均消耗酸性 溶液的体积为
溶液的体积为 .
.(4)滴定至接近终点时,控制标准溶液半滴滴入,其操作是用锥形瓶口内壁轻靠滴定管尖嘴悬挂的液滴.要使这半滴液体流入锥形瓶内的操作是
(5)平衡时
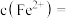
 、
、 的代数式表示),由此可计算出反应的平衡常数K.若盛装酸性
的代数式表示),由此可计算出反应的平衡常数K.若盛装酸性 溶液的滴定管未润洗,则计算得到的K值
溶液的滴定管未润洗,则计算得到的K值
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某实验小组利用下图所列装置进行“铁与水蒸气反应”的实验,并利用产物进一步制取FeCl3•6H2O晶体(图中夹持及尾气处理装置均已略去)。请回答下列问题:
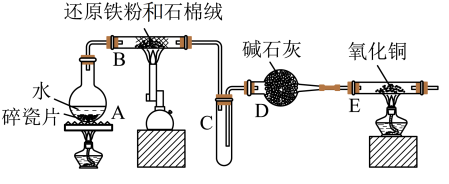
(1)装置B中发生反应的化学方程式是______________________________ .
(2)E中出现的现象是______________________ .
(3)该小组把B中反应后的产物加入到足量的盐酸中,用该溶液制取FeCl3•6H2O晶体.
①欲检验溶液中含有Fe3+,选用的试剂为________________ ,现象是_______________ .
②该实验小组同学用上述试剂没有检测到Fe3+,用离子方程式解释滤液中不存在Fe3+可能的原因:_______________________ .
③将此滤液中FeCl2完全氧化为FeCl3最好选择下列物质中的_______ .

(1)装置B中发生反应的化学方程式是
(2)E中出现的现象是
(3)该小组把B中反应后的产物加入到足量的盐酸中,用该溶液制取FeCl3•6H2O晶体.
①欲检验溶液中含有Fe3+,选用的试剂为
②该实验小组同学用上述试剂没有检测到Fe3+,用离子方程式解释滤液中不存在Fe3+可能的原因:
③将此滤液中FeCl2完全氧化为FeCl3最好选择下列物质中的
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】无水 常作为芳烃氯代反应的催化剂。某研究小组设计了如下流程,以废铁屑(含有少量碳和
常作为芳烃氯代反应的催化剂。某研究小组设计了如下流程,以废铁屑(含有少量碳和 杂质)为原料制备无水
杂质)为原料制备无水 。
。
已知:氯化亚砜(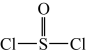 )熔点-101℃,沸点76℃,易水解。
)熔点-101℃,沸点76℃,易水解。
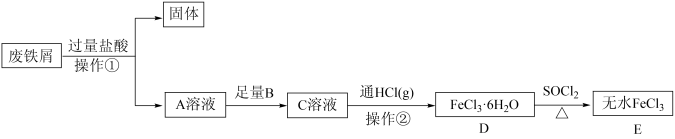
回答问题:
(1)操作①是过滤,用到的玻璃仪器有烧杯、玻璃棒和___________ 。
(2)为避免引入新的杂质,试剂B可以选用___________(填编号)。
(3)如何确定C溶液中是否含有二价铁___________
(4)操作②是蒸发结晶,加热的同时通入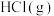 的目的是
的目的是___________ 。
(5)取少量D晶体,溶于水并滴加KSCN溶液,现象是___________ 。
(6)反应D→E的化学方程式为___________
(7)由D转化成E的过程中可能产生少量亚铁盐,写出一种可能的还原剂___________ ,并设计实验验证是该还原剂将 还原
还原___________ 。
 常作为芳烃氯代反应的催化剂。某研究小组设计了如下流程,以废铁屑(含有少量碳和
常作为芳烃氯代反应的催化剂。某研究小组设计了如下流程,以废铁屑(含有少量碳和 杂质)为原料制备无水
杂质)为原料制备无水 。
。已知:氯化亚砜(
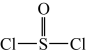 )熔点-101℃,沸点76℃,易水解。
)熔点-101℃,沸点76℃,易水解。
回答问题:
(1)操作①是过滤,用到的玻璃仪器有烧杯、玻璃棒和
(2)为避免引入新的杂质,试剂B可以选用___________(填编号)。
A. 溶液 溶液 | B. 水 水 | C. 水 水 | D. 溶液 溶液 |
(4)操作②是蒸发结晶,加热的同时通入
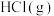 的目的是
的目的是(5)取少量D晶体,溶于水并滴加KSCN溶液,现象是
(6)反应D→E的化学方程式为
(7)由D转化成E的过程中可能产生少量亚铁盐,写出一种可能的还原剂
 还原
还原
您最近一年使用:0次
【推荐1】向溴水中加入足量乙醛溶液,可以看到溴水褪色。据此对溴水与乙醛发生的有机反应类型进行如下探究,请你完成下列填空:
Ⅰ.猜测:
(1)溴水与乙醛发生取代反应;
(2)溴水与乙醛发生加成反应;
(3)溴水与乙醛发生___ 反应。
Ⅱ.设计方案并论证:
为探究哪一种猜测正确,某研究性学习小组提出了如下两种实验方案:
方案1:检验褪色后溶液的酸碱性。
方案2:测定反应前用于溴水制备的Br2的物质的量和反应后Br-离子的物质的量。
(1)方案1是否可行?___ ?理由是___ 。
(2)假设测得反应前用于溴水制备的Br2的物质的量为amol,
若测得反应后n(Br-)=___ mol,则说明溴水与乙醛发生加成反应;
若测得反应后n(Br-)=___ mol,则说明溴水与乙醛发生取代反应;
若测得反应后n(Br-)=___ mol,则说明猜测(3)正确。
Ⅲ.实验验证:某同学在含0.005molBr2的10mL溶液中,加入足量乙醛溶液使其褪色;再加入过量AgNO3溶液,得到淡黄色沉淀1.88g(已知反应生成有机物与AgNO3不反应)。根据计算结果,推知溴水与乙醛反应的离子方程式为___ 。
Ⅳ.拓展:
请你设计对照实验,探究乙醛和乙醇的还原性强弱(填写下表)。
Ⅰ.猜测:
(1)溴水与乙醛发生取代反应;
(2)溴水与乙醛发生加成反应;
(3)溴水与乙醛发生
Ⅱ.设计方案并论证:
为探究哪一种猜测正确,某研究性学习小组提出了如下两种实验方案:
方案1:检验褪色后溶液的酸碱性。
方案2:测定反应前用于溴水制备的Br2的物质的量和反应后Br-离子的物质的量。
(1)方案1是否可行?
(2)假设测得反应前用于溴水制备的Br2的物质的量为amol,
若测得反应后n(Br-)=
若测得反应后n(Br-)=
若测得反应后n(Br-)=
Ⅲ.实验验证:某同学在含0.005molBr2的10mL溶液中,加入足量乙醛溶液使其褪色;再加入过量AgNO3溶液,得到淡黄色沉淀1.88g(已知反应生成有机物与AgNO3不反应)。根据计算结果,推知溴水与乙醛反应的离子方程式为
Ⅳ.拓展:
请你设计对照实验,探究乙醛和乙醇的还原性强弱(填写下表)。
| 实验操作步骤 | 实验现象 | 结论 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某实验小组拟探究铁的化合物(FeS2O6)的分解产物,设计如下实验。已知几种物质的物理性质如下表所示。
实验装置如图所示(加热和夹持装置省略)。
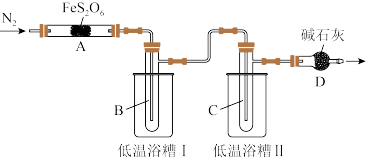
回答下列问题:
(1)仪器D的名称是_______ 。
(2)点燃酒精灯之前,通入一段时间N2,其目的是_______ 。
(3)低温浴槽II控制的温度范围为_______ 。
(4)甲、乙、丙三组分别进行实验,测得相关实验数据如下(不考虑损失且不考虑O2的存在,固体已完全分解):
①根据实验数据分析,甲组实验中A装置得到的纯净固体产物是_______ (填化学式)。
②经检测,乙组实验的固体产物为纯净物,写出A中发生的化学反应方程式:_______ 。
(5)为了进一步分析丙组实验得到的固体纯净物成分,他们取少量固体溶于稀硫酸中,将溶液分成两份,进行如下实验(不考虑O2的存在):
根据实验推知,丙组实验中FeS2O6分解生成的固体产物、SO3、SO2的物质的量之比为_______ 。
(6)为了进一步探究气体产物成分,将D仪器导出的气体通入酸化的KI-淀粉溶液中,一段时间后,若_______ (填实验现象),则说明有O2生成。
| 物质 | SO3 | SO2 | O2 |
| 熔点/°C | 16.8 | -75.5 | 218.4 |
| 沸点/°C | 44.8 | -10 | -182.9 |

回答下列问题:
(1)仪器D的名称是
(2)点燃酒精灯之前,通入一段时间N2,其目的是
(3)低温浴槽II控制的温度范围为
(4)甲、乙、丙三组分别进行实验,测得相关实验数据如下(不考虑损失且不考虑O2的存在,固体已完全分解):
| A处温度/°C | FeS2O6质量/g | 低温浴槽I净增质量/g | 低温浴槽II净增质量/g | |
| 甲 | T1 | 2.16 | 0 | 0.64 |
| 乙 | T2 | 4.32 | 0.80 | 1.92 |
| 丙 | T3 | 6.48 | 1.60 | 2.56 |
②经检测,乙组实验的固体产物为纯净物,写出A中发生的化学反应方程式:
(5)为了进一步分析丙组实验得到的固体纯净物成分,他们取少量固体溶于稀硫酸中,将溶液分成两份,进行如下实验(不考虑O2的存在):
| 实验 | 操作 | 现象 |
| a | 在一份溶液中滴加K3[Fe(CN)6]溶液 | 产生蓝色沉淀 |
| b | 在另一份溶液中滴加NH4SCN溶液 | 溶液变红色 |
(6)为了进一步探究气体产物成分,将D仪器导出的气体通入酸化的KI-淀粉溶液中,一段时间后,若
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某研究性学习小组设计了一组实验来探究元素周期律。
I.甲同学设计了一套实验方案,并记录了有关实验现象(表中“实验步骤”与“实验现象”前后不一定是对应关系)。请你帮助该同学整理并完成实验报告:
(1)实验内容:(填写与实验步骤对应的实验现象编号和实验①②对应的化学方程式)
①_______ ;
②_______ ;
(2)实验的结论:_______ 。
II.乙同学利用如图装置探究同主族元素非金属性的变化规律。
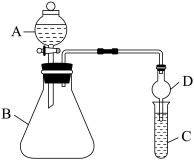
(1)仪器D的名称为_______ ,作用为_______ 。
(2)证明非金属性:Cl>I,C中为淀粉-碘化钾混合溶液,B中装有KClO3固体,则A中试剂为_______ ,B中发生反应的化学反应方程式_______ ,观察到C中_______ (填现象),即可证明。从环境保护的观点考虑,此装置缺少尾气处理装置,可用_______ 溶液吸收尾气。
(3)证明非金属性:C>Si,在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液。观察到C中_______ (填现象),发生反应的离子方程式_______ ,即可证明。
(4)丙同学认为实验结果不正确,应在A和C装置之间添加装有_______ 的洗气瓶,才能证明非金属性:C>Si。对丙同学的结论进行解释:__________ 。
I.甲同学设计了一套实验方案,并记录了有关实验现象(表中“实验步骤”与“实验现象”前后不一定是对应关系)。请你帮助该同学整理并完成实验报告:
| 实验步骤 | 实验现象 |
| ①镁条用砂纸打磨后放入试管,加少量水加热至沸腾;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,溶液变成红色 |
| ②向新制的Na2S溶液中滴加新制的氯水 | B.有气体产生,溶液变成浅红色 |
| ③将一小块金属钠放入滴有酚酞的冷水 | C.剧烈反应,迅速产生大量无色气体 |
| ④将镁条投入稀盐酸中 | D.反应不剧烈,产生无色气体 |
| ⑤将铝条投入稀盐酸中 | E.生成淡黄色沉淀 |
| 实验内容 | ① | ② | ③ | ④ | ⑤ |
| 实验现象(填A~F) |
②
(2)实验的结论:
II.乙同学利用如图装置探究同主族元素非金属性的变化规律。

(1)仪器D的名称为
(2)证明非金属性:Cl>I,C中为淀粉-碘化钾混合溶液,B中装有KClO3固体,则A中试剂为
(3)证明非金属性:C>Si,在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液。观察到C中
(4)丙同学认为实验结果不正确,应在A和C装置之间添加装有
您最近一年使用:0次