请按要求回答下列问题:
(1)钠在空气中燃烧生成淡黄色的固体,则其化学方程式为_______ ;
(2) 能溶于酸或强碱溶液生成盐和水,则是一种
能溶于酸或强碱溶液生成盐和水,则是一种_______ (填“酸性”、“碱性”或“两性”)氧化物;
(3)装氢氧化钠溶液的试剂瓶不能用玻璃塞,请用离子方程式表示原因:_______ 。
(4)某同学在做 的一次实验中,用过量的稀硝酸(其密度为1.05g/mL,
的一次实验中,用过量的稀硝酸(其密度为1.05g/mL, 的质量分数为12%)跟一定量的铁片反应,产生了标准状况下0.56L的一氧化氮,该稀硝酸的物质的量浓度为
的质量分数为12%)跟一定量的铁片反应,产生了标准状况下0.56L的一氧化氮,该稀硝酸的物质的量浓度为_______ ,被还原的 的物质的量为
的物质的量为_______ 。
(1)钠在空气中燃烧生成淡黄色的固体,则其化学方程式为
(2)
 能溶于酸或强碱溶液生成盐和水,则是一种
能溶于酸或强碱溶液生成盐和水,则是一种(3)装氢氧化钠溶液的试剂瓶不能用玻璃塞,请用离子方程式表示原因:
(4)某同学在做
 的一次实验中,用过量的稀硝酸(其密度为1.05g/mL,
的一次实验中,用过量的稀硝酸(其密度为1.05g/mL, 的质量分数为12%)跟一定量的铁片反应,产生了标准状况下0.56L的一氧化氮,该稀硝酸的物质的量浓度为
的质量分数为12%)跟一定量的铁片反应,产生了标准状况下0.56L的一氧化氮,该稀硝酸的物质的量浓度为 的物质的量为
的物质的量为
更新时间:2023-06-07 18:27:24
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】硝酸是一种具有强氧化性、腐蚀性的强酸,其还原产物因硝酸浓度的不同而变化,总体上说,硝酸浓度越高,平均每分子硝酸得到的电子数越少,浓硝酸的还原产物主要为 、稀硝酸的还原产物为
、稀硝酸的还原产物为 。实验室常用
。实验室常用 与浓
与浓 反应制取
反应制取 ,用
,用 与稀
与稀 反应制取
反应制取 。
。
(1)请写出实验室中用 与稀
与稀 反应制取
反应制取 的化学方程式并用双线桥标明电子的转移方向及数目:
的化学方程式并用双线桥标明电子的转移方向及数目:________________________________ 。
(2)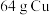 与适量的浓
与适量的浓 反应,铜全部作用后,共收集到
反应,铜全部作用后,共收集到 气体(标准状况),反应中消耗的
气体(标准状况),反应中消耗的 的物质的量是
的物质的量是________ (填序号)。产生的气体是________ ,其物质的量之比是________ 。
A.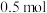 B.
B.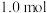 C.
C.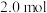 D.
D.
(3)实际上硝酸不仅可被还原为 或
或 ,浓度更低时硝酸还可以被还原为
,浓度更低时硝酸还可以被还原为 、
、 或
或 等,请将下列3种物质:
等,请将下列3种物质: 、
、 和
和 分别填入下面对应的横线上,并配平该反应的化学方程式。
分别填入下面对应的横线上,并配平该反应的化学方程式。_____ 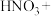
_____ 
_____ 
_____ 
_____ 
_____ 
 、稀硝酸的还原产物为
、稀硝酸的还原产物为 。实验室常用
。实验室常用 与浓
与浓 反应制取
反应制取 ,用
,用 与稀
与稀 反应制取
反应制取 。
。(1)请写出实验室中用
 与稀
与稀 反应制取
反应制取 的化学方程式并用双线桥标明电子的转移方向及数目:
的化学方程式并用双线桥标明电子的转移方向及数目:(2)
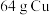 与适量的浓
与适量的浓 反应,铜全部作用后,共收集到
反应,铜全部作用后,共收集到 气体(标准状况),反应中消耗的
气体(标准状况),反应中消耗的 的物质的量是
的物质的量是A.
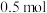 B.
B.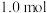 C.
C.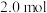 D.
D.
(3)实际上硝酸不仅可被还原为
 或
或 ,浓度更低时硝酸还可以被还原为
,浓度更低时硝酸还可以被还原为 、
、 或
或 等,请将下列3种物质:
等,请将下列3种物质: 、
、 和
和 分别填入下面对应的横线上,并配平该反应的化学方程式。
分别填入下面对应的横线上,并配平该反应的化学方程式。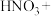





您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】下列反应或者现象主要体现了硝酸的什么性质?久置浓硝酸显黄色________ (填序号,下同),用稀硝酸清洗试管壁上的银________ ,稀硝酸清洗石灰水试剂瓶壁上的固体________ ,用浓硝酸清洗积碳的试管________ 。
①(强)氧化性 ②酸性 ③还原性 ④不稳定性 ⑤挥发性 ⑥脱水性 ⑦吸水性
①(强)氧化性 ②酸性 ③还原性 ④不稳定性 ⑤挥发性 ⑥脱水性 ⑦吸水性
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】SO2是主要大气污染物之一,其产生和治理是环境科学的主要研究方向。完成下列问题:
(1)SO2和O3是等电子体,有相似的结构质。以下关于O3的描述正确的是___________。(复选,填序号)
(2)SO2与CO2都属于酸性氧化物,以下关于两者比较正确的是___________。(复选,填序号)
(3)SO2能与稀硝酸反应生成NO,写出反应的化学方程式:___________ 。能否说明硝酸的酸性比硫酸强?说明理由___________ 。
(1)SO2和O3是等电子体,有相似的结构质。以下关于O3的描述正确的是___________。(复选,填序号)
| A.空间构型为直线形 | B.属于非电解质 |
| C.具有较强的氧化性 | D.属于极性分子 |
| A.都能使品红褪色 | B.都能使酸性KMnO4溶液褪色 |
| C.都能与Na2CO3反应 | D.都能与NaOH反应 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】月球含有H、He、N、Na、Mg、Si等元素,是人类未来的资源宝库。
(1)3He是高效核能原料,其原子核内中子数为_____________ 。
(2)Na的原子结构示意图为______ 。
(3)MgCl2在工业上应用广泛,可由MgO制备。
①月球上某矿石经处理得到的MgO中含有少量SiO2,用NaOH溶液除去SiO2的化学方程式为______ 。
②MgO与炭粉和氯气在一定条件下反应可制备MgCl2,尾气中的氯气可用足量冷的NaOH溶液完全吸收,则生成的盐为_________ 、_________ (写化学式)。
(1)3He是高效核能原料,其原子核内中子数为
(2)Na的原子结构示意图为
(3)MgCl2在工业上应用广泛,可由MgO制备。
①月球上某矿石经处理得到的MgO中含有少量SiO2,用NaOH溶液除去SiO2的化学方程式为
②MgO与炭粉和氯气在一定条件下反应可制备MgCl2,尾气中的氯气可用足量冷的NaOH溶液完全吸收,则生成的盐为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】500多年前,一艘载着天然苏打晶体的商船在航行中搁浅,船员们便在附近的沙滩上用几块苏打晶体支锅煮饭。之后他们惊奇地发现,在苏打与沙粒接触处出现了许多晶莹发亮的珠子。回答下列问题:
(1)请你分析一下,这种珠子可能是_______ (填序号,下同)。
A.水晶颗粒 B.无水碳酸钠 C.玻璃珠 D.晶体硅
(2)下列可用来熔融苏打晶体的坩埚是______ 。
A.玛瑙坩埚 B.石英坩埚 C.铁坩埚
(1)请你分析一下,这种珠子可能是
A.水晶颗粒 B.无水碳酸钠 C.玻璃珠 D.晶体硅
(2)下列可用来熔融苏打晶体的坩埚是
A.玛瑙坩埚 B.石英坩埚 C.铁坩埚
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】氮化硅(Si3N4)是一种优良的高温结构陶瓷,在工业生产和科技领域中有重要用途。工业上有多种方法来制备氮化硅,下面是几种常见的方法:
(1)方法一——直接氮化法:在1300~1400 ℃时,高纯粉状硅与纯氮气化合,其反应方程式为3Si+2N21300~1400 ℃,Si3N4。
(2)方法二——可以用NH3和SiH4(硅烷)在一定条件下反应,并在600 ℃的加热基板上生成氮化硅膜,其化学方程式为________________________________________________________ 。
(3)方法三——化学气相沉积法:在高温条件下利用四氯化硅气体、纯氮气、氢气反应生成氮化硅和氯化氢,与方法一相比,用此法制得的氮化硅纯度较高,其原因是_______________________ 。
(4)方法四——Si(NH2)4热分解法:先用四氯化硅与氨气反应生成Si(NH2)4和一种气体:________ (填化学式);然后使Si(NH2)4受热分解,分解后的另一种产物的化学式为________ 。
工业上制取高纯硅和四氯化硅的生产流程如下:

已知:X、高纯硅、原料B的主要成分都可与Z反应,Y与X在光照或点燃条件下可反应,Z的焰色呈黄色。
(5)写出焦炭与原料B中的主要成分反应的化学方程式:________________________________________________________ 。
(1)方法一——直接氮化法:在1300~1400 ℃时,高纯粉状硅与纯氮气化合,其反应方程式为3Si+2N21300~1400 ℃,Si3N4。
(2)方法二——可以用NH3和SiH4(硅烷)在一定条件下反应,并在600 ℃的加热基板上生成氮化硅膜,其化学方程式为
(3)方法三——化学气相沉积法:在高温条件下利用四氯化硅气体、纯氮气、氢气反应生成氮化硅和氯化氢,与方法一相比,用此法制得的氮化硅纯度较高,其原因是
(4)方法四——Si(NH2)4热分解法:先用四氯化硅与氨气反应生成Si(NH2)4和一种气体:
工业上制取高纯硅和四氯化硅的生产流程如下:

已知:X、高纯硅、原料B的主要成分都可与Z反应,Y与X在光照或点燃条件下可反应,Z的焰色呈黄色。
(5)写出焦炭与原料B中的主要成分反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】某课外实验小组从煤油中取出一块钠,用滤纸吸干 其表面的煤油,用刀切下数块,分别进行实验研究。
其表面的煤油,用刀切下数块,分别进行实验研究。
(1)钠块切面表面迅速变暗,反应的化学方程式为______ 。
(2)将其中一块钠放入坩埚中加热,反应现象为:钠熔化并燃烧_______ 。
(3)将一小块钠放入燃烧匙中,加热,迅速伸入盛有氯气的集气瓶中,反应的化学方程式为______________ 。
(4)钠在空气中的燃烧产物可用于呼吸面具或潜水艇中氧气的来源,涉及的主要反应的化学方程式为①________ ,②_______ 。若15.6g Na2O2参加反应,则最多可制得标准状况下氧气的体积为______ L。
 其表面的煤油,用刀切下数块,分别进行实验研究。
其表面的煤油,用刀切下数块,分别进行实验研究。(1)钠块切面表面迅速变暗,反应的化学方程式为
(2)将其中一块钠放入坩埚中加热,反应现象为:钠熔化并燃烧
(3)将一小块钠放入燃烧匙中,加热,迅速伸入盛有氯气的集气瓶中,反应的化学方程式为
(4)钠在空气中的燃烧产物可用于呼吸面具或潜水艇中氧气的来源,涉及的主要反应的化学方程式为①
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】钠、铝和铁是中学化学常见的三种重要金属。请回答下列问题:
(1)钠在空气中燃烧生成淡黄色的_______ (填“Na2O”或“Na2O2”); Al2O3能溶于酸或强碱溶液生成盐和水,则是一种_______ (填“酸性”、“碱性”或“两性”)氧化物;
(2)写出钠与水反应的化学方程式:_______ 。
(3)写出铝与NaOH溶液反应的化学方程式:_______ ;
(4)现有下列3种物质:①Na2O2、②NaHCO3、③Na2CO3,请回答:受热易分解的是_______ (填序号,下同),溶于水显碱性的是_______ ,与CO2反应产生的气体能使带火星木条复燃的是_______ 。
(1)钠在空气中燃烧生成淡黄色的
(2)写出钠与水反应的化学方程式:
(3)写出铝与NaOH溶液反应的化学方程式:
(4)现有下列3种物质:①Na2O2、②NaHCO3、③Na2CO3,请回答:受热易分解的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】现有下列物质:
①KCl ②CH4 ③NH4NO3 ④I2 ⑤Na2O2 ⑥HClO4 ⑦N2 ⑧CO ⑨SO2 ⑩金刚石 ⑪CH3CH2OH ⑫MgO ⑬MgCl2 ⑭KOH ⑮HCl ⑯Al2O3
请回答下列问题。
(1)两性氧化物是___ (填序号),其电子式为___ 。
(2)最简单的有机化合物是___ (填序号),用电子式表示其形成过程:___ 。
(3)属于共价化合物的是___ (填序号),含有共价键的离子化合物是___ (填序号)。
(4)由两种元素组成,且含有离子键和共价键的化合物为___ (填序号),这两种元素的单质反应生成该化合物的化学方程式为___ 。
①KCl ②CH4 ③NH4NO3 ④I2 ⑤Na2O2 ⑥HClO4 ⑦N2 ⑧CO ⑨SO2 ⑩金刚石 ⑪CH3CH2OH ⑫MgO ⑬MgCl2 ⑭KOH ⑮HCl ⑯Al2O3
请回答下列问题。
(1)两性氧化物是
(2)最简单的有机化合物是
(3)属于共价化合物的是
(4)由两种元素组成,且含有离子键和共价键的化合物为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是:_____ (填具体化学用语,下同)。
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是______ ,碱性最强的化合物的电子式是:_____ 。
(3)最高价氧化物是两性氧化物的元素是___ ;写出它的氧化物与氢氧化钠反应的离子方程式__ 。
(4)②氢化物与③的单质在一定条件下反应的化学方程式为:______ 。
(5)②可以形成多种氧化物,其中一种是红棕色气体,试用方程式说明该气体不宜采用排水法收集的原因________ 。
(6)用结构式表示元素①与③形成的化合物____ ,该化合物在固体时俗称___ ,属于____ 晶体,指出它的一种用途___ 。
主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是
(3)最高价氧化物是两性氧化物的元素是
(4)②氢化物与③的单质在一定条件下反应的化学方程式为:
(5)②可以形成多种氧化物,其中一种是红棕色气体,试用方程式说明该气体不宜采用排水法收集的原因
(6)用结构式表示元素①与③形成的化合物
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】铝及其化合物在生产生活中有着广泛的应用。
(1)Al﹣Mg合金焊接前用NaOH溶液处理铝表面Al2O3膜,其化学反应方程式为_______ 。
(2)某同学实验时发现Al﹣Mg合金与NaOH溶液反应时的速率比纯铝与NaOH溶液反应时的速率快,原因是_______ 。
(3)饮用水中的 对人类健康会产生危害。为了降低饮用水中
对人类健康会产生危害。为了降低饮用水中 的浓度,有研究人员建议在碱性条件下用铝粉将
的浓度,有研究人员建议在碱性条件下用铝粉将 还原为N2,该反应的离子方程式为
还原为N2,该反应的离子方程式为_______ 。
(4)碱式碳酸铝钠[NaaAlb(OH)c(CO3)d]可用作阻燃剂、抗酸剂等。其制备方法是控制温度、pH,向NaHCO3稀溶液中加入Al(OH)3,并搅拌,充分反应后过滤、洗涤、干燥,得碱式碳酸铝钠。
①碱式碳酸铝钠[NaaAlb(OH)c(CO3)d]中a、b、c、d之间的关系为_______ 。
②碱式碳酸铝钠作为阻燃剂的可能原因是产生阻燃性气体CO2、H2O本身及产物无毒且不可燃;_______ 。
③若pH过高,则对产品的影响是_______ 。
(1)Al﹣Mg合金焊接前用NaOH溶液处理铝表面Al2O3膜,其化学反应方程式为
(2)某同学实验时发现Al﹣Mg合金与NaOH溶液反应时的速率比纯铝与NaOH溶液反应时的速率快,原因是
(3)饮用水中的
 对人类健康会产生危害。为了降低饮用水中
对人类健康会产生危害。为了降低饮用水中 的浓度,有研究人员建议在碱性条件下用铝粉将
的浓度,有研究人员建议在碱性条件下用铝粉将 还原为N2,该反应的离子方程式为
还原为N2,该反应的离子方程式为(4)碱式碳酸铝钠[NaaAlb(OH)c(CO3)d]可用作阻燃剂、抗酸剂等。其制备方法是控制温度、pH,向NaHCO3稀溶液中加入Al(OH)3,并搅拌,充分反应后过滤、洗涤、干燥,得碱式碳酸铝钠。
①碱式碳酸铝钠[NaaAlb(OH)c(CO3)d]中a、b、c、d之间的关系为
②碱式碳酸铝钠作为阻燃剂的可能原因是产生阻燃性气体CO2、H2O本身及产物无毒且不可燃;
③若pH过高,则对产品的影响是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)将Al、Al2O3和Al(OH)3的混合物恰好与NaOH溶液反应,反应后溶液中溶质的化学式为_________ 。向反应后的溶液中通入少量CO2,反应的离子方程式为 _______________ 。
(2)在100mLFeBr2溶液中通入标准状况下2.24LCl2,溶液中有1/4的Br- 被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为______________ (结果保留两位小数)。
(3)三氟化氮(NF3)是一种无色无味的气体,它是微电子工业技术的关键原料之一,三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,请根据要求回答下列问题:
①写出该反应的化学方程式___________________ ,反应中生成0.2mol HNO3,转移的电子数目为__________ 。
②NF3无色、无臭,但一旦在空气中泄漏,还是易于发现,判断该气体泄漏时的现象是__________ 。
(2)在100mLFeBr2溶液中通入标准状况下2.24LCl2,溶液中有1/4的Br- 被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为
(3)三氟化氮(NF3)是一种无色无味的气体,它是微电子工业技术的关键原料之一,三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,请根据要求回答下列问题:
①写出该反应的化学方程式
②NF3无色、无臭,但一旦在空气中泄漏,还是易于发现,判断该气体泄漏时的现象是
您最近一年使用:0次



