研究硫及其化合物的应用价值对于社会发展意义重大。请回答以下问题:
(1)欲制备Na2S2O3,从氧化还原角度分析,下列方法合理的是___________(选填字母序号)。
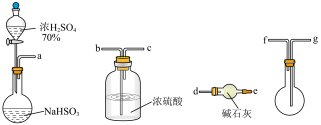
(2)用下图所示装置制备纯净的SO2(同时生成一种正盐),请写出发生装置中反应的化学方程式为___________ ,碱石灰的主要作用为___________ 。
(3)工业上回收利用SO2的一种途径是: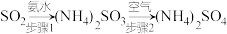 。
。
①写出少量SO2通入氨水发生的离子方程式___________ 。
②某实验小组为测定步骤2溶液中(NH4)2SO3的氧化率α,设计了以下实验方案。[提示:氧化率 ]
]
【方案一】一定条件下向100mL1mol∙L-的(NH4)2SO3溶液中通入空气后,先加入足量的稀盐酸,充分反应后,再加入足量BaCl2溶液,过滤、洗涤、烘干,得到沉淀18.64g。
I.计算(NH4)2SO3的氧化率α=___________ (用百分数表示)。
【方案二】一定条件下向100mLc0 mol∙L-1的(NH4)2SO3溶液中通入空气后,取20.00mL反应后的溶液于锥形瓶中,用浓度为c mol∙L-1的KMnO4标准溶液(经H2SO4酸化)滴定,滴定过程中锰元素被还原成Mn2+。重复操作三次,恰好完全反应时平均消耗KMnO4溶液的体积是Vml。
Ⅱ.写出滴定反应的离子方程式___________ 。
(1)欲制备Na2S2O3,从氧化还原角度分析,下列方法合理的是___________(选填字母序号)。
| A.Na2S+S | B.Na2SO3+S | C.Na2SO3+H2SO4 | D.SO2+Na2SO3 |

(3)工业上回收利用SO2的一种途径是:
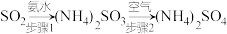 。
。①写出少量SO2通入氨水发生的离子方程式
②某实验小组为测定步骤2溶液中(NH4)2SO3的氧化率α,设计了以下实验方案。[提示:氧化率
 ]
]【方案一】一定条件下向100mL1mol∙L-的(NH4)2SO3溶液中通入空气后,先加入足量的稀盐酸,充分反应后,再加入足量BaCl2溶液,过滤、洗涤、烘干,得到沉淀18.64g。
I.计算(NH4)2SO3的氧化率α=
【方案二】一定条件下向100mLc0 mol∙L-1的(NH4)2SO3溶液中通入空气后,取20.00mL反应后的溶液于锥形瓶中,用浓度为c mol∙L-1的KMnO4标准溶液(经H2SO4酸化)滴定,滴定过程中锰元素被还原成Mn2+。重复操作三次,恰好完全反应时平均消耗KMnO4溶液的体积是Vml。
Ⅱ.写出滴定反应的离子方程式
更新时间:2023-07-17 21:09:55
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】加碘食盐所添加的含碘物质是碘酸钾(KIO3)。某化学兴趣小组欲自制碘酸钾,并测定所得产品的纯度,具体实验过程如下。完成下列填空。
(Ⅰ)碘酸钾的制取
反应原理:3Cl2+KI+6KOH 6KCl+KIO3+3H2O
6KCl+KIO3+3H2O
反应装置如图所示:
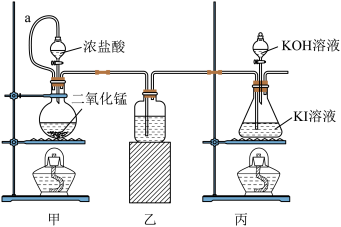
(1)装置 甲 为氯气发生装置,反应方程式为:____________________________________ 。
甲中橡胶管 a的作用是_____________________________________________________ 。
指出全套装置中存在的不足之处:____ 。
(2)用碘化钾固体配制一定物质的量浓度的 碘化钾溶液,下列仪器肯定不需要的是________________ (填仪器名称)。
(Ⅱ)分离提纯
步骤一 取丙中溶液,加入浓盐酸,搅拌、冷却、……,得到KH(IO3)2粗产品。
步骤二 将KH(IO3)2粗产品溶于水,加入KOH调节pH,蒸发结晶,得到KIO3产品。
(3)在完成(Ⅰ)碘酸钾的制取实验后,测得装置丙溶液中有KI剩余。若此时加入浓盐酸将导致碘酸钾的最终产率偏小,原因是_____________ (用离子反应方程式表示)。 将步骤一中所缺的操作补充完整______________________________________ 。
(Ⅲ)测定碘酸钾产品的纯度
称量wg碘酸钾产品,配成250mL溶液。取25.00mL,加入稍过量的KI与盐酸溶液,充分反应。然后加几滴淀粉指示剂,用0.1000 的Na2S2O3标准液滴定至终点,记录所消耗的标准液体积。(已知:2S2O
的Na2S2O3标准液滴定至终点,记录所消耗的标准液体积。(已知:2S2O + I2 = S4O
+ I2 = S4O + 2I- )
+ 2I- )
(4)经实验,测得消耗标准液的平均体积为VmL,试计算该碘酸钾产品的纯度:____ 。
(5)某同学欲利用家里常见的物质,模拟上述方法,检验自家所用食盐是否含有碘酸钾。为完成实验,请帮他选择所需要的试剂:家用食盐、干海带(含有 KI)、____ (限选居家生活中常用的物质)。
(Ⅰ)碘酸钾的制取
反应原理:3Cl2+KI+6KOH
 6KCl+KIO3+3H2O
6KCl+KIO3+3H2O反应装置如图所示:

(1)装置 甲 为氯气发生装置,反应方程式为:
甲中橡胶管 a的作用是
指出全套装置中存在的不足之处:
(2)用碘化钾固体配制一定物质的量浓度的 碘化钾溶液,下列仪器肯定不需要的是

(Ⅱ)分离提纯
步骤一 取丙中溶液,加入浓盐酸,搅拌、冷却、……,得到KH(IO3)2粗产品。
步骤二 将KH(IO3)2粗产品溶于水,加入KOH调节pH,蒸发结晶,得到KIO3产品。
(3)在完成(Ⅰ)碘酸钾的制取实验后,测得装置丙溶液中有KI剩余。若此时加入浓盐酸将导致碘酸钾的最终产率偏小,原因是
(Ⅲ)测定碘酸钾产品的纯度
称量wg碘酸钾产品,配成250mL溶液。取25.00mL,加入稍过量的KI与盐酸溶液,充分反应。然后加几滴淀粉指示剂,用0.1000
 的Na2S2O3标准液滴定至终点,记录所消耗的标准液体积。(已知:2S2O
的Na2S2O3标准液滴定至终点,记录所消耗的标准液体积。(已知:2S2O + I2 = S4O
+ I2 = S4O + 2I- )
+ 2I- )(4)经实验,测得消耗标准液的平均体积为VmL,试计算该碘酸钾产品的纯度:
(5)某同学欲利用家里常见的物质,模拟上述方法,检验自家所用食盐是否含有碘酸钾。为完成实验,请帮他选择所需要的试剂:家用食盐、干海带(含有 KI)、
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】“以废治废”是基于“绿色化学”观念治理污染的思路。用工业废碱渣(主要成分为 )吸收烟气中的
)吸收烟气中的 ,得到亚硫酸钠
,得到亚硫酸钠 粗品。其流程如下。
粗品。其流程如下。 的溶解,可采取的措施是
的溶解,可采取的措施是_______ (写出一种即可)。
(2)过程①进行的操作是_______ 。
(3)上述流程中;通入“含 的烟气”,发生反应的化学方程式为
的烟气”,发生反应的化学方程式为_______ 。
(4)上述流程中,加入NaOH后,发生反应的离子方程式为_______ 。
(5)设计实验证明亚硫酸钠粗品含有少量 的方案是:在一支试管中,加入少量亚硫酸钠粗品,用适量蒸馏水溶解,
的方案是:在一支试管中,加入少量亚硫酸钠粗品,用适量蒸馏水溶解,_______ ,出现白色沉淀,则证明含有 。
。
(6) 可用于处理酸性废水中的
可用于处理酸性废水中的 (转化为
(转化为 ),发生反应的离子方程式为
),发生反应的离子方程式为_______ 。
(7)某化工厂用如图所示工艺流程吸收烟气中的 。在标准状况下,当除去
。在标准状况下,当除去 时,消耗
时,消耗 的物质的量为
的物质的量为_______ mol。
 )吸收烟气中的
)吸收烟气中的 ,得到亚硫酸钠
,得到亚硫酸钠 粗品。其流程如下。
粗品。其流程如下。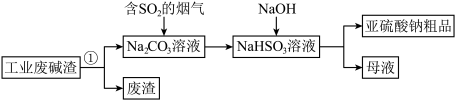
 的溶解,可采取的措施是
的溶解,可采取的措施是(2)过程①进行的操作是
(3)上述流程中;通入“含
 的烟气”,发生反应的化学方程式为
的烟气”,发生反应的化学方程式为(4)上述流程中,加入NaOH后,发生反应的离子方程式为
(5)设计实验证明亚硫酸钠粗品含有少量
 的方案是:在一支试管中,加入少量亚硫酸钠粗品,用适量蒸馏水溶解,
的方案是:在一支试管中,加入少量亚硫酸钠粗品,用适量蒸馏水溶解, 。
。(6)
 可用于处理酸性废水中的
可用于处理酸性废水中的 (转化为
(转化为 ),发生反应的离子方程式为
),发生反应的离子方程式为(7)某化工厂用如图所示工艺流程吸收烟气中的
 。在标准状况下,当除去
。在标准状况下,当除去 时,消耗
时,消耗 的物质的量为
的物质的量为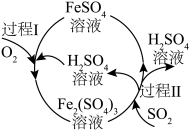
您最近一年使用:0次
【推荐3】亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,以下是过氧化氢法生产亚氯酸钠的工艺流程图:

回答下列问题:
(1)亚氯酸钠用作纸浆、纸张和各种纤维的漂白剂,是一种高效漂白剂,主要原因是亚氯酸钠具有___________ 性。
(2)写出制备ClO2的化学反应方程式:______________ 。
(3)可从“废液”中回收的主要物质是___________ (填化学式),“结晶”后经过滤即可获得粗产品。
(4)吸收塔的温度不能超过20°C,其目的是_____________ 。
(5)吸收塔内的反应的化学方程式为_____________ 。

回答下列问题:
(1)亚氯酸钠用作纸浆、纸张和各种纤维的漂白剂,是一种高效漂白剂,主要原因是亚氯酸钠具有
(2)写出制备ClO2的化学反应方程式:
(3)可从“废液”中回收的主要物质是
(4)吸收塔的温度不能超过20°C,其目的是
(5)吸收塔内的反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某化学兴趣小组用以下装置制备SO2并探究其部分性质。_______ ,装置B可贮存多余的SO2,B中试剂瓶内应盛放的液体是_______ 。
(2)若装置C中溶液无明显现象,装置D中溶液红色褪去,说明使品红水溶液褪色的含硫微粒是_______ (填化学式)。
(3)通入SO2后,E中溶液立即由棕黄色变成红棕色,将混合液静置12小时后,溶液变成浅绿色。查阅资料,发现溶液出现红棕色是因为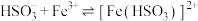 (红棕色)。
(红棕色)。
①溶液中产生 的离子方程式为
的离子方程式为_______ 。与该过程发生的其他化学反应相比, 与Fe3+反应生成[Fe(HSO3)]2+的活化能更
与Fe3+反应生成[Fe(HSO3)]2+的活化能更_______ (填“大”或“小”)。
②红棕色的[Fe(HSO3)]2+与Fe3+反应,溶液变成浅绿色,反应的离子方程式为_______ ;检验生成的阴离子的方法_______ 。
③为了缩短红棕色变为浅绿色的时间,该小组进行如下实验:
实验Ⅰ:往5 mL 1 mol/LFeCl3溶液中通入SO2,微热3分钟,溶液变为浅绿色。
实验Ⅱ:用浓盐酸酸化FeCl3溶液后再通入SO2,几分钟后,溶液变为浅绿色。
结论:通过_______ 可缩短浅绿色出现的时间。
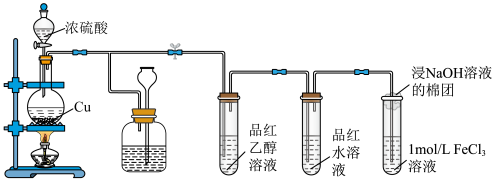
A B C D E
(1)装置A中制备SO2的化学反应方程式为(2)若装置C中溶液无明显现象,装置D中溶液红色褪去,说明使品红水溶液褪色的含硫微粒是
(3)通入SO2后,E中溶液立即由棕黄色变成红棕色,将混合液静置12小时后,溶液变成浅绿色。查阅资料,发现溶液出现红棕色是因为
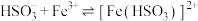 (红棕色)。
(红棕色)。①溶液中产生
 的离子方程式为
的离子方程式为 与Fe3+反应生成[Fe(HSO3)]2+的活化能更
与Fe3+反应生成[Fe(HSO3)]2+的活化能更②红棕色的[Fe(HSO3)]2+与Fe3+反应,溶液变成浅绿色,反应的离子方程式为
③为了缩短红棕色变为浅绿色的时间,该小组进行如下实验:
实验Ⅰ:往5 mL 1 mol/LFeCl3溶液中通入SO2,微热3分钟,溶液变为浅绿色。
实验Ⅱ:用浓盐酸酸化FeCl3溶液后再通入SO2,几分钟后,溶液变为浅绿色。
结论:通过
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】硫酸是一种重要的化学试剂。某实验小组的同学利用浓硫酸制取二氧化硫并探究其性质。请按要求回答下列问题。

(1)上图装置中的仪器a的名称是______________ 。
(2)将产生的二氧化硫通入品红溶液中,可观察到的现象是______________ 。
(3)上述实验所产生的二氧化硫尾气需用____________ 溶液吸收。
(4)现用18 mol/L的浓硫酸来配制500 mL 1.8 mol/L的硫酸溶液,所需浓硫酸的体积为_____ mL,配制时可供选择的仪器有:①玻璃棒 ②烧杯 ③胶头滴管 ④量筒。上述仪器中,还缺少的一种仪器是__________ (填数字代号)。

(1)上图装置中的仪器a的名称是
(2)将产生的二氧化硫通入品红溶液中,可观察到的现象是
(3)上述实验所产生的二氧化硫尾气需用
(4)现用18 mol/L的浓硫酸来配制500 mL 1.8 mol/L的硫酸溶液,所需浓硫酸的体积为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】二氧化氯是高效、低毒的消毒剂。已知: 是极易溶于水的气体,实验室制备及性质探究装置如图所示。回答下列问题:
是极易溶于水的气体,实验室制备及性质探究装置如图所示。回答下列问题:
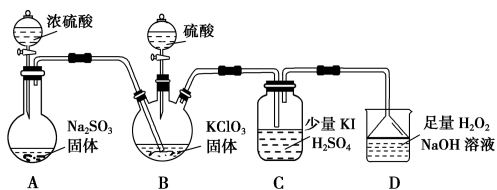
(1)装置B用于制备 ,同时还生成一种酸式盐,该反应的化学方程式为
,同时还生成一种酸式盐,该反应的化学方程式为_______ 。装置C中滴有几滴淀粉溶液,反应时有蓝色出现,淀粉的作用是_______ 。
(2)C装置的导管靠近而不接触液面,其目的是_______ 。
(3)若将C装置中的溶液改为 溶液,通入
溶液,通入 后溶液无明显现象。由此可以产生两种假设:假设
后溶液无明显现象。由此可以产生两种假设:假设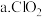 与
与 不反应。假设
不反应。假设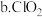 与
与 反应。
反应。
①你认为哪种假设正确,阐述原因:_______ 。
②请设计实验证明你的假设(仅用离子方程式表示):_______ 。
 是极易溶于水的气体,实验室制备及性质探究装置如图所示。回答下列问题:
是极易溶于水的气体,实验室制备及性质探究装置如图所示。回答下列问题:
(1)装置B用于制备
 ,同时还生成一种酸式盐,该反应的化学方程式为
,同时还生成一种酸式盐,该反应的化学方程式为(2)C装置的导管靠近而不接触液面,其目的是
(3)若将C装置中的溶液改为
 溶液,通入
溶液,通入 后溶液无明显现象。由此可以产生两种假设:假设
后溶液无明显现象。由此可以产生两种假设:假设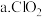 与
与 不反应。假设
不反应。假设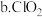 与
与 反应。
反应。①你认为哪种假设正确,阐述原因:
②请设计实验证明你的假设(仅用离子方程式表示):
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】碲(52Te)被誉为“国防与尖端技术的维生素”。工业上常用铜阳极泥(主要成分是Cu2Te、含Ag、Au等杂质)为原料提取碲并回收金属,其工艺流程如下:

已知:TeO2微溶于水,易与较浓的强酸、强碱反应。回答下列问题:
(1)已知Te为VIA族元素,TeO2被浓NaOH溶液溶解,所生成盐的化学式为____________ 。
(2)“酸浸2”时温度过高会使Te的浸出率降低,原因是________________________ 。
(3)“酸浸1”过程中,控制溶液的酸度使Cu2Te转化为TeO2,反应的化学方程式为____________ ;
“还原”过程中,发生反应的离子方程式为_____________________________ 。
(4)工业上也可用电解法从铜阳极泥中提取碲,方法是:将铜阳极泥在空气中焙烧使碲转化为TeO2,再用NaOH溶液碱浸,以石墨为电极电解所得溶液获得Te。电解过程中阴极上发生反应的电极方程式为____________________ 。在阳极区溶液中检验出有TeO42-存在,生成TeO42-的原因是_____________________ 。
(5)常温下,向l mol·L-1 Na2TeO3溶液中滴加盐酸,当溶液pH=5时,c(TeO32-):c(H2TeO3)=__________ 。(已知:H2TeO3的Ka1=1.0×10-3 Ka2=2.0×10-8)

已知:TeO2微溶于水,易与较浓的强酸、强碱反应。回答下列问题:
(1)已知Te为VIA族元素,TeO2被浓NaOH溶液溶解,所生成盐的化学式为
(2)“酸浸2”时温度过高会使Te的浸出率降低,原因是
(3)“酸浸1”过程中,控制溶液的酸度使Cu2Te转化为TeO2,反应的化学方程式为
“还原”过程中,发生反应的离子方程式为
(4)工业上也可用电解法从铜阳极泥中提取碲,方法是:将铜阳极泥在空气中焙烧使碲转化为TeO2,再用NaOH溶液碱浸,以石墨为电极电解所得溶液获得Te。电解过程中阴极上发生反应的电极方程式为
(5)常温下,向l mol·L-1 Na2TeO3溶液中滴加盐酸,当溶液pH=5时,c(TeO32-):c(H2TeO3)=
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】二氧化硫在食品加工中有着重要作用,但过量使用可能导致食品中残留量超标,会对人体健康造成不利影响。实验室可用下图装置制取并探究二氧化硫的性质。回答下列问题:

(1)①中试管内发生反应的化学方程式为_______ ,该反应中体现了浓H2SO4的酸性和_______ 性。在标准状况下生成224 mLSO2时,消耗的H2SO4的物质的量为_______ mol。
(2)实验过程中铜丝可以上下抽动,其作用为_______ 。
(3)②中试管内的溴水褪色,SO2表现出_______ 性,③中试管内的石蕊溶液出现的实验现象为_______ 。
(4)浸有NaOH溶液的棉团的作用为_______ 。

(1)①中试管内发生反应的化学方程式为
(2)实验过程中铜丝可以上下抽动,其作用为
(3)②中试管内的溴水褪色,SO2表现出
(4)浸有NaOH溶液的棉团的作用为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某同学设计了如图装置用于制取SO2,并验证SO2的部分性质,回答下列问题:
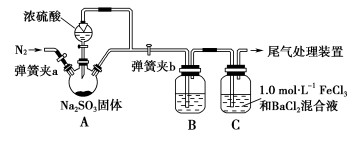
(1)装置A中用于添加浓硫酸的仪器名称为_______ 。
(2)某同学为了检验装置中A、B两部分的气密性,进行的操作是关闭弹簧夹a、打开弹簧夹b,用酒精灯在三口烧瓶下微热,观察到B中长导管口有明显气泡现象,他判断气密性良好。你认为是否合理_______ (填“合理”或“不合理”)。
(3)实验前要在装置中鼓入N2,目的是_______ 。
(4)为了验证SO2是酸性氧化物,B中可选用的试剂是_______(填字母)。
(5)装置C中可观察到白色沉淀现象,由此可验证SO2具有_______ 性,相关反应的总的离子方程式为_______ 。

(1)装置A中用于添加浓硫酸的仪器名称为
(2)某同学为了检验装置中A、B两部分的气密性,进行的操作是关闭弹簧夹a、打开弹簧夹b,用酒精灯在三口烧瓶下微热,观察到B中长导管口有明显气泡现象,他判断气密性良好。你认为是否合理
(3)实验前要在装置中鼓入N2,目的是
(4)为了验证SO2是酸性氧化物,B中可选用的试剂是_______(填字母)。
| A.无色酚酞溶液 | B.蓝色石蕊试剂 |
| C.红色品红溶液 | D.KI淀粉混合溶液 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】氯化亚铜(CuCl)可用作催化剂、杀菌剂和脱色剂,实验室制备CuCl实验步骤如下:


回答下列问题:
(1)步骤I中,配制0.50 mol/LCuCl2溶液时,不需要使用下列仪器中的___________ (填仪器名称)。
(2)步骤Ⅱ中,充分反应后铜元素转化为无色的[CuCl2]-,其发生可逆反应的离子方程式为___________ 。在加Cu粉前,通常加一定量的NaCl固体,其目的是___________ 。
(3)在进行制备[CuCl2]- 的实验时,为保持安全的实验环境,可以采取的措施是___________ 。
(4)步骤Ⅲ中,用无水乙醇洗涤沉淀的原因是___________ 。
(5)取2.500 g CuCl产品于锥形瓶中,加入稍过量的FeCl3溶液充分反应,再加50 mL水,以邻菲罗啉作指示剂,用1.000 mol/L Ce(SO4)2标准溶液滴定Fe2+,分析样品中CuCl的含量。
已知:滴定原理: Ce4+ +Fe2+ =Ce3++Fe3+; 邻菲罗啉可分别与Fe3+、Fe2+形成浅蓝色和红色的络离子。
①“再加50mL水”的目的是___________ 。
②滴定终点的现象是___________ 。
③若消耗Ce(SO4)2标准溶液的体积为24.00 mL,该样品中CuCl的质量分数是___________ 。


回答下列问题:
(1)步骤I中,配制0.50 mol/LCuCl2溶液时,不需要使用下列仪器中的

(2)步骤Ⅱ中,充分反应后铜元素转化为无色的[CuCl2]-,其发生可逆反应的离子方程式为
(3)在进行制备[CuCl2]- 的实验时,为保持安全的实验环境,可以采取的措施是
(4)步骤Ⅲ中,用无水乙醇洗涤沉淀的原因是
(5)取2.500 g CuCl产品于锥形瓶中,加入稍过量的FeCl3溶液充分反应,再加50 mL水,以邻菲罗啉作指示剂,用1.000 mol/L Ce(SO4)2标准溶液滴定Fe2+,分析样品中CuCl的含量。
已知:滴定原理: Ce4+ +Fe2+ =Ce3++Fe3+; 邻菲罗啉可分别与Fe3+、Fe2+形成浅蓝色和红色的络离子。
①“再加50mL水”的目的是
②滴定终点的现象是
③若消耗Ce(SO4)2标准溶液的体积为24.00 mL,该样品中CuCl的质量分数是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】我国化工专家侯德榜,改进氨碱法设计了“联合制碱法”,为世界制碱工业作出了突出贡献。生产流程如图 1:
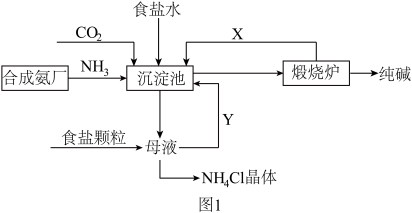
(1)完成有关反应的化学方程式
①沉淀池:_______
②煅烧炉_______
(2)联合制碱法的优点表述中,错误的是_______。
某实验小组,利用下列装置图 2 模拟“联合制碱法”的第一步反应。

(3)上述装置中接口连接顺序为_______。
(4)D 中应选用的液体为_______ 。
(5)为测定产品纯碱的成分和含量,做如下实验。假设产品纯碱中只含 NaCl、NaHCO3杂质:
i.检验产品纯碱中是否含有 NaCl,可取少量试样溶于水后,再滴加_______ 试剂,确定沉淀已经完全的操作是:_______ 。
ii.滴定法测定纯碱产品中 NaHCO3含量的方法是:准确称取纯碱样品 W g,放入锥形瓶中加蒸馏水溶解,加 1~2 滴酚酞指示剂,用 c mol∙L−1的 HCl 溶液滴定至溶液由红色变为无色(指示 +H+→
+H+→ 反应的终点),所用HCl溶液体积为 V1mL,再加1~2滴甲基橙指示剂,继续用 HCl 溶液滴定至溶液由黄色变为橙色,所用 HCl 溶液总体积为V2mL。则纯碱样品中NaHCO3质量分数为
反应的终点),所用HCl溶液体积为 V1mL,再加1~2滴甲基橙指示剂,继续用 HCl 溶液滴定至溶液由黄色变为橙色,所用 HCl 溶液总体积为V2mL。则纯碱样品中NaHCO3质量分数为_______ 。(用含 V1,V2,c,W 的代数式表示)

(1)完成有关反应的化学方程式
①沉淀池:
②煅烧炉
(2)联合制碱法的优点表述中,错误的是_______。
| A.生产原料为:食盐、NH3、CO2 | B.副产物氯化铵可做氮肥 |
| C.生产过程中可循环利用的物质只有 CO2 | D.原料利用率高 |
某实验小组,利用下列装置图 2 模拟“联合制碱法”的第一步反应。

(3)上述装置中接口连接顺序为_______。
| A.a 接 c;b 接 f、e 接 d | B.a 接d;b 接 f、e 接 c |
| C.b 接 d;a 接 e、f 接 c | D.b 接 c;a 接 f、e 接d |
(5)为测定产品纯碱的成分和含量,做如下实验。假设产品纯碱中只含 NaCl、NaHCO3杂质:
i.检验产品纯碱中是否含有 NaCl,可取少量试样溶于水后,再滴加
ii.滴定法测定纯碱产品中 NaHCO3含量的方法是:准确称取纯碱样品 W g,放入锥形瓶中加蒸馏水溶解,加 1~2 滴酚酞指示剂,用 c mol∙L−1的 HCl 溶液滴定至溶液由红色变为无色(指示
 +H+→
+H+→ 反应的终点),所用HCl溶液体积为 V1mL,再加1~2滴甲基橙指示剂,继续用 HCl 溶液滴定至溶液由黄色变为橙色,所用 HCl 溶液总体积为V2mL。则纯碱样品中NaHCO3质量分数为
反应的终点),所用HCl溶液体积为 V1mL,再加1~2滴甲基橙指示剂,继续用 HCl 溶液滴定至溶液由黄色变为橙色,所用 HCl 溶液总体积为V2mL。则纯碱样品中NaHCO3质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】现有含NaCl、Na2CO3·10H2O和NaHCO3的混合物,某同学设计如图所示的实验装置,通过测量反应产生的CO2和H2O的质量,来确定该混合物中各组分的质量分数。
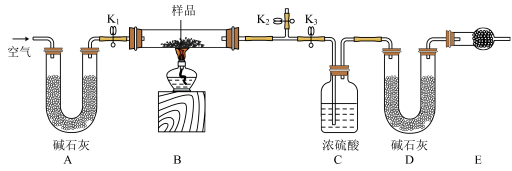
(1)实验步骤:
①按图(夹持仪器未画出)组装好实验装置后,首先进行的操作是___________ 。
②称取样品,并将其放入硬质玻璃管中;称量装浓硫酸的洗气瓶C的质量和装碱石灰的U形管D的质量。
③打开活塞K1、K2,关闭K3,缓缓鼓入空气数分钟,其目的是___________ 。
④关闭活塞K1、K2,打开K3,点燃酒精灯加热至不再产生气体。装置B中NaHCO3发生反应的化学方程式为___________ 。
⑤打开活塞K1,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C和U形管D的质量。
(2)关于该实验方案,请回答下列问题。
①若加热反应后不鼓入空气,对测定结果的影响是___________ 。
②E处干燥管中盛放的药品是___________ ,其作用是___________ ,如果实验中没有该装置,则会导致测得的NaHCO3的质量___________ (填“偏大”“偏小”或“无影响”)。

(1)实验步骤:
①按图(夹持仪器未画出)组装好实验装置后,首先进行的操作是
②称取样品,并将其放入硬质玻璃管中;称量装浓硫酸的洗气瓶C的质量和装碱石灰的U形管D的质量。
③打开活塞K1、K2,关闭K3,缓缓鼓入空气数分钟,其目的是
④关闭活塞K1、K2,打开K3,点燃酒精灯加热至不再产生气体。装置B中NaHCO3发生反应的化学方程式为
⑤打开活塞K1,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C和U形管D的质量。
(2)关于该实验方案,请回答下列问题。
①若加热反应后不鼓入空气,对测定结果的影响是
②E处干燥管中盛放的药品是
您最近一年使用:0次



