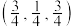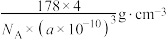氧、硫、铁可形成多种用途广泛的物质。 具有较强的氧化性。亚硫酰氯
具有较强的氧化性。亚硫酰氯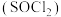 遇水发生水解反应生成
遇水发生水解反应生成 与
与 。
。 可用作锂离子电池的电极材料,电池工作时有
可用作锂离子电池的电极材料,电池工作时有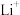 嵌入其中生成
嵌入其中生成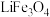 。
。 可用于生产
可用于生产 ,其一种晶胞结构如图1所示。工业上可电解
,其一种晶胞结构如图1所示。工业上可电解 与
与 混合溶液制备过二硫酸铵
混合溶液制备过二硫酸铵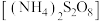 ,其结构如图2所示。酸与碱反应时放热,中和热为
,其结构如图2所示。酸与碱反应时放热,中和热为 。
。

对下列物质性质的解释不合理 的是
 具有较强的氧化性。亚硫酰氯
具有较强的氧化性。亚硫酰氯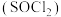 遇水发生水解反应生成
遇水发生水解反应生成 与
与 。
。 可用作锂离子电池的电极材料,电池工作时有
可用作锂离子电池的电极材料,电池工作时有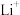 嵌入其中生成
嵌入其中生成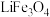 。
。 可用于生产
可用于生产 ,其一种晶胞结构如图1所示。工业上可电解
,其一种晶胞结构如图1所示。工业上可电解 与
与 混合溶液制备过二硫酸铵
混合溶液制备过二硫酸铵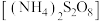 ,其结构如图2所示。酸与碱反应时放热,中和热为
,其结构如图2所示。酸与碱反应时放热,中和热为 。
。
对下列物质性质的解释
A. 的热稳定性强于 的热稳定性强于 , , 分子间存在氢键 分子间存在氢键 |
B. 易液化, 易液化, 是极性分子,分子间作用力较大 是极性分子,分子间作用力较大 |
C.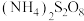 具有较强的氧化性, 具有较强的氧化性,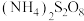 中含过氧键( 中含过氧键( ) ) |
D. 晶体中可嵌入 晶体中可嵌入 形成 形成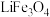 , , 可转化为 可转化为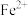 |
更新时间:2023-07-17 22:49:26
|
相似题推荐
【推荐1】 为原子序数依次增大的短周期主族元素,W与Z可形成两种常温下呈液态的化合物。Q的基态原子核外电子有29种运动状态,由
为原子序数依次增大的短周期主族元素,W与Z可形成两种常温下呈液态的化合物。Q的基态原子核外电子有29种运动状态,由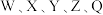 形成的一种化合物结构如图所示。
形成的一种化合物结构如图所示。 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为原子序数依次增大的短周期主族元素,W与Z可形成两种常温下呈液态的化合物。Q的基态原子核外电子有29种运动状态,由
为原子序数依次增大的短周期主族元素,W与Z可形成两种常温下呈液态的化合物。Q的基态原子核外电子有29种运动状态,由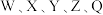 形成的一种化合物结构如图所示。
形成的一种化合物结构如图所示。 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是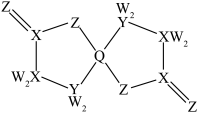
A.第一电离能: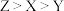 | B.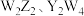 均为非极性分子 均为非极性分子 |
C. 该化合物中含 该化合物中含 键的数目为 键的数目为 | D.Q的基态原子价层电子排布式为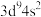 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】通常状况下,NCl3是一种油状液体,其分子的空间构型与氨分子的相似,下列有关NCl3的叙述正确的是
| A.NCl3分子是非极性分子 |
| B.NCl3分子中的所有原子均达到8电子稳定结构 |
| C.NBr3比NCl3易挥发 |
| D.NCl3分子中N-Cl键的键长比CCl4分子中C-Cl键的键长长 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】“类推”是一种重要的学习方法,但有时会产生错误的结论,下列类推结论中正确的
| A.第二周期元素氢化物的稳定性顺序是:HF>H2O>NH3;则第三周期元素氢化物的稳定性顺序也是:HCl>H2S>PH3 |
| B.IVA族元素氢化物沸点顺序是:GeH4>SiH4>CH4;则VA族元素氢化物沸点顺序也是:AsH3>PH3>NH3 |
| C.二甲苯的沸点顺序是:邻二甲苯>间二甲苯 >对二甲苯;则羟基苯甲醛的沸点顺序也是:邻羟基苯甲醛 >对羟基苯甲醛 |
| D.根据“相似相溶”,乙醇能与水以任意比互溶,则戊醇也能与水以任意比互溶 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
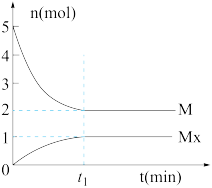
【推荐2】E是非金属性最强的元素,M是E的气态氢化物,在固定体积的密闭容器中,气体M存在如下关系:xM(g) Mx(g),反应物和生成物的物质的量随时间的变化关系如图。下列说法正确的是
Mx(g),反应物和生成物的物质的量随时间的变化关系如图。下列说法正确的是
 Mx(g),反应物和生成物的物质的量随时间的变化关系如图。下列说法正确的是
Mx(g),反应物和生成物的物质的量随时间的变化关系如图。下列说法正确的是
| A.M的沸点比同主族下一周期元素的气态氢化物沸点低 |
B.该反应的化学方程式是2HF (HF)2 (HF)2 |
C.t1时刻,保持温度不变,再充入1 mol M,重新达到平衡时,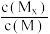 将增大 将增大 |
| D.平衡时混合气体的平均摩尔质量是33 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】“类推”是一种重要的学习方法,但有时会产生错误,下列“类推”得到的结论正确的是
| A.第二周期元素氢化物的稳定性顺序是:HF>H2O>NH3;则第三周期元素氢化物的稳定性顺序也是:HCl>H2S>PH3 |
| B.氢化物沸点顺序是:GeH4>SH4>CH4;则VA族元素氢化物沸点顺序也是:AsH3>PH3>NH3 |
| C.C=C的键能小于两倍的C-C,则N=N的键能小于两倍的N-N |
D.SO 和P4都为正四面体形,SO 和P4都为正四面体形,SO 中键角为109°28′,P4中键角也为109°28′ 中键角为109°28′,P4中键角也为109°28′ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】有关晶体的结构如图所示,下列说法中不正确的是


| A.在NaCl晶体中,距Cl-最近的Na+有6个,距Na+最近且相等的Na+共12个 |
| B.在CaF2晶体中,每个晶胞平均占有4个Ca2+,Ca2+的配位数是8 |
| C.在金刚石晶体中,每个碳原子被12个六元环共同占有,每个六元环最多有4个碳原子共面 |
| D.该气态团簇分子的分子式为EF或FE,其晶体不导电 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列有关说法正确的是
A.水合铜离子的模型如图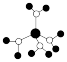 ,水合铜离子中存在极性共价键、配位键、离子键 ,水合铜离子中存在极性共价键、配位键、离子键 |
B. 晶体的晶胞如图 晶体的晶胞如图 ,距离 ,距离 最近的 最近的 组成正四面体 组成正四面体 |
C.H原子的电子云如图 ,H原子核外大多数电子在原子核附近运动 ,H原子核外大多数电子在原子核附近运动 |
D. K与氧形成的某化合物晶胞,其中黑球为 K与氧形成的某化合物晶胞,其中黑球为 ,由图可知该晶体化学式为 ,由图可知该晶体化学式为 |
您最近一年使用:0次

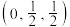 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。下列说法正确的是
。下列说法正确的是
 周围距离最近且相等的
周围距离最近且相等的 个数是6
个数是6