某兴趣小组同学为了克服传统铝热反应纸漏斗易燃烧、火星四射等缺点,将实验改成以下装置,取磁性氧化铁在图A装置中进行铝热反应,冷却后得到“铁块”混合物。
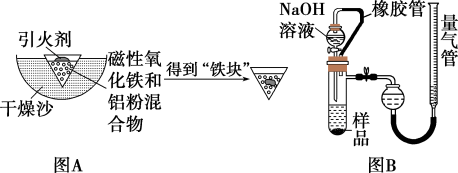
(1)实验中可以用蔗糖和浓硫酸代替镁条作引火剂,其原因是___________ 。
(2)该铝热反应的化学方程式为___________ 。
(3)取反应后的“铁块”研碎取样称量,加入图B装置中,滴入足量NaOH溶液充分反应,测量生成气体体积以计算样品中残留铝的百分含量。
①量气管在读数时必须进行的步骤是___________ 。
②取1g样品进行上述实验,共收集到44.8mL(换算成标准状况下)气体,则铝的百分含量为_______ 。
③装置中分液漏斗上端和试管用橡胶管连通,除了可以平衡压强让液体顺利滴入试管之外,还可以起到降低实验误差的作用。如果装置没有橡胶管,测出铝的百分含量将会________ (填“偏大”或“偏小”)。

(1)实验中可以用蔗糖和浓硫酸代替镁条作引火剂,其原因是
(2)该铝热反应的化学方程式为
(3)取反应后的“铁块”研碎取样称量,加入图B装置中,滴入足量NaOH溶液充分反应,测量生成气体体积以计算样品中残留铝的百分含量。
①量气管在读数时必须进行的步骤是
②取1g样品进行上述实验,共收集到44.8mL(换算成标准状况下)气体,则铝的百分含量为
③装置中分液漏斗上端和试管用橡胶管连通,除了可以平衡压强让液体顺利滴入试管之外,还可以起到降低实验误差的作用。如果装置没有橡胶管,测出铝的百分含量将会
22-23高一下·河南漯河·阶段练习 查看更多[2]
更新时间:2023-06-14 17:38:48
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】为了探究Cl2、SO2同时通入H2O中发生的反应,某校化学兴趣小组同学设计了如图所示的实验装置。
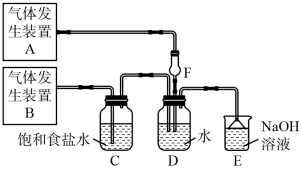
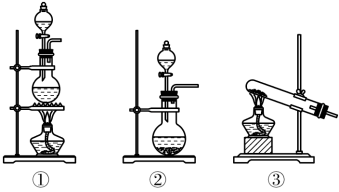
(1)该化学兴趣小组的同学为制取Cl2、SO2气体,现采用Na2SO3与70%的硫酸为原料制取SO2,采用MnO2和浓盐酸(12mol·L-1)为原料制取Cl2。在此实验中,发生装置A应选择图中三种装置中的_______ ,发生装置B应选择三种装置中的_______ (填序号),实验室制备该气体的化学方程式:_______
(2)D装置中主要反应的离子方程式为_______ 。
(3)E的作用是_______ ,F的作用_______
(4)将适量的蔗糖放入烧杯中,加少量水拌匀,再加适量浓硫酸,迅速搅拌,放出大量的热,同时观察到蔗糖逐渐变黑,体积膨胀,并放出有刺激性气味的气体。“体积膨胀,并放出有刺激性气味的气体(SO2)”。写出产生刺激性气味气体的化学方程式:_______ ;上述现象体现了浓硫酸的_______ (填序号)
①酸性 ②吸水性 ③脱水性 ④强氧化性

(1)该化学兴趣小组的同学为制取Cl2、SO2气体,现采用Na2SO3与70%的硫酸为原料制取SO2,采用MnO2和浓盐酸(12mol·L-1)为原料制取Cl2。在此实验中,发生装置A应选择图中三种装置中的

(2)D装置中主要反应的离子方程式为
(3)E的作用是
(4)将适量的蔗糖放入烧杯中,加少量水拌匀,再加适量浓硫酸,迅速搅拌,放出大量的热,同时观察到蔗糖逐渐变黑,体积膨胀,并放出有刺激性气味的气体。“体积膨胀,并放出有刺激性气味的气体(SO2)”。写出产生刺激性气味气体的化学方程式:
①酸性 ②吸水性 ③脱水性 ④强氧化性
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】家用甜味剂白糖和红糖的主要成分是蔗糖,某化学兴趣小组设计了如下装置探究浓硫酸和蔗糖反应的产物。
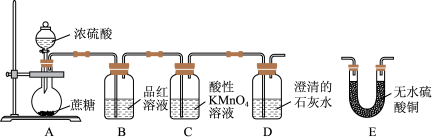
回答下列问题:
(1)A装置中可以观察到的实验现象为___________ 。写出生成气体的反应的化学方程式:___________ 。
(2)B装置中品红溶液褪色,证明A中反应有___________ 生成。A中的实验现象体现了浓硫酸的哪些性质:___________ 。
(3)C装置中发生反应的离子方程式为___________ 。
(4)D装置中澄清石灰水变浑浊,说明A中反应产生了___________ ,若要证明该实验中产生了水蒸气,应将装置E接在___________ 之间(选填“A、B”或“B、C”或“C、D”)。

回答下列问题:
(1)A装置中可以观察到的实验现象为
(2)B装置中品红溶液褪色,证明A中反应有
(3)C装置中发生反应的离子方程式为
(4)D装置中澄清石灰水变浑浊,说明A中反应产生了
您最近一年使用:0次
【推荐3】将适量的蔗糖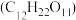 放入烧杯,滴入几滴水,搅拌均匀,然后加入适量的浓硫酸.可观察到固体变黑,片刻后,黑色物质急剧膨胀,同时产生大量刺激性气味的气体,放出大量的热.(如图所示)
放入烧杯,滴入几滴水,搅拌均匀,然后加入适量的浓硫酸.可观察到固体变黑,片刻后,黑色物质急剧膨胀,同时产生大量刺激性气味的气体,放出大量的热.(如图所示)

(1)固体变黑体现了浓硫酸的_______ 性(填“吸水”、“脱水”或“强氧化”)。
(2)确定刺激性气味气体的成分。
①将气体通入品红溶液后,溶液褪色,加热,颜色恢复.说明该气体中一定含有_______ 。
②将气体通入澄清石灰水,溶液变浑浊,_______ (填“能”或“不能”)证明气体中含有二氧化碳,其理由是_______ 。
③刺激性气味气体产生的原因可用如下化学方程式表示,完成化学方程式: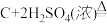
_______ 。
(3)为了检验盐中是否含有 ,正确的方法是
,正确的方法是_______ 。
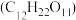 放入烧杯,滴入几滴水,搅拌均匀,然后加入适量的浓硫酸.可观察到固体变黑,片刻后,黑色物质急剧膨胀,同时产生大量刺激性气味的气体,放出大量的热.(如图所示)
放入烧杯,滴入几滴水,搅拌均匀,然后加入适量的浓硫酸.可观察到固体变黑,片刻后,黑色物质急剧膨胀,同时产生大量刺激性气味的气体,放出大量的热.(如图所示)
(1)固体变黑体现了浓硫酸的
(2)确定刺激性气味气体的成分。
①将气体通入品红溶液后,溶液褪色,加热,颜色恢复.说明该气体中一定含有
②将气体通入澄清石灰水,溶液变浑浊,
③刺激性气味气体产生的原因可用如下化学方程式表示,完成化学方程式:
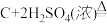
(3)为了检验盐中是否含有
 ,正确的方法是
,正确的方法是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如图所示(图中有些反应的生成物和反应的条件没有标出)。提示:黄绿色气体乙是氯气,金属Al可以与NaOH溶液反应生成H2,方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑。
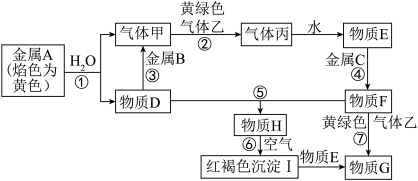
请回答下列问题:
(1)写出下列物质的化学式:B_______ ,丙_______ ,H_______ 。
(2)根据要求回答:
①D溶液和F溶液在空气中混合的现象:_______ ;
②反应③的离子方程式:_______ ;
③反应⑦的离子方程式:_______ ;
④反应⑥的化学方程式:_______ 。

请回答下列问题:
(1)写出下列物质的化学式:B
(2)根据要求回答:
①D溶液和F溶液在空气中混合的现象:
②反应③的离子方程式:
③反应⑦的离子方程式:
④反应⑥的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐2】工业上用铝土矿(主要成分为Al2O3,还有少量的Fe2O3 等杂质)提取氧化铝作冶炼铝的原料,提取的操作过程如下:
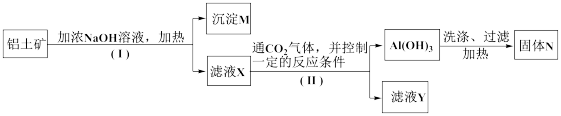
(1)I和II步骤中分离溶液和沉淀的操作,所用到的玻璃仪器 是:_________ ;
(2)沉淀M中除含有泥沙外,一定还含有_______ ,固体N是________ ;
(3)滤液X中,含铝元素的溶质的化学式为_______ ,它属于_____ (填“酸”、“碱”或“盐”)类物质;
(4)实验室里常往AlCl3溶液中加入___________ (填“氨水”或“NaOH溶液”)来制取Al(OH)3;
(5)将铝粉和氧化铁 的混合物点燃,反应放出大量的热量,生成的液态的铁用来焊接铁轨。
请写出反应的化学方程式:______________________ 。

(1)I和II步骤中分离溶液和沉淀的操作,所用到的
(2)沉淀M中除含有泥沙外,一定还含有
(3)滤液X中,含铝元素的溶质的化学式为
(4)实验室里常往AlCl3溶液中加入
(5)将铝粉和
请写出反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】某实验小组对中学课本中可生成氢气的反应进行了研究,总结出三个可以生成H2的反应:①Zn+盐酸;②Na+水;③Al+NaOH溶液。为点燃上述三个反应生成的H2,他们设计了如右图所示的装置图:请回答下列问题:

(1)写出Al和NaOH溶液反应的离子方程式_______________________________ 。
(2)在点燃H2之前必须先进行____________________________________________ 。
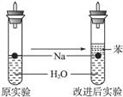
(3)实验小组在点燃用上述装置制得的H2时,①③实验获得成功,②却失败了。他们分析认为失败的原因是Na与H2O的反应速率太快,Na的用量又太少。于是他们准备增加钠的用量,可教师说太危险,你认为产生危险的原因是___________________________ 。
(4)实验小组查阅钠、苯(一种不溶于水的液态有机物)、水的密度分别为0.97 g·mL-1、0.88 g·mL-1、1.00 g·mL-1,并据此对实验进行了改进。在改进后的实验中H2的生成速率____________ 。(填“减慢”或“加快”)
(5)将4.6gNa和8.1gAl投入到足量的水中,所得溶液的体积为200mL,则生成标准状况下的H2的体积是___________ ?该溶液中溶质的物质的量浓度是__________________ ?

(1)写出Al和NaOH溶液反应的离子方程式
(2)在点燃H2之前必须先进行

(3)实验小组在点燃用上述装置制得的H2时,①③实验获得成功,②却失败了。他们分析认为失败的原因是Na与H2O的反应速率太快,Na的用量又太少。于是他们准备增加钠的用量,可教师说太危险,你认为产生危险的原因是
(4)实验小组查阅钠、苯(一种不溶于水的液态有机物)、水的密度分别为0.97 g·mL-1、0.88 g·mL-1、1.00 g·mL-1,并据此对实验进行了改进。在改进后的实验中H2的生成速率
(5)将4.6gNa和8.1gAl投入到足量的水中,所得溶液的体积为200mL,则生成标准状况下的H2的体积是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】已知A、C均为银白色金属单质,B为黑色磁性金属氧化物,它们之间的转化关系如下图(部分反应物和生成物省略),请回答下列问题:

(1)写出B的化学式__________________ 、H的化学式______________
(2)写出A与B反应的化学方程式_____________________
写出D+NaOH→H的化学方程式_____________________
写出G+C→E的离子方程式______________________

(1)写出B的化学式
(2)写出A与B反应的化学方程式
写出D+NaOH→H的化学方程式
写出G+C→E的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】利用金属活动性的不同,可以采取不同的方法冶炼金属,其中上述过程中的②就可以用铝热法炼铁,下图中所示装置为铝热反应的实验装置,请回答下列问题:
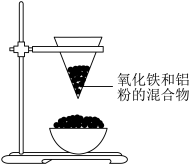
(1)该实验中还缺____ ;所缺实验用品的作用是____ ;引发铝热反应的操作为_____ 。
(2)Al、Al2O3、 Fe、 Fe2O3熔点、沸点数据如下:
①该同学推测,铝热反应所得到的熔融物应是铁铝合金。这种推测有一定的道理,理由是________ 。
②设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝。该实验所用试剂是_____ , 当观察到_______ 时,说明熔融物中含有金属铝。
③实验室欲完全溶解该熔融物,常选用稀硫酸,而不用稀硝酸,其理由是_____ 。

(1)该实验中还缺
(2)Al、Al2O3、 Fe、 Fe2O3熔点、沸点数据如下:
| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1462 |
| 沸点/℃ | 2467 | 2980 | 2750 | ____ |
②设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝。该实验所用试剂是
③实验室欲完全溶解该熔融物,常选用稀硫酸,而不用稀硝酸,其理由是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐3】铝土矿(主要成分为Al2O3,还有少量杂质)是提取氧化铝的原料。提取氧化铝的工艺流程如下: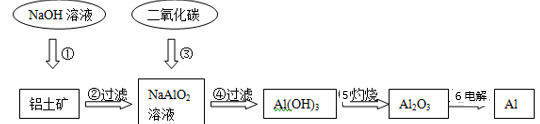
(1)请用离子方程式表示以上工艺流程中第①步反应:_______ 。
(2)写出以上工艺流程中第③步反应的化学方程式:_____ 。
(3)金属铝与氧化铁混合在高温下,会发生剧烈的反应。该反应的化学方程式_____________ 。请举一例该反应的用途_____________ 。
(4)电解熔融氧化铝制取金属铝,若有0.9mol电子发生转移.理论上能得到金属铝的质量是___________ 。

(1)请用离子方程式表示以上工艺流程中第①步反应:
(2)写出以上工艺流程中第③步反应的化学方程式:
(3)金属铝与氧化铁混合在高温下,会发生剧烈的反应。该反应的化学方程式
(4)电解熔融氧化铝制取金属铝,若有0.9mol电子发生转移.理论上能得到金属铝的质量是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】劳动实践课上同学们用草木灰给农作物施肥。课后同学查阅资料,得知草木灰是一种重要的农家肥,碳酸钾含量高。
【提出问题】
如何测定草木灰中碳酸钾的含量?
【查阅资料】
1.常见草木灰钾含量(以碳酸钾表示)如下表:
2.提取碳酸钾主要过程是:秸秆→草木灰→滤液→固体
(1)表格中钾含量最高的草木灰是_______ ,同学们选用这种秸秆灰提取碳酸钾。
【设计与实验】
实验一:提取碳酸钾
第一步:燃烧秸秆,收集草木灰,称取20.00g。
第二步:用60℃水浸洗草木灰(如图1)并过滤,浸洗滤渣2次,合并滤液。
第三步:蒸发滤液,烘干得到9.90g固体。
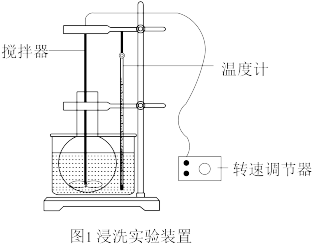
(2)图1实验中,用60℃的温水而不用冷水浸洗的原因是_______ 。
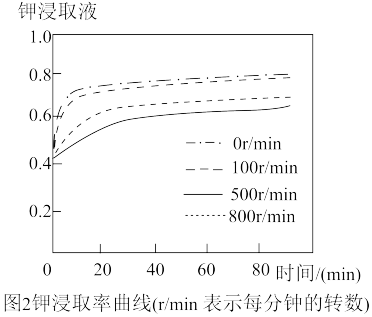
(3)根据图2,搅拌器转速控制在每分钟_______ 转,浸取时间为_______ 分钟,比较适宜。
实验二:测定碳酸钾含量
取实验一中所得固体3.30g进行图3实验。
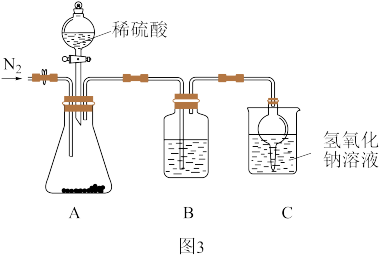
(4)实验中需缓慢滴入稀硫酸,原因是_______ 。
(5)装置B的作用是_______ 。
【数据与解释】
(6)称量图3中反应前后烧杯和其中溶液的总质量,增重0.92g。计算草木灰中碳酸钾的质量分数为_______ %,与表格中数据相比明显偏低,原因可能是_______ (填序号)。
a.烧杯中溶液与空气接触 b.固体含有其它钾盐 c.固体含有氯化钠
【反思与评价】
(7)我国秸秆产量巨大,可作为生物质发电的原料,还可利用其燃烧发电产生的草木灰提取碳酸钾,其优点有_______ (写一条)。
【提出问题】
如何测定草木灰中碳酸钾的含量?
【查阅资料】
1.常见草木灰钾含量(以碳酸钾表示)如下表:
| 草木灰种类 | 小灌木灰 | 稻草灰 | 小麦秆灰 | 棉壳灰 | 棉秆灰 | 向日葵杆灰 |
 (%) (%) | 8.66 | 2.63 | 20.26 | 32.28 | 16.44 | 51.97 |
(1)表格中钾含量最高的草木灰是
【设计与实验】
实验一:提取碳酸钾
第一步:燃烧秸秆,收集草木灰,称取20.00g。
第二步:用60℃水浸洗草木灰(如图1)并过滤,浸洗滤渣2次,合并滤液。
第三步:蒸发滤液,烘干得到9.90g固体。

(2)图1实验中,用60℃的温水而不用冷水浸洗的原因是
(3)根据图2,搅拌器转速控制在每分钟

实验二:测定碳酸钾含量
取实验一中所得固体3.30g进行图3实验。

(4)实验中需缓慢滴入稀硫酸,原因是
(5)装置B的作用是
【数据与解释】
(6)称量图3中反应前后烧杯和其中溶液的总质量,增重0.92g。计算草木灰中碳酸钾的质量分数为
a.烧杯中溶液与空气接触 b.固体含有其它钾盐 c.固体含有氯化钠
【反思与评价】
(7)我国秸秆产量巨大,可作为生物质发电的原料,还可利用其燃烧发电产生的草木灰提取碳酸钾,其优点有
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】回答下列问题:
(1)已知钠与冷水剧烈反应,钠与水反应的离子化学方程式:_______ 。
(2)测定Na2O和Na的混合物中金属钠的质量分数可用下图所示的几套仪器组合:
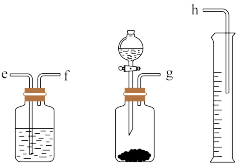
①用接口字母标出各仪器连接的顺序_______ 。
②有一块表面氧化成Na2O的金属钠,其质量为2.0g,实验后经测定共收集到0.02gH2,求样品中金属钠的质量分数是_______ 。
(3)已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下:3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O
①写出该反应的离子方程式_______ 。
②用单线桥标出该反应电子转移的方向和数目:_______ 。
③若19.2g铜与足量硝酸完全反应,则被还原的硝酸的质量为_______ g。
(1)已知钠与冷水剧烈反应,钠与水反应的离子化学方程式:
(2)测定Na2O和Na的混合物中金属钠的质量分数可用下图所示的几套仪器组合:

①用接口字母标出各仪器连接的顺序
②有一块表面氧化成Na2O的金属钠,其质量为2.0g,实验后经测定共收集到0.02gH2,求样品中金属钠的质量分数是
(3)已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下:3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O
①写出该反应的离子方程式
②用单线桥标出该反应电子转移的方向和数目:
③若19.2g铜与足量硝酸完全反应,则被还原的硝酸的质量为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】重铬酸钾( )是一种重要的化工原料,一般由铬铁矿制备。铬铁矿的主要成分为
)是一种重要的化工原料,一般由铬铁矿制备。铬铁矿的主要成分为 ,还含有
,还含有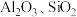 等杂质。制备流程如图所示:
等杂质。制备流程如图所示:
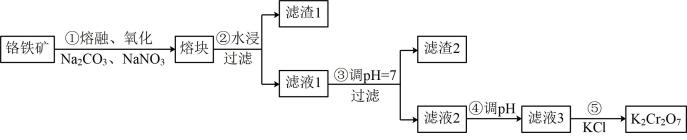
已知:Ⅰ.步骤①中仅考虑 作氧化剂、还原产物为
作氧化剂、还原产物为 ;
; (Ⅱ)氧化成
(Ⅱ)氧化成 ;反应有
;反应有 气体生成。
气体生成。
Ⅱ.碱性条件下, (Ⅵ)主要以
(Ⅵ)主要以 形式存在,加入过量酸则发生如下反应:
形式存在,加入过量酸则发生如下反应: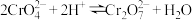 。
。
Ⅲ.有关物质的溶解度如图所示:
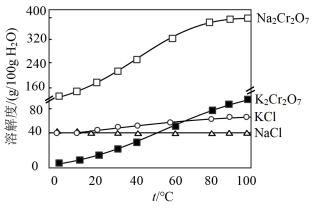
(1)请写出步骤①中 与
与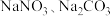 反应的化学反应方程式:
反应的化学反应方程式:_______ 。
(2)下列有关说法不正确 的是_______。
(3)向滤液3中加入适量的 固体,经过一系列操作可得到较大颗粒的
固体,经过一系列操作可得到较大颗粒的 固体。从下列选项中选择合适的操作补全步骤
固体。从下列选项中选择合适的操作补全步骤_______ 。
向滤液3中加入适量的 固体并溶解→(_______)→(_______)→(_______)→用(_______)洗涤→干燥
固体并溶解→(_______)→(_______)→(_______)→用(_______)洗涤→干燥
操作:a.蒸发浓缩至表面出现晶膜;b.蒸发结晶至大量晶体析出;c.过滤;d.趁热过滤;e.置于冰水浴中使其结晶析出;f.静置,使其缓慢结晶析出;g.用0℃冷水;h.用80℃热水;
(4)用滴定法测定产品中重铬酸钾的纯甲,滴定时的离子方程式为 。
。
步骤Ⅰ:称取重铬酸钾( ,相对分子质量为294)试样
,相对分子质量为294)试样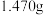 ,用
,用 容量瓶配成一定浓度的溶液。
容量瓶配成一定浓度的溶液。
步骤2:取 溶液于锥形瓶中,加入适量稀硫酸和足量
溶液于锥形瓶中,加入适量稀硫酸和足量 溶液(还原产物为
溶液(还原产物为 ),置于暗处一段时间。
),置于暗处一段时间。
步骤3:加入一定量的水,加入淀粉指示剂,用 标准溶液滴定,重复实验,平均消耗标准液
标准溶液滴定,重复实验,平均消耗标准液 。
。
①步骤3中滴定终点的现象是_______ 。
②测定产品中重铬酸钾的纯度为_______ 。
③测定的产品纯度比实际含量偏高,可能是由步骤2引起的,原因是_______ 。
 )是一种重要的化工原料,一般由铬铁矿制备。铬铁矿的主要成分为
)是一种重要的化工原料,一般由铬铁矿制备。铬铁矿的主要成分为 ,还含有
,还含有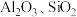 等杂质。制备流程如图所示:
等杂质。制备流程如图所示:
已知:Ⅰ.步骤①中仅考虑
 作氧化剂、还原产物为
作氧化剂、还原产物为 ;
; (Ⅱ)氧化成
(Ⅱ)氧化成 ;反应有
;反应有 气体生成。
气体生成。Ⅱ.碱性条件下,
 (Ⅵ)主要以
(Ⅵ)主要以 形式存在,加入过量酸则发生如下反应:
形式存在,加入过量酸则发生如下反应: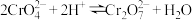 。
。Ⅲ.有关物质的溶解度如图所示:

(1)请写出步骤①中
 与
与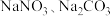 反应的化学反应方程式:
反应的化学反应方程式:(2)下列有关说法
| A.步骤①若在实验室中进行可选择陶瓷坩埚作反应容器 |
B.滤渣2的主要成分是 和含硅杂质 和含硅杂质 |
C.步骤④调 的试剂可选择浓盐酸 的试剂可选择浓盐酸 |
| D.步骤⑤的反应类型是复分解反应 |
 固体,经过一系列操作可得到较大颗粒的
固体,经过一系列操作可得到较大颗粒的 固体。从下列选项中选择合适的操作补全步骤
固体。从下列选项中选择合适的操作补全步骤向滤液3中加入适量的
 固体并溶解→(_______)→(_______)→(_______)→用(_______)洗涤→干燥
固体并溶解→(_______)→(_______)→(_______)→用(_______)洗涤→干燥操作:a.蒸发浓缩至表面出现晶膜;b.蒸发结晶至大量晶体析出;c.过滤;d.趁热过滤;e.置于冰水浴中使其结晶析出;f.静置,使其缓慢结晶析出;g.用0℃冷水;h.用80℃热水;
(4)用滴定法测定产品中重铬酸钾的纯甲,滴定时的离子方程式为
 。
。步骤Ⅰ:称取重铬酸钾(
 ,相对分子质量为294)试样
,相对分子质量为294)试样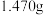 ,用
,用 容量瓶配成一定浓度的溶液。
容量瓶配成一定浓度的溶液。步骤2:取
 溶液于锥形瓶中,加入适量稀硫酸和足量
溶液于锥形瓶中,加入适量稀硫酸和足量 溶液(还原产物为
溶液(还原产物为 ),置于暗处一段时间。
),置于暗处一段时间。步骤3:加入一定量的水,加入淀粉指示剂,用
 标准溶液滴定,重复实验,平均消耗标准液
标准溶液滴定,重复实验,平均消耗标准液 。
。①步骤3中滴定终点的现象是
②测定产品中重铬酸钾的纯度为
③测定的产品纯度比实际含量偏高,可能是由步骤2引起的,原因是
您最近一年使用:0次



