现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如图所示(图中有些反应的生成物和反应的条件没有标出)。提示:黄绿色气体乙是氯气,金属Al可以与NaOH溶液反应生成H2,方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑。
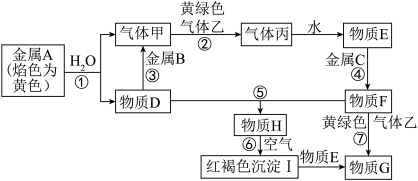
请回答下列问题:
(1)写出下列物质的化学式:B_______ ,丙_______ ,H_______ 。
(2)根据要求回答:
①D溶液和F溶液在空气中混合的现象:_______ ;
②反应③的离子方程式:_______ ;
③反应⑦的离子方程式:_______ ;
④反应⑥的化学方程式:_______ 。

请回答下列问题:
(1)写出下列物质的化学式:B
(2)根据要求回答:
①D溶液和F溶液在空气中混合的现象:
②反应③的离子方程式:
③反应⑦的离子方程式:
④反应⑥的化学方程式:
更新时间:2023-07-28 21:57:12
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】某小组想通过实验探究 Na、Mg、Al 三种金属元素性质的递变规律。
I.探究 Na、Mg、Al 分别与水反应的情况。
实验①:切一小块绿豆大小的金属 Na,用滤纸吸干其表面的煤油,将其投入盛有 100ml 水(含酚酞)的烧杯中。观察到 Na 与冷水发生剧烈反应,烧杯内溶液变红。
(1)与水反应生成氢氧化钠和氢气,写出该反应的化学方程式___________ 。
(2)上述反应中,作还原剂的是___________ 。
A.Na B.H2O C.NaOH
(3)上述反应中若有23克金属Na被充分反应,则产生气体在标况下的体积约为___________ L。
(4)溶液中,使酚酞试液变红的微粒是___________ 。
A.Na+ B.H+ C.OH-
实验②:分别取一小段镁条和铝条,放入两支试管中,向试管中各加入 2ml 水,再滴入2 滴酚酞试液,观察到试管中均无明显现象。
有同学提出实验②的设计存在问题,故对实验②作如下调整:
实验③:另取镁条和铝条,分别用砂纸打磨去除它们表面的氧化膜后,再进行以上实验 操作并加热。观察到:未加热时,反应现象均不明显;加热后镁条表面有气泡生成,溶液变红;加热后 Al 与水反应现象仍不明显。
(5)实验②的设计中未考虑到的因素是___________ 。
(6)通过上述实验,得出 Na、Mg、Al 的金属性由强到弱的顺序是___________ 。
Ⅱ.比较 NaOH、Mg(OH)2、Al(OH)3碱性的强弱。
实验④:在试管中加入2ml 0.5mol·L-1 Al2(SO4)3溶液,然后逐滴滴加 2mol·L-1 NaOH溶液至过量,边加边振荡。观察到试管中先出现白色沉淀后全部溶解。
实验⑤:在试管中加入2ml 1mol·L-1 MgSO4溶液,然后逐滴滴加2mol·L-1 NaOH 溶液至过量,边加边振荡。观察到试管中出现白色沉淀且不溶解。
(7)写出由实验④、⑤的实验现象可推导得出的结论。
(8)综上实验可知,NaOH、Mg(OH)2、Al(OH)3的碱性由强到弱的顺序是___________ 。
I.探究 Na、Mg、Al 分别与水反应的情况。
实验①:切一小块绿豆大小的金属 Na,用滤纸吸干其表面的煤油,将其投入盛有 100ml 水(含酚酞)的烧杯中。观察到 Na 与冷水发生剧烈反应,烧杯内溶液变红。
(1)与水反应生成氢氧化钠和氢气,写出该反应的化学方程式
(2)上述反应中,作还原剂的是
A.Na B.H2O C.NaOH
(3)上述反应中若有23克金属Na被充分反应,则产生气体在标况下的体积约为
(4)溶液中,使酚酞试液变红的微粒是
A.Na+ B.H+ C.OH-
实验②:分别取一小段镁条和铝条,放入两支试管中,向试管中各加入 2ml 水,再滴入2 滴酚酞试液,观察到试管中均无明显现象。
有同学提出实验②的设计存在问题,故对实验②作如下调整:
实验③:另取镁条和铝条,分别用砂纸打磨去除它们表面的氧化膜后,再进行以上实验 操作并加热。观察到:未加热时,反应现象均不明显;加热后镁条表面有气泡生成,溶液变红;加热后 Al 与水反应现象仍不明显。
(5)实验②的设计中未考虑到的因素是
(6)通过上述实验,得出 Na、Mg、Al 的金属性由强到弱的顺序是
Ⅱ.比较 NaOH、Mg(OH)2、Al(OH)3碱性的强弱。
实验④:在试管中加入2ml 0.5mol·L-1 Al2(SO4)3溶液,然后逐滴滴加 2mol·L-1 NaOH溶液至过量,边加边振荡。观察到试管中先出现白色沉淀后全部溶解。
实验⑤:在试管中加入2ml 1mol·L-1 MgSO4溶液,然后逐滴滴加2mol·L-1 NaOH 溶液至过量,边加边振荡。观察到试管中出现白色沉淀且不溶解。
(7)写出由实验④、⑤的实验现象可推导得出的结论。
| 现象 | 结论 | |
| ④ | 出现白色沉淀 | Al(OH)3的碱性比NaOH弱 |
| 沉淀全部溶解 | ||
| ⑤ | 出现白色沉淀 | |
| 沉淀不溶解 | Mg(OH)2无酸性 |
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】A、B、C、D、F五种物质的焰色反应均为黄色,A、B、C、D与盐酸反应均生成E,此外B还生成一种可燃性气体.而C、D还生成一种无色、无味气体H,该气体能使澄清石灰水变浑浊.D和A可反应生成C,F和H也可反应生成C和另一种无色、无味气体.请回答下列问题:
(1)写出下列反应的离子方程式:①D+盐酸_____________ ③D+A_______________
(2)写出F和H反应的化学方程式_______________
(1)写出下列反应的离子方程式:①D+盐酸
(2)写出F和H反应的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】某课外活动小组为了检验钠与水反应的产物,设计如图所示实验装置(夹持装置已略去)。首先在U形管内加入少量煤油和几粒钠块,再从U形管左端加入水(含有酚酞),赶出装置中空气后加热铜丝。

根据反应中观察到的现象,回答下列问题:
(1)U形管中溶液的颜色_______ ,说明有______ 生成。
(2)铜丝的变化现象:_________ ,说明有______ 生成。
(3)若ag钠与bmL水(设水的密度为1g/mL且水足量)完全反应,则该溶液中溶质的质量分数是_______ 。

根据反应中观察到的现象,回答下列问题:
(1)U形管中溶液的颜色
(2)铜丝的变化现象:
(3)若ag钠与bmL水(设水的密度为1g/mL且水足量)完全反应,则该溶液中溶质的质量分数是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】现有常见金属单质A、B、C和常见气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。

请根据以上信息回答 下列问题:
(1)写出下列物质的化学式: A____ B________ F_____ 丙______
(2)写出下列反应离子方程式:
反应③__________________________________________
反应⑤_________________________________________
反应⑥_________________________________________

请根据以上信息回答 下列问题:
(1)写出下列物质的化学式: A
(2)写出下列反应离子方程式:
反应③
反应⑤
反应⑥
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】铝和铁是生活中常见的两种金属。
(1)用铝箔包住金属钠,用针在铝箔上刺些小孔,用镊子夹住放入水中,可能发生反应的化学方程式表示为___________ 和___________ 。
(2)在高温下,Fe与水蒸气可发生反应。应用下图装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”。请回答该实验中的问题。

①写出该反应的化学方程式并用双线桥标出电子转移的方向和数目:___________ 。
②烧瓶底部放置了几片碎瓷片,碎瓷片的作用是___________ 。
③酒精灯和酒精喷灯首先点燃的是___________ 。
④现欲将5.6gFe完全溶解在稀硫酸中,加水后得200mL溶液。所得硫酸亚铁溶液的物质的量浓度是___________ ,反应中转移的电子数是___________ 。
(1)用铝箔包住金属钠,用针在铝箔上刺些小孔,用镊子夹住放入水中,可能发生反应的化学方程式表示为
(2)在高温下,Fe与水蒸气可发生反应。应用下图装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”。请回答该实验中的问题。

①写出该反应的化学方程式并用双线桥标出电子转移的方向和数目:
②烧瓶底部放置了几片碎瓷片,碎瓷片的作用是
③酒精灯和酒精喷灯首先点燃的是
④现欲将5.6gFe完全溶解在稀硫酸中,加水后得200mL溶液。所得硫酸亚铁溶液的物质的量浓度是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】含镁3%~5%的铝镁合金是轮船制造、化工生产、机械制造等行业的重要原料。现有一块质量为m g的铝镁合金,欲测定其中镁的质量分数,几位同学设计了以下不同的实验方案:
方案1:铝镁合金与足量盐酸反应,测定气体的质量为m 1g。
方案2:铝镁合金与足量氢氧化钠溶液反应,过滤、洗涤、烘干,测定剩余固体质量w1 g。
方案3:铝镁合金与过量的盐酸反应,在溶液中加入过量的氢氧化钠溶液,过滤、洗涤、灼烧,测定固体的质量w2 g。(说明:Al (OH)3 既可以与酸反应,也可以与碱反应)
(1)某化学实验小组利用如图所示的装置,按照方案1进行了实验。
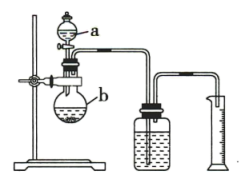
实验装置中有两处明显错误,请指出至少一种:_______ 。
(2)方案2中的化学方程式为_______ 。
(3)方案3中“过滤”操作中用到玻璃棒,玻璃棒的作用是_______ ,若按方案3进行实验,测得的镁的质量分数为_______ 。
方案1:铝镁合金与足量盐酸反应,测定气体的质量为m 1g。
方案2:铝镁合金与足量氢氧化钠溶液反应,过滤、洗涤、烘干,测定剩余固体质量w1 g。
方案3:铝镁合金与过量的盐酸反应,在溶液中加入过量的氢氧化钠溶液,过滤、洗涤、灼烧,测定固体的质量w2 g。(说明:Al (OH)3 既可以与酸反应,也可以与碱反应)
(1)某化学实验小组利用如图所示的装置,按照方案1进行了实验。

实验装置中有两处明显错误,请指出至少一种:
(2)方案2中的化学方程式为
(3)方案3中“过滤”操作中用到玻璃棒,玻璃棒的作用是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】已知A是一种常见金属,F 是一种红褐色沉淀,试根据图中转化关系,回答下列问题。
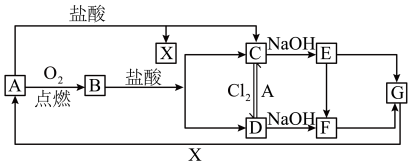
(1)写出A、C、F、G的化学式:A_________ ,C________ ,F________ ,G_________ 。
(2) 检验D中阳离子的方法为________________________
(3) 保存C溶液时要加固体A的原因__________________
(4) 写出下列转化的离子方程式或化学方程式。
①E→F 的化学反应方程式:_________________________
②C→D的离子反应方程式:_________________________

(1)写出A、C、F、G的化学式:A
(2) 检验D中阳离子的方法为
(3) 保存C溶液时要加固体A的原因
(4) 写出下列转化的离子方程式或化学方程式。
①E→F 的化学反应方程式:
②C→D的离子反应方程式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】物质A、B、C、D、E、F、G、H、I、J、K有下图转化关系,其中气体D为单质,试回答:
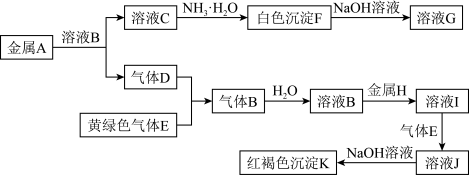
(1)写出下列物质的化学式:H是__________________ ;
(2)写出A与B溶液反应的离子方程式:__________________ ;
(3)写出反应“F→G”的化学方程式:__________________ ;
(4)如果想由溶液G再次制得白色沉淀F,可以加入____________ 试剂(填化学式);
(5)在溶液I中滴入NaOH溶液,可观察到的现象是:______________________ ;
(6)检验溶液J中的金属阳离子,可用_____________________________ 试剂(填化学式)。

(1)写出下列物质的化学式:H是
(2)写出A与B溶液反应的离子方程式:
(3)写出反应“F→G”的化学方程式:
(4)如果想由溶液G再次制得白色沉淀F,可以加入
(5)在溶液I中滴入NaOH溶液,可观察到的现象是:
(6)检验溶液J中的金属阳离子,可用
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】用不含Fe3+的FeSO4溶液与不含O2的蒸馏水配制的NaOH溶液反应制备Fe(OH)2。
(1)用硫酸亚铁晶体配制上述FeSO4溶液时,还需要加入稀硫酸和_______ ,原因是_______ ,对应的离子方程式_______ 。
(2)除去蒸馏水中溶解的O2常采用_______ 的方法。
(3)向FeSO4溶液中滴入氢氧化钠溶液后,沉淀颜色变化顺序为_______
A.红褐色、灰绿色、白色 B.白色、红褐色、黑色
C.白色、灰绿色、红褐色 D.蓝色、灰绿色、绿色
反应的化学方程式是_______ 。
(4)生成Fe(OH)2白色沉淀的操作是:用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液,这样操作的理由是_______ 。

(1)用硫酸亚铁晶体配制上述FeSO4溶液时,还需要加入稀硫酸和
(2)除去蒸馏水中溶解的O2常采用
(3)向FeSO4溶液中滴入氢氧化钠溶液后,沉淀颜色变化顺序为
A.红褐色、灰绿色、白色 B.白色、红褐色、黑色
C.白色、灰绿色、红褐色 D.蓝色、灰绿色、绿色
反应的化学方程式是
(4)生成Fe(OH)2白色沉淀的操作是:用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液,这样操作的理由是

您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】已知以下物质为铁及其化合物之间的相互转化:
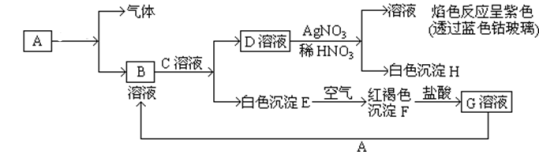
试回答:
(1)写出D的化学式___ ,H的化学式___ 。
(2)鉴别G溶液的试剂为___ 。
(3)写出由E转变成F的化学方程式___ 。

试回答:
(1)写出D的化学式
(2)鉴别G溶液的试剂为
(3)写出由E转变成F的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】现有金属单质A、B和气体甲、乙、丙以及物质C、D、E、F,它们之间能发生如下反应。(图中有些反应的产物和反应条件没有标出)请回答下列问题:
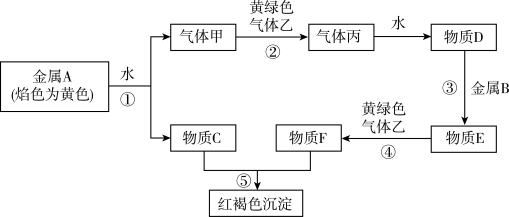
(1)A的化学式为_________ ,丙的化学式为_________ ;
(2)写出下列反应的离子方程式:
①_________ ;
③_________ ;
④_________ ;
⑤_________ 。
(3)写出C溶液与Al反应的化学方程式:_________ 。
(4)将过氧化钠投入到E溶液中,可以观察到的现象是:_________ 。

(1)A的化学式为
(2)写出下列反应的离子方程式:
①
③
④
⑤
(3)写出C溶液与Al反应的化学方程式:
(4)将过氧化钠投入到E溶液中,可以观察到的现象是:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】中学常见物质甲、乙、丙、X在定条件下有如图转化关系(部分反应物和产物已略去)。
甲 乙
乙 丙
丙
(1)若X是氧气,则甲不能是A_______ 。
A.C B.Na C.Al D.Fe
(2)若X是金属铁,甲是黄绿色气体, 则甲和丙溶液发生的离子反应为_______ 。
(3)若X为盐酸,甲、乙为含碳元素的钠盐,且丙为气体,写出乙的一种用途_______ 。
(4)若X为二氧化碳,甲、乙、丙均为含钙元素,则丙生成乙的化学方程式为_______ 。
甲
 乙
乙 丙
丙(1)若X是氧气,则甲不能是A
A.C B.Na C.Al D.Fe
(2)若X是金属铁,甲是黄绿色气体, 则甲和丙溶液发生的离子反应为
(3)若X为盐酸,甲、乙为含碳元素的钠盐,且丙为气体,写出乙的一种用途
(4)若X为二氧化碳,甲、乙、丙均为含钙元素,则丙生成乙的化学方程式为
您最近一年使用:0次



