化学反应方向的综合判据是判断反应能否白专进行的关键。由于反应的焓变、熵变随温度的变化较小,假设它们不随温度变化,根据下表数据。
(1)根据表中数据可知:反应①在______ 下(填“高温”、“低温”、“任何温度)正向能自发进行。
(2)有人提出采用适当的催化剂,用热分解法分解CO2,以减少CO2的排放,你认为是否可行?___________ (填“是”或“否”)。阐述判断的理由___________ 。
(3)利用综合判据,计算反应③能正向自发进行的温度范围___________ 。(写出过程)
| 化学反应 | AH/kJ·mol—1 | 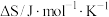 |
①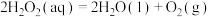 | -98 | 57.2 |
②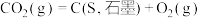 | 393.5 | -2.86 |
③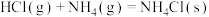 | -176 | -285 |
(2)有人提出采用适当的催化剂,用热分解法分解CO2,以减少CO2的排放,你认为是否可行?
(3)利用综合判据,计算反应③能正向自发进行的温度范围
22-23高二下·上海闵行·期末 查看更多[2]
上海市闵行中学2022-2023学年高二下学期期末(等级)考试化学试题(已下线)专题03 化学反应进行的方向和限度-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(上海专用)
更新时间:2023-06-18 13:50:13
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】反应A(g) B(g)+C(g)在容积为1.0L的密闭容器中进行,A的初始浓度为0.050mol/L。温度T1和T2下A的浓度与时间关系如图所示。回答下列问题:
B(g)+C(g)在容积为1.0L的密闭容器中进行,A的初始浓度为0.050mol/L。温度T1和T2下A的浓度与时间关系如图所示。回答下列问题:
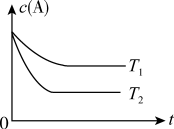
(1)上述反应的温度T1___ T2,平衡常数K(T1)____ K(T2)。(填“大于”、“小于”或“等于”)
(2)若温度T2时,5min后反应达到平衡,A的转化率为70%,则:
①平衡时体系总的物质的量为____ 。
②反应的平衡常数K=____ 。
③反应在0~5min区间的平均反应速率v(A)=____ 。
(3)物质(t-BuNO)2在正庚烷溶剂中发生如下反应:(t-BuNO)2 2(t-BuNO) ΔH=50.5kJ•mol-1。该反应的ΔS
2(t-BuNO) ΔH=50.5kJ•mol-1。该反应的ΔS____ 0(填“>”、“<”或“=”)。在____ 填(“较高”或“较低”)温度下有利于该反应自发进行。
 B(g)+C(g)在容积为1.0L的密闭容器中进行,A的初始浓度为0.050mol/L。温度T1和T2下A的浓度与时间关系如图所示。回答下列问题:
B(g)+C(g)在容积为1.0L的密闭容器中进行,A的初始浓度为0.050mol/L。温度T1和T2下A的浓度与时间关系如图所示。回答下列问题:
(1)上述反应的温度T1
(2)若温度T2时,5min后反应达到平衡,A的转化率为70%,则:
①平衡时体系总的物质的量为
②反应的平衡常数K=
③反应在0~5min区间的平均反应速率v(A)=
(3)物质(t-BuNO)2在正庚烷溶剂中发生如下反应:(t-BuNO)2
 2(t-BuNO) ΔH=50.5kJ•mol-1。该反应的ΔS
2(t-BuNO) ΔH=50.5kJ•mol-1。该反应的ΔS
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】已知2CO(g) CO2(g)+C(s),T=980K时,ΔH-TΔS=0
CO2(g)+C(s),T=980K时,ΔH-TΔS=0
(1)当体系温度低于980K时,估计ΔH-TΔS______ (填“大于”“小于”或“等于”)0,当体系温度高于980K时,估计ΔH-TΔS______ (填“大于”“小于”或“等于”)0。
(2)在冶金工业中,以C为还原剂,温度高于980K时的氧化产物是以______ 为主,温度低于980K时的氧化产物是以_____ 为主。
 CO2(g)+C(s),T=980K时,ΔH-TΔS=0
CO2(g)+C(s),T=980K时,ΔH-TΔS=0(1)当体系温度低于980K时,估计ΔH-TΔS
(2)在冶金工业中,以C为还原剂,温度高于980K时的氧化产物是以
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】一氧化碳是一种重要的化工原料。
(1)高炉炼铁中发生的反应之一是:
FeO(s)+CO(g)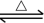 Fe(s)+CO2(g) △H=-1kJ/mol。
Fe(s)+CO2(g) △H=-1kJ/mol。
温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO的体积比将______
(填“增大”、“减小”或“不变”)。
已知1100℃时,该反应平衡常数K=0.263,现测得高炉中(CO2)=0.025mol/L,c(CO)=0.1mol/L,此时该反应_______ .
A.向正反应向向进行 B.处于平衡状态 C.向逆反应方向进行
(2)合成氨工业中需将原料气中的CO变成CO2除去。在密闭密器中将CO和H2O混合加热到800℃,达到下列平衡:
CO(g)+H2O(g)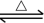 CO2(g)+H2(g) K=1.0
CO2(g)+H2(g) K=1.0
若平衡时n(H2O)/n(CO)=1,则CO转化为CO2的转化率为_______ 。
(3)用CO和H2经如下两步反应制得甲酸甲醛:
CO+2H2→CH3OH
CO+CH3OH→HCOOCH3
已知反应①中CO的转化率为80%,反应②中两种反应物的转化率均为85%,则2.52tCO最多可制得甲酸甲醛多少吨?(写出计算过程)。_______
(1)高炉炼铁中发生的反应之一是:
FeO(s)+CO(g)
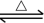 Fe(s)+CO2(g) △H=-1kJ/mol。
Fe(s)+CO2(g) △H=-1kJ/mol。温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO的体积比将
(填“增大”、“减小”或“不变”)。
已知1100℃时,该反应平衡常数K=0.263,现测得高炉中(CO2)=0.025mol/L,c(CO)=0.1mol/L,此时该反应
A.向正反应向向进行 B.处于平衡状态 C.向逆反应方向进行
(2)合成氨工业中需将原料气中的CO变成CO2除去。在密闭密器中将CO和H2O混合加热到800℃,达到下列平衡:
CO(g)+H2O(g)
 CO2(g)+H2(g) K=1.0
CO2(g)+H2(g) K=1.0若平衡时n(H2O)/n(CO)=1,则CO转化为CO2的转化率为
(3)用CO和H2经如下两步反应制得甲酸甲醛:
CO+2H2→CH3OH
CO+CH3OH→HCOOCH3
已知反应①中CO的转化率为80%,反应②中两种反应物的转化率均为85%,则2.52tCO最多可制得甲酸甲醛多少吨?(写出计算过程)。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】乙烯是世界上产量最大的化学产品之一,乙烯工业是石油化工产业的核心。
(1)甲醇制备乙烯的主要反应:
i.2CH3OH(g)=C2H4(g)+2H2O(g) ∆H1=−20.9 kJ/mol
ii.3CH3OH(g)=C3H6(g)+3H2O(g) ∆H2=−98.1 kJ/mol
iii.4CH3OH(g)=C4H8(g)+4H2O(g) ∆H3=−118.1 kJ/mol
①C3H6转化为C2H4的热化学方程式iv:2C3H6(g) =3C2H4(g) ∆H4=___________ ,该反应能自发进行的条件是___________ (填“较低”“较高”或“任意”)温度。
②恒温恒压下充入N2,反应i中C2H4的平衡产率将___________ (填“增大”、减小”或“不变”)。
(2)乙炔在Pd表面选择加氢生成乙烯的反应机理如图。其中吸附在Pd表面上的物种用*标注。

上述反应为___________ (填“放热”或“吸热”)反应,历程最小能垒(活化能)为___________ kJ/mol,该步骤的化学方程式为___________ 。
(1)甲醇制备乙烯的主要反应:
i.2CH3OH(g)=C2H4(g)+2H2O(g) ∆H1=−20.9 kJ/mol
ii.3CH3OH(g)=C3H6(g)+3H2O(g) ∆H2=−98.1 kJ/mol
iii.4CH3OH(g)=C4H8(g)+4H2O(g) ∆H3=−118.1 kJ/mol
①C3H6转化为C2H4的热化学方程式iv:2C3H6(g) =3C2H4(g) ∆H4=
②恒温恒压下充入N2,反应i中C2H4的平衡产率将
(2)乙炔在Pd表面选择加氢生成乙烯的反应机理如图。其中吸附在Pd表面上的物种用*标注。

上述反应为
您最近一年使用:0次
填空题
|
适中
(0.65)
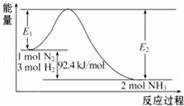
【推荐3】科学家一直致力于“人工固氮”的方法研究.用N2和H2合成NH3的能量变化如图所示。
(1)合成氨反应的热化学方程式_________________________ ,已知E2=212.4kJ/mol,则该反应正反应的活化能是______ 。
(2)反应体系中加入催化剂,反应速率______ ,E2的变化是______ 。(填“增大”、“减小”或“不变”)
(3)工业上常采用高温高压,使用催化剂的方法改变该反应的反应速率,在甲乙两个体积均为2L固定容积的密闭容器中,分别充入1molN2、3molH2和1molN2、3molH2、1molHe,反应速率甲__ 乙(填大于、小于或等于)。
(4)该反应的△S______ 0,(填大于、小于或等于),理论上在______ 条件下可以自发。
(1)合成氨反应的热化学方程式
(2)反应体系中加入催化剂,反应速率
(3)工业上常采用高温高压,使用催化剂的方法改变该反应的反应速率,在甲乙两个体积均为2L固定容积的密闭容器中,分别充入1molN2、3molH2和1molN2、3molH2、1molHe,反应速率甲
(4)该反应的△S
您最近一年使用:0次

 ,则:
,则:

