一氧化碳是一种重要的化工原料。
(1)高炉炼铁中发生的反应之一是:
FeO(s)+CO(g)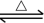 Fe(s)+CO2(g) △H=-1kJ/mol。
Fe(s)+CO2(g) △H=-1kJ/mol。
温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO的体积比将______
(填“增大”、“减小”或“不变”)。
已知1100℃时,该反应平衡常数K=0.263,现测得高炉中(CO2)=0.025mol/L,c(CO)=0.1mol/L,此时该反应_______ .
A.向正反应向向进行 B.处于平衡状态 C.向逆反应方向进行
(2)合成氨工业中需将原料气中的CO变成CO2除去。在密闭密器中将CO和H2O混合加热到800℃,达到下列平衡:
CO(g)+H2O(g)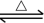 CO2(g)+H2(g) K=1.0
CO2(g)+H2(g) K=1.0
若平衡时n(H2O)/n(CO)=1,则CO转化为CO2的转化率为_______ 。
(3)用CO和H2经如下两步反应制得甲酸甲醛:
CO+2H2→CH3OH
CO+CH3OH→HCOOCH3
已知反应①中CO的转化率为80%,反应②中两种反应物的转化率均为85%,则2.52tCO最多可制得甲酸甲醛多少吨?(写出计算过程)。_______
(1)高炉炼铁中发生的反应之一是:
FeO(s)+CO(g)
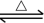 Fe(s)+CO2(g) △H=-1kJ/mol。
Fe(s)+CO2(g) △H=-1kJ/mol。温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO的体积比将
(填“增大”、“减小”或“不变”)。
已知1100℃时,该反应平衡常数K=0.263,现测得高炉中(CO2)=0.025mol/L,c(CO)=0.1mol/L,此时该反应
A.向正反应向向进行 B.处于平衡状态 C.向逆反应方向进行
(2)合成氨工业中需将原料气中的CO变成CO2除去。在密闭密器中将CO和H2O混合加热到800℃,达到下列平衡:
CO(g)+H2O(g)
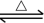 CO2(g)+H2(g) K=1.0
CO2(g)+H2(g) K=1.0若平衡时n(H2O)/n(CO)=1,则CO转化为CO2的转化率为
(3)用CO和H2经如下两步反应制得甲酸甲醛:
CO+2H2→CH3OH
CO+CH3OH→HCOOCH3
已知反应①中CO的转化率为80%,反应②中两种反应物的转化率均为85%,则2.52tCO最多可制得甲酸甲醛多少吨?(写出计算过程)。
2010·江苏南京·三模 查看更多[2]
更新时间:2016-12-09 00:29:22
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】有可逆反应A(g)+B(g) 2C(g),在不同温度下经过一定时间,混合物中C的体积分数与温度的关系如图所示。填写下列空白:
2C(g),在不同温度下经过一定时间,混合物中C的体积分数与温度的关系如图所示。填写下列空白:
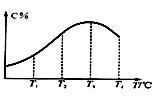
⑴反应在____________ 温度下达到平衡。
⑵正反应为__________ 热反应(填“放”或“吸”)。
⑶由T3向T4变化时,v正________ v逆(填“>”、“<”或“=”)。
 2C(g),在不同温度下经过一定时间,混合物中C的体积分数与温度的关系如图所示。填写下列空白:
2C(g),在不同温度下经过一定时间,混合物中C的体积分数与温度的关系如图所示。填写下列空白:
⑴反应在
⑵正反应为
⑶由T3向T4变化时,v正
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】目前烟气脱硝采用的技术有无催化剂的选择性还原法(SNCR)和使用催化剂的选择性还原法(SCR)。若用NH3作还原剂,则主要反应均可表示为: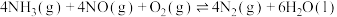
 ,其中体系温度对SNCR技术脱硝效率的影响如图所示:
,其中体系温度对SNCR技术脱硝效率的影响如图所示:
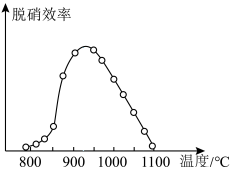
(1)当体系温度过高时,SNCR技术脱硝效率会降低,其原因是_______ ;
(2)SNCR与SCR技术相比,SCR技术的反应温度不能太高,其原因是_______ 。
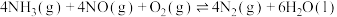
 ,其中体系温度对SNCR技术脱硝效率的影响如图所示:
,其中体系温度对SNCR技术脱硝效率的影响如图所示:
(1)当体系温度过高时,SNCR技术脱硝效率会降低,其原因是
(2)SNCR与SCR技术相比,SCR技术的反应温度不能太高,其原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】在1 L恒容密闭容器中充入一定量CH3OH发生反应:2CH3OH(g) CH3OCH3(g)+H2O(g)△H,测得CH3OH的浓度与温度的关系如图所示:
CH3OCH3(g)+H2O(g)△H,测得CH3OH的浓度与温度的关系如图所示:
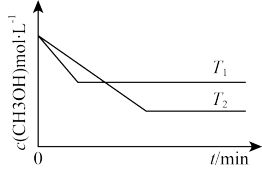
(1)△H_______ (填“>”“<”或“=”)0,说明理由_______ 。
(2)在T1时达到平衡后,再向容器中充入少量甲醇蒸气,CH3OH的平衡转化率_______ (填“增大”“减小”或“不变”)。
(3)工业上,利用水煤气合成CH3OH的反应表示如下:2H2(g)+CO(g) CH3OH(g)△H=-91.0 kJ·mol-1,向1 L的恒容密容器中加入0.1 mol H2和0.05 mol CO在一定温度下发生上述反应,10 min后反应达到平衡状态,测得放出的热量为3.64 kJ。
CH3OH(g)△H=-91.0 kJ·mol-1,向1 L的恒容密容器中加入0.1 mol H2和0.05 mol CO在一定温度下发生上述反应,10 min后反应达到平衡状态,测得放出的热量为3.64 kJ。
①从反应开始恰好平衡状态时,H2的平均反应速率v(H2)为_______ 。
②在温度不变条件下,上述反应达到平衡后再向容器中充入0.01 mol H2和0.05 mol CH3OH(g)时,平衡_______ (填“向左移动”、“向右移动”或“不移动”)。
(4)探究CH3OH合成反应化学平衡的影响因素,有利于提高CH3OH的产率。以CO2、H2为原料合成CH3OH涉及的主要反应如下:
Ⅰ.CO2(g)+3H2(g) = CH3OH(g)+H2O(g)△H=-49.5 kJ·mol-1
Ⅱ.CO(g)+2H2(g) = CH3OH(g)△H2=-90.4 kJ·mol-1
Ⅲ.CO2(g)+H2(g) = CO(g)+H2O(g)△H3
一定条件下,向体积为V L的恒容密闭容器中通入1 mol CO2和3 mol H2发生上述反应,达到平衡时,容器中CH3OH(g)为a mol,CO为b mol,此时H2O(g)的浓度为_______ mol·L-1(用含a、b、V的代数式表示,下同),反应Ⅲ的平衡常数为_______ 。
 CH3OCH3(g)+H2O(g)△H,测得CH3OH的浓度与温度的关系如图所示:
CH3OCH3(g)+H2O(g)△H,测得CH3OH的浓度与温度的关系如图所示:
(1)△H
(2)在T1时达到平衡后,再向容器中充入少量甲醇蒸气,CH3OH的平衡转化率
(3)工业上,利用水煤气合成CH3OH的反应表示如下:2H2(g)+CO(g)
 CH3OH(g)△H=-91.0 kJ·mol-1,向1 L的恒容密容器中加入0.1 mol H2和0.05 mol CO在一定温度下发生上述反应,10 min后反应达到平衡状态,测得放出的热量为3.64 kJ。
CH3OH(g)△H=-91.0 kJ·mol-1,向1 L的恒容密容器中加入0.1 mol H2和0.05 mol CO在一定温度下发生上述反应,10 min后反应达到平衡状态,测得放出的热量为3.64 kJ。①从反应开始恰好平衡状态时,H2的平均反应速率v(H2)为
②在温度不变条件下,上述反应达到平衡后再向容器中充入0.01 mol H2和0.05 mol CH3OH(g)时,平衡
(4)探究CH3OH合成反应化学平衡的影响因素,有利于提高CH3OH的产率。以CO2、H2为原料合成CH3OH涉及的主要反应如下:
Ⅰ.CO2(g)+3H2(g) = CH3OH(g)+H2O(g)△H=-49.5 kJ·mol-1
Ⅱ.CO(g)+2H2(g) = CH3OH(g)△H2=-90.4 kJ·mol-1
Ⅲ.CO2(g)+H2(g) = CO(g)+H2O(g)△H3
一定条件下,向体积为V L的恒容密闭容器中通入1 mol CO2和3 mol H2发生上述反应,达到平衡时,容器中CH3OH(g)为a mol,CO为b mol,此时H2O(g)的浓度为
您最近一年使用:0次
【推荐1】在一定温度下,向一容积为2 L的恒容密闭容器中充入4 mol SO2和2 mol O2,发生反应:2SO2(g)+O2(g) 2SO3(g) ∆H =-196 kJ/mol。经2 min后达到平衡,当反应达到平衡时,容器内压强变为起始时的0.8倍。请回答下列问题:
2SO3(g) ∆H =-196 kJ/mol。经2 min后达到平衡,当反应达到平衡时,容器内压强变为起始时的0.8倍。请回答下列问题:
(1)判断该反应达到平衡状态的标志是___________ (填字母);
a.SO2、O2、SO3三者的浓度之比为2:1:2 b.容器内气体的压强不变
c.容器内混合气体的密度保持不变 d.SO3的物质的量不再变化
e.SO2的生成速率和SO3的生成速率相等
(2)从反应开始到平衡的这段时间O2的转化率为___________ ,该温度下,该反应的平衡常数为___________ 。
(3)如图表示在密闭容器中达到平衡时,由于条件改变而引起反应速率的变化情况,a时刻改变的条件可能是___________ 。
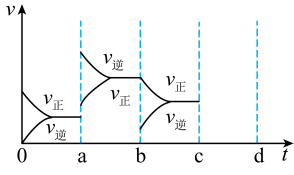
(4)在相同温度下,若起始时加入6mol SO2和3 mol O2,反应进行一段时间后,测得O2的浓度为 1.0mol•L-1,则此时该反应是否达到平衡状态___________ (填“是”与“否”),此时 V(正) ___________ V(逆)(填“大于”“小于”或“等于”)
 2SO3(g) ∆H =-196 kJ/mol。经2 min后达到平衡,当反应达到平衡时,容器内压强变为起始时的0.8倍。请回答下列问题:
2SO3(g) ∆H =-196 kJ/mol。经2 min后达到平衡,当反应达到平衡时,容器内压强变为起始时的0.8倍。请回答下列问题:(1)判断该反应达到平衡状态的标志是
a.SO2、O2、SO3三者的浓度之比为2:1:2 b.容器内气体的压强不变
c.容器内混合气体的密度保持不变 d.SO3的物质的量不再变化
e.SO2的生成速率和SO3的生成速率相等
(2)从反应开始到平衡的这段时间O2的转化率为
(3)如图表示在密闭容器中达到平衡时,由于条件改变而引起反应速率的变化情况,a时刻改变的条件可能是

(4)在相同温度下,若起始时加入6mol SO2和3 mol O2,反应进行一段时间后,测得O2的浓度为 1.0mol•L-1,则此时该反应是否达到平衡状态
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】钼(Mo)是一种难熔稀有金属,我国的钼储量居世界前列,钼及其合金在冶金、环保和航天等方面有着广泛的应用。碳酸钠作固硫剂并用氢还原辉钼矿的原理为MoS2(s)+4H2(g)+2Na2CO3(s) Mo(s)+2CO(g)+4H20(g)+2Na2S(s) △H,实验测得平衡时的有关变化曲线如图所示。
Mo(s)+2CO(g)+4H20(g)+2Na2S(s) △H,实验测得平衡时的有关变化曲线如图所示。

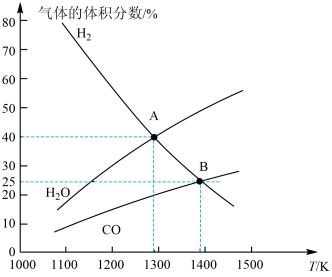
(a)不同压强下温度与H2平衡转化率的关系 (b)0.1MPa下温度与平衡时气体成分的关系
(1)由图(a)可知,该反应△H_______ 0(填“>”或“<”),p1、p2、p3由大到小的顺序为_______ ;
(2)由图(b)可知,B点时H2的平衡转化率为_______ ;
(3)A点对应的平衡常数K=_______ (MPa)2。(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
 Mo(s)+2CO(g)+4H20(g)+2Na2S(s) △H,实验测得平衡时的有关变化曲线如图所示。
Mo(s)+2CO(g)+4H20(g)+2Na2S(s) △H,实验测得平衡时的有关变化曲线如图所示。

(a)不同压强下温度与H2平衡转化率的关系 (b)0.1MPa下温度与平衡时气体成分的关系
(1)由图(a)可知,该反应△H
(2)由图(b)可知,B点时H2的平衡转化率为
(3)A点对应的平衡常数K=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】硫酸是重要的化工原料,生产过程中SO2催化氧化生成SO3的化学反应为:2SO2(g)+O2(g) 2SO3(g)。
2SO3(g)。
(1)实验测得SO2反应生成SO3的转化率与温度、压强有关,请根据下表信息,结合工业生产实际,选择最合适的生产条件是___________ 。
(2)反应2SO2(g)+O2(g)  2SO3(g)达到平衡后,改变下列条件,能使SO2(g)平衡浓度比原来减小的是___________(填字母)。
2SO3(g)达到平衡后,改变下列条件,能使SO2(g)平衡浓度比原来减小的是___________(填字母)。
(3)某温度下,SO2的平衡转化率(α)与体系总压强(P)的关系如图所示。2.0 molSO2和1.0mol O2置于10L密闭容器中,反应达平衡后,体系总压强为0.10 MPa。平衡状态由A变到B时,平衡常数K(A)___________ K(B)(填“>”、“<”或“=”)。

(4)在一个固定容积为5L的密闭容器中充入0.20mol SO2和0.10molO2 。t1时刻达到平衡,测得容器中含SO30.18mol。
①tl时刻达到平衡后,改变一个条件使化学反应速率发生如图所示的变化,则改变的条件是___________ 。
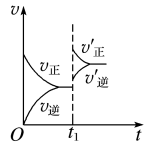
A.体积不变,向容器中通入少量O2
B.体积不变,向容器中通入少量SO2
C.缩小容器体积
D.升高温度
E.体积不变,向容器中通入少量氮气
② 若继续通入0.20mol SO2和0.10molO2 ,则平衡___________ 移动(填“向正反应方向”、“向逆反应方向”或“不”) 。
(5)某时刻反应达到平衡,混合气体平衡总压强为p,N2O4气体的平衡转化率为75%,则反应N2O4(g) 2NO2(g)的平衡常数Kp=
2NO2(g)的平衡常数Kp=__________ (用分数表示) [对于气相反应,用某组分B 的平衡压强p(B)代替物质的量浓度c(B)也可表示平衡常数,记作Kp,如p(B)=p·x(B),p为平衡总压强,x(B)为平衡系统中B的物质的量分数]
 2SO3(g)。
2SO3(g)。(1)实验测得SO2反应生成SO3的转化率与温度、压强有关,请根据下表信息,结合工业生产实际,选择最合适的生产条件是
压强 转化率 温度 | 1×105Pa | 5×105Pa | 10 ×105Pa | 15 ×105Pa |
| 400℃ | 0.9961 | 0.9972 | 0.9984 | 0.9988 |
| 500℃ | 0.9675 | 0.9767 | 0.9852 | 0.9894 |
| 600℃ | 0.8520 | 0.8897 | 0.9276 | 0.9468 |
 2SO3(g)达到平衡后,改变下列条件,能使SO2(g)平衡浓度比原来减小的是___________(填字母)。
2SO3(g)达到平衡后,改变下列条件,能使SO2(g)平衡浓度比原来减小的是___________(填字母)。| A.保持温度和容器体积不变,充入1molO2(g) |
| B.保持温度和容器体积不变,充入2mol SO3(g) |
| C.降低温度 |
| D.在其他条件不变时,减小容器的容积 |

(4)在一个固定容积为5L的密闭容器中充入0.20mol SO2和0.10molO2 。t1时刻达到平衡,测得容器中含SO30.18mol。
①tl时刻达到平衡后,改变一个条件使化学反应速率发生如图所示的变化,则改变的条件是

A.体积不变,向容器中通入少量O2
B.体积不变,向容器中通入少量SO2
C.缩小容器体积
D.升高温度
E.体积不变,向容器中通入少量氮气
② 若继续通入0.20mol SO2和0.10molO2 ,则平衡
(5)某时刻反应达到平衡,混合气体平衡总压强为p,N2O4气体的平衡转化率为75%,则反应N2O4(g)
 2NO2(g)的平衡常数Kp=
2NO2(g)的平衡常数Kp=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】氢气是合成氨的重要原料,合成氨反应的化学方程式为N2(g)+3H2(g)⇌2NH3(g),该反应为放热反应,且每生成2 mol NH3,放出92.4 kJ的热量。
(1)当合成氨反应达到平衡后,若上述反应在2min后的t1~t6内反应速率与反应时间图象如图,在每一时刻均改变一个影响反应速率的因素,请填写下列时刻改变的条件:
在t1时___________ ,在t3时___________ 。在t4时___________ 。

(2)如图N2的转化率最高是时间段___________。
(3)在一定温度下,向一个容积为1 L的容器中通入2 mol氮气和8 mol氢气及固体催化剂,使之反应。已知平衡时容器内气体的压强为起始时的80%。
①N2的转化率为___________ 。
②反应达到平衡时,放出的热量___________ (填字母)。
A.小于92.4 kJ B.等于92.4 kJ
C.大于92.4 kJ D.可能大于、小于或等于92.4 kJ
(1)当合成氨反应达到平衡后,若上述反应在2min后的t1~t6内反应速率与反应时间图象如图,在每一时刻均改变一个影响反应速率的因素,请填写下列时刻改变的条件:
在t1时

(2)如图N2的转化率最高是时间段___________。
| A.t0-t1 | B.t2-t3 | C.t3-t4 | D.t5-t6 |
①N2的转化率为
②反应达到平衡时,放出的热量
A.小于92.4 kJ B.等于92.4 kJ
C.大于92.4 kJ D.可能大于、小于或等于92.4 kJ
您最近一年使用:0次
【推荐2】(1)①某温度下,等物质的量的碘和环戊烯(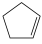 )在刚性容器内发生反应:
)在刚性容器内发生反应: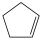 (g)+I2(g)===
(g)+I2(g)=== (g)+2HI(g),起始总压为105 Pa,平衡时总压增加了20%,环戊烯的转化率为
(g)+2HI(g),起始总压为105 Pa,平衡时总压增加了20%,环戊烯的转化率为________ ,该反应的平衡常数Kp=________ Pa。达到平衡后,欲增加环戊烯的平衡转化率,可采取的措施有________ (填标号)。
A.通入惰性气体 B.提高温度
C.增加环戊烯浓度 D.增加碘浓度
②环戊二烯容易发生聚合生成二聚体,该反应为可逆反应。不同温度下,溶液中环戊二烯浓度与反应时间的关系如图所示,下列说法正确的是________ (填标号)。
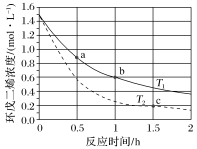
A.T1>T2
B.a点的反应速率小于c点的反应速率
C.a点的正反应速率大于b点的逆反应速率
D.b点时二聚体的浓度为0.45 mol·L-1
(2) 298 K时,将20 mL 3x mol·L-1Na3AsO3、20 mL 3x mol·L-1 I2和20 mL NaOH溶液混合,发生反应:AsO33- (aq)+I2(aq)+2OH-(aq) AsO43- (aq)+2I-(aq)+H2O(l)。溶液中c(AsO
AsO43- (aq)+2I-(aq)+H2O(l)。溶液中c(AsO )与反应时间(t)的关系如图所示。
)与反应时间(t)的关系如图所示。

下列可判断反应达到平衡状态的是________ (填标号)。
a.溶液的pH不再变化
b.v(I-)=2v(AsO33-)
c.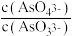 不再变化
不再变化
d.c(I-)=y mol·L-1
(3)已知反应2HI(g) H2(g)+I2(g),ΔH>0,由实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用下图表示。当升高到某一温度时,反应重新达到平衡,相应的点分别为
H2(g)+I2(g),ΔH>0,由实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用下图表示。当升高到某一温度时,反应重新达到平衡,相应的点分别为______________ (填字母)。

 )在刚性容器内发生反应:
)在刚性容器内发生反应: (g)+I2(g)===
(g)+I2(g)=== (g)+2HI(g),起始总压为105 Pa,平衡时总压增加了20%,环戊烯的转化率为
(g)+2HI(g),起始总压为105 Pa,平衡时总压增加了20%,环戊烯的转化率为A.通入惰性气体 B.提高温度
C.增加环戊烯浓度 D.增加碘浓度
②环戊二烯容易发生聚合生成二聚体,该反应为可逆反应。不同温度下,溶液中环戊二烯浓度与反应时间的关系如图所示,下列说法正确的是

A.T1>T2
B.a点的反应速率小于c点的反应速率
C.a点的正反应速率大于b点的逆反应速率
D.b点时二聚体的浓度为0.45 mol·L-1
(2) 298 K时,将20 mL 3x mol·L-1Na3AsO3、20 mL 3x mol·L-1 I2和20 mL NaOH溶液混合,发生反应:AsO33- (aq)+I2(aq)+2OH-(aq)
 AsO43- (aq)+2I-(aq)+H2O(l)。溶液中c(AsO
AsO43- (aq)+2I-(aq)+H2O(l)。溶液中c(AsO )与反应时间(t)的关系如图所示。
)与反应时间(t)的关系如图所示。
下列可判断反应达到平衡状态的是
a.溶液的pH不再变化
b.v(I-)=2v(AsO33-)
c.
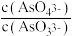 不再变化
不再变化d.c(I-)=y mol·L-1
(3)已知反应2HI(g)
 H2(g)+I2(g),ΔH>0,由实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用下图表示。当升高到某一温度时,反应重新达到平衡,相应的点分别为
H2(g)+I2(g),ΔH>0,由实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用下图表示。当升高到某一温度时,反应重新达到平衡,相应的点分别为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ.在一定温度下,4L密闭容器内某一反应中气体M、气体N的物质的量随时间变化的曲线如图: 时刻,正逆反应速率大小
时刻,正逆反应速率大小
___________  。(填“>”“=”或“<”)
。(填“>”“=”或“<”)
(2)若 min,计算反应开始至
min,计算反应开始至 时刻用M的浓度变化表示的平均反应速率
时刻用M的浓度变化表示的平均反应速率___________ 。
(3) 时刻化学反应达到平衡,反应物的转化率为
时刻化学反应达到平衡,反应物的转化率为___________ 。
(4)写出反应的化学方程式___________ 。
(5)如果升高温度,则
___________ (填“增大”“减小”或“不变”)。
Ⅱ.某同学设计如下实验方案探究影响锌与稀硫酸反应速率的因素,有关数据如下表所示:
(6)①本实验待测数据可以是___________ ,实验Ⅰ和实验Ⅱ可以探究___________ ,对锌与稀硫酸反应速率的影响。
②实验Ⅲ和实验Ⅳ的目的是___________ 。
(7)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
表中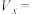
___________ 。
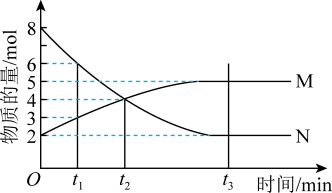
 时刻,正逆反应速率大小
时刻,正逆反应速率大小
 。(填“>”“=”或“<”)
。(填“>”“=”或“<”)(2)若
 min,计算反应开始至
min,计算反应开始至 时刻用M的浓度变化表示的平均反应速率
时刻用M的浓度变化表示的平均反应速率(3)
 时刻化学反应达到平衡,反应物的转化率为
时刻化学反应达到平衡,反应物的转化率为(4)写出反应的化学方程式
(5)如果升高温度,则

Ⅱ.某同学设计如下实验方案探究影响锌与稀硫酸反应速率的因素,有关数据如下表所示:
| 序号 | 纯锌粉/g | 2.0 硫酸溶液/mL 硫酸溶液/mL | 温度/℃ | 硫酸铜固体/g | 加入蒸馏水/mL |
| Ⅰ | 2.0 | 50.0 | 25 | 0 | 0 |
| Ⅱ | 2.0 | 40.0 | 25 | 0 | 10.0 |
| Ⅲ | 2.0 | 50.0 | 25 | 0.2 | 0 |
| Ⅳ | 2.0 | 50.0 | 25 | 4.0 | 0 |
(6)①本实验待测数据可以是
②实验Ⅲ和实验Ⅳ的目的是
(7)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
| 实验序号 | 体积V/mL | ||||
 溶液 溶液 | 水 | KI溶液 |  溶液 溶液 | 淀粉溶液 | |
| ① | 10.0 | 0.0 | 4.0 | 4.0 | 2.0 |
| ② | 9.0 | 1.0 | 4.0 | 4.0 | 2.0 |
| ③ | 8.0 |  | 4.0 | 4.0 | 2.0 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】化学反应都伴随着能量的变化。回答下列问题:
(1)可用焓变和熵变来判断化学反应进行的方向,下列都是能自发进行的化学反应,其中是吸热反应且反应后嫡增的是___________(填字母)。
(2)一种分解海水制氢气的方法为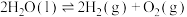 。如图为该反应的能量变化示意图,使用催化剂
。如图为该反应的能量变化示意图,使用催化剂 后,图中A点将
后,图中A点将___________ (填“升高”、“降低”或“不变”)。

(3)已知: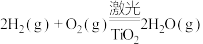

②部分化学键的键能数据如表:
由此计算x=___________ 。(用含a、c、d的代数式表示)
(4)火箭推进器中盛有强还原剂液态肼( )和强氧化剂液态过氧化氢。将16g液态肼和足量
)和强氧化剂液态过氧化氢。将16g液态肼和足量 ,混合完全反应,生成氮气和水蒸气,放出320.9kJ的热量(相当于25℃、101kPa下测得的热量),则该反应的热化学方程式为
,混合完全反应,生成氮气和水蒸气,放出320.9kJ的热量(相当于25℃、101kPa下测得的热量),则该反应的热化学方程式为___________ 。
(1)可用焓变和熵变来判断化学反应进行的方向,下列都是能自发进行的化学反应,其中是吸热反应且反应后嫡增的是___________(填字母)。
A. | B. |
C. | D.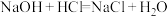 |
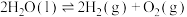 。如图为该反应的能量变化示意图,使用催化剂
。如图为该反应的能量变化示意图,使用催化剂 后,图中A点将
后,图中A点将
(3)已知:
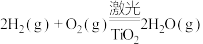

②部分化学键的键能数据如表:
| 化学键 |  |  |  |
 | x | c | d |
(4)火箭推进器中盛有强还原剂液态肼(
 )和强氧化剂液态过氧化氢。将16g液态肼和足量
)和强氧化剂液态过氧化氢。将16g液态肼和足量 ,混合完全反应,生成氮气和水蒸气,放出320.9kJ的热量(相当于25℃、101kPa下测得的热量),则该反应的热化学方程式为
,混合完全反应,生成氮气和水蒸气,放出320.9kJ的热量(相当于25℃、101kPa下测得的热量),则该反应的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知在不同温度下,甲烷隔绝空气有可能发生如下两个裂解反应:①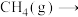
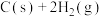 ,②
,②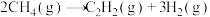 。某同学为了得到用天然气制取炭黑的允许温度范围和最佳温度,查阅资料,得到如下热力学数据:
。某同学为了得到用天然气制取炭黑的允许温度范围和最佳温度,查阅资料,得到如下热力学数据:
反应①的 ,
,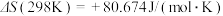
反应②的 ,
,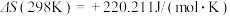
已知,上述反应的焓变和熵变随温度变化很小。请帮助这位同学回答下列问题:
(1)反应①在__________ (填“高温”或“低温”)下能自发进行。
(2)反应①能否自发进行是由__________ (填“焓变”或“熵变”)决定的。
(3)制取炭黑的允许温度范围:__________ 。
(4)为了提高甲烷的炭化程度,下列温度最合适的是__________ (填标号)。
A.905.2K B.927K C.1273K D.2000K
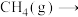
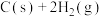 ,②
,②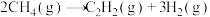 。某同学为了得到用天然气制取炭黑的允许温度范围和最佳温度,查阅资料,得到如下热力学数据:
。某同学为了得到用天然气制取炭黑的允许温度范围和最佳温度,查阅资料,得到如下热力学数据:反应①的
 ,
,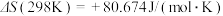
反应②的
 ,
,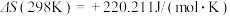
已知,上述反应的焓变和熵变随温度变化很小。请帮助这位同学回答下列问题:
(1)反应①在
(2)反应①能否自发进行是由
(3)制取炭黑的允许温度范围:
(4)为了提高甲烷的炭化程度,下列温度最合适的是
A.905.2K B.927K C.1273K D.2000K
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】填空。
(1)(2023·湖北宜昌市协作体高二上学期期中)甲烷是重要的气体燃料和化工原料,由CH4制取合成气(CO、H2)的反应原理为CH4(g)+H2O(g)⇌CO(g)+3H2(g) ΔH>0。当体系温度等于TK时ΔH−TΔS=0,温度大于T时ΔH−TΔS___________ (填“>”“<”或“=”)0。
(2)(2023·四川内江市高二上学期期末)反应I(2NH3(g)+CO2(g)⇌H2NCOONH4 ΔH1<0)在___________ (填“高温”、“低温”或“任何温度”)下能自发进行。
(3)(2023·新疆生产建设兵团部分名校高二上学期期中)已知:H2(g)+C2H4(g)⇌C2H6(g) ΔH=-137kJ·mol-1。该反应在___________ (填“低温”、“高温”或“任何温度”)下能自发进行。
(1)(2023·湖北宜昌市协作体高二上学期期中)甲烷是重要的气体燃料和化工原料,由CH4制取合成气(CO、H2)的反应原理为CH4(g)+H2O(g)⇌CO(g)+3H2(g) ΔH>0。当体系温度等于TK时ΔH−TΔS=0,温度大于T时ΔH−TΔS
(2)(2023·四川内江市高二上学期期末)反应I(2NH3(g)+CO2(g)⇌H2NCOONH4 ΔH1<0)在
(3)(2023·新疆生产建设兵团部分名校高二上学期期中)已知:H2(g)+C2H4(g)⇌C2H6(g) ΔH=-137kJ·mol-1。该反应在
您最近一年使用:0次



