任何化学反应都伴随着能量的变化,通过化学反应,化学能可转化为热能、电能等不同形式的能量。
(1)H2可用于工业合成氨气,已知拆开1 mol H-H、1 mol N≡N分别需要吸收的能量为 436 kJ、946 kJ,形成1 mol N-H会放出能量 391 kJ,则在反应N2+3H2 2NH3中,每生成2 mol NH3
2NH3中,每生成2 mol NH3___________ (填“吸收”或“放出”)热量___________ kJ。
(2)Mg、Al设计成如图所示原电池装置:
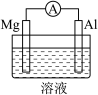
①若溶液为盐酸,Mg为___________ (填“正”或“负”)极;
②若溶液为氢氧化钠溶液,负极的电极反应方程式为___________ 。
(3)电化学法处理SO2是目前研究的热点。利用过氧化氢吸收SO2可消除SO2污染,设计装置如图所示。
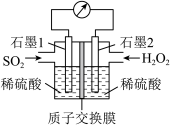
①质子通过交换膜向___________ (填“左”或“右”)移动;
②正极的电极反应式为___________ 。
③若11.2 L(折合为标准状况) SO2参与反应,则迁移H+的物质的量为___________ 。
(1)H2可用于工业合成氨气,已知拆开1 mol H-H、1 mol N≡N分别需要吸收的能量为 436 kJ、946 kJ,形成1 mol N-H会放出能量 391 kJ,则在反应N2+3H2
 2NH3中,每生成2 mol NH3
2NH3中,每生成2 mol NH3(2)Mg、Al设计成如图所示原电池装置:

①若溶液为盐酸,Mg为
②若溶液为氢氧化钠溶液,负极的电极反应方程式为
(3)电化学法处理SO2是目前研究的热点。利用过氧化氢吸收SO2可消除SO2污染,设计装置如图所示。

①质子通过交换膜向
②正极的电极反应式为
③若11.2 L(折合为标准状况) SO2参与反应,则迁移H+的物质的量为
更新时间:2023-06-19 19:59:09
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】Ⅰ.完成下列问题
(1)从能量的变化和反应的快慢等角度研究反应:2H2(g)+O2(g)=2H2O(g)。
①已知该反应为放热反应,下图能正确表示该反应中能量变化的是_______ 。
a.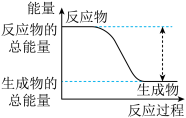 b.
b. 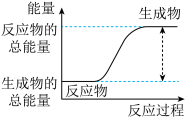
②从断键和成键的角度分析上述反应中能量的变化,化学键的键能如下表所示:
则生成1molH2O(g)可以放出热量_______ kJ。
(2)下列反应中,属于放热反应的是_______ ,属于吸热反应的是_______ 。
a.盐酸与烧碱溶液反应
b.Ba(OH)2•8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑
c.氢气在氧气中燃烧生成水
d.高温煅烧石灰石使其分解
e.铝和盐酸反应
f.葡萄糖在人体内氧化分解
Ⅱ.完成下列问题
(3)FeCl3溶液常用于腐蚀印刷电路铜板,发生 2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原 电池, 则负极所用电极材料为_______ 。
(4)H2和 O2组合形成的燃料电池的结构如图(电解液是稀硫酸):
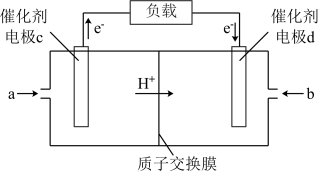
电极 d 的电极反应式为_______ 。
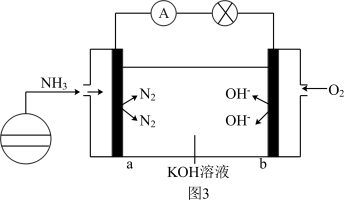
(5)氨氧燃料电池具有很大的发展潜力,其工作原理如图 3 所示。a电极上的反应式为_______ 。
(6)高铁电池是一种新型可充电电池。高铁电池的总反应式为: 3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH。已知负极反应式为 Zn-2e-+2OH-=Zn(OH)2,则正极反应为
3Zn(OH)2+2Fe(OH)3+4KOH。已知负极反应式为 Zn-2e-+2OH-=Zn(OH)2,则正极反应为_______ 。
(1)从能量的变化和反应的快慢等角度研究反应:2H2(g)+O2(g)=2H2O(g)。
①已知该反应为放热反应,下图能正确表示该反应中能量变化的是
a.
 b.
b. 
②从断键和成键的角度分析上述反应中能量的变化,化学键的键能如下表所示:
| 化学键 | H-H | O=O | H-O |
| 键能(kJ·mol-1) | 436 | 496 | 463 |
则生成1molH2O(g)可以放出热量
(2)下列反应中,属于放热反应的是
a.盐酸与烧碱溶液反应
b.Ba(OH)2•8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑
c.氢气在氧气中燃烧生成水
d.高温煅烧石灰石使其分解
e.铝和盐酸反应
f.葡萄糖在人体内氧化分解
Ⅱ.完成下列问题
(3)FeCl3溶液常用于腐蚀印刷电路铜板,发生 2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原 电池, 则负极所用电极材料为
(4)H2和 O2组合形成的燃料电池的结构如图(电解液是稀硫酸):

电极 d 的电极反应式为
(5)氨氧燃料电池具有很大的发展潜力,其工作原理如图 3 所示。a电极上的反应式为

(6)高铁电池是一种新型可充电电池。高铁电池的总反应式为: 3Zn+2K2FeO4+8H2O
 3Zn(OH)2+2Fe(OH)3+4KOH。已知负极反应式为 Zn-2e-+2OH-=Zn(OH)2,则正极反应为
3Zn(OH)2+2Fe(OH)3+4KOH。已知负极反应式为 Zn-2e-+2OH-=Zn(OH)2,则正极反应为
您最近一年使用:0次
【推荐2】研究化学反应中的能量和速率变化对生产、生活有着重要意义。
I.某些常见化学键的键能(将 气体分子AB断裂为中性气态原子A和B所需的能量或A和B合成1molAB气体所放出的能量)数据如下表:
气体分子AB断裂为中性气态原子A和B所需的能量或A和B合成1molAB气体所放出的能量)数据如下表:
(1) 完全燃烧生成
完全燃烧生成 和气态水放出的能量为
和气态水放出的能量为___________ kJ。该反应中反应物的总能量___________ (填“>”、“<”或“=”)生成物的总能量。
II.实验室模拟热气循环法合成尿素, 与
与 在一定条件下发生反应:
在一定条件下发生反应: 。
。
为了验证反应温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如表所示。
(2)控制变量是科学研究的重要方法,因此表中数据:
________ ,
________ 。
(3)对比实验①③,目的是验证___________ (填“反应温度”或“催化剂的比表面积”)对化学反应速率的影响规律。
(4)一定温度下,向1L密闭容器中充入 和
和 发生反应:
发生反应: ,若起始压强为
,若起始压强为 ,反应2min后该反应达到化学平衡状态,平衡时的压强是起始时的0.8倍,则0~2min内,
,反应2min后该反应达到化学平衡状态,平衡时的压强是起始时的0.8倍,则0~2min内,
___________  ,
, 的平衡转化率为
的平衡转化率为___________ %。
(5)下列情况中,一定能说明上述反应达到平衡的是___________(填标号)。
(6)“碳呼吸电池”是一种新型化学电源,其工作原理如图。当得到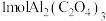 时,电路中转移的电子的物质的量为
时,电路中转移的电子的物质的量为___________ mol。

I.某些常见化学键的键能(将
 气体分子AB断裂为中性气态原子A和B所需的能量或A和B合成1molAB气体所放出的能量)数据如下表:
气体分子AB断裂为中性气态原子A和B所需的能量或A和B合成1molAB气体所放出的能量)数据如下表:| 化学键 |  |  |  |  |
键能/( ) ) | 414 | 803 | 463 | 498 |
(1)
 完全燃烧生成
完全燃烧生成 和气态水放出的能量为
和气态水放出的能量为II.实验室模拟热气循环法合成尿素,
 与
与 在一定条件下发生反应:
在一定条件下发生反应: 。
。为了验证反应温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如表所示。
| 实验编号 | 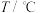 |  初始浓度/( 初始浓度/( ) ) |  初始浓度/( 初始浓度/( ) ) | 催化剂的比表面积/(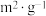 ) ) |
| ① | 280 |  | 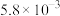 | 82 |
| ② |  |  | 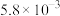 | 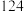 |
| ③ | 350 | a | 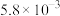 | 82 |
(2)控制变量是科学研究的重要方法,因此表中数据:


(3)对比实验①③,目的是验证
(4)一定温度下,向1L密闭容器中充入
 和
和 发生反应:
发生反应: ,若起始压强为
,若起始压强为 ,反应2min后该反应达到化学平衡状态,平衡时的压强是起始时的0.8倍,则0~2min内,
,反应2min后该反应达到化学平衡状态,平衡时的压强是起始时的0.8倍,则0~2min内,
 ,
, 的平衡转化率为
的平衡转化率为(5)下列情况中,一定能说明上述反应达到平衡的是___________(填标号)。
A. 的体积分数保持不变 的体积分数保持不变 |
| B.反应体系中气体的密度保持不变 |
C.反应消耗 ,同时生成 ,同时生成 |
D. 的质量保持不变 的质量保持不变 |
(6)“碳呼吸电池”是一种新型化学电源,其工作原理如图。当得到
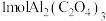 时,电路中转移的电子的物质的量为
时,电路中转移的电子的物质的量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】为了探究化学能与热能的转化,某实验小组设计了如图所示的三套实验装置:
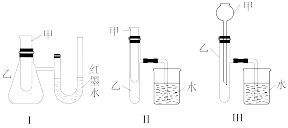
(1)上述 个装置中,不能证明“铜与浓硝酸反应是吸热反应还是放热反应”的是
个装置中,不能证明“铜与浓硝酸反应是吸热反应还是放热反应”的是 不能用手触摸和使用温度计
不能用手触摸和使用温度计
_______ 。
(2)某同学选用装置Ⅰ进行实验 实验前
实验前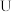 形管里液面左右相平
形管里液面左右相平 ,在甲试管里加入适量氢氧化钠溶液与稀盐酸,
,在甲试管里加入适量氢氧化钠溶液与稀盐酸,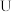 形管中可观察到的现象是
形管中可观察到的现象是_______ ,说明该反应属于_______  填“吸热”或“放热”
填“吸热”或“放热” 反应。
反应。
(3)为定量测定(2)中反应的反应热,使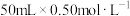 盐酸与
盐酸与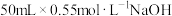 溶液在简易量热计中进行中和反应。该实验中
溶液在简易量热计中进行中和反应。该实验中 的浓度大于
的浓度大于 的浓度的作用是
的浓度的作用是_______ 。
(4)已知一些化学键的键能数据如表所示:
请根据键能数据估算 和
和 反应生成
反应生成 和
和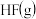 的热化学方程式:
的热化学方程式:_______ 。

(1)上述
 个装置中,不能证明“铜与浓硝酸反应是吸热反应还是放热反应”的是
个装置中,不能证明“铜与浓硝酸反应是吸热反应还是放热反应”的是 不能用手触摸和使用温度计
不能用手触摸和使用温度计
(2)某同学选用装置Ⅰ进行实验
 实验前
实验前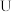 形管里液面左右相平
形管里液面左右相平 ,在甲试管里加入适量氢氧化钠溶液与稀盐酸,
,在甲试管里加入适量氢氧化钠溶液与稀盐酸, 形管中可观察到的现象是
形管中可观察到的现象是 填“吸热”或“放热”
填“吸热”或“放热” 反应。
反应。(3)为定量测定(2)中反应的反应热,使
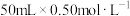 盐酸与
盐酸与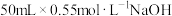 溶液在简易量热计中进行中和反应。该实验中
溶液在简易量热计中进行中和反应。该实验中 的浓度大于
的浓度大于 的浓度的作用是
的浓度的作用是(4)已知一些化学键的键能数据如表所示:
| 化学键 |  |  |  |  |
键能 | 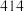 | 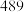 |  | 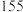 |
 和
和 反应生成
反应生成 和
和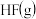 的热化学方程式:
的热化学方程式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】(I)某兴趣小组的同学用如图所示装置研究有关电化学的问题。当闭合该装置的电键时,观察到电流表的指针发生了偏转。
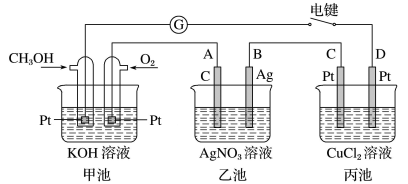
请回答下列问题:
(1)甲池为_______ (填“原电池”“电解池”或“电镀池”),通入CH3OH电极的电极反应式为_______ 。
(2)乙池中A(石墨)电极的名称为_______ (填“正极”“负极”“阴极”或“阳极”),乙池总反应式为_______ 。
(3)当乙池中B极质量增加5.40g时,甲池中理论上消耗O2的体积为_______ mL(标准状况下),丙池中析出_______ g铜。
(II)氯碱工业是高能耗产业,一种将电解池与燃料电池相组合的新工艺节能超过30%。在这种工艺设计中,相关物料的传输与转化关系如图所示,其中的电极未标出,所用的离子交换膜都只允许阳离子通过。
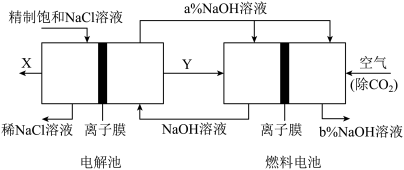
(4)图中X_______ (填化学式)比较图示中a%与b%的大小_______ 。
(5)写出燃料电池中的电极反应式:负极电极反应式_______
(6)当生成的X气体为2mol时,理论上通入空气的体积(标况)为_______ L

请回答下列问题:
(1)甲池为
(2)乙池中A(石墨)电极的名称为
(3)当乙池中B极质量增加5.40g时,甲池中理论上消耗O2的体积为
(II)氯碱工业是高能耗产业,一种将电解池与燃料电池相组合的新工艺节能超过30%。在这种工艺设计中,相关物料的传输与转化关系如图所示,其中的电极未标出,所用的离子交换膜都只允许阳离子通过。

(4)图中X
(5)写出燃料电池中的电极反应式:负极电极反应式
(6)当生成的X气体为2mol时,理论上通入空气的体积(标况)为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】氮氧化物和二氧化硫对环境的影响很大,为加大对环境治理的力度,对含氮氧化物和二氧化硫的处理是一个重要的课题。
(1)N2和O2生成NO时的能量变化情况如下图所示。

则N2(g)和O2(g)反应生成NO(g)的反应是_________ (填“吸热”或“放热”) 反应。
(2)在体积为2 L的密闭容器中充入0.5 mol NO2和1 mol CO,一定条件 下发生反应:NO2(g)+CO(g) CO2(g)+NO(g),2 min时,测得容器中NO的物质的量为0.2 mol。
CO2(g)+NO(g),2 min时,测得容器中NO的物质的量为0.2 mol。
①该段时间内,用CO2表示的平均反应速率为______________ 。
②下列事实能说明此反应在该条件下已经达到化学平衡状态的是____________ 。
A.容器内气体总质量保持不变
B. NO2的物质的量浓度不再改变
C. NO2和CO的物质的量之比保持不变
D. 容器内气体总压强保持不变
(3)碳热还原法脱硝:即用碳将氮氧化物(NO)转化为无毒物质,写出反应的化学方程式____________ ,NO脱除效率在无氧和有氧条件下随温度的变化如下图所示,有氧条件更有利于NO低温脱除,但高于600°C脱除率开始下降,下降的原因可能是______________ 。

(4)空气质子交换法治理SO2,其原理是将含有SO2的烟气与O2通过原电池反应制得硫酸,负极的电极反应式是_________________ 。
(1)N2和O2生成NO时的能量变化情况如下图所示。

则N2(g)和O2(g)反应生成NO(g)的反应是
(2)在体积为2 L的密闭容器中充入0.5 mol NO2和1 mol CO,一定条件 下发生反应:NO2(g)+CO(g)
 CO2(g)+NO(g),2 min时,测得容器中NO的物质的量为0.2 mol。
CO2(g)+NO(g),2 min时,测得容器中NO的物质的量为0.2 mol。①该段时间内,用CO2表示的平均反应速率为
②下列事实能说明此反应在该条件下已经达到化学平衡状态的是
A.容器内气体总质量保持不变
B. NO2的物质的量浓度不再改变
C. NO2和CO的物质的量之比保持不变
D. 容器内气体总压强保持不变
(3)碳热还原法脱硝:即用碳将氮氧化物(NO)转化为无毒物质,写出反应的化学方程式

(4)空气质子交换法治理SO2,其原理是将含有SO2的烟气与O2通过原电池反应制得硫酸,负极的电极反应式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】根据要求,回答下列问题:
I.把化学能转化为电能的装置叫做原电池。_______ 。
(2)装置④中,正极材料是_______ ;负极的电极反应式为_______ ;电池工作时,总反应的离子方程式为_______ ;烧杯中 向
向_______ 电极移动(填“Cu”或“Ag”);导线中电子的流动方向为_______ (填“Cu到Ag”或“Ag到Cu”)。
II.某同学利用铁与盐酸的反应,探究影响反应速率的因素(实验所用铁的质量相等且铁块的形状相同,盐酸均过量),实验设计如下:
(1)若四组实验均以收集到448mL(标准状况)氢气为标准,则上述实验中还需要测定的数据是_______ 。
(2)实验1和2是探究_______ 对该反应速率的影响。实验_______ 和_______ 是探究温度对该反应速率的影响。
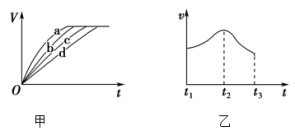
(3)不同时间t产生的氢气体积V如图甲所示,曲线c对应的实验编号是_______ 。每一组实验中产生氢气的速率v随时间t变化的曲线如图乙所示,其中t1~t2速率变化的主要原因是_______ 。______ 。
I.把化学能转化为电能的装置叫做原电池。
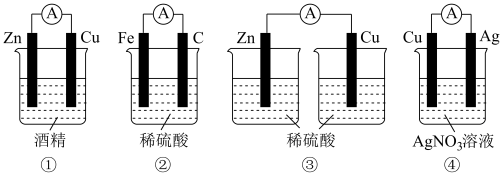
(2)装置④中,正极材料是
 向
向II.某同学利用铁与盐酸的反应,探究影响反应速率的因素(实验所用铁的质量相等且铁块的形状相同,盐酸均过量),实验设计如下:
| 实验编号 | 盐酸浓度/( ) ) | 铁的状态 | 温度/K |
| 1 | 2.00 | 块状 | 293 |
| 2 | 4.00 | 块状 | 293 |
| 3 | 4.00 | 粉末 | 293 |
| 4 | 4.00 | 块状 | 313 |
(2)实验1和2是探究
(3)不同时间t产生的氢气体积V如图甲所示,曲线c对应的实验编号是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】建设“美丽中国”首先要做好环境保护与治理.氮氧化物(NOx)是严重的大气污染物,能引起雾霾、光化学烟雾、酸雨等环境问题.
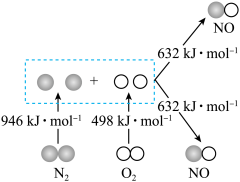
Ⅰ.汽车发动机工作时会引发N2和O2反应,生成NOx等污染大气,其中生成NO的能量变化如图所示:______ (填“吸收”或“放出”)______ kJ热量,1mol 和1mol
和1mol 的总能量
的总能量______ (填“大于”“等于”或“小于”)2mol 的总能量。
的总能量。
Ⅱ.某科研机构设计了几种如下转化氮氧化物的方案.请回答下列问题:
方案1:利用CO在催化剂条件下还原: 。向甲、乙两个容积均为2L的恒容密闭容器中分别充入2molNO2(g)和3molCO(g),分别在不同温度下反应.反应过程中测得CO2物质的量如下表:
。向甲、乙两个容积均为2L的恒容密闭容器中分别充入2molNO2(g)和3molCO(g),分别在不同温度下反应.反应过程中测得CO2物质的量如下表:
(2)①甲容器中,NO2的平衡转化率为______ ;
②温度为T1℃时,0~8min内用CO表示的平均反应速率v(CO)=______ mol·L-1·min-1;
③10min时,反应速率:甲______ (填“>”“<”或“=”)乙,其判断依据是______ ;
(3)在恒温、恒容密闭容器中进行上述反应,下列不能说明该反应一定达到平衡状态的是______ (填标号).
A.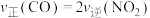 B.混合气体的密度不变
B.混合气体的密度不变
C.容器内气体颜色不变 D.气体平均相对分子质量不变
E.容器内
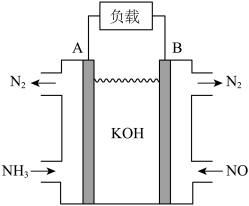
方案2:利用NH3可消除大气污染物NO,可将反应设计为原电池提供电能,如图所示;______ (填“正”或“负”)极;该电池的总反应式为______ 。
Ⅰ.汽车发动机工作时会引发N2和O2反应,生成NOx等污染大气,其中生成NO的能量变化如图所示:
 和1mol
和1mol 的总能量
的总能量 的总能量。
的总能量。Ⅱ.某科研机构设计了几种如下转化氮氧化物的方案.请回答下列问题:
方案1:利用CO在催化剂条件下还原:
 。向甲、乙两个容积均为2L的恒容密闭容器中分别充入2molNO2(g)和3molCO(g),分别在不同温度下反应.反应过程中测得CO2物质的量如下表:
。向甲、乙两个容积均为2L的恒容密闭容器中分别充入2molNO2(g)和3molCO(g),分别在不同温度下反应.反应过程中测得CO2物质的量如下表:容器 | 甲(T1/℃) | 乙(T2/℃) | ||||||||
反应时间/min | 0 | 4 | 8 | 10 | 20 | 0 | 8 | 10 | 20 | 21 |
n(CO2)/mol | 0 | 0.8 | 1.2 | 1.2 | 1.2 | 0 | 1.0 | 1.2 | 2.0 | 2.0 |
(2)①甲容器中,NO2的平衡转化率为
②温度为T1℃时,0~8min内用CO表示的平均反应速率v(CO)=
③10min时,反应速率:甲
(3)在恒温、恒容密闭容器中进行上述反应,下列不能说明该反应一定达到平衡状态的是
A.
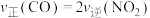 B.混合气体的密度不变
B.混合气体的密度不变C.容器内气体颜色不变 D.气体平均相对分子质量不变
E.容器内

方案2:利用NH3可消除大气污染物NO,可将反应设计为原电池提供电能,如图所示;
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】羟胺( )为无色固体,结构可视为
)为无色固体,结构可视为 替代
替代 中1个
中1个 ,羟胺具有和
,羟胺具有和 类似的弱碱性,可以与盐酸反应生成盐酸羟胺(
类似的弱碱性,可以与盐酸反应生成盐酸羟胺( ),盐酸羟胺是一种盐,易溶于水,溶解后完全电离为
),盐酸羟胺是一种盐,易溶于水,溶解后完全电离为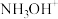 和
和 。
。
(1) 中
中 元素的化合价是
元素的化合价是_______ 。
(2)过氧化氢催化氧化氨水法制备盐酸羟胺的原理如下:
步骤1: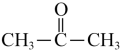 +NH3+H2O2
+NH3+H2O2 X+2H2O
X+2H2O
步骤2:X+HCl+H2O⇌NH2OH HCl+
HCl+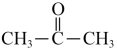
资料:丙酮( )是一种易溶于水的无色液体,沸点为
)是一种易溶于水的无色液体,沸点为 。
。
① 的分子式为
的分子式为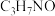 ,其核磁共振氢谱只有两个吸收峰,红外光谱显示其分子结构中存在羟基和碳氮双键。
,其核磁共振氢谱只有两个吸收峰,红外光谱显示其分子结构中存在羟基和碳氮双键。 的结构简式是
的结构简式是_______ 。
②步骤1中,相同反应时间氨的转化率随温度变化如图1。温度高于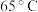 时,随温度上升氨的转化率变化的原因是
时,随温度上升氨的转化率变化的原因是_______ 。 的平衡转化率随温度变化如图2。该反应为
的平衡转化率随温度变化如图2。该反应为_______ (填“吸热”或“放热”)反应。_______ (1点即可)。
(3)电化学法制备盐酸羟胺:
向两侧电极分别通入 和
和 ,以盐酸为电解质,组装原电池以制备盐酸羟胺。装置(图3)和正极反应机理图(图4):
,以盐酸为电解质,组装原电池以制备盐酸羟胺。装置(图3)和正极反应机理图(图4):______ 。
②一段时间后,正极区的 与反应前相比
与反应前相比_______ (填“增大”、“减小”或“不变”)(不考虑溶液体积的变化)。
 )为无色固体,结构可视为
)为无色固体,结构可视为 替代
替代 中1个
中1个 ,羟胺具有和
,羟胺具有和 类似的弱碱性,可以与盐酸反应生成盐酸羟胺(
类似的弱碱性,可以与盐酸反应生成盐酸羟胺( ),盐酸羟胺是一种盐,易溶于水,溶解后完全电离为
),盐酸羟胺是一种盐,易溶于水,溶解后完全电离为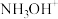 和
和 。
。(1)
 中
中 元素的化合价是
元素的化合价是(2)过氧化氢催化氧化氨水法制备盐酸羟胺的原理如下:
步骤1:
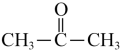 +NH3+H2O2
+NH3+H2O2 X+2H2O
X+2H2O步骤2:X+HCl+H2O⇌NH2OH
 HCl+
HCl+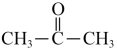
资料:丙酮(
 )是一种易溶于水的无色液体,沸点为
)是一种易溶于水的无色液体,沸点为 。
。①
 的分子式为
的分子式为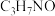 ,其核磁共振氢谱只有两个吸收峰,红外光谱显示其分子结构中存在羟基和碳氮双键。
,其核磁共振氢谱只有两个吸收峰,红外光谱显示其分子结构中存在羟基和碳氮双键。 的结构简式是
的结构简式是②步骤1中,相同反应时间氨的转化率随温度变化如图1。温度高于
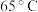 时,随温度上升氨的转化率变化的原因是
时,随温度上升氨的转化率变化的原因是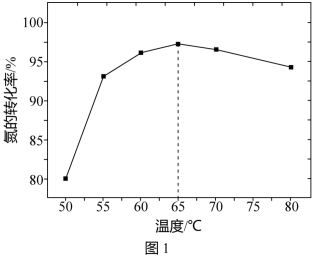
 的平衡转化率随温度变化如图2。该反应为
的平衡转化率随温度变化如图2。该反应为
(3)电化学法制备盐酸羟胺:
向两侧电极分别通入
 和
和 ,以盐酸为电解质,组装原电池以制备盐酸羟胺。装置(图3)和正极反应机理图(图4):
,以盐酸为电解质,组装原电池以制备盐酸羟胺。装置(图3)和正极反应机理图(图4):
②一段时间后,正极区的
 与反应前相比
与反应前相比
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】碳和氮、硫是动植物体中的重要组成元素,向大气中过度排放二氧化碳会造成温室效应,氮氧化物会产生光化学烟雾,SO2会形成酸雨,目前,这些有毒有害气体的处理成为科学研究的重要内容。
(1)已知热化学方程式:
①2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) △H1
②C(s)+ O2(g)=CO2(g) △H2
③H2(g)+ O2(g)=H2O(l) △H3
O2(g)=H2O(l) △H3
则反应④2C(s)+H2(g)=C2H2(g)的△H 为_________________________ 。(用含△H1、△H2、△H3关系式表示)
(2)用活性炭还原法可以处理氮氧化物。某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO(g) N2+CO2(g) △H<0。在Tl℃时,反应进行到不同时间测得各物质的浓度(单位:mol/L)如下:
N2+CO2(g) △H<0。在Tl℃时,反应进行到不同时间测得各物质的浓度(单位:mol/L)如下:
①10〜20min内,NO的平均反应速率v(NO)=___________ ,
②30min后,只改变某-条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是________ (填字母编号)。
a.通入一定量的NO b.加入一定量的c
c.适当升高反应体系的温度 d.加入合适的催化剂
e.适当缩小容器的体积
③若保持与上述反应前30min的反应条件不变,起始时NO的浓度为2.50mol/L,则反应达平衡时c(NO)
=_________ mol/L。NO的转化率______ (填“增大”“减小”或“不变”)。
④下列说法中可以说明该反应已达到平衡状态的是_________ 。
a.体系内混合气体的密度保持不变 b.NO、N2、CO2、的物质的量之比为2∶1∶1
c.容器内气体的总压强保持不变 d. NO体积分数不再改变
(3)SO2在一定条件下可与氧气构成原电池。下图是利用该电池在铁表面镀铜的装置示意图:

①该电池的负极反应:____________________ ;
②当甲中消耗2.24LO2(标准状况)时,乙中________ (填“a”或“b”)增重________ g。
(1)已知热化学方程式:
①2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) △H1
②C(s)+ O2(g)=CO2(g) △H2
③H2(g)+
 O2(g)=H2O(l) △H3
O2(g)=H2O(l) △H3则反应④2C(s)+H2(g)=C2H2(g)的△H 为
(2)用活性炭还原法可以处理氮氧化物。某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO(g)
 N2+CO2(g) △H<0。在Tl℃时,反应进行到不同时间测得各物质的浓度(单位:mol/L)如下:
N2+CO2(g) △H<0。在Tl℃时,反应进行到不同时间测得各物质的浓度(单位:mol/L)如下:0 | 10 | 20 | 30 | 40 | 50 | |
NO | 1.00 | 0.68 | 0.50 | 0.50 | 0.60 | 0.60 |
N2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
CO2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
①10〜20min内,NO的平均反应速率v(NO)=
②30min后,只改变某-条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是
a.通入一定量的NO b.加入一定量的c
c.适当升高反应体系的温度 d.加入合适的催化剂
e.适当缩小容器的体积
③若保持与上述反应前30min的反应条件不变,起始时NO的浓度为2.50mol/L,则反应达平衡时c(NO)
=
④下列说法中可以说明该反应已达到平衡状态的是
a.体系内混合气体的密度保持不变 b.NO、N2、CO2、的物质的量之比为2∶1∶1
c.容器内气体的总压强保持不变 d. NO体积分数不再改变
(3)SO2在一定条件下可与氧气构成原电池。下图是利用该电池在铁表面镀铜的装置示意图:

①该电池的负极反应:
②当甲中消耗2.24LO2(标准状况)时,乙中
您最近一年使用:0次



