往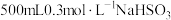 溶液中逐滴加入KIO3溶液,加入的KIO3和生成的I2的物质的量的关系曲线如图所示(不考虑物质与水发生的反应及弱电解质的电离)。
溶液中逐滴加入KIO3溶液,加入的KIO3和生成的I2的物质的量的关系曲线如图所示(不考虑物质与水发生的反应及弱电解质的电离)。
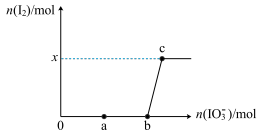
回答下列问题:
(1)NaHSO3在水中的电离方程式为___________ 。
(2)a点溶液的pH___________ (填“>”、“<”或“=”)7,判断的理由为___________ (用离子方程式表示)。
(3)b点溶液中所含的阳离子有___________ (填离子符号)。
(4)b→c的离子方程式为___________ 。
(5)往c点溶液中加入淀粉溶液,可以观察到的现象为___________ 。
(6)x=___________ 。
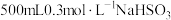 溶液中逐滴加入KIO3溶液,加入的KIO3和生成的I2的物质的量的关系曲线如图所示(不考虑物质与水发生的反应及弱电解质的电离)。
溶液中逐滴加入KIO3溶液,加入的KIO3和生成的I2的物质的量的关系曲线如图所示(不考虑物质与水发生的反应及弱电解质的电离)。
回答下列问题:
(1)NaHSO3在水中的电离方程式为
(2)a点溶液的pH
(3)b点溶液中所含的阳离子有
(4)b→c的离子方程式为
(5)往c点溶液中加入淀粉溶液,可以观察到的现象为
(6)x=
更新时间:2023/07/25 21:49:00
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】有下列物质:①Na2CO3·10H2O晶体 ②铜 ③硫酸溶液 ④CO2 ⑤NaHSO4固体 ⑥Ba(OH)2固体 ⑦红褐色的氢氧化铁胶体 ⑧氨水 ⑨蔗糖 ⑩Al2(SO4)3固体。
(1)上述物质属于电解质的有___________ (填编号,下同)。属于非电解质的是___________ 。
(2)17.1 g⑩溶于水配成 250 mL 溶液, SO 的物质的量浓度为
的物质的量浓度为___________ 。
(3)写出固体⑤溶于水中的电离方程式___________ 。
(4)胶体是一种常见的分散系,向煮沸的蒸馏水中逐滴加入几滴饱和的___________ (填化学式)溶液,继续煮沸至___________ ,停止加热,可制得Fe(OH)3胶体,制取Fe(OH)3胶体的化学方程式为___________ 。162.5 g FeCl3与沸水形成的Fe(OH)3胶体粒子数___________ NA(填“>”,“<”“=”)
(1)上述物质属于电解质的有
(2)17.1 g⑩溶于水配成 250 mL 溶液, SO
 的物质的量浓度为
的物质的量浓度为(3)写出固体⑤溶于水中的电离方程式
(4)胶体是一种常见的分散系,向煮沸的蒸馏水中逐滴加入几滴饱和的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】I.有以下物质:①石墨②铝③酒精④氨水⑤二氧化碳⑥碳酸钠固体⑦氢氧化钡溶液⑧纯醋酸⑨氧化钠固体⑩氯化氢气体⑪熔融氯化钠。
(1)其中能导电的是________ (填序号,下同);属于非电解质的是________ ;属于电解质的是________ 。
(2)写出物质⑥溶于水的电离方程式:__________
(3)写出物质⑥和⑩在水中反应的化学方程式:____________
II.(1)下列叙述正确的是________ 。
A.固体氯化钠不导电,所以氯化钠不是电解质
B.铜丝能导电,所以铜是电解质
C.氯化氢水溶液能导电,所以氯化氢是电解质
D.SO3 溶于水能导电,所以 SO3 是电解质
(2)关于酸、碱、盐的下列各种说法中,正确的是_______ 。
A.化合物电离时,生成的阳离子有氢离子的是酸
B.化合物电离时,生成的阴离子有氢氧根离子的是碱
C.化合物电离时,生成金属阳离子和酸根离子的是盐
D.NH4Cl电离的电离方程式是:NH4Cl=NH4++Cl-,所以NH4Cl不是盐
(1)其中能导电的是
(2)写出物质⑥溶于水的电离方程式:
(3)写出物质⑥和⑩在水中反应的化学方程式:
II.(1)下列叙述正确的是
A.固体氯化钠不导电,所以氯化钠不是电解质
B.铜丝能导电,所以铜是电解质
C.氯化氢水溶液能导电,所以氯化氢是电解质
D.SO3 溶于水能导电,所以 SO3 是电解质
(2)关于酸、碱、盐的下列各种说法中,正确的是
A.化合物电离时,生成的阳离子有氢离子的是酸
B.化合物电离时,生成的阴离子有氢氧根离子的是碱
C.化合物电离时,生成金属阳离子和酸根离子的是盐
D.NH4Cl电离的电离方程式是:NH4Cl=NH4++Cl-,所以NH4Cl不是盐
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】钠是一种非常活泼、具有广泛应用的金属。
(1)金属钠通常保存在_______ 里,以隔绝空气。
(2)已知用金属钠制取氧化钠,可有多种方法:
①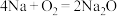 ;②
;② ;③
;③
在上述三种方法中最好的是_______ (填序号)。
(3)汽车安全气囊的气体发生剂 可由金属钠生产,某汽车安全气囊内含
可由金属钠生产,某汽车安全气囊内含 、
、 和
和 等物质。注:
等物质。注: 中钠为+1价。
中钠为+1价。
①当气体发生较严重的碰撞时,引发 分解的反应为
分解的反应为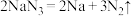 ,从而为气囊充气,用单线桥法标出该反应的电子转移方向和数目
,从而为气囊充气,用单线桥法标出该反应的电子转移方向和数目_______ 。
②产生的 立即与
立即与 发生置换反应生成
发生置换反应生成 ,化学方程式是
,化学方程式是_______ 。
③ 是冷却剂,能吸收上述过程释放的热量,并使自身分解。
是冷却剂,能吸收上述过程释放的热量,并使自身分解。 起冷却作用时,发生分解反应的化学方程式为
起冷却作用时,发生分解反应的化学方程式为_______ 。
(4)工业上通过电解 生产金属钠:
生产金属钠: ,过程如下:
,过程如下:
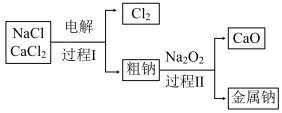
已知:电解时需要将 加热至熔融状态。
加热至熔融状态。 的熔点为
的熔点为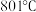 ,为降低能耗,通常加入
,为降低能耗,通常加入 把熔点降至约
把熔点降至约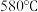 。
。
①把 固体加热至熔融状态,目的是
固体加热至熔融状态,目的是___ (用化学符号表示)。
②粗钠中含有少量杂质 ,过程II除去
,过程II除去 的化学方程式为
的化学方程式为___ 。(不必写反应条件)
(1)金属钠通常保存在
(2)已知用金属钠制取氧化钠,可有多种方法:
①
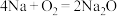 ;②
;② ;③
;③
在上述三种方法中最好的是
(3)汽车安全气囊的气体发生剂
 可由金属钠生产,某汽车安全气囊内含
可由金属钠生产,某汽车安全气囊内含 、
、 和
和 等物质。注:
等物质。注: 中钠为+1价。
中钠为+1价。①当气体发生较严重的碰撞时,引发
 分解的反应为
分解的反应为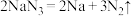 ,从而为气囊充气,用单线桥法标出该反应的电子转移方向和数目
,从而为气囊充气,用单线桥法标出该反应的电子转移方向和数目②产生的
 立即与
立即与 发生置换反应生成
发生置换反应生成 ,化学方程式是
,化学方程式是③
 是冷却剂,能吸收上述过程释放的热量,并使自身分解。
是冷却剂,能吸收上述过程释放的热量,并使自身分解。 起冷却作用时,发生分解反应的化学方程式为
起冷却作用时,发生分解反应的化学方程式为(4)工业上通过电解
 生产金属钠:
生产金属钠: ,过程如下:
,过程如下:
已知:电解时需要将
 加热至熔融状态。
加热至熔融状态。 的熔点为
的熔点为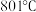 ,为降低能耗,通常加入
,为降低能耗,通常加入 把熔点降至约
把熔点降至约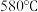 。
。①把
 固体加热至熔融状态,目的是
固体加热至熔融状态,目的是②粗钠中含有少量杂质
 ,过程II除去
,过程II除去 的化学方程式为
的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】有A、B、C、D四种化合物分别由K+、Ba2+、CO 、OH-、
、OH-、 中的两种组成。他们具有下列性质:①A不溶于水和盐酸:②B不溶于水但溶于盐酸并放出无色无味气体E:③C的水溶液呈碱性,与稀硫酸反应生成A;④D可溶于水,与稀硫酸作用时放出气体E,E可使澄清石灰水变浑浊。
中的两种组成。他们具有下列性质:①A不溶于水和盐酸:②B不溶于水但溶于盐酸并放出无色无味气体E:③C的水溶液呈碱性,与稀硫酸反应生成A;④D可溶于水,与稀硫酸作用时放出气体E,E可使澄清石灰水变浑浊。
(1)推断A、C的化学式:A___ ;C___ 。
(2)写出下列反应的离子方程式。
①D与氯化钙反应:___ 。
②B与盐酸反应:___ 。
③C与稀硫酸反应:___ 。
 、OH-、
、OH-、 中的两种组成。他们具有下列性质:①A不溶于水和盐酸:②B不溶于水但溶于盐酸并放出无色无味气体E:③C的水溶液呈碱性,与稀硫酸反应生成A;④D可溶于水,与稀硫酸作用时放出气体E,E可使澄清石灰水变浑浊。
中的两种组成。他们具有下列性质:①A不溶于水和盐酸:②B不溶于水但溶于盐酸并放出无色无味气体E:③C的水溶液呈碱性,与稀硫酸反应生成A;④D可溶于水,与稀硫酸作用时放出气体E,E可使澄清石灰水变浑浊。(1)推断A、C的化学式:A
(2)写出下列反应的离子方程式。
①D与氯化钙反应:
②B与盐酸反应:
③C与稀硫酸反应:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】下列反应的离子方程式正确的是__
①往硝酸银溶液中滴加少量氨水:Ag++2NH3=[Ag(NH3)2]+
②以石墨作电极电解氯化铝溶液:2Cl-+2H2O 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
③石灰石溶于醋酸:CaCO3+2CH3COOH=2CH3COO-+Ca2++CO2↑+H2O
④氯气与水反应:Cl2+H2O⇌2H++Cl-+ClO-
⑤Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-=2Fe2++I2
⑥浓烧碱溶液中加入铝片:Al+2OH-= +H2↑
+H2↑
⑦等物质的量的Ba(OH)2与NH4HSO4在稀溶液中反应:Ba2++2OH-+H++ +
+ =BaSO4↓+NH3·H2O+H2O
=BaSO4↓+NH3·H2O+H2O
⑧Na2S溶液呈碱性:S2-+2H2O⇌H2S+2OH-
⑨过量的SO2通入NaOH溶液中:SO2+2OH-= +H2O
+H2O
⑩NaNO2溶液中加入酸性KMnO4溶液:2 +5
+5 +6H+=2Mn2++5
+6H+=2Mn2++5 +3H2O
+3H2O
①往硝酸银溶液中滴加少量氨水:Ag++2NH3=[Ag(NH3)2]+
②以石墨作电极电解氯化铝溶液:2Cl-+2H2O
 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑③石灰石溶于醋酸:CaCO3+2CH3COOH=2CH3COO-+Ca2++CO2↑+H2O
④氯气与水反应:Cl2+H2O⇌2H++Cl-+ClO-
⑤Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-=2Fe2++I2
⑥浓烧碱溶液中加入铝片:Al+2OH-=
 +H2↑
+H2↑⑦等物质的量的Ba(OH)2与NH4HSO4在稀溶液中反应:Ba2++2OH-+H++
 +
+ =BaSO4↓+NH3·H2O+H2O
=BaSO4↓+NH3·H2O+H2O⑧Na2S溶液呈碱性:S2-+2H2O⇌H2S+2OH-
⑨过量的SO2通入NaOH溶液中:SO2+2OH-=
 +H2O
+H2O⑩NaNO2溶液中加入酸性KMnO4溶液:2
 +5
+5 +6H+=2Mn2++5
+6H+=2Mn2++5 +3H2O
+3H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】现有下列几种常见物质:①CH3Cl、②O3、③P4、④C60、⑤CO2、⑥HCN、⑦H2O、⑧NH3、⑨BF3、⑩CH4。
(1)这几种物质中,含非极性共价键形成的是______________ (填序号,下同);属于非极性分子的是_______________ 。
(2)属于极性键形成的非极性分子是_______________ ;
(3)将 溶于水,破坏
溶于水,破坏 中的
中的_______________ 键,写出其电离方程式_______________ 。
(4)已知铁的电离能数据如下:
则,铁的第四电离能( )大于第三电离能(
)大于第三电离能( )的可能原因是:
)的可能原因是:_______________ 。
(1)这几种物质中,含非极性共价键形成的是
(2)属于极性键形成的非极性分子是
(3)将
 溶于水,破坏
溶于水,破坏 中的
中的(4)已知铁的电离能数据如下:
电离能/( |
|
|
|
| …… |
Fe | 759 | 1561 | 2597 | 5290 | …… |
 )大于第三电离能(
)大于第三电离能( )的可能原因是:
)的可能原因是:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】Fe2O3/Al2O3负载型催化剂(其中Fe2O3为催化剂,Al2O3为载体)可用于脱除烟气中的SO2,该负载型催化剂的制备和SO2的脱除过程如下:
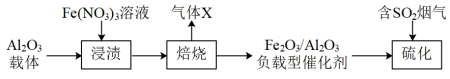
(1)浸渍。常温下,用Fe(NO3)3酸性溶液浸渍Al2O3载体6h。浸渍所得溶液中除Fe3+外,含有的阳离子还有_______ (填化学式)。
(2)焙烧。将浸渍所得混合物烘干后,在500℃焙烧12h,制得Fe2O3/Al2O3负载型催化剂。准确称取2.000g负载型催化剂样品,置于250mL锥形瓶中,加入适量稀盐酸,加热溶解后,滴加稍过量的SnCl2溶液(Sn2+将Fe3+还原为Fe2+),充分反应后,除去过量的Sn2+。用5.000×10-2mol·L-1K2C2O7溶液滴定至终点(滴定过程中Cr2O 与Fe2+反应生成Cr3+和Fe3+),消耗K2Cr2O7溶液12.00mL。计算该Fe2O3/Al2O3负载型催化剂的负载量
与Fe2+反应生成Cr3+和Fe3+),消耗K2Cr2O7溶液12.00mL。计算该Fe2O3/Al2O3负载型催化剂的负载量_______ (写出计算过程)。[负载量= 100%]
100%]
(3)硫化。400℃时,将一定比例SO2和H2的混合气体以一定流速通过装有Fe2O3/Al2O3负载型催化剂的反应器。
①硫化过程不仅可有效脱除SO2,同时还获得单质S,其化学方程式为_______ 。
②研究表明,硫化过程中实际起催化作用的是反应初期生成的FeS2,硫化过程中还检测到H2S。FeS2催化硫化的过程可描述如下:_______ ,最后S再与FeS反应转化为FeS2。

(1)浸渍。常温下,用Fe(NO3)3酸性溶液浸渍Al2O3载体6h。浸渍所得溶液中除Fe3+外,含有的阳离子还有
(2)焙烧。将浸渍所得混合物烘干后,在500℃焙烧12h,制得Fe2O3/Al2O3负载型催化剂。准确称取2.000g负载型催化剂样品,置于250mL锥形瓶中,加入适量稀盐酸,加热溶解后,滴加稍过量的SnCl2溶液(Sn2+将Fe3+还原为Fe2+),充分反应后,除去过量的Sn2+。用5.000×10-2mol·L-1K2C2O7溶液滴定至终点(滴定过程中Cr2O
 与Fe2+反应生成Cr3+和Fe3+),消耗K2Cr2O7溶液12.00mL。计算该Fe2O3/Al2O3负载型催化剂的负载量
与Fe2+反应生成Cr3+和Fe3+),消耗K2Cr2O7溶液12.00mL。计算该Fe2O3/Al2O3负载型催化剂的负载量 100%]
100%](3)硫化。400℃时,将一定比例SO2和H2的混合气体以一定流速通过装有Fe2O3/Al2O3负载型催化剂的反应器。
①硫化过程不仅可有效脱除SO2,同时还获得单质S,其化学方程式为
②研究表明,硫化过程中实际起催化作用的是反应初期生成的FeS2,硫化过程中还检测到H2S。FeS2催化硫化的过程可描述如下:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】下图是依据一定的分类标准,对某些物质与水反应情况进行分类的分类图。请根据你所学的知识,按要求填空:
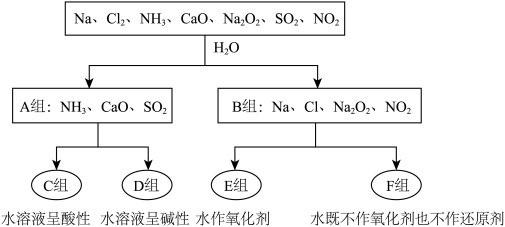
(1)根据物质与水反应的情况,分成A、B组的分类依据是________ 。
(2)A组中的CaO经常用作食品包装袋中的干燥剂,CaO所属的物质类别为________ (填序号)。
①金属氧化物②酸性氧化物③碱性氧化物④两性氧化物
(3)D组中的气体水溶液呈弱碱性,用电离方程式表示其水溶液呈弱碱性的原因:________ 。
(4)F组中与水反应,氧化剂与还原剂的物质的量之比为1∶1的物质是________ 。(填化学式)。
(5)过量的铁粉与Cl2共热时发生反应的化学方程式为____________________ 。

(1)根据物质与水反应的情况,分成A、B组的分类依据是
(2)A组中的CaO经常用作食品包装袋中的干燥剂,CaO所属的物质类别为
①金属氧化物②酸性氧化物③碱性氧化物④两性氧化物
(3)D组中的气体水溶液呈弱碱性,用电离方程式表示其水溶液呈弱碱性的原因:
(4)F组中与水反应,氧化剂与还原剂的物质的量之比为1∶1的物质是
(5)过量的铁粉与Cl2共热时发生反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】近年来我国航天事业飞速发展,请回答下列问题:
(1)嫦娥五号返回器携带月壤着陆,月壤含有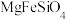 ,请用氧化物表示该物质
,请用氧化物表示该物质_______ 。
(2)铜与浓硫酸共热反应的化学方程式___________ 。
(3)神舟十二号全面使用国产芯片,其中制作芯片刻蚀液为硝酸与氢氟酸的混合溶液,其工艺涉及的反应为: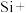
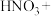
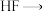



①配平上述方程式,并在方程式上面用“双线桥”标明电子转移的方向和数目___________ ;
②该反应中 表现的性质:
表现的性质:_______ ,氧化剂与还原剂的物质的量之比为:_______ ;
③反应中转移0.3mol电子时生成标准状况下的NO_______ L,将生成的NO完全转化为 需要
需要 的物质的量为:
的物质的量为:_____ 。
(1)嫦娥五号返回器携带月壤着陆,月壤含有
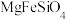 ,请用氧化物表示该物质
,请用氧化物表示该物质(2)铜与浓硫酸共热反应的化学方程式
(3)神舟十二号全面使用国产芯片,其中制作芯片刻蚀液为硝酸与氢氟酸的混合溶液,其工艺涉及的反应为:
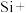
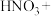
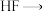



①配平上述方程式,并在方程式上面用“双线桥”标明电子转移的方向和数目
②该反应中
 表现的性质:
表现的性质:③反应中转移0.3mol电子时生成标准状况下的NO
 需要
需要 的物质的量为:
的物质的量为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】为消除燃煤烟气中含有的SO2、NOx,研究者提出若干烟气“脱硫”、“脱硝”的方法。
(1)下列物质中,能吸收SO2的有___________ (填序号)。
a.氨水 b.酸性KMnO4溶液 c.BaCl2溶液 d.Na2CO3溶液
(2)向燃煤中加入适量石灰石,高温时将SO2转化为CaSO4的化学方程式是___________ 。
(3)选择性催化还原法(SCR)“脱硝”。在催化剂的作用下,选取还原剂将烟气中的NO进行无害化处理。NH3还原NO的化学方程式是___________ 。
(4)以NaClO溶液作为吸收剂进行一体化“脱硫”、“脱硝”。控制溶液的pH=5.5,将烟气中的SO2、NO转化为SO 、NO
、NO ,均为放热反应。
,均为放热反应。
①NaClO溶液吸收烟气中SO2的离子方程式是___________ 。
②一定时间内,温度对硫、硝脱除率的影响曲线如下图,SO2的脱除率高于NO,可能的原因是___________ (写出1种即可)。 和Cl−的物质的量之比为
和Cl−的物质的量之比为___________ 。
(1)下列物质中,能吸收SO2的有
a.氨水 b.酸性KMnO4溶液 c.BaCl2溶液 d.Na2CO3溶液
(2)向燃煤中加入适量石灰石,高温时将SO2转化为CaSO4的化学方程式是
(3)选择性催化还原法(SCR)“脱硝”。在催化剂的作用下,选取还原剂将烟气中的NO进行无害化处理。NH3还原NO的化学方程式是
(4)以NaClO溶液作为吸收剂进行一体化“脱硫”、“脱硝”。控制溶液的pH=5.5,将烟气中的SO2、NO转化为SO
 、NO
、NO ,均为放热反应。
,均为放热反应。①NaClO溶液吸收烟气中SO2的离子方程式是
②一定时间内,温度对硫、硝脱除率的影响曲线如下图,SO2的脱除率高于NO,可能的原因是
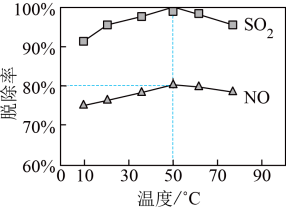
 和Cl−的物质的量之比为
和Cl−的物质的量之比为
您最近一年使用:0次
【推荐2】向27.2gCu和 的混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成
的混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成 和
和 ,在所得溶液中加入
,在所得溶液中加入 的
的 溶液1.0L,此时溶液显中性,金属离子已完全沉淀,沉淀质量为39.2g。求(写出计算过程):
溶液1.0L,此时溶液显中性,金属离子已完全沉淀,沉淀质量为39.2g。求(写出计算过程):
(1)原固体混合物中Cu和 的物质的量之比为
的物质的量之比为___________ ;
(2)产生的 在标准状况下的体积是
在标准状况下的体积是___________ L;
(3)硝酸的物质的量浓度是___________  。
。
 的混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成
的混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成 和
和 ,在所得溶液中加入
,在所得溶液中加入 的
的 溶液1.0L,此时溶液显中性,金属离子已完全沉淀,沉淀质量为39.2g。求(写出计算过程):
溶液1.0L,此时溶液显中性,金属离子已完全沉淀,沉淀质量为39.2g。求(写出计算过程):(1)原固体混合物中Cu和
 的物质的量之比为
的物质的量之比为(2)产生的
 在标准状况下的体积是
在标准状况下的体积是(3)硝酸的物质的量浓度是
 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】元素化合物在日常生活、化工生产和环境科学中有着重要的用途。
(1)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸后溶液中大量存在的阳离子是______________ 。
(2)自然界中Cr主要以+3价和+6价形式存在。Cr2O72-中的Cr能引起细胞的突变,可以用亚硫酸钠在酸性条件下将Cr2O72-还原。写出反应的离子方程式:____________ 。
(3)当皮肤划破时可用FeCl3溶液应急止血,其主要原因是_________________ 。 用氯化铁固体配制成 98mL 0.1mol/L 的溶液,配制过程中所需要的玻璃仪器有量筒、玻璃棒、烧杯、胶头滴管、__________________________ 。
(4)高铁酸钾(K2FeO4)是一种既能杀菌、消毒、又能絮凝净水的水处理剂。工业制备高铁酸钾的反应离子方程式Fe(OH)3+ C1O-+ OH-→ FeO42-+ C1-+ H2O(未配平),配平后的离子方程式为:________________________________ ,每生成1mol K2FeO4, 转移的电子数是_________ 。
(1)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸后溶液中大量存在的阳离子是
(2)自然界中Cr主要以+3价和+6价形式存在。Cr2O72-中的Cr能引起细胞的突变,可以用亚硫酸钠在酸性条件下将Cr2O72-还原。写出反应的离子方程式:
(3)当皮肤划破时可用FeCl3溶液应急止血,其主要原因是
(4)高铁酸钾(K2FeO4)是一种既能杀菌、消毒、又能絮凝净水的水处理剂。工业制备高铁酸钾的反应离子方程式Fe(OH)3+ C1O-+ OH-→ FeO42-+ C1-+ H2O(未配平),配平后的离子方程式为:
您最近一年使用:0次

 )
)



