微量实验具有用量少,污染小,操作简单,现象明显等特点,硬质玻璃管可用于气体微量实验的场所。如图所示,将浓硫酸滴入培养皿后,会产生一种无色的气体。一段时间后,a、b、c、d四个棉球都褪为白色 。
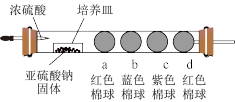
(1)a棉球变白后,微热该处一段时间,棉球又恢复红色,则a棉球上滴有的溶液为_______ 。
(2)b棉球上滴有的溶液为___________ 。发生反应的化学方程式为___________ 。
(3)c棉球上滴有酸性高锰酸钾溶液,它变为白色原因与___________ (填“a”、或“b”)棉球相同,说明无色气体具有___________ 性。
(4)d棉球上滴有NaOH溶液(混有酚酞),棉球变为白色说明无色气体溶于水显_______ 性。
(5)装置末端通入充满硫化氢溶液中,现象是___________ ,反应的化学反应方程式为___________ 。说明无色气体具有___________ 性。

(1)a棉球变白后,微热该处一段时间,棉球又恢复红色,则a棉球上滴有的溶液为
(2)b棉球上滴有的溶液为
(3)c棉球上滴有酸性高锰酸钾溶液,它变为白色原因与
(4)d棉球上滴有NaOH溶液(混有酚酞),棉球变为白色说明无色气体溶于水显
(5)装置末端通入充满硫化氢溶液中,现象是
更新时间:2023-06-21 08:17:54
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】 是一种性质非常活泼的氧化物,能与许多物质反应并表现出不同的化学性质,某同学利用如图所示装置制取
是一种性质非常活泼的氧化物,能与许多物质反应并表现出不同的化学性质,某同学利用如图所示装置制取 并探究其性质。
并探究其性质。

相关试剂瓶中的试剂如下表:
(1)装置A中反应的化学方程式为_______ 。
(2)X是有色溶液,反应后溶液褪色。若X是溴水,相应反应的离子方程式为_______ ;若装置C中的现象能表明 有漂白性,则X是
有漂白性,则X是_______ (填序号)。
A.KMnO4溶液 B.品红溶液 C.氯水 D.FeCl3溶液
(3)装置D中没有沉淀生成而装置E中有乳白色沉淀生成,则装置D中没有沉淀生成的原因是_______ ,装置E中生成淡黄色沉淀的同时生成了一种强碱,则该反应的化学方程式为_______ 。
(4)装置F中 溶液的作用是
溶液的作用是_______ 。
 是一种性质非常活泼的氧化物,能与许多物质反应并表现出不同的化学性质,某同学利用如图所示装置制取
是一种性质非常活泼的氧化物,能与许多物质反应并表现出不同的化学性质,某同学利用如图所示装置制取 并探究其性质。
并探究其性质。
相关试剂瓶中的试剂如下表:
| B | C | D | E | F | |
| 试剂 | 石蕊试液 | X |  溶液 溶液 |  溶液 溶液 |  溶液 溶液 |
(2)X是有色溶液,反应后溶液褪色。若X是溴水,相应反应的离子方程式为
 有漂白性,则X是
有漂白性,则X是A.KMnO4溶液 B.品红溶液 C.氯水 D.FeCl3溶液
(3)装置D中没有沉淀生成而装置E中有乳白色沉淀生成,则装置D中没有沉淀生成的原因是
(4)装置F中
 溶液的作用是
溶液的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】非金属元素硫在化工生产中扮演重要角色,实验室制备及探究某些含硫化合物。
Ⅰ.利用 和
和 反应合成硫酰氯
反应合成硫酰氯 ,已知
,已知 的熔点为
的熔点为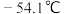 ,沸点为69.1℃,在空气中遇水蒸气发生剧烈反应,并产生大量HCl白雾,100℃以上分解生成
,沸点为69.1℃,在空气中遇水蒸气发生剧烈反应,并产生大量HCl白雾,100℃以上分解生成 和
和 。实验室合成
。实验室合成 的原理:
的原理: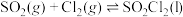 ,且反应会放出大量的热。实验装置如图所示(夹持仪器已省略),请回答下列问题:
,且反应会放出大量的热。实验装置如图所示(夹持仪器已省略),请回答下列问题:_____ 。
(2)装置戊上方分液漏斗中最好选用_____ (填字母)。
a.蒸馏水 b.饱和食盐水 c. 盐酸 d.浓氢氧化钠溶液
盐酸 d.浓氢氧化钠溶液
(3)装置乙和丁盛放的试剂均是浓硫酸,其作用是_____ 。
(4)装置丙放置在冰水浴中的原因是_____ 。
Ⅱ.探究 使品红溶液褪色的原因
使品红溶液褪色的原因
操作1:将 通入品红溶液中,品红溶液褪色。
通入品红溶液中,品红溶液褪色。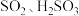 、
、_____ 。
已知:品红是一种棕红色晶体状有机染料,微溶于水,溶于乙醇和酸,溶液呈红色。
②实验设计:小组结合以上信息,设计如下实验证明使品红褪色的微粒不是 请完成表格。
请完成表格。
Ⅰ.利用
 和
和 反应合成硫酰氯
反应合成硫酰氯 ,已知
,已知 的熔点为
的熔点为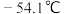 ,沸点为69.1℃,在空气中遇水蒸气发生剧烈反应,并产生大量HCl白雾,100℃以上分解生成
,沸点为69.1℃,在空气中遇水蒸气发生剧烈反应,并产生大量HCl白雾,100℃以上分解生成 和
和 。实验室合成
。实验室合成 的原理:
的原理: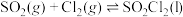 ,且反应会放出大量的热。实验装置如图所示(夹持仪器已省略),请回答下列问题:
,且反应会放出大量的热。实验装置如图所示(夹持仪器已省略),请回答下列问题: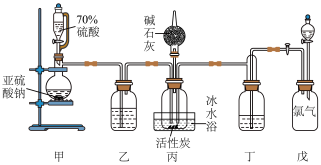
(2)装置戊上方分液漏斗中最好选用
a.蒸馏水 b.饱和食盐水 c.
 盐酸 d.浓氢氧化钠溶液
盐酸 d.浓氢氧化钠溶液(3)装置乙和丁盛放的试剂均是浓硫酸,其作用是
(4)装置丙放置在冰水浴中的原因是
Ⅱ.探究
 使品红溶液褪色的原因
使品红溶液褪色的原因操作1:将
 通入品红溶液中,品红溶液褪色。
通入品红溶液中,品红溶液褪色。
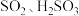 、
、已知:品红是一种棕红色晶体状有机染料,微溶于水,溶于乙醇和酸,溶液呈红色。
②实验设计:小组结合以上信息,设计如下实验证明使品红褪色的微粒不是
 请完成表格。
请完成表格。| 操作2 | 现象 |
| 不褪色 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某学习小组设计实验,探究二氧化硫的漂白性和还原性。
(1)漂白性
甲同学用如图所示装置(气密性良好)进行实验,观察到如下现象:Ⅰ中红色褪去,Ⅱ中无变化。

①甲同学作对照实验的目的是______________________________________ 。
②足量碱石灰的作用是__________________________________________ 。
甲同学由此得出的实验结论是___________________________________________ 。
(2)还原性:
乙同学将SO2通入FeCl3溶液中,使其充分反应。
①SO2与FeCl3反应的离子方程式是_________ ,检验该反应所得含氧酸根离子的方法是______ 。
②实验中观察到溶液由黄色变为红棕色,静置一段时间,变为浅绿色。资料显示:红棕色为FeSO3 (墨绿色难溶物)与FeCl3溶液形成的混合色。 则②中红棕色变为浅绿色的原因是__________________ 。
乙同学得出的实验结论是:二氧化硫可还原三氯化铁。
(1)漂白性
甲同学用如图所示装置(气密性良好)进行实验,观察到如下现象:Ⅰ中红色褪去,Ⅱ中无变化。

①甲同学作对照实验的目的是
②足量碱石灰的作用是
甲同学由此得出的实验结论是
(2)还原性:
乙同学将SO2通入FeCl3溶液中,使其充分反应。
①SO2与FeCl3反应的离子方程式是
②实验中观察到溶液由黄色变为红棕色,静置一段时间,变为浅绿色。资料显示:红棕色为FeSO3 (墨绿色难溶物)与FeCl3溶液形成的混合色。 则②中红棕色变为浅绿色的原因是
乙同学得出的实验结论是:二氧化硫可还原三氯化铁。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某化学兴趣小组为探究SO2的性质,按图所示装置进行实验。(已知:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O)
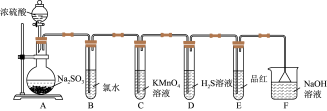
请回答下列问题:
(1)装置A中盛放浓硫酸和亚硫酸钠的仪器名称分别是____________ 、_____________ 。
(2)装置B中的现象是___________________________ 。
(3)装置C中的现象是_____________ ,表现了SO2的_________ (填氧化性或还原性)。
(4)装置D中的现象是_______________ ,表现了SO2的_________ (填氧化性或还原性)。
(5)装置E的现象是_______________ ,表现了SO2具有___________ 性。
(6)装置F的作用是__________________ ,漏斗的作用是____________________ 。

请回答下列问题:
(1)装置A中盛放浓硫酸和亚硫酸钠的仪器名称分别是
(2)装置B中的现象是
(3)装置C中的现象是
(4)装置D中的现象是
(5)装置E的现象是
(6)装置F的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某研究小组用如图装置进行SO2与FeCl3溶液反应的相关实验(夹持装置已略去)。
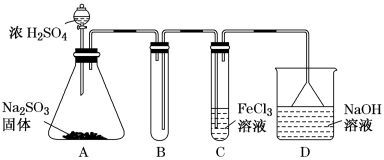
(1)A中的化学方程式为_______________________________________ 。
(2)通入足量SO2时C中观察到的现象为________________________________ 。
(3)根据以上现象,该小组同学认为SO2与FeCl3溶液发生氧化还原反应。
①写出SO2与FeCl3溶液反应的离子_________________________________ 。
②请设计实验方案检验有Fe2+生成__________________________________ 。
③该小组同学向C试管反应后的溶液中加入硝酸酸化的BaCl2溶液,若出现白色沉淀,即可证明反应生成了SO42-。该做法_______ (填“合理”或“不合理”),理由是___________ 。
(4)D装置中倒置漏斗的作用是__________ 。
(5)为了验证SO2具有还原性,实验中可以代替FeCl3的试剂有________ 。
a.浓硫酸 b.酸性KMnO4溶液 c.碘水 d.NaCl溶液

(1)A中的化学方程式为
(2)通入足量SO2时C中观察到的现象为
(3)根据以上现象,该小组同学认为SO2与FeCl3溶液发生氧化还原反应。
①写出SO2与FeCl3溶液反应的离子
②请设计实验方案检验有Fe2+生成
③该小组同学向C试管反应后的溶液中加入硝酸酸化的BaCl2溶液,若出现白色沉淀,即可证明反应生成了SO42-。该做法
(4)D装置中倒置漏斗的作用是
(5)为了验证SO2具有还原性,实验中可以代替FeCl3的试剂有
a.浓硫酸 b.酸性KMnO4溶液 c.碘水 d.NaCl溶液
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】黄铁矿(FeS2)是一种重要的含硫矿物,可用于制备硫酸和冶炼金属铁。利用黄铁矿可生产硫酸,其流程如图所示:____ 。
(2)炉渣经稀硫酸溶解后,过滤,可得黄色的溶液,若将炉气通入溶液中,可发现黄色溶液变为浅绿色,而后又变成黄色,其可能的原因为____ 、____ 。(用离子方程式表示)
(3)含有Fe2+、Fe3+的硫酸盐混合溶液可用于回收硫单质,其转化关系如图所示。其中反应①中作氧化剂的是____ (填离子符号或化学式),该图示中总反应的化学方程式为____ 。____ ;净化除尘后的气体中SO2含量(体积分数)的计算式是____ (用含V、b的代数式表示)。
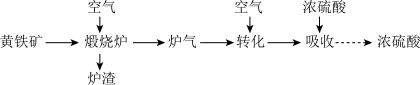
(2)炉渣经稀硫酸溶解后,过滤,可得黄色的溶液,若将炉气通入溶液中,可发现黄色溶液变为浅绿色,而后又变成黄色,其可能的原因为
(3)含有Fe2+、Fe3+的硫酸盐混合溶液可用于回收硫单质,其转化关系如图所示。其中反应①中作氧化剂的是

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】浩瀚的海洋里蕴藏着丰富的化学资源,从海带中提取碘单质和从海水中提取溴单质的工艺流程如图。回答下列问题:
I.海带提碘
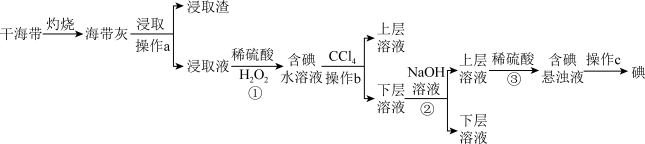
(1)在实验室进行干海带的灼烧操作时,是将海带放入___________ (填仪器名称)中,用酒精灯充分加热灰化。
(2)浸取液中碘主要以 存在,写出①发生反应的离子方程式
存在,写出①发生反应的离子方程式___________ ,实验步骤①后若检验溶液中碘单质的存在,具体方法是___________ 。
(3)向含有 的水溶液中加入
的水溶液中加入 振荡静置后的实验现象
振荡静置后的实验现象___________ 。
(4)步骤②中加入浓 溶液发生反应的化学方程式为
溶液发生反应的化学方程式为___________ ,步骤③反应中氧化剂与还原剂物质的量之比为___________ 。
(5)步骤②③是利用化学转化法将富集在四氯化碳中的碘单质重新富集在水中,该方法称为___________ 法。
(6)操作c的名称为___________ 。
Ⅱ.海水提溴
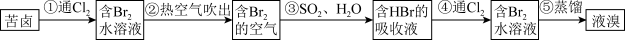
(7)流程中能说明同主族元素性质递变规律的反应为___________ (写出离子方程式)。
(8)步骤③化学方程式为___________ 。
I.海带提碘

(1)在实验室进行干海带的灼烧操作时,是将海带放入
(2)浸取液中碘主要以
 存在,写出①发生反应的离子方程式
存在,写出①发生反应的离子方程式(3)向含有
 的水溶液中加入
的水溶液中加入 振荡静置后的实验现象
振荡静置后的实验现象(4)步骤②中加入浓
 溶液发生反应的化学方程式为
溶液发生反应的化学方程式为(5)步骤②③是利用化学转化法将富集在四氯化碳中的碘单质重新富集在水中,该方法称为
(6)操作c的名称为
Ⅱ.海水提溴
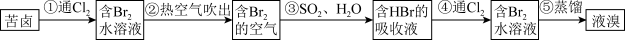
(7)流程中能说明同主族元素性质递变规律的反应为
(8)步骤③化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】X、Y、Z、M、G五种主族元素分属三个短周期,且原子序数依次增大。X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子。
(1)Y在元素周期表中的位置为______ 。
(2)上述元素的最高价氧化物对应的水化物酸性最强的是_______ (写化学式),非金属气态氢化物还原性最强的是______ (写化学式)。
(3)X、Y、Z、M组成两种盐的溶液反应可产生MY2气体,写出其反应离子方程式:_______ 。
(4)M的氧化物与G的单质的水溶液均有漂白性,相同条件下,同体积M的氧化物与G单质混合通入品红溶液,品红溶液____ (填褪色或不褪色)。
(5)Y的氢化物沸点比硒化氢(H2Se)的沸点高,其原因是_________ 。
(1)Y在元素周期表中的位置为
(2)上述元素的最高价氧化物对应的水化物酸性最强的是
(3)X、Y、Z、M组成两种盐的溶液反应可产生MY2气体,写出其反应离子方程式:
(4)M的氧化物与G的单质的水溶液均有漂白性,相同条件下,同体积M的氧化物与G单质混合通入品红溶液,品红溶液
(5)Y的氢化物沸点比硒化氢(H2Se)的沸点高,其原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某化学兴趣小组在实验室用除去表面氧化物的铁钉(碳素钢)与浓硫酸共热制取SO2并完成相关性质探究(不考虑水蒸气)。(已知:C+2H2SO4(浓) CO2+2SO2↑+2H2O)
CO2+2SO2↑+2H2O)
(1)有同学认为制得的SO2中可能混有杂质,其化学式为_________ 。
为验证气体成分,兴趣小组同学设计了如图所示装置进行了实验探究。_________ ;装置C中品红溶液的作用是_________ 。
(3)装置H的作用为_________ 。
兴趣小组设计如图装置验证二氧化硫的化学性质。___________ ;
为验证SO2的还原性,取试管b中充分反应后的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液加入品红溶液,红色褪去;
方案Ⅱ:向第二份溶液加入BaCl2溶液,产生白色沉淀;
方案Ⅲ:向第三份溶液中加入AgNO3溶液,有白色沉淀生成。
(5)上述方案中合理的是___________ (填Ⅰ、Ⅱ或Ⅲ);试管b中发生反应的离子方程式为___________ 。
(6)如果用硫酸溶液和 固体反应制取
固体反应制取 装置如图所示。其中
装置如图所示。其中 导管的作用是
导管的作用是________ 。 含量(假设空气中无其他还原性气体)。
含量(假设空气中无其他还原性气体)。 (标准状况下),最终所得固体质量为
(标准状况下),最终所得固体质量为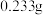 ,通过计算确定该空气中二氧化硫的含量是
,通过计算确定该空气中二氧化硫的含量是________ 。(结果精确到 )
)
 CO2+2SO2↑+2H2O)
CO2+2SO2↑+2H2O)(1)有同学认为制得的SO2中可能混有杂质,其化学式为
为验证气体成分,兴趣小组同学设计了如图所示装置进行了实验探究。
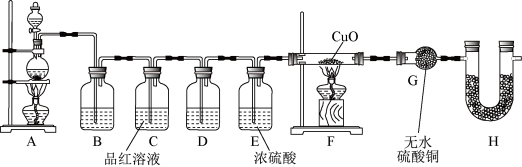
(3)装置H的作用为
兴趣小组设计如图装置验证二氧化硫的化学性质。

为验证SO2的还原性,取试管b中充分反应后的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液加入品红溶液,红色褪去;
方案Ⅱ:向第二份溶液加入BaCl2溶液,产生白色沉淀;
方案Ⅲ:向第三份溶液中加入AgNO3溶液,有白色沉淀生成。
(5)上述方案中合理的是
(6)如果用硫酸溶液和
 固体反应制取
固体反应制取 装置如图所示。其中
装置如图所示。其中 导管的作用是
导管的作用是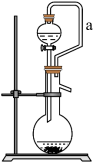
 含量(假设空气中无其他还原性气体)。
含量(假设空气中无其他还原性气体)。
 (标准状况下),最终所得固体质量为
(标准状况下),最终所得固体质量为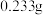 ,通过计算确定该空气中二氧化硫的含量是
,通过计算确定该空气中二氧化硫的含量是 )
)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】氨基甲酸铵(NH2COONH4)是一种白色固体,可由两种常见气体制取,其易分解、易水解,可用于医药、氨化剂等。某科研小组利用以下装置制备氨基甲酸铵。回答下列问题:

(1)写出a中的固体药品的名称________ ,制取氨气的原理为___________ (结合化学方程式并用简要的文字加以说明)。
(2)恒压滴液漏斗的作用是________ 。
(3)有同学建议该CO2发生装置直接改用如下装置代替,你认为他的改进有何优点(试述一种):________ 。
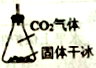
(4)反应器C中发生反应的化学方程式为________ 。
(5) 双通玻璃管的作用________ ;b中溶液的作用________ 。
(6)上述制得的氨基甲酸铵可能含有碳酸氢铵、碳酸铵中的一种或两种。
①设计方案,进行成分探究,请填写表中空格。
限选试剂: 蒸馏水、稀HNO3、BaCl2溶液、Ba(OH)2溶液、AgNO3溶液、稀盐酸。
实验步骤
预期现象和结论
步骤1: 取少量固体样品于试管中,加入蒸馏水至固体溶解。
得到无色溶液
步骤2: 向试管中加入过量的BaCl2溶液,静置。
溶液不变浑浊,则证明固体中不含有________ 。
步骤3: 取步骤2的上层清液于试管中加入少量 的______ 。
溶液变浑浊,则证明固体中含有_______ 。
②根据①的结论: 取氨基甲酸铵样品15.80g,用上题步骤经充分处理后,过滤、洗涤、干燥,测得沉淀质量为5.91g 。则样品中氨基甲酸铵的质量分数为________ 。

(1)写出a中的固体药品的名称
(2)恒压滴液漏斗的作用是
(3)有同学建议该CO2发生装置直接改用如下装置代替,你认为他的改进有何优点(试述一种):

(4)反应器C中发生反应的化学方程式为
(5) 双通玻璃管的作用
(6)上述制得的氨基甲酸铵可能含有碳酸氢铵、碳酸铵中的一种或两种。
①设计方案,进行成分探究,请填写表中空格。
限选试剂: 蒸馏水、稀HNO3、BaCl2溶液、Ba(OH)2溶液、AgNO3溶液、稀盐酸。
实验步骤
预期现象和结论
步骤1: 取少量固体样品于试管中,加入蒸馏水至固体溶解。
得到无色溶液
步骤2: 向试管中加入过量的BaCl2溶液,静置。
溶液不变浑浊,则证明固体中不含有
步骤3: 取步骤2的上层清液于试管中加入少量 的
溶液变浑浊,则证明固体中含有
②根据①的结论: 取氨基甲酸铵样品15.80g,用上题步骤经充分处理后,过滤、洗涤、干燥,测得沉淀质量为5.91g 。则样品中氨基甲酸铵的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某探究性学习小组同学进行“铁与水蒸气反应所得固体物质的成分、性质及再利用”实验探究,请你参与其中。
探究一:用如图所示装置进行“铁与水蒸气反应”的实验.(夹持仪器已省略)

(1)硬质玻璃管B中发生反应的化学方程式为________________________ 。
(2)装置D的作用是________________________ 。
(3)装置E中可观察到的现象是____________________ 。
探究二:设计如下实验方案确定反应后硬质玻璃管B中黑色固体的成分。
(4)待硬质玻璃管B冷却后,取少许其中的固体继续进行下图实验。

①试剂a是________________ 。
②现象1为__________________ ,该过程涉及的离子反应方程式为__________________ 。
③若现象2中溶液未变红色,请从硬质玻璃管B中固体物质的成分分析可能的原因___________________ 。
【实验拓展】
(5)将铜片放入0.1 mol/LFeCl3溶液中,反应一定时间后取出铜片,溶液中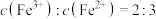 ,则反应后溶液中Cu2+与Fe3+的物质的量之比为
,则反应后溶液中Cu2+与Fe3+的物质的量之比为___________ 。
探究一:用如图所示装置进行“铁与水蒸气反应”的实验.(夹持仪器已省略)

(1)硬质玻璃管B中发生反应的化学方程式为
(2)装置D的作用是
(3)装置E中可观察到的现象是
探究二:设计如下实验方案确定反应后硬质玻璃管B中黑色固体的成分。
(4)待硬质玻璃管B冷却后,取少许其中的固体继续进行下图实验。

①试剂a是
②现象1为
③若现象2中溶液未变红色,请从硬质玻璃管B中固体物质的成分分析可能的原因
【实验拓展】
(5)将铜片放入0.1 mol/LFeCl3溶液中,反应一定时间后取出铜片,溶液中
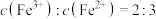 ,则反应后溶液中Cu2+与Fe3+的物质的量之比为
,则反应后溶液中Cu2+与Fe3+的物质的量之比为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某同学在研究元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验方案”与“实验现象”前后不一定是对应关系)。
请你帮助该同学整理并完成实验报告。
(1)实验目的:研究__________________ 元素性质递变规律。
(2)实验用品:试剂:金属钠、镁条、铝条、稀盐酸、新制氯水、新制Na2S溶液、AlCl3溶液、NaOH溶液、酚酞溶液等。
仪器:______ 、______ 、滤纸、试管夹、胶头滴管、镊子、小刀、玻璃片、砂纸、火柴等。
(3)实验内容:(填写与实验步骤对应的实验现象的编号和①②的化学方程式及此实验的结论)
①___________________________________________________ ;
②___________________________________________________ ;
此实验的结论:__________________________________________________ 。
| 实验步骤 | 实验现象 |
| ①将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色 |
| ②向新制的Na2S溶液中滴加新制的氯水 | B.有气体产生,溶液变成浅红色 |
| ③将一小块金属钠放入滴有酚酞溶液的冷水中 | C.剧烈反应,迅速产生大量无色气体 |
| ④将镁条投入稀盐酸中 | D.反应不十分剧烈,产生无色气体 |
| ⑤将铝条投入稀盐酸中 | E.生成白色胶状沉淀,继而沉淀消失 |
| ⑥向AlCl3溶液中滴加NaOH溶液至过量 | F.生成淡黄色沉淀 |
请你帮助该同学整理并完成实验报告。
(1)实验目的:研究
(2)实验用品:试剂:金属钠、镁条、铝条、稀盐酸、新制氯水、新制Na2S溶液、AlCl3溶液、NaOH溶液、酚酞溶液等。
仪器:
(3)实验内容:(填写与实验步骤对应的实验现象的编号和①②的化学方程式及此实验的结论)
| 实验内容 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 实验现象(填A~F) |
②
此实验的结论:
您最近一年使用:0次



