短周期的五种元素A、B、C、D、E,原子序数依次增大。A、B、C三种元素电子层数之和是5。A、B两元素原子最外层电子数之和等于C元素原子最外层电子数;B元素原子最外电子层上的电子数是它的电子层数的2倍,A与D可以形成原子个数比分别为1∶1和2∶1的两种液态化合物;E单质用于净化水质。
请回答:
(1)写出D在元素周期表中的位置_____________________ ,
E的原子结构示意图是________ 。
下列可以验证C与D两元素原子得电子能力强弱的实验事实是____ (填写编号)。
A.比较这两种元素的气态氢化物的沸点
B.比较只有这两种元素所形成的化合物中的化合价
C.比较这两种元素的气态氢化物的稳定性
D.比较这两种元素的单质与氢气化合的难易
(2)由A、B两种元素组成的最简单的化合物,写出其电子式____ 。
(3)均由A、B、C、D四种元素组成的甲、乙两种化合物,都既可以与盐酸反应又可以与NaOH溶液反应,甲为无机盐,其化学式为____ ,乙为天然高分子化合物的水解产物,且是同类物质中相对分子质量最小的,其结构简式为___________ 。
(4)胶态磁流体在医学上有重要的用途,而纳米级Fe3O4是磁流体中的重要粒子,其制备过程可简单表示如下:
①将化合物CA3通入等物质的量的FeSO4、Fe2(SO4)3的混合溶液中,生成两种碱,写出该反应过程的总的离子方程式___________________________________ 。
②上述反应生成的两种碱继续作用,得到Fe3O4。
(5)已知下表数据:
若使混合液中FeSO4、Fe2(SO4)3的浓度均为2.0 mol·L-1,则混合液中c(OH-)不得大于____ mol·L-1。
请回答:
(1)写出D在元素周期表中的位置
E的原子结构示意图是
下列可以验证C与D两元素原子得电子能力强弱的实验事实是
A.比较这两种元素的气态氢化物的沸点
B.比较只有这两种元素所形成的化合物中的化合价
C.比较这两种元素的气态氢化物的稳定性
D.比较这两种元素的单质与氢气化合的难易
(2)由A、B两种元素组成的最简单的化合物,写出其电子式
(3)均由A、B、C、D四种元素组成的甲、乙两种化合物,都既可以与盐酸反应又可以与NaOH溶液反应,甲为无机盐,其化学式为
(4)胶态磁流体在医学上有重要的用途,而纳米级Fe3O4是磁流体中的重要粒子,其制备过程可简单表示如下:
①将化合物CA3通入等物质的量的FeSO4、Fe2(SO4)3的混合溶液中,生成两种碱,写出该反应过程的总的离子方程式
②上述反应生成的两种碱继续作用,得到Fe3O4。
(5)已知下表数据:
| 物质 | Fe(OH)2 | Fe(OH)3 |
| Ksp/25 ℃ | 2.0×10-16 | 4.0×10-36 |
12-13高三上·浙江温州·开学考试 查看更多[3]
更新时间:2016-12-09 05:29:39
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】现有部分短周期元素的性质或原子结构如下表:
(1)Y形成的双原子分子中的化学键为_____________ (填“极性键”或“非极性键”)。
(2)元素X的一种同位素可测定文物年代,这种同位素的符号是________ 。
(3)元素Y与氢元素形成一种分子YH3,写出该粒子的电子式:________ 。
(4)元素Z与元素T相比,非金属性较强的是__________ (用元素符号表示),下列表述中能证明这一事实的是________ 。
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
(5)T、X、Z三种元素的最高价氧化物的水化物的酸性由强到弱的顺序是________________________ (用化学式表示)。
元素编号 | 元素性质或原子结构 |
T | M层上的电子数是原子核外电子层数的2倍 |
X | 最外层电子数是次外层电子数的2倍 |
Y | 常温下单质 为双 为双 原子分子,其氢化物水溶液呈碱性 原子分子,其氢化物水溶液呈碱性 |
Z | 元素最高正价是+7价 |
(2)元素X的一种同位素可测定文物年代,这种同位素的符号是
(3)元素Y与氢元素形成一种分子YH3,写出该粒子的电子式:
(4)元素Z与元素T相比,非金属性较强的是
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
(5)T、X、Z三种元素的最高价氧化物的水化物的酸性由强到弱的顺序是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】随原子序数递增,八种短周期元素(用字母x、y等表示)原子半径的相对大小、最高正价或最低负价的变化如图所示。回答下列问题:
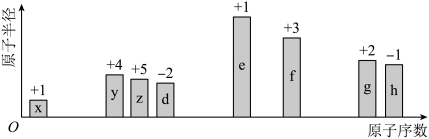
(1)f在元素周期表中的位置位于_____ 。
(2)写出f单质与e的最高价氧化物对应的水化物反应的离子方程式:_____ 。
(3)写出y、z、d的最简单氢化物的稳定性由强到弱的顺序_____ (用化学式表示)。
(4)写出元素y用于测定文物年代的一种同位素的原子符号_____ ,该同位素形成的最高价氧化物69 g中所含质子的数目为_____ (用阿伏加德罗常数的值NA表示)。
(5)y的最高价氧化物的电子式:_____ 。
(6)d的一种氢化物分子中既含非极性键又含极性键,其结构式为_____ 。

(1)f在元素周期表中的位置位于
(2)写出f单质与e的最高价氧化物对应的水化物反应的离子方程式:
(3)写出y、z、d的最简单氢化物的稳定性由强到弱的顺序
(4)写出元素y用于测定文物年代的一种同位素的原子符号
(5)y的最高价氧化物的电子式:
(6)d的一种氢化物分子中既含非极性键又含极性键,其结构式为
您最近一年使用:0次
【推荐3】有A、B、C、D、E五种原子序数依次增大的元素,其中A、B、C、D属于短周期,A原子最外层电子数等于次外层的电子数2倍,C元素在地壳中的含量最高,D元素的原子在短周期主族元素中原子半径最大。E是第四周期中成单电子最多的元素,根据以上条件,回答下列问题:
(1)指出D元素在元素周期表中的位置:___________ 。
(2)画出AC2的电子式:___________ 。
(3)写出C和D元素的简单离子半径大小关系:___________ (用离子称号表示)。
(4)判断B的简单氢化物的分子极性___________ (填“极性”或“非极性”)。
(5)比较B、C二种元素的第一电离能的大小顺序:___________ (用元素符号表示)。
(6)写出E原子的价层电子排布式:___________ 。
(1)指出D元素在元素周期表中的位置:
(2)画出AC2的电子式:
(3)写出C和D元素的简单离子半径大小关系:
(4)判断B的简单氢化物的分子极性
(5)比较B、C二种元素的第一电离能的大小顺序:
(6)写出E原子的价层电子排布式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】镍、钴元素在锂电池材料和国防工业方面应用广泛。一种利用酸浸出法从冶金厂废炉渣(含Ni、Co及少量Cu、Mg、Ca的化合物)中提取镍和钴的工艺流程如图:

已知:i.Ksp(CaF2)=1.0×10-10,Ksp(MgF2)=7.5×10-11;
ii.NiSO4在水中的溶解度随温度升高明显增大,不溶于乙醇和苯。
回答下列问题:
(1)“酸浸渣”主要成分的名称为_______ 。
(2)基态Co原子的核外M层电子排布式为_______ 。Co的核电荷数比Ni小1,但Co的相对原子质量比却Ni的略大,原因是_______ 。
(3)“除铁”的离子方程式为_______ 。
(4)“除钙镁”时,pH不宜过低的原因是_______ 。Ca2+和Mg2+沉淀完全。时,溶液中c(F-)最小为_______ mol·L-1
(5)“萃取”原理为Co2+(aq)+2HA(有机相)⇌Co(A)2(有机相)+2H+(aq)。“反萃取”时为促进Co2+的转移,应选择的实验条件或采取的实验操作有①_______ ;②多次萃取。
(6)获得NiSO4(s)的“一系列操作”中洗涤产品可选用_______ (填字母标号)试剂。
a.冷水 b.乙醇 c.苯

已知:i.Ksp(CaF2)=1.0×10-10,Ksp(MgF2)=7.5×10-11;
ii.NiSO4在水中的溶解度随温度升高明显增大,不溶于乙醇和苯。
回答下列问题:
(1)“酸浸渣”主要成分的名称为
(2)基态Co原子的核外M层电子排布式为
(3)“除铁”的离子方程式为
(4)“除钙镁”时,pH不宜过低的原因是
(5)“萃取”原理为Co2+(aq)+2HA(有机相)⇌Co(A)2(有机相)+2H+(aq)。“反萃取”时为促进Co2+的转移,应选择的实验条件或采取的实验操作有①
(6)获得NiSO4(s)的“一系列操作”中洗涤产品可选用
a.冷水 b.乙醇 c.苯
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】在实验室中从废旧钴酸锂离子电池的正极材料(在铝箔上涂覆活性物质LiCoO2)中回收钴、锂的操作流程如图:

回答下列问题:
(1)拆解废旧电池获取正极材料前,先将其浸入NaCl溶液中,使电池短路而放电,此时溶液温度升高,该过程中能量的主要转化方式为____ 。
(2)“过滤”所得滤液用盐酸处理可得到氢氧化铝,反应的化学方程式为____ 。
(3)“酸浸”时主要反应的离子方程式为____ ;若硫酸、Na2S2O3溶液用一定浓度的盐酸替代,也可以达到“酸浸”的目的,但会产生____ (填化学式)污染环境。
(4)“沉钴”时,调pH所用的试剂是____ ;“沉钴”后溶液中c(Co2+)=____ 。已知:Ksp[Co(OH)2]=1.09×l0-15。
(5)在空气中加热Co(OH)2,使其转化为钴的氧化物。加热过程中,固体质量与温度的关系如图所示。290~500℃,发生反应的化学方程式为____ 。

(6)根据图判断,“沉锂”中获得Li2CO3固体的操作主要包括____ 、____ 、洗涤、干燥等步骤。


回答下列问题:
(1)拆解废旧电池获取正极材料前,先将其浸入NaCl溶液中,使电池短路而放电,此时溶液温度升高,该过程中能量的主要转化方式为
(2)“过滤”所得滤液用盐酸处理可得到氢氧化铝,反应的化学方程式为
(3)“酸浸”时主要反应的离子方程式为
(4)“沉钴”时,调pH所用的试剂是
(5)在空气中加热Co(OH)2,使其转化为钴的氧化物。加热过程中,固体质量与温度的关系如图所示。290~500℃,发生反应的化学方程式为

(6)根据图判断,“沉锂”中获得Li2CO3固体的操作主要包括

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】五氧化二钒(V2O5)在冶金、化工等领域有重要应用。实验室以含钒废料(含V2O3、FeO、CuO、MnO、SiO2、Al2O3、有机物)为原料制备V2O5的一种流程如图:
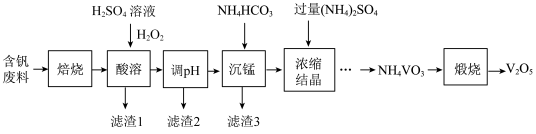
已知:25℃时,难溶电解质的溶度积常数如表所示:
(1)“焙烧”的目的是______ 。
(2)酸溶时加入H2O2的目的是_______ 。
(3)常温下,若“调pH”为7,Cu2+是否能沉淀完全:______ (填“是”或“否”)(溶液中离子浓度小于10-5mol•L-1时,认为该离子沉淀完全)。
(4)“沉锰”需将温度控制在70℃左右,温度不能过高或过低的原因为______ 。
(5)结晶所得的NH4VO3需进行水洗、干燥。证明NH4VO3已洗涤干净的实验操作及现象_____ 。
(6)为测定该产品的纯度,兴趣小组同学准确称取V2O5产品2.000g,加入过量稀硫酸使其完全反应,生成(VO2)2SO4,并配成100mL溶液。取10.00mL溶液用0.1000mol•L-1的H2C2O4标准溶液滴定,滴定到终点时消耗标准液10.00mL。已知滴定过程中H2C2O4被氧化为CO2,VO 黄色(被还原为VO2+蓝色),该反应的离子方程式:
黄色(被还原为VO2+蓝色),该反应的离子方程式:______ ;该产品的纯度为______ 。

已知:25℃时,难溶电解质的溶度积常数如表所示:
| 难溶电解质 | Cu(OH)2 | Mn(OH)2 | Al(OH)3 |
| Ksp | 2.2×10-20 | 4×10-14 | 1.9×10-33 |
(2)酸溶时加入H2O2的目的是
(3)常温下,若“调pH”为7,Cu2+是否能沉淀完全:
(4)“沉锰”需将温度控制在70℃左右,温度不能过高或过低的原因为
(5)结晶所得的NH4VO3需进行水洗、干燥。证明NH4VO3已洗涤干净的实验操作及现象
(6)为测定该产品的纯度,兴趣小组同学准确称取V2O5产品2.000g,加入过量稀硫酸使其完全反应,生成(VO2)2SO4,并配成100mL溶液。取10.00mL溶液用0.1000mol•L-1的H2C2O4标准溶液滴定,滴定到终点时消耗标准液10.00mL。已知滴定过程中H2C2O4被氧化为CO2,VO
 黄色(被还原为VO2+蓝色),该反应的离子方程式:
黄色(被还原为VO2+蓝色),该反应的离子方程式:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】已知A,B,C,D,E是元素周期表中1~36号元素,其原子序数依次增大,且A,B,C,D为主族元素.A与另外四种元素既不在同一周期,也不在同一主族.B和C同主族,D和E同周期;元素E是周期表中的第7列元素,D的最外层电子数与最内层电子数相同,D跟B可形成离子化合物,其晶胞结构(其中B原子在晶胞内部)如图。
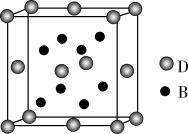
请回答下列问题:
(1)C-的电子排布式为___ ;E元素原子的价电子排布式为___ 。
(2)元素B与氮元素可以形成化合物NB3,其中N﹣B键的化学键类型为___ ,根据价层电子对互斥理论可以判断NB3的空间构型为___ ,NB3分子中N原子的杂化方式为杂化___ 。
(3)A,B形成的化合物AB的相对分子质量比A,C形成的化合物AC的相对分子质量小,但AB的沸点比AC高,其原因是___ 。
(4)从晶胞图可以得出:D与B形成的离子化合物的化学式为___ 。
(5)含有D元素的化合物焰色反应为___ 色。

请回答下列问题:
(1)C-的电子排布式为
(2)元素B与氮元素可以形成化合物NB3,其中N﹣B键的化学键类型为
(3)A,B形成的化合物AB的相对分子质量比A,C形成的化合物AC的相对分子质量小,但AB的沸点比AC高,其原因是
(4)从晶胞图可以得出:D与B形成的离子化合物的化学式为
(5)含有D元素的化合物焰色反应为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】现有部分短周期元素的性质或原子结构如下:
(1)X的无中子原子的符号为____________ ,Y的原子结构示意图为_____________ ,Q在元素周期表中的位置为___________________ 。
(2)Y、Z的最高价氧化物对应的水化物的碱性由强到弱的顺序是_______________________ (用化学式表示),写出两者反应的离子方程式:__________________________________________ 。
(3)M、W两种元素中非金属性较强的是______________ (用元素符号表示),下列表述中能证明这一事实的____________________ (填序号),
a. 常温下,M的单质与W的单质的状态不同
b. 向W的氢化物中通入M2,有淡黄色固体析出
c. M、W形成的化合物中W元素为正价
| 元素 | 元素的性质或原子结构 |
| X | 该元素的一种原子无中子 |
| Y | 原子半径最大的短周期元素 |
| Z | 第三周期元素中简单离子半径最小 |
| M | 地壳中含量最多的元素 |
| Q | 其氧化物是光导纤维的基本原料 |
| W | 其核电荷数为M元素核电荷数的2倍 |
(2)Y、Z的最高价氧化物对应的水化物的碱性由强到弱的顺序是
(3)M、W两种元素中非金属性较强的是
a. 常温下,M的单质与W的单质的状态不同
b. 向W的氢化物中通入M2,有淡黄色固体析出
c. M、W形成的化合物中W元素为正价
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】已知X、Y、Z、W四种元素分别是元素周期表中三个连续短周期的元素,且原子序数依次增大。X、W同主族,Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z原子的最外层电子数之和。Y与X形成的分子中有3个共价键。Z原子最外层电子数是次外层电子数的3倍,试推断:
(1)X、Z两种元素的元素符号为:X________ 、Z________ 。
(2)由以上元素中两两形成的化合物中:溶于水显碱性的气态氢化物的电子式为________ ,它的共价键属于________ (填“极性”或“非极性”)键;含有离子键和非极性共价键的化合物的电子式为__________ ;含有极性共价键和非极性共价键的化合物的结构式为_________ 。
(3)由X、Y、Z所形成的常见离子化合物是________ (写化学式),该化合物与W的最高价氧化物对应的水化物的浓溶液加热时反应的离子方程式为_______________________________ 。
X与W形成的化合物与水反应时,水作________ (填“氧化剂”或“还原剂”)。
(1)X、Z两种元素的元素符号为:X
(2)由以上元素中两两形成的化合物中:溶于水显碱性的气态氢化物的电子式为
(3)由X、Y、Z所形成的常见离子化合物是
X与W形成的化合物与水反应时,水作
您最近一年使用:0次



