A、B、C、D是四种常见气体单质。E的相对分子质量比F小16,且F为红棕色。有关的转化关系如图所示(反应条件与部分反应的生成物略去)。
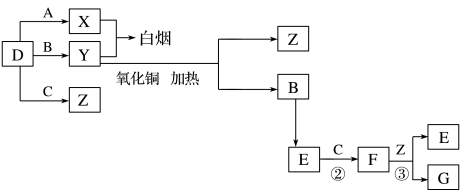
请回答下列问题:
(1)B的电子式为___________ 。
(2)Y与氧化铜反应,每生成1 mol B消耗3mol氧化铜,该反应的化学方程式为___________ 。
(3)反应③的化学方程式为___________ 。
(4)Y与E在一定条件下可反应生成B和Z,这是一个具有实际意义的反应,可消除E对环境的污染,该反应的化学方程式为___________ 。
(5)气体F和气体SO2在通常条件下同时通入盛有BaCl2溶液的洗气瓶中(如图所示),有沉淀生成,该反应的离子方程式为___________ 。


请回答下列问题:
(1)B的电子式为
(2)Y与氧化铜反应,每生成1 mol B消耗3mol氧化铜,该反应的化学方程式为
(3)反应③的化学方程式为
(4)Y与E在一定条件下可反应生成B和Z,这是一个具有实际意义的反应,可消除E对环境的污染,该反应的化学方程式为
(5)气体F和气体SO2在通常条件下同时通入盛有BaCl2溶液的洗气瓶中(如图所示),有沉淀生成,该反应的离子方程式为

更新时间:2023-07-10 13:11:26
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】如图所示:下图为A → E五种含同种元素的物质相互转化的关系图,其中A、B、C、D常温下都是气体,D呈红棕色。按要求回答下列问题:
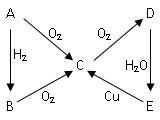
(1) A物质的电子式_______ ;B物质是含______ 键
的______ 分子(填“极性”或者“非极性”)
(2)下列反应的化学方程式为:
①B→C:_____________________________________________
②D→E:_____________________________________________
(3)实验室制取B的化学方程式为:__________________________________________ ,通常用___________ 来干燥B气体;
已知B可以与灼热的氧化铜反应得到A气体和金属铜,则该反应的化学方程式为:________________________________________________ 。

(1) A物质的电子式
的
(2)下列反应的化学方程式为:
①B→C:
②D→E:
(3)实验室制取B的化学方程式为:
已知B可以与灼热的氧化铜反应得到A气体和金属铜,则该反应的化学方程式为:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】图为元素周期表的一部分,根据表中列出的10种元素,回答下列问题。
(1)O和S中,原子半径较大的是_______ 。(填元素符号)
(2)CH4和SiH4中,沸点较高的是_______ 。(填化学式)
(3)新制氯水有漂白作用,是因为其中含有_______ 。(填化学式)
(4)元素最高价氧化物对应水化物中,两性氢氧化物是_______ 。(填化学式)
(5)用电子式表示HCl的形成过程_______ 。
 | I A | II A | III A | IV A | VA | VI A | VII A | 0 |
| 2 | C | N | O | Ne | ||||
| 3 | Na | Mg | Al | Si | S | Cl |
(2)CH4和SiH4中,沸点较高的是
(3)新制氯水有漂白作用,是因为其中含有
(4)元素最高价氧化物对应水化物中,两性氢氧化物是
(5)用电子式表示HCl的形成过程
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】已知A、B、C、D、E五种短周期元素,原子序数大小顺序为:C>A>B>D>E,A、C同周期,B、C同主族,A和B形成的离子化合物A2B中离子的电子数相同,其电子总数为30,D和E可形成4核10电子分子。请回答下面的问题:
(1)写出五种元素的符号:A___________ ;B___________ ;C___________ ;D___________ ;E___________ 。
(2)写出A2B的电子式:___________ 。
(3)写出下列物质的电子式:
D元素的单质___________ ;
E和B元素形成的化合物___________ 。
A、B、E三种元素形成的化合物___________ ;
D和E元素形成的化合物___________ 。
(1)写出五种元素的符号:A
(2)写出A2B的电子式:
(3)写出下列物质的电子式:
D元素的单质
E和B元素形成的化合物
A、B、E三种元素形成的化合物
D和E元素形成的化合物
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】水钴矿的主要成分为CoO、Co2O3、 Co(OH)3, 还含SiO2及少量Al2O3、Fe2O3、 CuO、MnO2 等。 一种利用水钻矿制取CoCl2·6H2O的工艺流程如下:

已知部分沉淀的有关数据如下表(“沉淀完全”是指溶液中离子浓度低于1.0 ×10-5mol·L-1)。
请回答下列问题:
(1)写出“浸出”时Co2O3发生反应的离子方程式_______ ,分析加入Na2SO3的必要性_______ 。
(2)写出NaClO3发生主要反应的离子方程式_______ 。若向“浸出液”中加NaClO3时不慎过量,可能会引起什么不良后果_______ 。
(3)假设“氧化”后溶液中Co2+的浓度为0.2 mol·L-1, 通过简要计算说明“沉淀”时应控制溶液pH的范围_______ 。
(4)“系列操作”中包含3个基本实验操作,依次写出它们的名称_______ 、_______ 、_______ 。
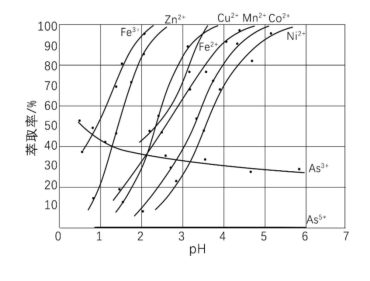
(5)某种萃取剂对部分离子的萃取率与溶液pH的关系如图所示。请写出2条萃取规律_______ 、_______ ,并说明本流程是否可用该萃取剂进行萃取_______ 。
 .
.

已知部分沉淀的有关数据如下表(“沉淀完全”是指溶液中离子浓度低于1.0 ×10-5mol·L-1)。
| 沉淀 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Cu(OH)2 | Mn(OH)2 |
| 沉淀完全时pH | 5.2 | 2.8 | 8.3 | 9.4 | 6.7 | 10.1 |
| 沉淀溶解时pH | 7.8 | — | — | 14 | — | — |
请回答下列问题:
(1)写出“浸出”时Co2O3发生反应的离子方程式
(2)写出NaClO3发生主要反应的离子方程式
(3)假设“氧化”后溶液中Co2+的浓度为0.2 mol·L-1, 通过简要计算说明“沉淀”时应控制溶液pH的范围
(4)“系列操作”中包含3个基本实验操作,依次写出它们的名称
(5)某种萃取剂对部分离子的萃取率与溶液pH的关系如图所示。请写出2条萃取规律
 .
.
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】实验室有如下物质:①Fe ②酒精 ③CaCO3④熔融的K2SO4 ⑤饱和FeCl3溶液⑥CO 2⑦NH4HCO3 ⑧稀盐酸⑨NaHSO4回答下列问题:
(1)某同学将③④⑨归为一类,他的分类依据是_______ 。
A.都属于酸式盐 B.都属于盐 C.都易溶于水
(2)以上物质属于电解质的有_______ (填编号,下同)
(3)以上物质能导电的有_______ 。
(4)写出⑦在水中的电离方程式_______ 。
(5)向 溶液中滴加Ba(OH)2溶液至中性,写出反应的离子方程式
溶液中滴加Ba(OH)2溶液至中性,写出反应的离子方程式_______ 。
(6)现有甲、乙、丙三名同学分别进行Fe(OH)3胶体的制备实验。
I.甲同学向饱和氯化铁溶液中加入少量的NaOH溶液;
II.乙同学直接加热饱和FeCl3溶液;
III.丙同学向25mL沸水中逐滴加入5~6滴FeCl3饱和溶液,继续煮沸至液体呈红褐色,停止加热。
①其中操作正确的同学是_______ ;他的操作中涉及到的化学反应方程式为_______ 。
②证明有Fe(OH)3胶体生成的现象是_______ 。
(1)某同学将③④⑨归为一类,他的分类依据是
A.都属于酸式盐 B.都属于盐 C.都易溶于水
(2)以上物质属于电解质的有
(3)以上物质能导电的有
(4)写出⑦在水中的电离方程式
(5)向
 溶液中滴加Ba(OH)2溶液至中性,写出反应的离子方程式
溶液中滴加Ba(OH)2溶液至中性,写出反应的离子方程式(6)现有甲、乙、丙三名同学分别进行Fe(OH)3胶体的制备实验。
I.甲同学向饱和氯化铁溶液中加入少量的NaOH溶液;
II.乙同学直接加热饱和FeCl3溶液;
III.丙同学向25mL沸水中逐滴加入5~6滴FeCl3饱和溶液,继续煮沸至液体呈红褐色,停止加热。
①其中操作正确的同学是
②证明有Fe(OH)3胶体生成的现象是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】我国科学家研发的“液态阳光”计划通过太阳能发电电解水制氢,再采用高选择性催化剂将二氧化碳加氢制备甲醇。
(1)制备甲醇主反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H=-48.7kJ/mol。
CH3OH(g)+H2O(g)△H=-48.7kJ/mol。
该过程中还存在一个生成CO的副反应,结合反应:CO(g)+2H2(g)=CH3OH(g)△H=-90.0kJ/mol
写出该副反应的热化学方程式:_______ 。
(2)将CO2和H2按物质的量比1:3混合,以固定流速通过盛放Cu/Zn/A/Zr催化剂的反应器,在相同时间内,不同温度下的实验数据如图所示。 。
。
①催化剂活性最好的温度为_______ 。
a.483K b.503 K c.1523 K d.543 K
②温度由523K升到543K,CO2的平衡转化率和CH3OH的实验产率均降低,解释原因:_______ 。
(3)使用Cu2O-ZnO薄膜电极作阴极,通过电催化法将二氧化碳转化为甲醇。
①将铜箔放入煮沸的饱和磕酸铜溶液中,制得Cu2O薄膜电极。反应的离子方程式为_______ 。
②用Cu2O薄膜电极作阴极,Zn(NO3)2溶液作电解液,采用电沉积法制备Cu2O-ZnO薄膜电极,制备完成后电解液中检测到了 制备ZnO薄膜的电极反应式为
制备ZnO薄膜的电极反应式为_______ 。
(1)制备甲醇主反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)△H=-48.7kJ/mol。
CH3OH(g)+H2O(g)△H=-48.7kJ/mol。该过程中还存在一个生成CO的副反应,结合反应:CO(g)+2H2(g)=CH3OH(g)△H=-90.0kJ/mol
写出该副反应的热化学方程式:
(2)将CO2和H2按物质的量比1:3混合,以固定流速通过盛放Cu/Zn/A/Zr催化剂的反应器,在相同时间内,不同温度下的实验数据如图所示。

 。
。①催化剂活性最好的温度为
a.483K b.503 K c.1523 K d.543 K
②温度由523K升到543K,CO2的平衡转化率和CH3OH的实验产率均降低,解释原因:
(3)使用Cu2O-ZnO薄膜电极作阴极,通过电催化法将二氧化碳转化为甲醇。
①将铜箔放入煮沸的饱和磕酸铜溶液中,制得Cu2O薄膜电极。反应的离子方程式为
②用Cu2O薄膜电极作阴极,Zn(NO3)2溶液作电解液,采用电沉积法制备Cu2O-ZnO薄膜电极,制备完成后电解液中检测到了
 制备ZnO薄膜的电极反应式为
制备ZnO薄膜的电极反应式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】现有A、B、C、D、E、F、G、H、M九种物质,其中A为淡黄色粉末,B为日常生活中常见的无色无味液体,E为无色气体单质,F的水溶液与石灰水混合可得D的溶液,G为黄绿色气体单质,H是“84”消毒液的有效成分,它们之间的相互转化关系如图所示,其他与题无关的生成物均已略去。

请回答下列问题:
(1)写出H的化学式:_______ ,C的化学式:_______ 。
(2)化合物A中非金属元素的化合价是_______ ,由此判断该物质_______ (填字母)。
a.只有氧化性 b.只有还原性 c.既有氧化性又有还原性
(3)写出反应④的化学方程式:_______ ;
(4)反应①~⑤中,不属于氧化还原反应的是_______ (填序号)。
(5)检验F中阳离子的实验方法:_______

请回答下列问题:
(1)写出H的化学式:
(2)化合物A中非金属元素的化合价是
a.只有氧化性 b.只有还原性 c.既有氧化性又有还原性
(3)写出反应④的化学方程式:
(4)反应①~⑤中,不属于氧化还原反应的是
(5)检验F中阳离子的实验方法:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】下列图示中,A为一种常见的单质,B、C、D、E是含有A元素的常见化合物。它们的焰色试验均为黄色。
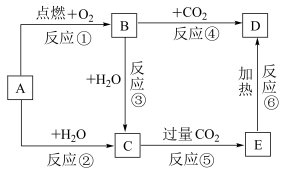
回答下列问题:
(1)写出化学式:A___ ,D___ 。
(2)以上反应中不属于氧化还原反应的有___ (填序号)。
(3)反应③的离子方程式:___ 。氧化剂为___ ;氧化产物为___ 。
(4)向D溶液中通入CO2反应的化学方程式:____ 。

回答下列问题:
(1)写出化学式:A
(2)以上反应中不属于氧化还原反应的有
(3)反应③的离子方程式:
(4)向D溶液中通入CO2反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
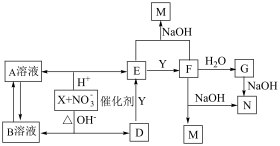
【推荐3】已知:X、Y分别是地壳中含量最高的金属和非金属元素的单质,D、E、F为气体,X在酸性或碱性溶液中均可与NO3-发生氧化还原反应,气体D和G反应可生成盐,气体D和A溶液反应生成白色沉淀,气体E和F在NaOH溶液中按1:1反应钠盐M,各物质转化关系如下:
请回答下列问题:
(1)M的化学式__________ 。
(2)请写出D的溶液与A溶液反应的离子方程式:___________
(3)写出X在碱性条件下与NO3-反应的离子方程式:_____________
(4)标况下,若E,F的混合气体共48mL,恰好被10mL菜浓度的NaOH溶液吸收,则该NaOH溶液浓度为______ mol,若反应后所得溶液中M和N的浓度之比为7:1,则原来气体中E与F的体积比为________ 。

请回答下列问题:
(1)M的化学式
(2)请写出D的溶液与A溶液反应的离子方程式:
(3)写出X在碱性条件下与NO3-反应的离子方程式:
(4)标况下,若E,F的混合气体共48mL,恰好被10mL菜浓度的NaOH溶液吸收,则该NaOH溶液浓度为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】某同学在学习元素化合物知识的过程中,发现含有相同元素的物质间在一定条件下存在
转化规律,绘制出如下转化关系图,图中A、B、C、D是由短周期元素组成的物质。

请回答:
(1)若A为单质,其焰色反应为黄色,C为淡黄色固体。则组成A的元素在周期表中的位置是__ ,C的电子式为__ 。
(2)若A为能使湿润红色石蕊试纸变蓝的气体,C为红棕色气体。
①A→B反应的化学方程式是__ 。过量的A的水溶液与AlCl3溶液反应离子方程式为__ 。
②A与C反应生成E和水,E是空气中含量最多的气体。当生成19.6gE时,转移电子的物质的量为__ mol。
(3)若B为能使品红溶液褪色的无色刺激性的气体,B→C反应的化学方程式是__ ,B与KMnO4溶液反应离子方程式为__ 。
转化规律,绘制出如下转化关系图,图中A、B、C、D是由短周期元素组成的物质。

请回答:
(1)若A为单质,其焰色反应为黄色,C为淡黄色固体。则组成A的元素在周期表中的位置是
(2)若A为能使湿润红色石蕊试纸变蓝的气体,C为红棕色气体。
①A→B反应的化学方程式是
②A与C反应生成E和水,E是空气中含量最多的气体。当生成19.6gE时,转移电子的物质的量为
(3)若B为能使品红溶液褪色的无色刺激性的气体,B→C反应的化学方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】A、B、C、D四种物质之间有下图所示的转化关系。
已知:A是气体单质,C 是红棕色气体。

回答下列问题:
(1)写出C的化学式:________ ;
(2)在上图D→B的过程中,D表现出强_____ (填“氧化性”或“还原性”);
(3)写出C→D转化的化学方程式__________________________________
(4)D→B的离子方程式_____________________________________________
(5)C 是红棕色气体,若A是气态氢化物,则A的电子式为___________
已知:A是气体单质,C 是红棕色气体。

回答下列问题:
(1)写出C的化学式:
(2)在上图D→B的过程中,D表现出强
(3)写出C→D转化的化学方程式
(4)D→B的离子方程式
(5)C 是红棕色气体,若A是气态氢化物,则A的电子式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】已知氨可以与灼热的氧化铜反应生成氮气和金属铜,用下面示意图中的装置可以实现该反应。

试回答下列问题:
(1)请写出A中反应的化学方程式为_______ 。
(2)仪器B中盛放_______ 作为干燥剂去除气体中的水蒸气。
a.碱石灰 b.浓硫酸
(3)实验时在C中加入CuO,发生反应的化学方程式是_______ 。
(4)反应结束后取下D试管,向其中滴加几滴酚酞试液,观察到的现象是_______ ,产生该现象的原因是_______ 。(用恰当的化学用语表示)
(5)装置E中收集到的物质是_______ 。(填化学式)
(6)向10gCu和CuO组成的混合物中,加入一定量的稀硝酸溶液,恰好使混合物完全溶解,同时收集到标准状况下NO2.24L。请回答以下问题:
①写出Cu与稀硝酸反应的离子方程式_______ 。
②计算原混合物中铜的质量分数__________ 。

试回答下列问题:
(1)请写出A中反应的化学方程式为
(2)仪器B中盛放
a.碱石灰 b.浓硫酸
(3)实验时在C中加入CuO,发生反应的化学方程式是
(4)反应结束后取下D试管,向其中滴加几滴酚酞试液,观察到的现象是
(5)装置E中收集到的物质是
(6)向10gCu和CuO组成的混合物中,加入一定量的稀硝酸溶液,恰好使混合物完全溶解,同时收集到标准状况下NO2.24L。请回答以下问题:
①写出Cu与稀硝酸反应的离子方程式
②计算原混合物中铜的质量分数
您最近一年使用:0次



