1-乙基-3-甲基咪唑双(三氟甲基磺酰基)酰亚胺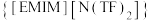 是一种室温离子液体,可以用作合成
是一种室温离子液体,可以用作合成 纳米颗粒的绿色溶剂,其结构如图所示:
纳米颗粒的绿色溶剂,其结构如图所示:
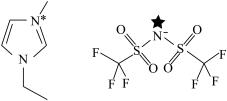
下列说法错误的是
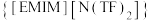 是一种室温离子液体,可以用作合成
是一种室温离子液体,可以用作合成 纳米颗粒的绿色溶剂,其结构如图所示:
纳米颗粒的绿色溶剂,其结构如图所示:
下列说法错误的是
A.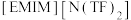 中含有离子键共价键 中含有离子键共价键 |
B.结构中标“★”氮原子的杂化类型为 |
| C.电负性:F>O>N |
D.熔点: |
更新时间:2023-07-10 19:23:24
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】现有四种元素的基态原子的电子排布式如下:①1s22s22p63s23p4 ②1s22s22p63s23p3 ③1s22s22p3 ④1s22s22p5,则下列有关比较中正确的是
| A.第一电离能:④>③>②>① | B.最高正化合价:④>③=②>① |
| C.电负性:④>③>②>① | D.原子半径:①>②>③>④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】利用原子结构及元素周期律表相关知识得到的以下结论中不正确的是
A.第ⅠA族元素的原子半径: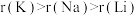 |
B.基态 价层电子的轨道表示式: 价层电子的轨道表示式: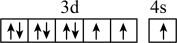 |
C.酸性: |
| D.电负性:C<N<O |
您最近一年使用:0次
【推荐1】下列关于该有机物的说法不正确的是
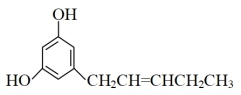

| A.既有σ键又有π键 | B.O-H键的极性强于C-H键的极性 |
| C.该物质分子中没有手性碳原子 | D.该物质中所有碳原子都是sp2杂化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某种化合物的结构如图所示。其中X、Y、Z、Q、W为原子序数依次增大的五种短周期主族元素,Q核外最外层电子数与Y核外电子总数相同,X的原子半径是元素周期表中最小的。下列叙述正确的是


A.电负性: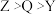 |
B.简单离子半径: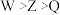 |
| C.Y的氢化物的沸点能大于Q的氢化物的沸点 |
| D.该化合物中Z和Y原子的杂化方式都相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列比较中,错误的是
| A.范德华力:He>HBr>HCl |
| B.键角:CO2>CH2O(甲醛)>NH3 |
| C.键能:HF>HCl>HBr 键长:C-H>N-H |
| D.晶格能:MgO>CaO>BaO 熔点:金刚石>晶体硅 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列解释中,不正确的是
| A.水在结冰时体积膨胀,是由于水分子中存在分子间氢键 |
B.水很稳定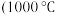 以上才会部分分解 以上才会部分分解 是因为水中含有大量的氢键所致 是因为水中含有大量的氢键所致 |
C.MgO的熔点比 高主要是因为MgO的晶格能比 高主要是因为MgO的晶格能比 大 大 |
| D.碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列有关含氯的物质或微粒说法不正确 的是
A.随Cl元素化合价升高, 、 、 、 、 、 、 和 和 的氧化性增强 的氧化性增强 |
B. 、 、 和 和 中心原子轨道的杂化类型均为sp3 中心原子轨道的杂化类型均为sp3 |
| C.NaF、NaCl、NaBr的熔点依次降低,原因是晶体的晶格能随离子核间距的增大而减小 |
| D.配合物Pt(NH3)2Cl2存在顺反异构体,分别称为顺铂和反铂。顺铂为极性分子,相同温度时在水中的溶解度大于反铂 |
您最近一年使用:0次

 、
、 、
、 分子内键角依次减小
分子内键角依次减小 与
与 结构相似,含有的σ键与π键个数比均为1∶1
结构相似,含有的σ键与π键个数比均为1∶1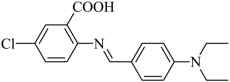
 、
、 两种杂化方式
两种杂化方式

