以下反应可表示获得乙醇并用作汽车燃料的过程,下列有关说法正确的是
①6CO2(g)+6H2O(l)=C6H12O6(s)+6O2(g) ΔH1
②C6H12O6(s)=2C2H5OH(l)+2CO2(g) ΔH2
③C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l) ΔH3
①6CO2(g)+6H2O(l)=C6H12O6(s)+6O2(g) ΔH1
②C6H12O6(s)=2C2H5OH(l)+2CO2(g) ΔH2
③C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l) ΔH3
| A.2ΔH3=-ΔH1-2ΔH2 |
| B.ΔH3、ΔH1、ΔH2均为ΔH<0 |
| C.在不同油耗汽车中发生反应③,ΔH3相同 |
| D.植物的光合作用通过反应①将热能转化为化学能 |
23-24高二上·全国·课时练习 查看更多[3]
福建省宁德第一中学2023-2024学年高二上学期9月月考化学试题(已下线)专题01 反应热、焓变与热化学方程式【考点清单】(讲+练)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)作业(三) 反应热的计算
更新时间:2023-08-14 21:15:57
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】室温下,将 溶于水会使溶液温度降低,热效应为
溶于水会使溶液温度降低,热效应为 ,将
,将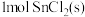 溶于水会使溶液温度升高,热效应为
溶于水会使溶液温度升高,热效应为 ;
; 受热分解的化学方程式为
受热分解的化学方程式为 ,热效应为
,热效应为 。则下列判断正确的是
。则下列判断正确的是
 溶于水会使溶液温度降低,热效应为
溶于水会使溶液温度降低,热效应为 ,将
,将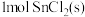 溶于水会使溶液温度升高,热效应为
溶于水会使溶液温度升高,热效应为 ;
; 受热分解的化学方程式为
受热分解的化学方程式为 ,热效应为
,热效应为 。则下列判断正确的是
。则下列判断正确的是A. | B.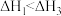 | C. | D. |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在25℃101kPa下,白磷(化学式为P4)、红磷(化学式为P)燃烧的热化学方程式分别为
P4(s)+5O2(g)=P4O10(s);△H=-3093.2kJ/mol
4P(s)+5O2(g)=P4O10(s);△H=-2954.0kJ/mol
由此判断,下列说法正确的是
P4(s)+5O2(g)=P4O10(s);△H=-3093.2kJ/mol
4P(s)+5O2(g)=P4O10(s);△H=-2954.0kJ/mol
由此判断,下列说法正确的是
| A.由红磷转化为白磷是吸热反应,等质量时红磷能量比白磷高 |
| B.由红磷转化为白磷是放热反应,等质量时红磷能量比白磷低 |
| C.由红磷转化为白磷是放热反应,等质量时红磷能量比白磷高 |
| D.由红磷转化为白磷是吸热反应,等质量时红磷能量比白磷低 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】把温度为20℃,浓度为1.0mol/L的硫酸溶液和2.2mol/L的碱液各50mL混合,搅动,测得酸碱混合物的温度变化数据如下(溶液密度为1g/mL,比热容为4.184kJ/(kg·℃))
则NH3+H2O NH3·H2O的∆H为
NH3·H2O的∆H为
| 反应物 | 起始温度T1/℃ | 终止温度T2/℃ |
| H2SO4+NaOH | 20 | 33.6 |
| H2SO4+NH3·H2O | 20 | 32.6 |
 NH3·H2O的∆H为
NH3·H2O的∆H为| A.+4.2kJ | B.+2.1kJ | C.-2.1kJ | D.-4.2kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】已知在10.8g碳不完全燃烧所得气体中,CO占1/3体积,CO2占2/3体积且C(s)+1/2 O2(g)=CO(g),△H=-110 kJ/mol;CO(g)+1/2O2(g)=CO2(g),△H=-280 kJ/mol。与这些碳完全燃烧相比,损失的热量是
| A.39 kJ | B.248 kJ |
| C.84 kJ | D.326 kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】X(g)+3Y(g) 2Z(g)ΔH= -a kJ/mol,一定条件下,将2 mol X和6 mol Y通入2L的恒容密闭容器中,反应5 min,测得Y的物质的量为1.8 mol,下列说法正确的是()
2Z(g)ΔH= -a kJ/mol,一定条件下,将2 mol X和6 mol Y通入2L的恒容密闭容器中,反应5 min,测得Y的物质的量为1.8 mol,下列说法正确的是()
 2Z(g)ΔH= -a kJ/mol,一定条件下,将2 mol X和6 mol Y通入2L的恒容密闭容器中,反应5 min,测得Y的物质的量为1.8 mol,下列说法正确的是()
2Z(g)ΔH= -a kJ/mol,一定条件下,将2 mol X和6 mol Y通入2L的恒容密闭容器中,反应5 min,测得Y的物质的量为1.8 mol,下列说法正确的是()| A.5 min内,Y的平均反应速率为4.2 mol·L-1·s-1 |
| B.第5 min时,X的反应速率为0.14 mol ·L-1·s-1 |
| C.升高温度,Z的分解速率加快 |
| D.5 min内,X和Y反应放出的热量为a kJ |
您最近一年使用:0次




