在一定温度下,对冰醋酸加水稀释的过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示。请回答下列问题:
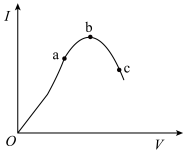
(1)a、b、c三点对应的溶液中,c(H+)由小到大的顺序为___________ 。
(2)a、b、c三点对应的溶液中,CH3COOH的电离程度最大的是___________ 。
(3)若使c点对应的溶液中的c(CH3COO-)增大,则下列措施中,可行的是___________ (填字母,下同)。
A.加热 B.加入NaOH稀溶液 C.加入K2CO3固体
D.加水 E.加入CH3COONa固体 F.加入锌粒
(4)在稀释过程中,随着醋酸浓度的减小,下列始终保持增大趋势的是___________。

(1)a、b、c三点对应的溶液中,c(H+)由小到大的顺序为
(2)a、b、c三点对应的溶液中,CH3COOH的电离程度最大的是
(3)若使c点对应的溶液中的c(CH3COO-)增大,则下列措施中,可行的是
A.加热 B.加入NaOH稀溶液 C.加入K2CO3固体
D.加水 E.加入CH3COONa固体 F.加入锌粒
(4)在稀释过程中,随着醋酸浓度的减小,下列始终保持增大趋势的是___________。
| A.c(H+) | B.n(H+) | C.CH3COOH分子数 | D. |
更新时间:2023-08-14 23:42:04
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】已知: 时,三种酸的电离平衡常数如下表所示:
时,三种酸的电离平衡常数如下表所示:
回答下列问题:
(1) 的电离方程式为
的电离方程式为_______ 。
(2)上述三种酸分子的酸性由强到弱的顺序为_______ (用分子式填写)。
(3)向 溶液中加入
溶液中加入 溶液时,溶液中
溶液时,溶液中
_______ (填“增大”、“减小”或“不变”,下同),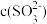
_______ 。
(4)用蒸馏水稀释 的
的 溶液,下列各式表示的数值随水量的增加而减小的是_______(填序号)。
溶液,下列各式表示的数值随水量的增加而减小的是_______(填序号)。
(5)将 通入饱和
通入饱和 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为_______ ;将 通入
通入 溶液中,发生反应的离子方程式为
溶液中,发生反应的离子方程式为_______ 。
(6)向 的
的 溶液中滴加等体积的一定浓度的稀硫酸,此时测得溶液中的
溶液中滴加等体积的一定浓度的稀硫酸,此时测得溶液中的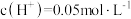 ,则溶液中
,则溶液中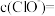
_______  。
。
 时,三种酸的电离平衡常数如下表所示:
时,三种酸的电离平衡常数如下表所示:| 化学式 |  |  |  |
| 电离平衡常数 |   | 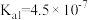 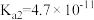 | 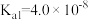 |
回答下列问题:
(1)
 的电离方程式为
的电离方程式为(2)上述三种酸分子的酸性由强到弱的顺序为
(3)向
 溶液中加入
溶液中加入 溶液时,溶液中
溶液时,溶液中
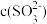
(4)用蒸馏水稀释
 的
的 溶液,下列各式表示的数值随水量的增加而减小的是_______(填序号)。
溶液,下列各式表示的数值随水量的增加而减小的是_______(填序号)。A. | B.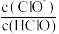 | C. | D. |
 通入饱和
通入饱和 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为 通入
通入 溶液中,发生反应的离子方程式为
溶液中,发生反应的离子方程式为(6)向
 的
的 溶液中滴加等体积的一定浓度的稀硫酸,此时测得溶液中的
溶液中滴加等体积的一定浓度的稀硫酸,此时测得溶液中的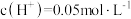 ,则溶液中
,则溶液中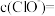
 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】根据下列化合物:①NaOH,②H2SO4,③CH3COOH,④NaCl,⑤CH3COONa,⑥NH4Cl,⑦CH3COONH4,⑧NH4HSO4,⑨NH3•H2O,请回答下列问题:
(1)NH4Cl溶液中离子浓度大小顺序为_____________ 。
(2)常温下,pH=11的CH3COONa溶液中,水电离出来的c(OH﹣)=_________ ;在pH=3的CH3COOH溶液中,水电离出来的c(H+)=___________ 。
(3)已知水存在如下平衡:H2O+H2O⇌H3O++OH﹣△H>0,现欲使平衡向右移动,且所得溶液显酸性,选择的下列方法是_________ 。
A.向水中加入NaHSO4固体 B.向水中加NaHCO3固体
C.加热至100℃[其中c(H+)=1×10﹣6mol/L] D.向水中加入NH4Cl固体
(4)在常温下,NH3•H2O的电离常数为1.810-5,若浓度均为0.1mol/L、等体积的NaOH和NH3•H2O分别加水稀释m倍、n倍,稀释后两种溶液的pH都变成9,则 m_________ n(填“<”、“>”或“=”)。
(5)物质的量浓度相同的⑥、⑦、⑧、⑨四种稀溶液中,NH4+浓度由大到小的顺序是(填序号)_____ 。
(1)NH4Cl溶液中离子浓度大小顺序为
(2)常温下,pH=11的CH3COONa溶液中,水电离出来的c(OH﹣)=
(3)已知水存在如下平衡:H2O+H2O⇌H3O++OH﹣△H>0,现欲使平衡向右移动,且所得溶液显酸性,选择的下列方法是
A.向水中加入NaHSO4固体 B.向水中加NaHCO3固体
C.加热至100℃[其中c(H+)=1×10﹣6mol/L] D.向水中加入NH4Cl固体
(4)在常温下,NH3•H2O的电离常数为1.810-5,若浓度均为0.1mol/L、等体积的NaOH和NH3•H2O分别加水稀释m倍、n倍,稀释后两种溶液的pH都变成9,则 m
(5)物质的量浓度相同的⑥、⑦、⑧、⑨四种稀溶液中,NH4+浓度由大到小的顺序是(填序号)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】 时,三种酸的电离平衡常数如下:
时,三种酸的电离平衡常数如下:
回答下列问题:
(1)一般情况下,当温度升高时,
_____ (填“增大”“减小”或“不变”)。
(2)用蒸馏水稀释 的次氯酸,下列各式表示的数值随水量的增加而增大的是_____。(填字母序号,下同)
的次氯酸,下列各式表示的数值随水量的增加而增大的是_____。(填字母序号,下同)
(3)下列能使醋酸溶液中 的电离程度增大,而电离平衡常数不变的是_____。
的电离程度增大,而电离平衡常数不变的是_____。
(4)依上表数据写出向NaClO溶液中通少量 的离子方程式:
的离子方程式:_____ 。
 时,三种酸的电离平衡常数如下:
时,三种酸的电离平衡常数如下:| 化学式 | HClO |  |  |
| 电离平衡常数 |  |  | 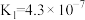 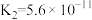 |
(1)一般情况下,当温度升高时,

(2)用蒸馏水稀释
 的次氯酸,下列各式表示的数值随水量的增加而增大的是_____。(填字母序号,下同)
的次氯酸,下列各式表示的数值随水量的增加而增大的是_____。(填字母序号,下同)A. | B. | C.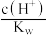 | D. |
 的电离程度增大,而电离平衡常数不变的是_____。
的电离程度增大,而电离平衡常数不变的是_____。| A.升高温度 | B.加水稀释 |
C.加少量的 固体 固体 | D.加少量氢氧化钠浓溶液 |
 的离子方程式:
的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】水是生命的源泉、工业的血液、城市的血脉。要保护好河流,因为河水是主要的饮用水源,污染物通过饮用水可直接毒害人体,也可通过食物链和灌溉农田间接危及健康。请回答下列问题:
(1)纯水在T ℃时,pH=6,该温度下0.1 mol·L-1的NaOH溶液中,由水电离出的c(OH-)=________ mol·L-1。
(2)25 ℃时,向水中加入少量碳酸钠固体,得到pH为11的溶液,其主要水解反应的离子方程式为____________________ ,由水电离出的c(OH-)=________ mol·L-1。
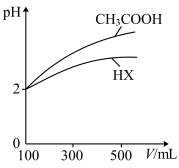
(3)体积均为100 mL、pH均为2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离平衡常数________ (填“大于”“小于”或“等于”)CH3COOH的电离平衡常数。
(4)电离平衡常数是衡量弱电解质电离程度的物理量。已知:
在25 ℃时,有等浓度的NaCN溶液、Na2CO3溶液和CH3COONa溶液,三溶液的pH由大到小的顺序为________ (用化学式表示)。

(1)纯水在T ℃时,pH=6,该温度下0.1 mol·L-1的NaOH溶液中,由水电离出的c(OH-)=
(2)25 ℃时,向水中加入少量碳酸钠固体,得到pH为11的溶液,其主要水解反应的离子方程式为
(3)体积均为100 mL、pH均为2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离平衡常数
(4)电离平衡常数是衡量弱电解质电离程度的物理量。已知:
| 化学式 | 电离常数(25 ℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
在25 ℃时,有等浓度的NaCN溶液、Na2CO3溶液和CH3COONa溶液,三溶液的pH由大到小的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】弱电解质的研究是重要课题。
(1)①25℃时,已知不同pH条件下,水溶液中碳元素的存在形态如图所示。下列说法不正确的是______ (填字母)。

a.pH=8时,溶液中含碳元素的微粒主要是HCO
b.A点溶液中H2CO3和HCO 浓度相同
浓度相同
c.当c(HCO )=c(CO
)=c(CO )时,c(H+)>c(OH-)
)时,c(H+)>c(OH-)
②向上述pH=8.4的水溶液中加入NaOH溶液时发生反应的离子方程式是______ 。
(2)H2CO3以及其他部分弱酸的电离平衡常数如表:
①H2S、H2CO3、HClO的酸性由强到弱的顺序为______ 。
②将少量CO2气体通入NaClO溶液中,写出该反应的离子方程式:______ 。
(3)常温下,已知0.1mol/L一元酸HCOOH(甲酸)溶液中 =1×10-8。
=1×10-8。
①0.1mol/LHCOOH溶液的pH=______ 。
②取10mL0.1mol/L的HCOOH溶液稀释至100倍,下列有关说法正确的是______ (填字母)。
A.所有离子的浓度在稀释过程中都会减小 B.稀释后溶液的pH=5
C.稀释后甲酸的电离度会增大 D.与稀释前比较,稀释后水的电离程度增大
(4)现有0.1mol•L-1氨水10mL,加蒸馏水稀释到1L后,下列变化中正确的是______ 。
①电离程度增大 ②c(NH3•H2O)增大 ③NH 数目增多 ④c(OH-)增大 ⑤导电性增强 ⑥
数目增多 ④c(OH-)增大 ⑤导电性增强 ⑥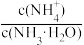 增大 ⑦
增大 ⑦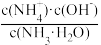 减小
减小
(1)①25℃时,已知不同pH条件下,水溶液中碳元素的存在形态如图所示。下列说法不正确的是

a.pH=8时,溶液中含碳元素的微粒主要是HCO

b.A点溶液中H2CO3和HCO
 浓度相同
浓度相同c.当c(HCO
 )=c(CO
)=c(CO )时,c(H+)>c(OH-)
)时,c(H+)>c(OH-)②向上述pH=8.4的水溶液中加入NaOH溶液时发生反应的离子方程式是
(2)H2CO3以及其他部分弱酸的电离平衡常数如表:
| 弱酸 | H2S | H2CO3 | HClO |
| 电离平衡常数(25℃) | Ka1=1.1×10-7 Ka2=1.3×10-13 | Ka1=4.5×10-7 Ka2=4.7×10-11 | Ka=4.8×10-8 |
②将少量CO2气体通入NaClO溶液中,写出该反应的离子方程式:
(3)常温下,已知0.1mol/L一元酸HCOOH(甲酸)溶液中
 =1×10-8。
=1×10-8。①0.1mol/LHCOOH溶液的pH=
②取10mL0.1mol/L的HCOOH溶液稀释至100倍,下列有关说法正确的是
A.所有离子的浓度在稀释过程中都会减小 B.稀释后溶液的pH=5
C.稀释后甲酸的电离度会增大 D.与稀释前比较,稀释后水的电离程度增大
(4)现有0.1mol•L-1氨水10mL,加蒸馏水稀释到1L后,下列变化中正确的是
①电离程度增大 ②c(NH3•H2O)增大 ③NH
 数目增多 ④c(OH-)增大 ⑤导电性增强 ⑥
数目增多 ④c(OH-)增大 ⑤导电性增强 ⑥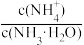 增大 ⑦
增大 ⑦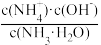 减小
减小| A.①②③ | B.①③⑤ | C.①③⑥ | D.②④⑥ |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】根据电离平衡常数(用Ka表示)的大小可以判断弱电解质的相对强弱。25℃时,有关物质的电离平衡常数如下表所示:
(1)25℃时,H2S、HClO、H2CO3、H2SO3的酸性由强到弱的顺序为:_______ 。
(2)25℃时,0.01mol·L-1的HClO溶液中的c(H+)为_______ ,将此HClO溶液加水稀释(设温度不变),下列各量增大的是_______ (填写字母)。
A.c(H+) B.c(H+)·c(OH-) C. D.
D.
(3)相同条件下,0.1mol·L-1下列溶液中,pH最大的是_______。
(4)根据H2SO3的电离平衡常数计算25℃时0.06mol·L-1Na2SO3溶液的pH=_______ 。(忽略 的第二步水解)
的第二步水解)
(5)25℃时,向NaClO溶液中通入少量CO2,发生反应的离子方程式为_______ 。
| 酸 | H2S | HClO | H2CO3 | H2SO3 |
| 电离平衡常数(25℃) | Ka1=1.1×10-7Ka2=1.3×10-13 | Ka1=4.0×10-8 | Ka1=4.5×10-7 Ka2=4.7×10-11 | Ka1=1.4×10-2 Ka2=6.0×10-8 |
(2)25℃时,0.01mol·L-1的HClO溶液中的c(H+)为
A.c(H+) B.c(H+)·c(OH-) C.
 D.
D.
(3)相同条件下,0.1mol·L-1下列溶液中,pH最大的是_______。
| A.NaHSO4 | B.NaCl | C.Na2CO3 | D.Na2SO3 |
 的第二步水解)
的第二步水解)(5)25℃时,向NaClO溶液中通入少量CO2,发生反应的离子方程式为
您最近一年使用:0次



