下表是几种常见弱酸的电离平衡常数(25℃),回答下列各题:
(1)当温度升高时,K值_____ (填“增大”“减小”或“不变”)。
(2)下列能使醋酸溶液中CH3COOH的电离程度增大,而电离平衡常数不变的操作是_____ (填序号)。
A.升高温度
B.加水稀释
C.加少量的CH3COONa固体
D.加少量冰醋酸
E.加氢氧化钠固体
(3)已知草酸是一种二元弱酸,其电离常数K1=5.4×10-2,K2=5.4×10-5,写出草酸的电离方程式_____ 、_____ ,试从电离平衡移动的角度解释K1≫K2的原因_____ 。
(4)用食醋浸泡有水垢的水壶,可以清除其中的水垢,通过该事实_____ (填“能”或“不能”)比较醋酸与碳酸的酸性强弱,请设计一个简单的实验验证醋酸与碳酸的酸性强弱。方案:_____ 。
| 酸 | CH3COOH | HNO2 | HCN | HClO |
| 电离平衡常数(Ka) | 1.8×10-5 | 4.6×10-4 | 5×10-10 | 3×10-8 |
(2)下列能使醋酸溶液中CH3COOH的电离程度增大,而电离平衡常数不变的操作是
A.升高温度
B.加水稀释
C.加少量的CH3COONa固体
D.加少量冰醋酸
E.加氢氧化钠固体
(3)已知草酸是一种二元弱酸,其电离常数K1=5.4×10-2,K2=5.4×10-5,写出草酸的电离方程式
(4)用食醋浸泡有水垢的水壶,可以清除其中的水垢,通过该事实
23-24高二上·全国·课时练习 查看更多[1]
更新时间:2023-08-15 17:25:58
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】25℃时,50mL 0.10mol/L的醋酸中存在着如下平衡:CH3COOH  CH3COO―+H+。若分别作如下改变,对上述平衡有何影响
CH3COO―+H+。若分别作如下改变,对上述平衡有何影响
(1)加入少量冰醋酸,平衡将_______________________ ,溶液中c(H+)将________________ ;
(2)加入一定量蒸馏水,平衡将__________________ ,溶液中c(H+)将__________ ;
(3)加入少量0.10mol/L盐酸,平衡将________________ ,溶液中c(H+)将_________________ ;
(4)加入20 mL 0.10mol/L的NaOH溶液,平衡将__________________ ,溶液中c(H+)将__________________ 。
 CH3COO―+H+。若分别作如下改变,对上述平衡有何影响
CH3COO―+H+。若分别作如下改变,对上述平衡有何影响(1)加入少量冰醋酸,平衡将
(2)加入一定量蒸馏水,平衡将
(3)加入少量0.10mol/L盐酸,平衡将
(4)加入20 mL 0.10mol/L的NaOH溶液,平衡将
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】描述弱电解质电离情况可以用电离度和电离平衡常数表示,下表是常温下几种弱酸的电离平衡常数(Ka)和弱碱的电离平衡常数(Kb)
下表是常温下几种难(微)溶物的溶度积常数(Ksp):
请回答下列问题:
(l)写出HCN的电离方程式:___________ ,HClO的电子式__________ 。
(2)表中所给的四种酸中,酸性最强的是__________ (用化学式表示)。下列能使醋酸溶液中CH3COOH的电离程度增大且电离常数改变的操作是__________ (填字母序号)。
A.加少量冰醋酸B.降低温度C.加水稀释D.升高温度E.加少量的CH3COONa固体
(3)CH3COONH4的水溶液呈__________ (选填“酸性”、“中性”或“碱性”),该溶液中存在的各离子浓度大小关系是__________ 。
(4)工业中常将BaSO4转化为BaCO3后,再将其制成各种可溶性的钡盐(如BaCl2)。具体做法是用饱和的纯碱溶液浸泡BaSO4粉末,并不断补充纯碱,最后BaSO4转化为BaCO3。现有足量BasO4悬浊液,在该悬浊液中加纯碱粉末并不断搅拌,为使SO42-物质的量浓度不小于0.02 mol·L-1,则溶液中CO32-物质的量浓度应≥__________ mol·L-1。
| 酸或碱 | 电离平衡常数(Ka或Kb) |
| CH3COOH | 1.8×10-5 |
| HNO2 | 4.6×10-4 |
| HCN | 5×10-10 |
| HClO | 3×10-8 |
| NH3∙H2O | 1.8×10-5 |
下表是常温下几种难(微)溶物的溶度积常数(Ksp):
| 难(微)溶物 | 溶度积常数(Ksp) |
| BaSO4 | 1×10-10 |
| BaCO3 | 2.6×10-9 |
| CaSO4 | 7×10-5 |
| CaCO3 | 5×10-9 |
请回答下列问题:
(l)写出HCN的电离方程式:
(2)表中所给的四种酸中,酸性最强的是
A.加少量冰醋酸B.降低温度C.加水稀释D.升高温度E.加少量的CH3COONa固体
(3)CH3COONH4的水溶液呈
(4)工业中常将BaSO4转化为BaCO3后,再将其制成各种可溶性的钡盐(如BaCl2)。具体做法是用饱和的纯碱溶液浸泡BaSO4粉末,并不断补充纯碱,最后BaSO4转化为BaCO3。现有足量BasO4悬浊液,在该悬浊液中加纯碱粉末并不断搅拌,为使SO42-物质的量浓度不小于0.02 mol·L-1,则溶液中CO32-物质的量浓度应≥
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某小组研究25℃下CH3COOH 电离平衡的影响因素。
提出假设:稀释CH3COOH 溶液或改变CH3COO⁻浓度,CH3COOH电离平衡会发生移动。
设计方案并完成实验:用浓度均为0.1mol/L 的 CH3COOH和 CH3COONa溶液,按下表配制总体积相同的系列溶液。
测定 pH,记录数据。
(1)根据表中信息, 补充数据: a=___________ , b=___________ 。
(2)由实验I和II可知,稀释CH3COOH 溶液, 电离平衡_____ (填“正”或“逆”)向移动,结合表中数据,给出判断理由:___________ 。由实验II~VIII可知,增大 CH3COO⁻浓度,CH3COOH电离平衡向逆向移动。[实验结论]假设成立
提出假设:稀释CH3COOH 溶液或改变CH3COO⁻浓度,CH3COOH电离平衡会发生移动。
设计方案并完成实验:用浓度均为0.1mol/L 的 CH3COOH和 CH3COONa溶液,按下表配制总体积相同的系列溶液。
测定 pH,记录数据。
| 序号 | V(CH3COOH)/mL | V(CH3COONa)/mL | V(H2O)/mL | n(CH3COONa):n(CH3COOH) | pH |
| I | 40.00 | / | / | 0 | 2.86 |
| Ⅱ | 4.00 | / | 36.00 | 0 | 3.36 |
| 实验III~VI省略 | |||||
| Ⅶ | 4.00 | a | b | 3:4 | 4.53 |
| VIII | 4.00 | 4.00 | 32.00 | 1:1 | 4.65 |
(1)根据表中信息, 补充数据: a=
(2)由实验I和II可知,稀释CH3COOH 溶液, 电离平衡
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.现有常温下pH=2的HCl溶液甲和pH=2的CH3COOH溶液乙,请根据下列操作回答问题:
(1)常温下0.1mol·L-1的CH3COOH溶液加水稀释过程中,下列表达式的数据一定变小的是_____ 。
A.c(H+) B. C.c(H+)·c(OH-)
C.c(H+)·c(OH-)
(2)取10mL的乙溶液,加入等体积的水,CH3COOH的电离平衡________ (填“向左”“向右”或“不”)移动;另取10mL的乙溶液,加入少量无水醋酸钠固体(假设加入固体前后溶液体积保持不变),待固体溶解后,溶液中 的比值将
的比值将________ (填“增大”“减小”或“无法确定”)。
(3)取等体积的甲、乙两溶液,分别用等浓度的NaOH稀溶液中和,则消耗NaOH溶液体积的大小关系为V(甲)________ (填“>”“<”或“=”)V(乙)。
(4)已知25℃时,下列酸的电离平衡常数如下:
下列四种离子结合H+能力最强的是________ 。
A.HCO B.CO
B.CO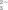 C.ClO- D.CH3COO-
C.ClO- D.CH3COO-
写出下列反应的离子方程式:HClO+Na2CO3(少量):______________________
Ⅱ.室温下,0.1 mol·L-l的KOH溶液滴10.00mL 0.10 mol·L-l H2C2O4 (二元弱酸)溶液,所得滴定曲线如图(混合溶液的体积可看成混合前溶液的体积之和)。请回答下列问题:
(5)点③所示溶液中所有离子的浓度由大到小的顺序为:________________________ 。点④所示溶液中:c(K+)+c(H2C2O4)+c(HC2O4−)+c(C2O42−)=________ mol/L。
(1)常温下0.1mol·L-1的CH3COOH溶液加水稀释过程中,下列表达式的数据一定变小的是
A.c(H+) B.
 C.c(H+)·c(OH-)
C.c(H+)·c(OH-) (2)取10mL的乙溶液,加入等体积的水,CH3COOH的电离平衡
 的比值将
的比值将(3)取等体积的甲、乙两溶液,分别用等浓度的NaOH稀溶液中和,则消耗NaOH溶液体积的大小关系为V(甲)
(4)已知25℃时,下列酸的电离平衡常数如下:
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.8×10-5 | K1=4.3×10-7 K2=4.7×10-11 | 3.0×10-8 |
下列四种离子结合H+能力最强的是
A.HCO
 B.CO
B.CO C.ClO- D.CH3COO-
C.ClO- D.CH3COO-写出下列反应的离子方程式:HClO+Na2CO3(少量):
Ⅱ.室温下,0.1 mol·L-l的KOH溶液滴10.00mL 0.10 mol·L-l H2C2O4 (二元弱酸)溶液,所得滴定曲线如图(混合溶液的体积可看成混合前溶液的体积之和)。请回答下列问题:

(5)点③所示溶液中所有离子的浓度由大到小的顺序为:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下图表示在0.1 mol·L-1的某一元弱酸溶液中,溶液的pH随加入NaOH溶液的体积V的变化情况。
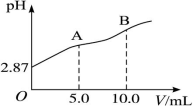
(1)恰好完全中和时(B点)溶液的pH_______ 7(填“>”“<”或“=”),理由是______________ 。
(2)当弱电解质AB在水溶液里达到平衡时:AB A++B-,即有K电离=
A++B-,即有K电离=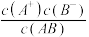 ,一定温度下,电离常数不随溶液浓度改变而改变,求本题中一元弱酸的电离常数
,一定温度下,电离常数不随溶液浓度改变而改变,求本题中一元弱酸的电离常数______ 。
(3)求A点的pH。(lg1.35=0.13 lg1.8=0.26)____________

(1)恰好完全中和时(B点)溶液的pH
(2)当弱电解质AB在水溶液里达到平衡时:AB
 A++B-,即有K电离=
A++B-,即有K电离=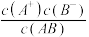 ,一定温度下,电离常数不随溶液浓度改变而改变,求本题中一元弱酸的电离常数
,一定温度下,电离常数不随溶液浓度改变而改变,求本题中一元弱酸的电离常数(3)求A点的pH。(lg1.35=0.13 lg1.8=0.26)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】根据所学知识回答问题
Ⅰ、常温下,用“酸性”“碱性”“中性”或“不确定”填空。
(1)相同浓度的HCl和NaOH溶液等体积混合。___________ 。
(2)pH=2的HCl和pH=12的NaOH溶液等体积混合。___________ 。
(3)pH=2的HCl和pH=12的NH3·H2O等体积混合。___________ 。
Ⅱ、25 ℃时,部分物质的电离平衡常数如表所示:
(4)上述五种酸的酸性由强到弱的顺序是___________ 。
(5)该温度下,0.10 mol·L-1 HNO2溶液中的c(H+)=___________ mol·L-1。
(6)25 ℃时,向NaClO溶液中通入少量的CO2,发生反应的离子方程式为___________ 。
(7)下列能使醋酸溶液中CH3COOH的电离程度增大,而电离平衡常数不变的操作是___________ (填序号)。
A.升高温度 B.加水稀释 C.加少量CH3COONa固体
D.加入少量冰醋酸 E.加入少量NaOH固体(温度不变)
Ⅰ、常温下,用“酸性”“碱性”“中性”或“不确定”填空。
(1)相同浓度的HCl和NaOH溶液等体积混合。
(2)pH=2的HCl和pH=12的NaOH溶液等体积混合。
(3)pH=2的HCl和pH=12的NH3·H2O等体积混合。
Ⅱ、25 ℃时,部分物质的电离平衡常数如表所示:
化学式 | 电离平衡常数(Ka或Kb) |
CH3COOH | 1.8×10-5 |
HNO2 | 4.9×10-4 |
HCN | 5×10-10 |
HClO | 3×10-8 |
H2CO3 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
NH3·H2O | 1.8×10-5 |
(5)该温度下,0.10 mol·L-1 HNO2溶液中的c(H+)=
(6)25 ℃时,向NaClO溶液中通入少量的CO2,发生反应的离子方程式为
(7)下列能使醋酸溶液中CH3COOH的电离程度增大,而电离平衡常数不变的操作是
A.升高温度 B.加水稀释 C.加少量CH3COONa固体
D.加入少量冰醋酸 E.加入少量NaOH固体(温度不变)
您最近一年使用:0次



