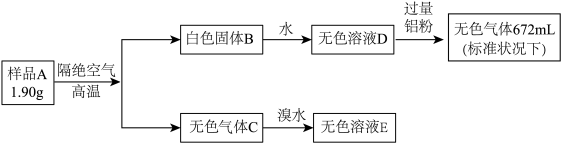
某化合物A含有3种元素,现有研究小组对其进行如下实验:
(1)组成A的元素有___________ (写元素符号)。
(2)A的化学式为___________ 。
(3)写出气体C与溴水反应的离子方程式___________ 。
(4)样品A与双氧水反应,得到溶液F,溶液F的溶质之一为强酸,写出化学方程式;___________ 。
(1)组成A的元素有
(2)A的化学式为
(3)写出气体C与溴水反应的离子方程式
(4)样品A与双氧水反应,得到溶液F,溶液F的溶质之一为强酸,写出化学方程式;
更新时间:2023-08-16 18:32:18
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】铼是一种熔点高、耐磨、耐腐蚀的金属,广泛用于航天器的结构材料和石油裂化的催化剂等。工业上用富铼渣(主要含 制得铼粉,其工艺流程如下图所示:
制得铼粉,其工艺流程如下图所示:

回答下列问题:
(1)提高铼浸出率的方法有_______ 、_______ 。
(2)浸出反应中 转化为两种强酸,请写出铼浸出反应的离子方程式
转化为两种强酸,请写出铼浸出反应的离子方程式_______ 。浸渣的主要成分是_______ 。酸浸相同时间,测得铼的浸出率与温度关系如图所示,分析T1℃时铼的浸出率最高的原因是_______ 。

(3)废液中含有的金属离子主要有_______ 。
(4)实验室中,操作Ⅲ所用主要仪器名称为_______ ,已知高铼酸铵是白色片状晶体,微溶于冷水,易溶于热水。欲得纯度更高的高铼酸铵晶体,可通过_______ 方法提纯。
(5)高铼酸铵热分解得到 写出氢气在800℃时还原
写出氢气在800℃时还原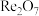 ,制得铼粉的化学方程式
,制得铼粉的化学方程式_______ 。
(6)整个工艺流程中可循环利用的物质有:H2SO4、_______ 、_______ 。
 制得铼粉,其工艺流程如下图所示:
制得铼粉,其工艺流程如下图所示:
回答下列问题:
(1)提高铼浸出率的方法有
(2)浸出反应中
 转化为两种强酸,请写出铼浸出反应的离子方程式
转化为两种强酸,请写出铼浸出反应的离子方程式
(3)废液中含有的金属离子主要有
(4)实验室中,操作Ⅲ所用主要仪器名称为
(5)高铼酸铵热分解得到
 写出氢气在800℃时还原
写出氢气在800℃时还原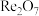 ,制得铼粉的化学方程式
,制得铼粉的化学方程式(6)整个工艺流程中可循环利用的物质有:H2SO4、
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】实验室利用CuCl2溶液与SO2气体制备CuCl的装置如图所示(夹持装置略)。
已知氯化亚铜是一种白色固体,微溶于水,不溶于酒精;在空易气中被迅速氧化。

实验步骤:
I.打开止水夹,通入一段时间N 2后,关上止水夹;打开分液漏斗旋塞,向三颈瓶中加盐酸调pH至2~3,打开止水夹,通入SO2,溶液中产生白色沉淀;待反应完全后,再通一段时间的N 2。
II.反应混合液经一系列过程得CuCl粗产品,纯化后得CuCl产品。
回答下列问题:
(1)①步骤I中反应前通入氮气的目的是___________ 。
②装置A中发生反应的离子方程式为___________ 。
③装置B的作用为___________ ;装置C中的试剂为___________ 。
(2)步骤II中一系列过程为___________。
(3)现取实验中的CuCl2溶液制得CuCl2·xH2O。
①CuCl2·xH2O晶体直接加热能否得到纯净的无水CuCl2 (填“能”或“不能”,若不能请说明正确的方法)___________ 。
②为测定x值进行如下实验:a.用电子天平称取3.420g的CuCl2·xH2O晶体;b.在坩埚中充分灼烧;c.在干燥器中冷却;d.称量所得黑色固体质量;e.重复b~d操作直至连续两次称量差值不超过0.001g。若最终得到黑色固体质量为1.600g,则
___________ 。
已知氯化亚铜是一种白色固体,微溶于水,不溶于酒精;在空易气中被迅速氧化。

实验步骤:
I.打开止水夹,通入一段时间N 2后,关上止水夹;打开分液漏斗旋塞,向三颈瓶中加盐酸调pH至2~3,打开止水夹,通入SO2,溶液中产生白色沉淀;待反应完全后,再通一段时间的N 2。
II.反应混合液经一系列过程得CuCl粗产品,纯化后得CuCl产品。
回答下列问题:
(1)①步骤I中反应前通入氮气的目的是
②装置A中发生反应的离子方程式为
③装置B的作用为
(2)步骤II中一系列过程为___________。
| A.减压过滤 水洗 干燥 | B.普通过滤 水洗 干燥 |
| C.减压过滤 乙醇洗 干燥 | D.普通过滤 乙醇洗 干燥 |
①CuCl2·xH2O晶体直接加热能否得到纯净的无水CuCl2 (填“能”或“不能”,若不能请说明正确的方法)
②为测定x值进行如下实验:a.用电子天平称取3.420g的CuCl2·xH2O晶体;b.在坩埚中充分灼烧;c.在干燥器中冷却;d.称量所得黑色固体质量;e.重复b~d操作直至连续两次称量差值不超过0.001g。若最终得到黑色固体质量为1.600g,则

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】铋(Bi)因无毒与不致癌性而有很多特殊用途,其化合物广泛应用于电子、医药等领域。由辉铋矿(主要成分为 ,含杂质
,含杂质 等)制备
等)制备 的工艺如下:
的工艺如下:

回答下列问题:
(1)铋元素位于元素周期表第六周期ⅤA族,用轨道表示式表示基态铋原子最外层结构___________ ,铋的氢化物的热稳定性___________ (填“大于”或“小于”)氨。
(2)“浸出”前,辉铋矿会先进行粉碎,目的是___________ 。
(3)已知“浸出液”中含有 离子,则“浸出”时
离子,则“浸出”时 与
与 溶液反应的化学方程式为
溶液反应的化学方程式为___________ 。
(4)“精炼”时,粗铋应作___________ 材料(填“阴极”或“阳极”)。
(5)碱式硝酸铋直接灼烧也能得到 ,上述工艺中转化为碱式碳酸铋再灼烧,除了能改良产品性状,另一优点是
,上述工艺中转化为碱式碳酸铋再灼烧,除了能改良产品性状,另一优点是___________ ;“母液2”中可回收的主要物质是___________ (填写物质的化学式)。
 ,含杂质
,含杂质 等)制备
等)制备 的工艺如下:
的工艺如下:
回答下列问题:
(1)铋元素位于元素周期表第六周期ⅤA族,用轨道表示式表示基态铋原子最外层结构
(2)“浸出”前,辉铋矿会先进行粉碎,目的是
(3)已知“浸出液”中含有
 离子,则“浸出”时
离子,则“浸出”时 与
与 溶液反应的化学方程式为
溶液反应的化学方程式为(4)“精炼”时,粗铋应作
(5)碱式硝酸铋直接灼烧也能得到
 ,上述工艺中转化为碱式碳酸铋再灼烧,除了能改良产品性状,另一优点是
,上述工艺中转化为碱式碳酸铋再灼烧,除了能改良产品性状,另一优点是
您最近一年使用:0次
【推荐1】化合物X•3H2O是一种黄色晶体,X由四种元素组成。X•3H2O晶体的摩尔质量在400~500g/mol之间。取一定量的X•3H2O晶体完成如图转化,其中A为无色有毒气体,B、C、D是三种酸根相同的盐,B中阳离子具有较强的还原性,C溶液的焰色反应为紫色。
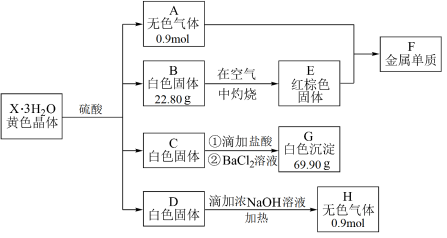
(1)A与E反应生成F的化学反应在工业上可以用来___________ 。
(2)B的化学式为___________ 。
(3)单质F与过量稀硝酸反应的化学方程式为___________ 。
(4)实验室制备气体H的化学方程式是___________ 。
(5)已知该黄色晶体受热脱水过程的热重曲线(样品质量随温度的变化曲线)如图所示。

试确定150℃时固体物质的化学式___________ 。
(6)查阅资料知:该晶体可用作食盐中的抗结剂,虽然其自身毒性很低,但其水溶液与酸反应放出极毒的气体;加热至一定温度时能分解产生剧毒物质。据此判断,烹饪食品时应注意的问题是___________ 。

(1)A与E反应生成F的化学反应在工业上可以用来
(2)B的化学式为
(3)单质F与过量稀硝酸反应的化学方程式为
(4)实验室制备气体H的化学方程式是
(5)已知该黄色晶体受热脱水过程的热重曲线(样品质量随温度的变化曲线)如图所示。

试确定150℃时固体物质的化学式
(6)查阅资料知:该晶体可用作食盐中的抗结剂,虽然其自身毒性很低,但其水溶液与酸反应放出极毒的气体;加热至一定温度时能分解产生剧毒物质。据此判断,烹饪食品时应注意的问题是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
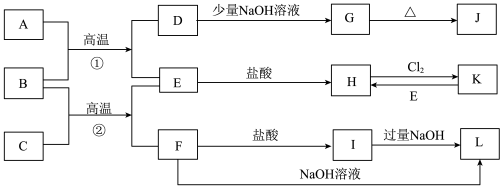
【推荐2】下图中,B、D、E、F、G是氧化物,F、K是氢化物,C、H是日常生活中常见的金属单质,J是黄绿色气态单质,M与氨水反应生成的O是白色沉淀。在B、H、L、M、N、O中含有同种元素,I是基础化学工业的重要产品(图中部分反应物和生成物没有列出)。
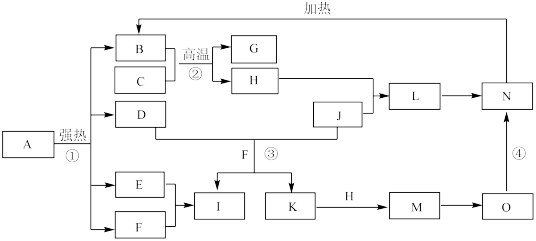
请按要求回答:
(1)H元素在周期表中的位置_____________________________ 。
(2)反应③的离子方程式__________________________________ ;
反应④的化学方程式______________________ 。
(3)实验室用固体L配制溶液的方法是:____________________ 。
(4)由L的饱和溶液可以制得胶体,胶体中粒子直径的大小范围是____________ 。若要提纯该胶体,采用的方法叫_______ 。

请按要求回答:
(1)H元素在周期表中的位置
(2)反应③的离子方程式
反应④的化学方程式
(3)实验室用固体L配制溶液的方法是:
(4)由L的饱和溶液可以制得胶体,胶体中粒子直径的大小范围是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐1】某实验小组利用如图装置模拟古法硫酸生产方法并进行SO2性质探究。
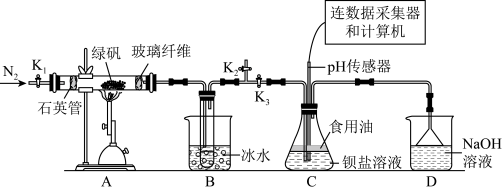 -
-
已知A中反应的化学方程式2FeSO4•7H2O Fe2O3+SO2↑+SO3↑+14H2O。
Fe2O3+SO2↑+SO3↑+14H2O。
实验开始前打开活塞K1、K2,关闭活塞K3,通入一段时间N2后,关闭活塞K1、K2,打开活区K3,高温加热绿矾。
完成下列填空:
(1)先通入一段时间N2的目的是____ ;D装置的作用____ 。
(2)B中所得硫酸溶液的质量分数理论值为____ (保留三位小数)。
为探究SO2与钡盐溶液的反点,在装置C中先后四次加入不同的溶液:
得到如图pH-t图:
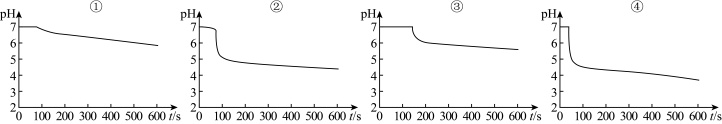
(3)曲线①显缓慢下降趋势,这是因为____ 。曲线②出现骤降,表明溶液中生成了____ (填物质名称)。
(4)对比分析上述四组数据,可得出的结论是____ (任写2条)。
(5)为对接气法收集到的SO2气体进行含量测定,将2240mL(已折算为标准状况)通入足量的Ba(NO3)2溶液中,经过滤、洗涤、烘干,最终得到沉淀20.97g,则SO2气体的体积分数为____ 。若该实验数据较实际值偏大,则可能的原因是____ (选填编号)。
a.气体通入速率过快 b.未用食用油覆盖液面
c.收集的气体中有CO2 d.沉淀未进行恒重操作
 -
-已知A中反应的化学方程式2FeSO4•7H2O
 Fe2O3+SO2↑+SO3↑+14H2O。
Fe2O3+SO2↑+SO3↑+14H2O。实验开始前打开活塞K1、K2,关闭活塞K3,通入一段时间N2后,关闭活塞K1、K2,打开活区K3,高温加热绿矾。
完成下列填空:
(1)先通入一段时间N2的目的是
(2)B中所得硫酸溶液的质量分数理论值为
为探究SO2与钡盐溶液的反点,在装置C中先后四次加入不同的溶液:
| ① | ② | ③ | ④ |
| 已煮沸的BaCl2溶液 | 未煮沸的BaCl2溶液 | 已煮沸的Ba(NO3)2溶液 | 未煮沸的Ba(NO3)2溶液 |
| 注:锥形瓶中溶液体积相同,钡盐溶液浓度相同;油层厚度一致,通入SO2流速一致。 | |||

(3)曲线①显缓慢下降趋势,这是因为
(4)对比分析上述四组数据,可得出的结论是
(5)为对接气法收集到的SO2气体进行含量测定,将2240mL(已折算为标准状况)通入足量的Ba(NO3)2溶液中,经过滤、洗涤、烘干,最终得到沉淀20.97g,则SO2气体的体积分数为
a.气体通入速率过快 b.未用食用油覆盖液面
c.收集的气体中有CO2 d.沉淀未进行恒重操作
您最近一年使用:0次
【推荐2】回答下列问题:
(1)利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。某工厂对制革工业污泥中 (Ⅲ)的处理工艺流程如下:
(Ⅲ)的处理工艺流程如下:
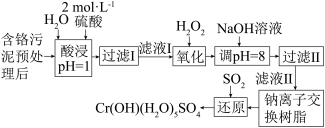
已知:硫酸浸取液中的金属离子主要是 ,其次是
,其次是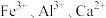 和
和 。
。
① 的作用是将滤液Ⅰ中的
的作用是将滤液Ⅰ中的 转化为
转化为 ,写出此反应的离子方程式:
,写出此反应的离子方程式:_______ 。
②写出上述流程中用 进行还原时发生反应的离子方程式:
进行还原时发生反应的离子方程式:_______ 。
(2) 常用作陶瓷材料,可由锆英砂(主要成分为
常用作陶瓷材料,可由锆英砂(主要成分为 ,也可表示为
,也可表示为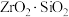 ,还含少量
,还含少量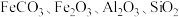 等杂质)通过如下方法制取:
等杂质)通过如下方法制取:
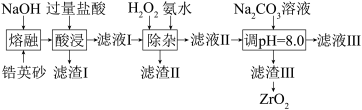
已知: 能与烧碱反应生成可溶于水的
能与烧碱反应生成可溶于水的 ,
, 与酸反应生成
与酸反应生成 。
。
①“熔融”过程中, 发生反应的化学方程式为
发生反应的化学方程式为_______ 。
②滤渣Ⅲ的成分是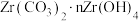 。“调
。“调 ”时,所发生反应的离子方程式为
”时,所发生反应的离子方程式为_______ 。滤渣Ⅲ制备 的方法是
的方法是_______ 。
(1)利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。某工厂对制革工业污泥中
 (Ⅲ)的处理工艺流程如下:
(Ⅲ)的处理工艺流程如下:
已知:硫酸浸取液中的金属离子主要是
 ,其次是
,其次是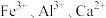 和
和 。
。①
 的作用是将滤液Ⅰ中的
的作用是将滤液Ⅰ中的 转化为
转化为 ,写出此反应的离子方程式:
,写出此反应的离子方程式:②写出上述流程中用
 进行还原时发生反应的离子方程式:
进行还原时发生反应的离子方程式:(2)
 常用作陶瓷材料,可由锆英砂(主要成分为
常用作陶瓷材料,可由锆英砂(主要成分为 ,也可表示为
,也可表示为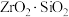 ,还含少量
,还含少量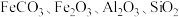 等杂质)通过如下方法制取:
等杂质)通过如下方法制取:
已知:
 能与烧碱反应生成可溶于水的
能与烧碱反应生成可溶于水的 ,
, 与酸反应生成
与酸反应生成 。
。①“熔融”过程中,
 发生反应的化学方程式为
发生反应的化学方程式为②滤渣Ⅲ的成分是
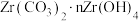 。“调
。“调 ”时,所发生反应的离子方程式为
”时,所发生反应的离子方程式为 的方法是
的方法是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐3】硫元素常见化合价有 、
、 、
、 价,其中处于中间价态的
价,其中处于中间价态的 价硫既有氧化性又有还原性,主要表现为较强的还原性。某学习小组在实验室设计如下实验研究
价硫既有氧化性又有还原性,主要表现为较强的还原性。某学习小组在实验室设计如下实验研究 价硫元素。
价硫元素。
Ⅰ. 制备:
制备:
(1)实验室用 固体与质量分数约为70%的浓硫酸反应制取
固体与质量分数约为70%的浓硫酸反应制取 ,相应化学方程式为:
,相应化学方程式为:_______ ;
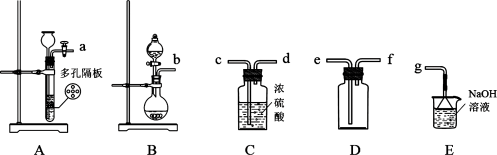
(2)选用图中装置,收集干燥的 ,其最佳连接顺序为:_______→_______→_______→_______→_______→_______→_______→_______(按气流方向,用小写字母表示,部分装置可以重复使用)。
,其最佳连接顺序为:_______→_______→_______→_______→_______→_______→_______→_______(按气流方向,用小写字母表示,部分装置可以重复使用)。_______
Ⅱ.实验探究 的还原性:向盛有
的还原性:向盛有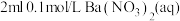 的试管中,缓慢通入
的试管中,缓慢通入 气体,试管内有白色沉淀产生。
气体,试管内有白色沉淀产生。
(3)配制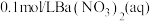 时所用蒸馏水必须先除去溶液中溶解的
时所用蒸馏水必须先除去溶液中溶解的 ,最简单的方法是
,最简单的方法是_______ 。
(4)将 分别通入无氧、有氧且浓度均为
分别通入无氧、有氧且浓度均为 的
的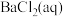 和
和 中,探究
中,探究 和
和 哪种微粒起到了主要氧化作用,实验记录如下:
哪种微粒起到了主要氧化作用,实验记录如下:
①曲线a所示溶液 降低,说明
降低,说明 能与水反应生成
能与水反应生成_______ (填化学式);
②曲线b所示溶液中的反应可按如下方式进行,请完成并配平该离子方程式:_______ 。

③曲线c所示溶液中所发生的反应中氧化剂和还原剂的物质的量之比是_______ ;
④结合上述实验,可以推测, 溶液(有氧)中,氧化
溶液(有氧)中,氧化 的主要微粒是
的主要微粒是_______ ,其理由是_______ 。
 、
、 、
、 价,其中处于中间价态的
价,其中处于中间价态的 价硫既有氧化性又有还原性,主要表现为较强的还原性。某学习小组在实验室设计如下实验研究
价硫既有氧化性又有还原性,主要表现为较强的还原性。某学习小组在实验室设计如下实验研究 价硫元素。
价硫元素。Ⅰ.
 制备:
制备:(1)实验室用
 固体与质量分数约为70%的浓硫酸反应制取
固体与质量分数约为70%的浓硫酸反应制取 ,相应化学方程式为:
,相应化学方程式为:(2)选用图中装置,收集干燥的
 ,其最佳连接顺序为:_______→_______→_______→_______→_______→_______→_______→_______(按气流方向,用小写字母表示,部分装置可以重复使用)。
,其最佳连接顺序为:_______→_______→_______→_______→_______→_______→_______→_______(按气流方向,用小写字母表示,部分装置可以重复使用)。
Ⅱ.实验探究
 的还原性:向盛有
的还原性:向盛有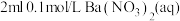 的试管中,缓慢通入
的试管中,缓慢通入 气体,试管内有白色沉淀产生。
气体,试管内有白色沉淀产生。(3)配制
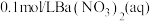 时所用蒸馏水必须先除去溶液中溶解的
时所用蒸馏水必须先除去溶液中溶解的 ,最简单的方法是
,最简单的方法是(4)将
 分别通入无氧、有氧且浓度均为
分别通入无氧、有氧且浓度均为 的
的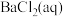 和
和 中,探究
中,探究 和
和 哪种微粒起到了主要氧化作用,实验记录如下:
哪种微粒起到了主要氧化作用,实验记录如下:| 实验记录 | |
| pH变化 | 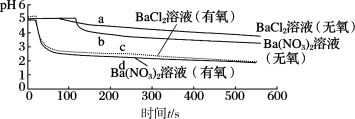 |
| 溶液中是否产生沉淀 |  溶液(无氧)中无白色沉淀 溶液(无氧)中无白色沉淀 溶液(有氧)中有白色沉淀 溶液(有氧)中有白色沉淀 溶液(无氧)中有白色沉淀 溶液(无氧)中有白色沉淀 溶液(有氧)中有白色沉淀 溶液(有氧)中有白色沉淀 |
 降低,说明
降低,说明 能与水反应生成
能与水反应生成②曲线b所示溶液中的反应可按如下方式进行,请完成并配平该离子方程式:

③曲线c所示溶液中所发生的反应中氧化剂和还原剂的物质的量之比是
④结合上述实验,可以推测,
 溶液(有氧)中,氧化
溶液(有氧)中,氧化 的主要微粒是
的主要微粒是
您最近一年使用:0次