化学反应与能量变化
化学反应过程中,不仅有物质的变化,同时还伴随能量变化。研究化学反应中的能量变化有重要意义。
(1)下列反应中属于吸热反应的是________
(2)已知充分燃烧1 mol乙炔气体(分子式为C2H2)时生成二氧化碳气体和液态水,并放出热量b kJ,则乙炔燃烧的热化学方程式正确的是________
(3)分别取 的盐酸与
的盐酸与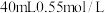 的氢氧化钠溶液混合进行中和热的测定,下列说法正确的是________
的氢氧化钠溶液混合进行中和热的测定,下列说法正确的是________
(4)下列说法正确的是________
(5)如图是某化学反应中的能量变化图。
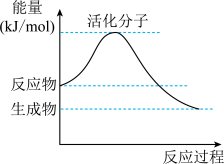
①该反应是___________ (填“吸热”或“放热”)反应。
②请在图中标注出该反应的活化能 。
。_________
(6)298K,100KPa时,把 和
和 放在某密闭容器中进行反应,热化学方程式如下:
放在某密闭容器中进行反应,热化学方程式如下:
 ,测得反应放出的热量总是少于9 kJ/mol,其原因是
,测得反应放出的热量总是少于9 kJ/mol,其原因是___________ 。
化学反应过程中,不仅有物质的变化,同时还伴随能量变化。研究化学反应中的能量变化有重要意义。
(1)下列反应中属于吸热反应的是________
| A.氢气燃烧 | B.铝粉和氧化铁粉末的反应 |
| C.浓硫酸稀释 | D.Ba(OH)2·8H2O和NH4Cl固体的反应 |
A.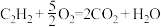 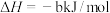 |
B.  |
C. 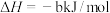 |
D.  |
 的盐酸与
的盐酸与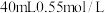 的氢氧化钠溶液混合进行中和热的测定,下列说法正确的是________
的氢氧化钠溶液混合进行中和热的测定,下列说法正确的是________
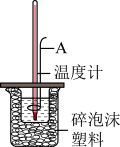
| A.仪器A是金属搅拌棒 |
| B.稍过量的氢氧化钠是确保盐酸完全反应 |
| C.酸碱混合时,NaOH溶液应缓缓倒入小烧杯中,不断搅拌 |
| D.用氢氧化钡和硫酸代替氢氧化钠和盐酸溶液,结果也是正确的 |
| A.焓变或熵变均可以单独作为反应自发性的判据 |
| B.能自发进行的反应一定能迅速发生 |
C. 、 、 的反应在低温时能自发进行 的反应在低温时能自发进行 |
D.两种物质反应,无论方程式的书写形式如何, 均不变 均不变 |

①该反应是
②请在图中标注出该反应的活化能
 。
。(6)298K,100KPa时,把
 和
和 放在某密闭容器中进行反应,热化学方程式如下:
放在某密闭容器中进行反应,热化学方程式如下:
 ,测得反应放出的热量总是少于9 kJ/mol,其原因是
,测得反应放出的热量总是少于9 kJ/mol,其原因是
22-23高一下·上海浦东新·期末 查看更多[2]
更新时间:2023-07-21 08:37:42
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】美国Bay等工厂使用石油热裂解的副产物甲烷来制取氢气,其生产流程如图所示:
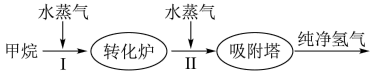
(1)此流程的第Ⅱ步反应为:CO(g)+H2O(g) H2(g)+CO2(g),该反应的化学平衡常数表达式为K=
H2(g)+CO2(g),该反应的化学平衡常数表达式为K=____________ ;反应的平衡常数随温度的变化如下表所示。
从上表可以推断:此反应是__________ (填“吸”或“放”)热反应。
在830 ℃下,若开始时向恒容密闭容器中充入CO与H2O均为1 mol,则达到平衡后CO的转化率为________ 。
(2)此流程的第Ⅱ步反应CO(g)+H2O(g) H2(g)+CO2(g),在830 ℃时,以下表的物质的量(单位为mol)投入恒容反应器发生上述反应,其中反应开始时,向正反应方向进行的有
H2(g)+CO2(g),在830 ℃时,以下表的物质的量(单位为mol)投入恒容反应器发生上述反应,其中反应开始时,向正反应方向进行的有________ (填实验编号)。
(3)在一个不传热的固定容积的容器中,判断此流程的第Ⅱ步反应达到平衡的标志是________ (填序号)。
①体系的压强不再发生变化 ②混合气体的密度不变 ③混合气体的平均相对分子质量不变 ④各组分的物质的量浓度不再改变 ⑤体系的温度不再发生变化 ⑥v(CO2正)=v(H2O逆)
(4)下图表示此流程的第Ⅱ步反应在t1时刻达到平衡,在t2时刻分别因改变某个条件而发生变化的情况:图中t2时刻发生改变的条件可能是________________________ (写出两种)。
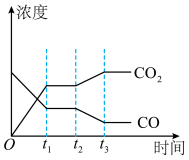

(1)此流程的第Ⅱ步反应为:CO(g)+H2O(g)
 H2(g)+CO2(g),该反应的化学平衡常数表达式为K=
H2(g)+CO2(g),该反应的化学平衡常数表达式为K=| 温度/℃ | 400 | 500 | 830 | 1 000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
从上表可以推断:此反应是
在830 ℃下,若开始时向恒容密闭容器中充入CO与H2O均为1 mol,则达到平衡后CO的转化率为
(2)此流程的第Ⅱ步反应CO(g)+H2O(g)
 H2(g)+CO2(g),在830 ℃时,以下表的物质的量(单位为mol)投入恒容反应器发生上述反应,其中反应开始时,向正反应方向进行的有
H2(g)+CO2(g),在830 ℃时,以下表的物质的量(单位为mol)投入恒容反应器发生上述反应,其中反应开始时,向正反应方向进行的有| 实验编号 | n(CO) | n(H2O) | n(H2) | n(CO2) |
| A | 1 | 5 | 2 | 3 |
| B | 2 | 2 | 1 | 1 |
| C | 0.5 | 2 | 1 | 1 |
(3)在一个不传热的固定容积的容器中,判断此流程的第Ⅱ步反应达到平衡的标志是
①体系的压强不再发生变化 ②混合气体的密度不变 ③混合气体的平均相对分子质量不变 ④各组分的物质的量浓度不再改变 ⑤体系的温度不再发生变化 ⑥v(CO2正)=v(H2O逆)
(4)下图表示此流程的第Ⅱ步反应在t1时刻达到平衡,在t2时刻分别因改变某个条件而发生变化的情况:图中t2时刻发生改变的条件可能是

您最近一年使用:0次
【推荐2】回答下列问题:
(1)在一个小烧杯里加入约20g已研磨成粉末的氢氧化钡晶体[Ba(OH)2·8H2O],将小烧杯放在事先已滴有3~4滴水的玻璃片上,再向烧杯中加入约10gNH4Cl晶体,并立即用玻璃棒搅拌,使Ba(OH)2·8H2O与NH4Cl充分反应。
①写出反应的化学方程式:_______ 。
②根据_______ (现象),可知上述反应中反应物的总能量_______ (填“大于”“小于”或“等于”)生成物的总能量。
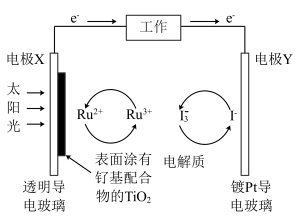
(2)钉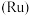 基配合物光敏染料敏化太阳能电池工作时的反应为
基配合物光敏染料敏化太阳能电池工作时的反应为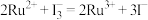 ,装置如图所示。该电池的负极为
,装置如图所示。该电池的负极为_______ (填“电极X”或“电极Y”),负极对应的产物为_______ ;正极反应式为_______ 。
(3)CS2是一种重要的化工原料。工业上可以利用硫(S8)与CH4为原料制备CS2,S8受热分解成气态 ,发生反应
,发生反应 (该反应条件下所有物质均为气态)。某温度下,若
(该反应条件下所有物质均为气态)。某温度下,若 完全分解成气态
完全分解成气态 。在一定温度下,恒容密闭容器中,
。在一定温度下,恒容密闭容器中, 与
与 物质的量之比为2∶1时开始反应。回答下列问题:
物质的量之比为2∶1时开始反应。回答下列问题:
①当 的体积分数为10%时,
的体积分数为10%时, 的转化率为
的转化率为_______ 。
②当以下数值不变时,能说明该反应达到平衡的是_______ (填字母)。
a.气体密度 b.气体总压 c. 与
与 体积比 d.
体积比 d. 的体积分数
的体积分数
(4)在新型RuO2催化剂作用下,使HCl转化为Cl2的反应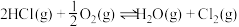 具有更好的催化活性。一定条件下测得反应过程中
具有更好的催化活性。一定条件下测得反应过程中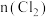 的数据如下:
的数据如下:
则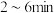 内以
内以 的物质的量变化表示的反应速率为
的物质的量变化表示的反应速率为_______  。
。
(1)在一个小烧杯里加入约20g已研磨成粉末的氢氧化钡晶体[Ba(OH)2·8H2O],将小烧杯放在事先已滴有3~4滴水的玻璃片上,再向烧杯中加入约10gNH4Cl晶体,并立即用玻璃棒搅拌,使Ba(OH)2·8H2O与NH4Cl充分反应。
①写出反应的化学方程式:
②根据
(2)钉
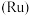 基配合物光敏染料敏化太阳能电池工作时的反应为
基配合物光敏染料敏化太阳能电池工作时的反应为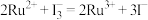 ,装置如图所示。该电池的负极为
,装置如图所示。该电池的负极为
(3)CS2是一种重要的化工原料。工业上可以利用硫(S8)与CH4为原料制备CS2,S8受热分解成气态
 ,发生反应
,发生反应 (该反应条件下所有物质均为气态)。某温度下,若
(该反应条件下所有物质均为气态)。某温度下,若 完全分解成气态
完全分解成气态 。在一定温度下,恒容密闭容器中,
。在一定温度下,恒容密闭容器中, 与
与 物质的量之比为2∶1时开始反应。回答下列问题:
物质的量之比为2∶1时开始反应。回答下列问题:①当
 的体积分数为10%时,
的体积分数为10%时, 的转化率为
的转化率为②当以下数值不变时,能说明该反应达到平衡的是
a.气体密度 b.气体总压 c.
 与
与 体积比 d.
体积比 d. 的体积分数
的体积分数(4)在新型RuO2催化剂作用下,使HCl转化为Cl2的反应
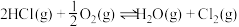 具有更好的催化活性。一定条件下测得反应过程中
具有更好的催化活性。一定条件下测得反应过程中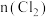 的数据如下:
的数据如下: | 0 | 2 | 4 | 6 | 8 |
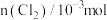 | 0 | 1.8 | 3.7 | 5.4 | 7.2 |
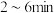 内以
内以 的物质的量变化表示的反应速率为
的物质的量变化表示的反应速率为 。
。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】乙醇在一定条件下可以转化为乙醛,乙醛可进一步被氧化成乙酸。某兴趣小组进行两组实验探究,实验装置如下图所示(装置气密性已检查)。
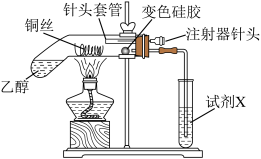
已知:变色硅胶吸收水分后会由蓝色变成粉红色。
实验Ⅰ:通过注射器针头鼓入空气的条件下进行实验。
(1)乙醛中官能团的结构简式为_______ ,下列可用于检验该官能团的试剂是_______ (填字母选项)。
a.银氨溶液 b. 溶液 c.
溶液 c. -淀粉溶液
-淀粉溶液
(2)开始实验时先加热铜网,再通过注射器针头缓慢鼓入空气,该过程中铜丝产生实验现象为_______ ,同时变色硅胶由蓝色变成粉红色,写出乙醇催化氧化的化学反应方程式_______ 。
(3)在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该反应是_______ (填“吸热”或“放热”)反应。
(4)为检验上述实验收集的产物,该小组同学继续进行如下实验并得出相应结论。
实验①~③中的结论不合理的是_______ (填序号),原因是_______ 。
实验Ⅱ:在没有鼓入空气的条件下进行实验。
(5)乙醇蒸气能发生催化氧化生成乙醛,变色硅胶不变色,则该反应的化学方程式为_______ 。

已知:变色硅胶吸收水分后会由蓝色变成粉红色。
实验Ⅰ:通过注射器针头鼓入空气的条件下进行实验。
(1)乙醛中官能团的结构简式为
a.银氨溶液 b.
 溶液 c.
溶液 c. -淀粉溶液
-淀粉溶液(2)开始实验时先加热铜网,再通过注射器针头缓慢鼓入空气,该过程中铜丝产生实验现象为
(3)在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该反应是
(4)为检验上述实验收集的产物,该小组同学继续进行如下实验并得出相应结论。
| 实验序号 | 试剂 和反应条件 和反应条件 | 现象 | 结论 |
| ① | 酸性 溶液 溶液 | 紫红色褪去 | 产物含有乙醛 |
| ② | 新制氢氧化铜悬浊液,加热 | 生成砖红色沉淀 | 产物含有乙醛 |
| ③ | 含酚酞的 溶液 溶液 | 浅红色褪去 | 产物可能含有乙酸 |
实验Ⅱ:在没有鼓入空气的条件下进行实验。
(5)乙醇蒸气能发生催化氧化生成乙醛,变色硅胶不变色,则该反应的化学方程式为
您最近一年使用:0次
【推荐1】多晶硅是制作光伏电池的关键材料。以下是由粗硅制备多晶硅的简易过程。
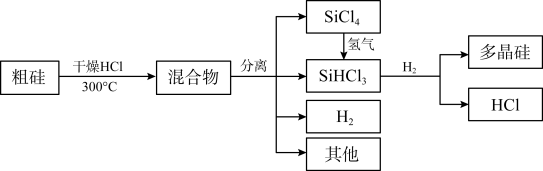
回答下列问题:
Ⅰ.硅粉与 在300℃时反应生成
在300℃时反应生成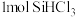 气体和
气体和 ,放出
,放出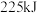 热量,该反应的热化学方程式为
热量,该反应的热化学方程式为_____________ 。 的电子式为
的电子式为__________________ 。
Ⅱ.将 氢化为
氢化为 有三种方法,对应的反应依次为:
有三种方法,对应的反应依次为:
①

②

③

(1)氢化过程中所需 高纯度
高纯度 可用惰性电极电解
可用惰性电极电解 溶液制备,写出产生
溶液制备,写出产生 的电极名称
的电极名称______ (填“阳极”或“阴极”),该电极反应方程式为_______________ 。
(2)反应③的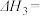
_______________ (用 ,
,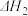 表示)。
表示)。
(3)由粗硅制备多晶硅过程中循环使用的物质除 、
、 和
和 外,还有
外,还有______ (填分子式)。

回答下列问题:
Ⅰ.硅粉与
 在300℃时反应生成
在300℃时反应生成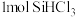 气体和
气体和 ,放出
,放出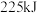 热量,该反应的热化学方程式为
热量,该反应的热化学方程式为 的电子式为
的电子式为Ⅱ.将
 氢化为
氢化为 有三种方法,对应的反应依次为:
有三种方法,对应的反应依次为:①


②


③


(1)氢化过程中所需
 高纯度
高纯度 可用惰性电极电解
可用惰性电极电解 溶液制备,写出产生
溶液制备,写出产生 的电极名称
的电极名称(2)反应③的
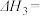
 ,
,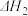 表示)。
表示)。(3)由粗硅制备多晶硅过程中循环使用的物质除
 、
、 和
和 外,还有
外,还有
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】 (肼)是一种燃料,也是重要还原剂。
(肼)是一种燃料,也是重要还原剂。
(1)肼常作火箭发射的燃料。已知: 与足量
与足量 完全反应生成气体
完全反应生成气体 和水蒸气时放出akJ热量;
和水蒸气时放出akJ热量; 。写出
。写出 与
与 反应的热化学方程式:
反应的热化学方程式:_______ 。发射火箭时,发射场产生大量红棕色烟雾,用化学平衡移动原理和化学用语解释这一现象:_______ 。
(2)酸碱质子理论认为:凡是能接受质子的分子或离子则为碱,接受质子的能力越强,碱性越强。已知: ,
, 。由此可知,
。由此可知, 、
、 、
、 碱性由强到弱的顺序为
碱性由强到弱的顺序为_______ 。
(3) 是二元弱碱,在水中第一步电离方程式为
是二元弱碱,在水中第一步电离方程式为_______ 。
(4)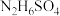 溶液中
溶液中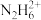 、
、 、
、 、
、 离子浓度由大到小排序为
离子浓度由大到小排序为_______ 。
(5)浙江大学吴浩斌课题组最近设计肼燃料电池,如图所示。
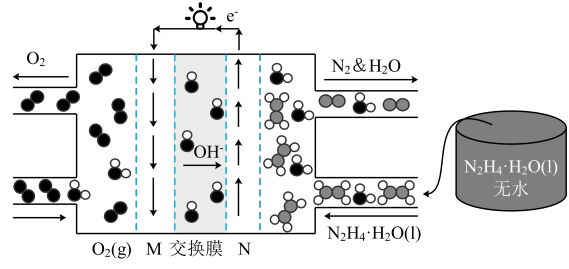
①交换膜类型是_______ 。
②负极反应式为_______ 。
③标准状况下, 参与电极反应,理论上转移
参与电极反应,理论上转移_______ mol电子。
 (肼)是一种燃料,也是重要还原剂。
(肼)是一种燃料,也是重要还原剂。(1)肼常作火箭发射的燃料。已知:
 与足量
与足量 完全反应生成气体
完全反应生成气体 和水蒸气时放出akJ热量;
和水蒸气时放出akJ热量; 。写出
。写出 与
与 反应的热化学方程式:
反应的热化学方程式:(2)酸碱质子理论认为:凡是能接受质子的分子或离子则为碱,接受质子的能力越强,碱性越强。已知:
 ,
, 。由此可知,
。由此可知, 、
、 、
、 碱性由强到弱的顺序为
碱性由强到弱的顺序为(3)
 是二元弱碱,在水中第一步电离方程式为
是二元弱碱,在水中第一步电离方程式为(4)
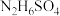 溶液中
溶液中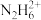 、
、 、
、 、
、 离子浓度由大到小排序为
离子浓度由大到小排序为(5)浙江大学吴浩斌课题组最近设计肼燃料电池,如图所示。

①交换膜类型是
②负极反应式为
③标准状况下,
 参与电极反应,理论上转移
参与电极反应,理论上转移
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】W、X、Y、Z是原子序数依次增大的同一短周期元素,W是金属元素,X是地壳中含量最多的金属元素,且W、X的最高价氧化物的水化物相互反应生成盐和水;Y、Z是非金属元素,Y与W可形成离子化合物W2Y;G在Y的前一周期,其原子最外层比Y原子最外层少1个电子。
(1)写出化合物W2Y的电子式_______________ 。
(2)W、X的最高价氧化物的水化物相互反应的离子方程式为_____________ 。
(3)G的气态氢化物与Y的最高价氧化物的水化物恰好反应生成的正盐溶液中,离子浓度由大到小的顺序为_________________ ,其水溶液显酸性的原因是(用离子方程式表示)_______________ 。
(4)298K时,Z的最高价氧化物为无色液体,0.25mol该物质与一定量水混合得到Z的最高价氧化物的水化物的稀溶液,并放出akJ的热量。该反应的热化学方程式为_________ 。
(1)写出化合物W2Y的电子式
(2)W、X的最高价氧化物的水化物相互反应的离子方程式为
(3)G的气态氢化物与Y的最高价氧化物的水化物恰好反应生成的正盐溶液中,离子浓度由大到小的顺序为
(4)298K时,Z的最高价氧化物为无色液体,0.25mol该物质与一定量水混合得到Z的最高价氧化物的水化物的稀溶液,并放出akJ的热量。该反应的热化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某实验小组用0.50 mol·L-1 NaOH溶液和0.50 mol·L-1 硫酸溶液进行中和热的测定。
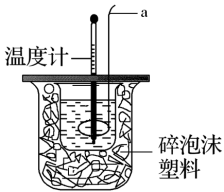
(1)测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示,其中仪器a的名称为_____________ ;
(2)写出该反应中和热的热化学方程式(中和热为57.3 kJ·mol-1)______________ ;
(3)取50 mL NaOH溶液和30 mL硫酸溶液进行实验,实验数据如下表。
① 请填写下表中的空白:
② 近似认为0.50 mol·L-1 NaOH溶液和0.50 mol·L-1 硫酸溶液的密度都是1 g·cm-3,中和后生成溶液的比热容c=4.18kJ·(kg·℃)-1。则中和热ΔH=________________________ (取小数点后一位);
③ 上述实验数据结果与57.3 kJ·mol-1有偏差, 产生偏差的原因不可能是(填字母)________ 。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度

(1)测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示,其中仪器a的名称为
(2)写出该反应中和热的热化学方程式(中和热为57.3 kJ·mol-1)
(3)取50 mL NaOH溶液和30 mL硫酸溶液进行实验,实验数据如下表。
① 请填写下表中的空白:
| 温度 实验次数 | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 26.2 | 31.2 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
② 近似认为0.50 mol·L-1 NaOH溶液和0.50 mol·L-1 硫酸溶液的密度都是1 g·cm-3,中和后生成溶液的比热容c=4.18kJ·(kg·℃)-1。则中和热ΔH=
③ 上述实验数据结果与57.3 kJ·mol-1有偏差, 产生偏差的原因不可能是(填字母)
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】化学反应伴随能量变化,获取反应能量变化有多条途径。回答下列问题:
(1)理论研究表明,在101kPa和298K下,HCN(g)=HNC(g)异构化反应过程的能量变化如图所示,计算可得:HCN(g)=HNC(g) ∆H=_____ kJ•mol-1。HCN与HNC稳定性较强的是_____ 。
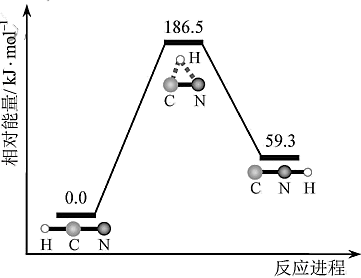
(2)已知:
计算可得:HCN(g)=HNC(g) ∆H=______ kJ•mol-1(用含a、b的式子表示)。
(3)已知:4gCH4完全燃烧生成CO2(g)、H2O(l)时放出热量222.5kJ,则表示甲烷燃烧热的热化学方程式为_____ 。
(4)实验室用50mL0.50mol/L盐酸、50mL0.55mol/LNaOH溶液和如图所示装置,进行测定中和热的实验。
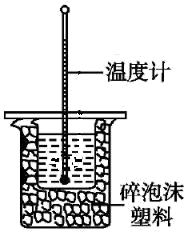
①实验装置中尚缺少的一种实验用品是_____ 。
②若测得中和热的数值偏低,请你分析可能的原因是_____ 。
A.测量盐酸的温度后,温度计没有用水冲洗干净
B.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓
C.做本实验的当天室温较高
D.将50mL0.55mol/L氢氧化钠溶液取成了50mL0.55mol/L的氨水
E.在量取盐酸时仰视读数
(1)理论研究表明,在101kPa和298K下,HCN(g)=HNC(g)异构化反应过程的能量变化如图所示,计算可得:HCN(g)=HNC(g) ∆H=

(2)已知:
| 化学键种类 | C—H | N—H |
| 键能(kJ/mol) | a | b |
(3)已知:4gCH4完全燃烧生成CO2(g)、H2O(l)时放出热量222.5kJ,则表示甲烷燃烧热的热化学方程式为
(4)实验室用50mL0.50mol/L盐酸、50mL0.55mol/LNaOH溶液和如图所示装置,进行测定中和热的实验。

①实验装置中尚缺少的一种实验用品是
②若测得中和热的数值偏低,请你分析可能的原因是
A.测量盐酸的温度后,温度计没有用水冲洗干净
B.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓
C.做本实验的当天室温较高
D.将50mL0.55mol/L氢氧化钠溶液取成了50mL0.55mol/L的氨水
E.在量取盐酸时仰视读数
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】I.海带中含有丰富的碘元素,某化学兴趣小组设计如下流程图提取碘:
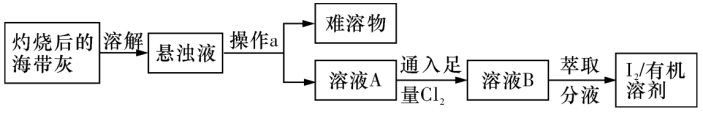
请回答下列问题:
(1)操作a的名称是____ (填“过滤”或“蒸发”)。
(2)溶液A中通入足量Cl2的目的是将I-氧化为I2,也能达到该目的的物质是___ (填“双氧水”或“稀盐酸”)。
(3)在萃取时,可选用的萃取剂为___ (填“酒精”或“四氯化碳”)。
(4)已知I2与H2发生反应:I2(g)+H2(g)⇌2HI(g)。一定条件下,将1molI2和1molH2充入1L的密闭容器中,5min后测得I2的物质的量0.6mol用I2表示该反应的化学反应速率是____ 。
II.实验室利用如图装置进行中和热的测定,取50mL0.50mol/L盐酸、50mL0.55mol/LNaOH溶液进行反应,请回答下列问题:
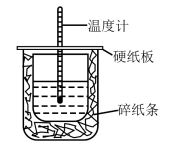
(5)该装置还缺少的玻璃仪器为_____ 。
(6)下列操作使测得中和热偏大的是____ 。
A.测量酸的温度后没有清洗温度计在测量碱
B.在量取盐酸时仰视读数
C.使用铜棒搅拌反应液
D.将盐酸的体积量取为52.0ml

请回答下列问题:
(1)操作a的名称是
(2)溶液A中通入足量Cl2的目的是将I-氧化为I2,也能达到该目的的物质是
(3)在萃取时,可选用的萃取剂为
(4)已知I2与H2发生反应:I2(g)+H2(g)⇌2HI(g)。一定条件下,将1molI2和1molH2充入1L的密闭容器中,5min后测得I2的物质的量0.6mol用I2表示该反应的化学反应速率是
II.实验室利用如图装置进行中和热的测定,取50mL0.50mol/L盐酸、50mL0.55mol/LNaOH溶液进行反应,请回答下列问题:

(5)该装置还缺少的玻璃仪器为
(6)下列操作使测得中和热偏大的是
A.测量酸的温度后没有清洗温度计在测量碱
B.在量取盐酸时仰视读数
C.使用铜棒搅拌反应液
D.将盐酸的体积量取为52.0ml
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】氟化工被称为“黄金产业”,在国民经济和社会发展中占有重要地位。我国某公司利用萤石(主要成分为 ,及少量
,及少量 、
、 等)制备无水氟化铝的主要工艺流程如下所示。
等)制备无水氟化铝的主要工艺流程如下所示。 的熔点
的熔点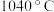 ,沸点
,沸点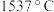 ;
;
③常温下, 。
。
请回答下列问题:
(1)在进入回转窑前,需要将萤石粉碎,其目的是_______ 。
(2)“回转窑反应”的温度控制在 之间,写出在回转窑获得
之间,写出在回转窑获得 的化学方程式:
的化学方程式:_______ 。
(3)在回转窑中的炉渣里还含有 ,将该物质在
,将该物质在 热分解,可获得两种气体(其中一种为
热分解,可获得两种气体(其中一种为 ),用多元醇选择性吸收产生的
),用多元醇选择性吸收产生的 气体,经过一系列工艺得到高纯
气体,经过一系列工艺得到高纯 。则多元醇能从两种气体中选择性吸收
。则多元醇能从两种气体中选择性吸收 的原理是
的原理是_______ 。
(4)经冷凝、精馏、脱气后的 与
与 在流化床、多级气流床中,在
在流化床、多级气流床中,在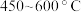 条件下进行一系列反应,由
条件下进行一系列反应,由 和
和 制备无水
制备无水 的反应的
的反应的 _______(填标号)。
_______(填标号)。
(5)常温下,向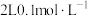 的
的 溶液中加入
溶液中加入 固体充分反应后可得
固体充分反应后可得 ,测得溶液中
,测得溶液中 的浓度为
的浓度为 ,则加入的
,则加入的 固体的物质的量为
固体的物质的量为_______ 。
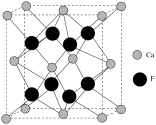
(6)已知萤石 立方晶胞参数
立方晶胞参数 ,结构如图所示,该
,结构如图所示,该 的晶体密度为
的晶体密度为_______  (列出计算式,设阿伏加德罗常数的值为
(列出计算式,设阿伏加德罗常数的值为 )。
)。
 ,及少量
,及少量 、
、 等)制备无水氟化铝的主要工艺流程如下所示。
等)制备无水氟化铝的主要工艺流程如下所示。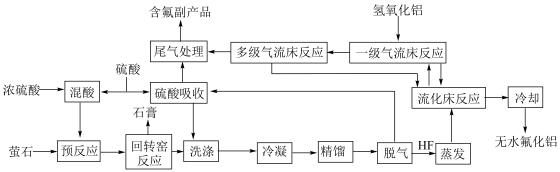
 的熔点
的熔点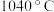 ,沸点
,沸点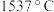 ;
;③常温下,
 。
。请回答下列问题:
(1)在进入回转窑前,需要将萤石粉碎,其目的是
(2)“回转窑反应”的温度控制在
 之间,写出在回转窑获得
之间,写出在回转窑获得 的化学方程式:
的化学方程式:(3)在回转窑中的炉渣里还含有
 ,将该物质在
,将该物质在 热分解,可获得两种气体(其中一种为
热分解,可获得两种气体(其中一种为 ),用多元醇选择性吸收产生的
),用多元醇选择性吸收产生的 气体,经过一系列工艺得到高纯
气体,经过一系列工艺得到高纯 。则多元醇能从两种气体中选择性吸收
。则多元醇能从两种气体中选择性吸收 的原理是
的原理是(4)经冷凝、精馏、脱气后的
 与
与 在流化床、多级气流床中,在
在流化床、多级气流床中,在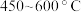 条件下进行一系列反应,由
条件下进行一系列反应,由 和
和 制备无水
制备无水 的反应的
的反应的 _______(填标号)。
_______(填标号)。| A.大于0 | B.小于0 | C.等于0 | D.无法确定 |
(5)常温下,向
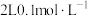 的
的 溶液中加入
溶液中加入 固体充分反应后可得
固体充分反应后可得 ,测得溶液中
,测得溶液中 的浓度为
的浓度为 ,则加入的
,则加入的 固体的物质的量为
固体的物质的量为(6)已知萤石
 立方晶胞参数
立方晶胞参数 ,结构如图所示,该
,结构如图所示,该 的晶体密度为
的晶体密度为 (列出计算式,设阿伏加德罗常数的值为
(列出计算式,设阿伏加德罗常数的值为 )。
)。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】温室气体CO2转化为甲酸(HCOOH)既具有经济技术意义,又具有环保意义,而且甲酸还是重要的液态储氢原料,在一定条件下又可以分解释放氢气,实现能量循环。因此以CO2为碳源制备HCOOH已成为一碳化学研究的热点。
(1)已知CO2+H2→HCOOH ΔG(即ΔH-TΔS)=34.3kJ/mol。该反应在理论上属于原子经济性100%的绿色工艺,但是该反应不能自发进行,判断依据是______ ,因此不利用该反应直接制备甲酸。
(2)在实践中,CO2制备得到甲酸的一种流程如图:

资料:部分酸的电离常数(18℃-25℃时数据)
①写出过程II的离子方程式______ 。
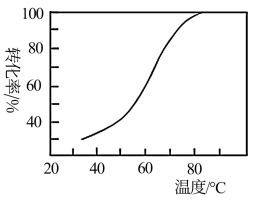
②过程II中,其他条件不变, 转化为HCOO-的转化率如图所示。在40℃-80℃范围内,转化率迅速上升,其主要原因是
转化为HCOO-的转化率如图所示。在40℃-80℃范围内,转化率迅速上升,其主要原因是______ 。
③过程III的化学方程式是______ (任写一个)。
(3)电催化合成甲酸因活化容易且能在常温常压下反应,因此具有广阔前景。某CO2电催化反应器示意图如图所示。
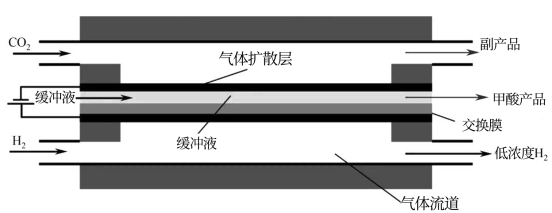
①阴极的电极反应式是______ 。
②该电解反应得到的副产品除H2外,还可能有______ (任写一个)。
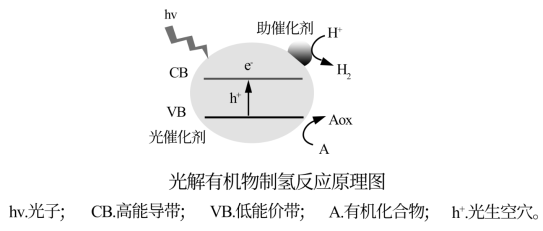
(4)甲酸催化释氢是一种较为理想的技术。如图所示为甲酸释氢原理,图中Aox的化学式是______ 。
(1)已知CO2+H2→HCOOH ΔG(即ΔH-TΔS)=34.3kJ/mol。该反应在理论上属于原子经济性100%的绿色工艺,但是该反应不能自发进行,判断依据是
(2)在实践中,CO2制备得到甲酸的一种流程如图:

资料:部分酸的电离常数(18℃-25℃时数据)
| 物质 | Ka | 物质 | Ka |
| HCOOH | 1.7×10-4 | H2CO3 | Ka1=1.7×10-4 Ka2=5.6×10-11 |
②过程II中,其他条件不变,
 转化为HCOO-的转化率如图所示。在40℃-80℃范围内,转化率迅速上升,其主要原因是
转化为HCOO-的转化率如图所示。在40℃-80℃范围内,转化率迅速上升,其主要原因是
③过程III的化学方程式是
(3)电催化合成甲酸因活化容易且能在常温常压下反应,因此具有广阔前景。某CO2电催化反应器示意图如图所示。

①阴极的电极反应式是
②该电解反应得到的副产品除H2外,还可能有
(4)甲酸催化释氢是一种较为理想的技术。如图所示为甲酸释氢原理,图中Aox的化学式是

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】以煤炭为原料,通入一定比例空气和水蒸气,经过系列反应可得满足不同需求的原料气。
Ⅰ.在C和 的反应体系中:
的反应体系中:
反应1:

反应2:
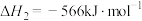
反应3:

(1)反应3对应的
___________ kJ/mol;
___________ 0(填“>、=或<”)。
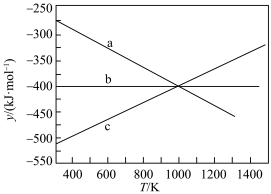
(2)设 ,反应1、2和3的y随温度的变化关系如图所示。图中对应于反应3的线条是
,反应1、2和3的y随温度的变化关系如图所示。图中对应于反应3的线条是___________ 。(填“a、b或c”)。
(3)一定压强下,随着温度升高,气体中CO与 的物质的量之比___________。
的物质的量之比___________。
(4)水煤气反应:
 。工业生产水煤气时,通常交替通入合适量的空气和水蒸气与煤炭反应,其理由是
。工业生产水煤气时,通常交替通入合适量的空气和水蒸气与煤炭反应,其理由是___________ 。
(5)已知 ,
, ,
, ,则水的沸点是
,则水的沸点是___________ K(结果保留一位小数,写出计算过程)。
Ⅱ.合成氨工业原料氢气用水、煤、天然气等为原料制得。反应如下: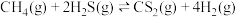

(6)在恒温恒容条件下,可作为反应达到平衡状态的判断依据是___________。
(7)在恒压条件下,以 的组成的混合气体发生反应,达到平衡状态时,四种组分物质的量分数随温度的变化如图所示。图中表示
的组成的混合气体发生反应,达到平衡状态时,四种组分物质的量分数随温度的变化如图所示。图中表示 、
、 变化的曲线分别是
变化的曲线分别是___________ 、___________ 。
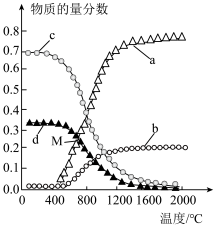
(8)M点对应温度下, 的转化率是
的转化率是___________ 。
(9)某温度下上述反应达到平衡后,保持其它条件不变,升高温度对反应速率影响的图像是___________(填编号)
(10)二氧化碳加氢制甲醇的总反应可表示为: ,该反应一般认为通过如下步骤实现:
,该反应一般认为通过如下步骤实现:
①

②

若反应①为慢反应,下列示意图中能体现上述反应能量变化的是___________(填编号)
Ⅰ.在C和
 的反应体系中:
的反应体系中:反应1:


反应2:

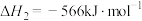
反应3:


(1)反应3对应的


(2)设
 ,反应1、2和3的y随温度的变化关系如图所示。图中对应于反应3的线条是
,反应1、2和3的y随温度的变化关系如图所示。图中对应于反应3的线条是
(3)一定压强下,随着温度升高,气体中CO与
 的物质的量之比___________。
的物质的量之比___________。| A.不变 | B.增大 | C.减小 | D.无法判断 |
(4)水煤气反应:

 。工业生产水煤气时,通常交替通入合适量的空气和水蒸气与煤炭反应,其理由是
。工业生产水煤气时,通常交替通入合适量的空气和水蒸气与煤炭反应,其理由是(5)已知
 ,
, ,
, ,则水的沸点是
,则水的沸点是Ⅱ.合成氨工业原料氢气用水、煤、天然气等为原料制得。反应如下:
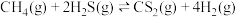

(6)在恒温恒容条件下,可作为反应达到平衡状态的判断依据是___________。
| A.混合气体密度不变 | B. 与 与 的物质的量之比为保持不变 的物质的量之比为保持不变 |
C. | D.容器内压强不变 |
(7)在恒压条件下,以
 的组成的混合气体发生反应,达到平衡状态时,四种组分物质的量分数随温度的变化如图所示。图中表示
的组成的混合气体发生反应,达到平衡状态时,四种组分物质的量分数随温度的变化如图所示。图中表示 、
、 变化的曲线分别是
变化的曲线分别是
(8)M点对应温度下,
 的转化率是
的转化率是(9)某温度下上述反应达到平衡后,保持其它条件不变,升高温度对反应速率影响的图像是___________(填编号)
A.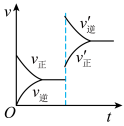 | B.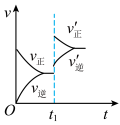 |
C.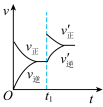 | D. |
(10)二氧化碳加氢制甲醇的总反应可表示为:
 ,该反应一般认为通过如下步骤实现:
,该反应一般认为通过如下步骤实现:①


②


若反应①为慢反应,下列示意图中能体现上述反应能量变化的是___________(填编号)
A.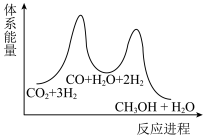 | B.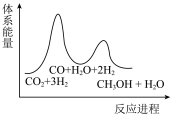 |
C.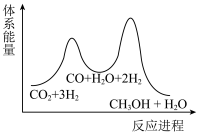 | D.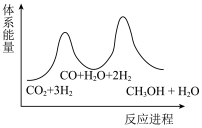 |
您最近一年使用:0次



