A、B、C、D、E、F、G均为短周期元素,原子序数依次递增。A元素原子核内无中子,B元素原子最外层电子数是次外层电子数的2倍,D是地壳中含量最多的元素,E是短周期中金属性最强的元素,F与G位置相邻,G是同周期元素中原子半径最小的主族元素。请回答下列问题:
(1)C在元素周期中的位置为_____ ,G的原子结构示意图是_____ 。
(2)D与E按原子个数比1∶1形成化合物甲,其化学式为_____ ,向甲中滴加足量水时发生反应的化学方程式是_____ 。
(3)E、F、G形成的简单离子,半径由大到小顺序是_____ (用离子符号表示)。
(4)B、C、D的简单氢化物的还原性强弱顺序为_____ (填分子式,下同),热稳定性强弱顺序为_____ 。
(5)F、G的最高价氧化物的水化物的分子式为_____ ,酸性较强的为_____ 。
(1)C在元素周期中的位置为
(2)D与E按原子个数比1∶1形成化合物甲,其化学式为
(3)E、F、G形成的简单离子,半径由大到小顺序是
(4)B、C、D的简单氢化物的还原性强弱顺序为
(5)F、G的最高价氧化物的水化物的分子式为
22-23高一下·云南红河·期末 查看更多[2]
更新时间:2023-07-26 16:21:04
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】 是制造锌钡白和锌盐的主要原料,也可用作印染媒染剂、木材和皮革的保存剂等。工业上常用菱锌矿(主要成分为
是制造锌钡白和锌盐的主要原料,也可用作印染媒染剂、木材和皮革的保存剂等。工业上常用菱锌矿(主要成分为 ,杂质为
,杂质为 以及Ca、Mg、Fe、Cu等的氧化物)制备
以及Ca、Mg、Fe、Cu等的氧化物)制备 ,工艺流程如下:
,工艺流程如下:

(1)将菱锌矿制成粉的目的是_____ 。
(2)实验室将浓硫酸稀释成稀硫酸的操作是_______ 。写出一个证明硫的非金属性比硅强的化学方程式:____ 。
(3) 是
是________ (填“酸性”、“碱性”或“两性”)氧化物,写出证明其为该性质氧化物的离子方程式:_____ 。
(4)过滤时所用到的玻璃仪器有玻璃棒、_______ 。
(5)请用电子式表示 的形成过程:
的形成过程:______ 。
(6)HF的水溶液称为氢氟酸,请写出它的一种用途:_____ 。
 是制造锌钡白和锌盐的主要原料,也可用作印染媒染剂、木材和皮革的保存剂等。工业上常用菱锌矿(主要成分为
是制造锌钡白和锌盐的主要原料,也可用作印染媒染剂、木材和皮革的保存剂等。工业上常用菱锌矿(主要成分为 ,杂质为
,杂质为 以及Ca、Mg、Fe、Cu等的氧化物)制备
以及Ca、Mg、Fe、Cu等的氧化物)制备 ,工艺流程如下:
,工艺流程如下:
(1)将菱锌矿制成粉的目的是
(2)实验室将浓硫酸稀释成稀硫酸的操作是
(3)
 是
是(4)过滤时所用到的玻璃仪器有玻璃棒、
(5)请用电子式表示
 的形成过程:
的形成过程:(6)HF的水溶液称为氢氟酸,请写出它的一种用途:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】已知六种短周期元素A、B、C、D、E、M的原子序数依次增大,A的原子核内没有中子,A、D同主族,C、M同主族,A和B可形成5核10电子的阳离子,C与D形成的离子化合物 中阴、阳离子的电子数相同,E的最高价氧化物的水化物可与D、M的最高价氧化物的水化物反应,试回答下列问题:
中阴、阳离子的电子数相同,E的最高价氧化物的水化物可与D、M的最高价氧化物的水化物反应,试回答下列问题:
(1)C在元素周期表中的位置是___________ ,写出C元素的两种同素异形体的化学式___________ 。
(2)写出A和B形成4核10电子分子的电子式是___________ 。
(3)C、D、M的简单离子半径由大到小的顺序为___________ (用离子符号表示)。
(4)A、C、D可形成多种二元化合物,下列说法不正确的是___________(填字母)。
(5)含有E元素的一种复盐可用作净水剂,该盐的化学式为___________ ,该盐溶液中加入足量 溶液,反应的离子方程式为
溶液,反应的离子方程式为___________ 。
(6)不能说明Cl元素的非金属性比M元素强的事实是___________ (填序号)。
① 通入M的氢化物的水溶液中,溶液变浑浊
通入M的氢化物的水溶液中,溶液变浑浊
②盐酸比M的氢化物的水溶液酸性强
③M的简单阴离子比 易被氧化
易被氧化
④ 比M的氢化物稳定
比M的氢化物稳定
⑤铁与氯气在加热条件下反应生成氯化铁,铁与M单质在加热条件下反应生成某化亚铁
 中阴、阳离子的电子数相同,E的最高价氧化物的水化物可与D、M的最高价氧化物的水化物反应,试回答下列问题:
中阴、阳离子的电子数相同,E的最高价氧化物的水化物可与D、M的最高价氧化物的水化物反应,试回答下列问题:(1)C在元素周期表中的位置是
(2)写出A和B形成4核10电子分子的电子式是
(3)C、D、M的简单离子半径由大到小的顺序为
(4)A、C、D可形成多种二元化合物,下列说法不正确的是___________(填字母)。
A.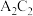 和 和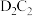 中都含共价键 中都含共价键 |
| B.A、D可形成离子化合物 |
C. 、 、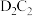 中阴阳离子个数比均为 中阴阳离子个数比均为 |
D. 和 和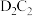 均能溶于 均能溶于 ,并发生化合反应 ,并发生化合反应 |
 溶液,反应的离子方程式为
溶液,反应的离子方程式为(6)不能说明Cl元素的非金属性比M元素强的事实是
①
 通入M的氢化物的水溶液中,溶液变浑浊
通入M的氢化物的水溶液中,溶液变浑浊②盐酸比M的氢化物的水溶液酸性强
③M的简单阴离子比
 易被氧化
易被氧化④
 比M的氢化物稳定
比M的氢化物稳定⑤铁与氯气在加热条件下反应生成氯化铁,铁与M单质在加热条件下反应生成某化亚铁
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】I.某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验。
(1)将钠、钾、镁、铝各1 mol分别投入到足量的同浓度的盐酸中,试预测实验结果:____ 与盐酸反应最剧烈,____ 与盐酸反应产生的气体最多。
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明非金属性:Cl____ S(填“> ”或“<”),反应的离子方程式为_____ 。
II.利用如图装置可验证同主族元素非金属性的变化规律。

(3)实验步骤:
连接仪器、_____ 、加药品后,打开_____ 的活塞滴入液体,然后……(填步骤中所的操作或仪器)
(4)若要证明非金属性:Cl>I,C中为淀粉碘化钾混合溶液,B中装有KMnO4固体,则A中试剂为____ ,观察到C中溶液_____ (填现象),即可证明非金属性:Cl>I。从环境保护的角度考虑,此装置缺少尾气处理装置,可用____ 吸收尾气。
(5)若要证明非金属性是C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液。能说明碳元素的非金属性比硅元素非金属性强的实验现象是____ 。但有的同学认为根据本实验的B装置中有气体产生,还可以证明氯元素的非金属性强于碳元素,你认为这种说法是否正确___ (填“是”或“否”)。
(1)将钠、钾、镁、铝各1 mol分别投入到足量的同浓度的盐酸中,试预测实验结果:
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明非金属性:Cl
II.利用如图装置可验证同主族元素非金属性的变化规律。

(3)实验步骤:
连接仪器、
(4)若要证明非金属性:Cl>I,C中为淀粉碘化钾混合溶液,B中装有KMnO4固体,则A中试剂为
(5)若要证明非金属性是C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液。能说明碳元素的非金属性比硅元素非金属性强的实验现象是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D、E五种主族元素,它们的原子序数依次增大且均小于20。A、B为同周期相邻元素,二者化合而成的一种气体化合物为红棕色;D是地壳中含量最高的金属元素;C的原子半径在同周期原子半径中最大;A、B的原子最外层电子数之和等于C、D、E原子的最外层电子数之和。
请回答下列问题:
(1)A的简单氢化物化学式:___________ ,D的高价氧化物化学式:_____________ 。
(2)C、D、E的简单离子半径由大到小的顺序:_________________ (用离子符号填写)。
(3)A、B的非金属性由强到弱顺序为________________________ (用元素符号表示)。
(4)C的单质与水反应的离子方程式为_______________
(5)D的单质与C的最高价氧化物对应水化物的水溶液反应的化学方程式为________
请回答下列问题:
(1)A的简单氢化物化学式:
(2)C、D、E的简单离子半径由大到小的顺序:
(3)A、B的非金属性由强到弱顺序为
(4)C的单质与水反应的离子方程式为
(5)D的单质与C的最高价氧化物对应水化物的水溶液反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】元素周期表是化学史上重要的里程碑之一,下表是现行长式周期表的一部分。结合下表用化学用语回答问题:
(1)上表元素①~⑦中,非金属性最强的是___________ 。
(2)元素⑦为铁元素,其在周期表中的位置为___________ ,写出其单质与⑤的单质反应的化学方程式___________ 。
(3)可以用元素③的氢化物的水溶液溶蚀玻璃生产磨砂玻璃,写出反应的化学方程式___________ 。
(4)元素②④⑥简单离子半径由大到小为___________ 。
(5)元素④与元素①形成化合物X,写出X的电子式___________ ,其化学键类型为___________ ,X在野外能做生氢剂,其与水反应生氢的反应中,氧化剂为___________ 。
| ① | |||||||||||||||||
| ② | ③ | ||||||||||||||||
| ④ | ⑤ | ||||||||||||||||
| ⑥ | ⑦ | ||||||||||||||||
(2)元素⑦为铁元素,其在周期表中的位置为
(3)可以用元素③的氢化物的水溶液溶蚀玻璃生产磨砂玻璃,写出反应的化学方程式
(4)元素②④⑥简单离子半径由大到小为
(5)元素④与元素①形成化合物X,写出X的电子式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下图为元素周期表的一部分。根据元素①~⑦在周期表中的位置,按要求回答下列问题。
(1)元素①~⑦的单质中氧化性最强的是___________ 。(填化学式)
(2)元素③⑤⑥的原子的半径从大到小的顺序是___________ 。(用元素符号表示)
(3)元素②的简单气态氢化物的沸点高于元素⑥的,原因是___________ 。
(4)元素②④⑦按原子数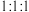 组成化合物甲,甲中所含化学键的类型是
组成化合物甲,甲中所含化学键的类型是___________ 。
(5)元素①与④组成的化合物可与水反应,写出反应的化学方程式___________ 。
(6)元款④⑥⑦的最高价氧化物对应的水化物分别为A、B、C.相同条件下。相同物质的量浓度的A、B、C的水溶液中 最大的是
最大的是___________ 。(填化学式)
(7)元素①与⑦组成的化合物为乙。用电子式表示乙的形成过程___________ 。
| 族 周期 | ⅠA | 0 | ||||||
| ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| ② | ③ | |||||||
| ④ | ⑤ | ⑥ | ⑦ |
(2)元素③⑤⑥的原子的半径从大到小的顺序是
(3)元素②的简单气态氢化物的沸点高于元素⑥的,原因是
(4)元素②④⑦按原子数
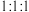 组成化合物甲,甲中所含化学键的类型是
组成化合物甲,甲中所含化学键的类型是(5)元素①与④组成的化合物可与水反应,写出反应的化学方程式
(6)元款④⑥⑦的最高价氧化物对应的水化物分别为A、B、C.相同条件下。相同物质的量浓度的A、B、C的水溶液中
 最大的是
最大的是(7)元素①与⑦组成的化合物为乙。用电子式表示乙的形成过程
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】X、Y、Z、R、Q、M是六种短周期元素,原子序数依次增大,是原子半径最小的元素,Y的气态氢化物能使湿润的红色石蕊试纸变蓝,Z为地壳中含量最多的元素,R与X同主族;Y、R、Q最外层电子数之和为8,M的单质黄绿色有害气体。请回答下列问题:
(1) 在元素周期表中的位置为
在元素周期表中的位置为______ .
(2) 、Q、M简单离子半径由大到小的顺序为
、Q、M简单离子半径由大到小的顺序为 写元素离子符号
写元素离子符号
______ .
(3) 、Y、Z三种元素形成盐类化合物的水溶液呈酸性的原因:
、Y、Z三种元素形成盐类化合物的水溶液呈酸性的原因: 用离子方程式表示
用离子方程式表示
______  溶液中所含离子浓度由大到小的顺序为
溶液中所含离子浓度由大到小的顺序为______ .
(4) 的电子式为
的电子式为______ ,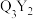 与水可剧烈反应,产生沉淀与气体,反应的化学方程式为
与水可剧烈反应,产生沉淀与气体,反应的化学方程式为______ .
(5) 、Z两元素形成的原子个数比为1:1的化合物中含有的化学键类型为
、Z两元素形成的原子个数比为1:1的化合物中含有的化学键类型为______ .
(6) 的单质与R的最高价氧化物对应的水化物反应的离子方程式为
的单质与R的最高价氧化物对应的水化物反应的离子方程式为______ .
(1)
 在元素周期表中的位置为
在元素周期表中的位置为(2)
 、Q、M简单离子半径由大到小的顺序为
、Q、M简单离子半径由大到小的顺序为 写元素离子符号
写元素离子符号
(3)
 、Y、Z三种元素形成盐类化合物的水溶液呈酸性的原因:
、Y、Z三种元素形成盐类化合物的水溶液呈酸性的原因: 用离子方程式表示
用离子方程式表示
 溶液中所含离子浓度由大到小的顺序为
溶液中所含离子浓度由大到小的顺序为(4)
 的电子式为
的电子式为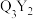 与水可剧烈反应,产生沉淀与气体,反应的化学方程式为
与水可剧烈反应,产生沉淀与气体,反应的化学方程式为(5)
 、Z两元素形成的原子个数比为1:1的化合物中含有的化学键类型为
、Z两元素形成的原子个数比为1:1的化合物中含有的化学键类型为(6)
 的单质与R的最高价氧化物对应的水化物反应的离子方程式为
的单质与R的最高价氧化物对应的水化物反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】I.表中所示为元素周期表的一部分,参照元素①~⑨在表中的位置,请回答下列问题:
(1)③、④、⑦的离子半径由大到小的顺序是_____ (用离子符号表示)。
(2)下列事实不能说明元素⑦的非金属性比元素⑥的非金属性强的是_____ (填字母)。
(3)已知周期表中存在对角相似规则,处于对角线位置的元素化学性质相似,⑧的氧化物、氢氧化物也有两性,写出⑧的氢氧化物与④的最高价氧化物的水化物反应的化学方程式(生成的盐中阴、阳离子个数比为1:2):_____ 。
(4)⑥的一种氧化物可用作海水提溴时的溴单质吸收剂,该反应的化学方程式为:______ 。
II.现有部分短周期元素的性质与原子(或分子)结构如表:
(5)下列能够证明Y的金属性比Z强的是_____ 。
(6)关于T元素,下列说法正确的是_____ 。
| IA | 0 | |||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ⑧ | ⑨ | ② | ③ | ||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ||||
(2)下列事实不能说明元素⑦的非金属性比元素⑥的非金属性强的是
| A.⑦的单质与⑥的简单氢化物溶液反应,溶液变浑浊 |
| B.⑦的单质可以将铁氧化为正三价,而⑥的单质将铁氧化为正二价 |
| C.⑦的氢化物为强酸,而⑥的氢化物为弱酸 |
| D.⑦和⑥两元素的简单氢化物受热分解,前者的分解温度高 |
(4)⑥的一种氧化物可用作海水提溴时的溴单质吸收剂,该反应的化学方程式为:
II.现有部分短周期元素的性质与原子(或分子)结构如表:
| 元素编号 | 元素性质与原子(或分子)结构 |
| T | T元素的单质常用于制造芯片和太阳能电池 |
| Y | 原子的M层比K层少1个电子 |
| Z | Z的单质可与某些金属氧化物反应用于焊接钢轨 |
| A.Y离子的氧化性比Z离子的氧化性强 |
| B.1molY从足量的稀硫酸中置换出的氢气比1molZ置换出的氢气多 |
| C.Y的最高价氧化物的水化物的碱性比Z的最高价氧化物的水化物碱性强 |
| D.Y在常温下能与水剧烈反应,而Z不能 |
| A.T的氧化物常被用来制造光导纤维 |
| B.自然界中存在T的单质 |
| C.T的氧化物既可以与HF反应又可以与NaOH反应,因此该氧化物为两性氧化物 |
| D.可以用T的氧化物溶于水制取T的含氧酸 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】W、X、Y和Z都是周期表中前20号元素,其中W的原子序数均大于X、Y、Z,已知:
①W的阳离子和Y的阴离子具有相同的核外电子排布,且能形成组成为WY的化合物;
②Y和Z属同族元素,它们能形成两种常见化合物;
③X和Z属同一周期元素,它们能形成两种气态化合物;
④W和X能形成组成为WX2的化合物;
⑤X和Y不在同一周期,它们能形成组成为XY2的化合物。
请回答:
(1)W元素是________ ;Z元素是________ 。
(2)化合物WY和WX2的化学式分别是____________ 和 ____________ 。
(3)写出Y和Z形成的两种常见化合物之一的分子式是________________ 。
(4)写出X和Z形成的一种气态化合物跟WZ反应的化学方程式:____________________________________ 。
①W的阳离子和Y的阴离子具有相同的核外电子排布,且能形成组成为WY的化合物;
②Y和Z属同族元素,它们能形成两种常见化合物;
③X和Z属同一周期元素,它们能形成两种气态化合物;
④W和X能形成组成为WX2的化合物;
⑤X和Y不在同一周期,它们能形成组成为XY2的化合物。
请回答:
(1)W元素是
(2)化合物WY和WX2的化学式分别是
(3)写出Y和Z形成的两种常见化合物之一的分子式是
(4)写出X和Z形成的一种气态化合物跟WZ反应的化学方程式:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】周期表前四周期的元素A、B、C、D、E原子序数依次增大。A的核外电子总数与其周期数相同,B的价电子层中有3个未成对电子,C的最外层电子数为其内层电子数的3倍,D与C同族;E的最外层只有2个电子,但次外层有18个电子。回答下列问题:
(1)常温下(BA4)DC4溶液显______ 性,用离子方程式解释原因______ 。
(2)B、C、D中第一电离能最大的是______ (填元素符号),基态E原子电子占据最高能级的电子云轮廓图为______ 。
(3)A和其他元素形成的二元共价化合物中,有一种分子空间构形呈三角锥形,该分子极易溶于水,却不溶于CCl4,请解释原因______ ;分子中既含有极性共价键、又含有非极性共价键的化合物是______ (填化学式,写一种)。
(4)A2C内的C—A键、A2C分子间的范德华力和氢键,从强到弱依次是______ 。A3C+中A—C—A键角比A2C中的______ (填“大”或“小”或“相等”)
(5)与E同周期的元素中,基态原子在4s轨道上只有1个电子的元素共有______ 种。
(1)常温下(BA4)DC4溶液显
(2)B、C、D中第一电离能最大的是
(3)A和其他元素形成的二元共价化合物中,有一种分子空间构形呈三角锥形,该分子极易溶于水,却不溶于CCl4,请解释原因
(4)A2C内的C—A键、A2C分子间的范德华力和氢键,从强到弱依次是
(5)与E同周期的元素中,基态原子在4s轨道上只有1个电子的元素共有
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】X、Y、Z、Q、E五种元素中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳中含量(质量分数)最多的元素,Q的核电荷数是X与Z的核电荷数之和,E在元素周期表的各元素中电负性最大。请回答下列问题:
(1)X、Y的元素符号依次为___________ 、___________ ;
(2)XZ2与YZ2分子的立体结构分别是___________ 和___________ ;
(3)Q的元素符号是___________ ,它属于第___________ 周期,它的核外电子排布式为___________ ,在形成化合物时它的最高化合价为___________ ;
(4)用氢键表示式写出E的氢化物溶液中存在的所有氢键___________ 。
(1)X、Y的元素符号依次为
(2)XZ2与YZ2分子的立体结构分别是
(3)Q的元素符号是
(4)用氢键表示式写出E的氢化物溶液中存在的所有氢键
您最近一年使用:0次



