依据图示关系,下列说法不正确的是
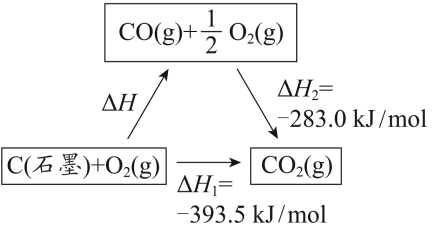

| A.石墨燃烧是放热反应 |
| B.1molC(石墨)和 1molCO 分别在足量 O2中燃烧, 全部转化为 CO2,前者放热多 |
| C.ΔH=ΔH1+ΔH2 |
| D.化学反应的ΔH,只与反应体系的始态和终态有关,与反应途径无关 |
21-22高二上·重庆大足·阶段练习 查看更多[3]
重庆市大足中学2021-2022学年高二上学期第一次月考化学试题(已下线)专题02 盖斯定律、反应热的计算【考点清单】(讲+练)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)福建省龙岩市一级校联盟2023-2024学年高二上学期11月期中考试化学试题
更新时间:2023-08-19 10:32:32
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】向绝热恒容密闭容器中通入1 mol SO2和1 mol NO2,发生反应SO2(g)+NO2(g) SO3(g)+NO(g),正反应速率随时间变化如图所示。下列有关说法不正确的是
SO3(g)+NO(g),正反应速率随时间变化如图所示。下列有关说法不正确的是

 SO3(g)+NO(g),正反应速率随时间变化如图所示。下列有关说法不正确的是
SO3(g)+NO(g),正反应速率随时间变化如图所示。下列有关说法不正确的是
| A.生成物的总能量低于反应物的总能量 |
| B.c点容器内气体颜色不再改变 |
| C.当Δt1=Δt2时,SO2的转化率:a~b段小于b~c段 |
| D.c~d段,反应物浓度减小是影响正反应速率下降的主要因素 |
您最近一年使用:0次
【推荐2】H2O2是重要的消毒剂,研究其分解反应有重要意义。KI能加快H2O2的分解。
①2H2O2=2H2O+O2↑
②H2O2+I-= H2O+IO-;H2O2+IO- =H2O+O2↑+I-
H2O2分解反应过程中能量变化如图所示。下列判断不正确 的是

①2H2O2=2H2O+O2↑
②H2O2+I-= H2O+IO-;H2O2+IO- =H2O+O2↑+I-
H2O2分解反应过程中能量变化如图所示。下列判断

| A.KI在反应中起催化剂的作用 |
| B.H2O2+I-=H2O+IO-是吸热反应 |
| C.KI降低了反应的活化能,反应速率加快 |
| D.加入KI后,2H2O2=2H2O+O2↑的反应热变小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】把煤作为燃料可通过下列两种途径:
途径I:C(s)+O2(g)=CO2(g) △H1
途径II:制水煤气C(s)+H2O(g)=CO(g)+H2(g) △H2
水煤气燃烧2CO(g)+O2(g)=2CO2(g) △H3
2H2(g)+O2(g)=2H2O(g) △H4
下列说法正确的是

途径I:C(s)+O2(g)=CO2(g) △H1
途径II:制水煤气C(s)+H2O(g)=CO(g)+H2(g) △H2
水煤气燃烧2CO(g)+O2(g)=2CO2(g) △H3
2H2(g)+O2(g)=2H2O(g) △H4
下列说法正确的是

| A.途径I的能量变化可用图表示 |
B.△H1=△H2+ (△H3+△H4) (△H3+△H4) |
| C.等质量的煤通过以上两种途径放热:途径I放出的热量<途径II放出的热量 |
| D.如果增大途径II中H2O(g)的用量,则△H2将变大 |
您最近一年使用:0次
【推荐2】通过以下反应均可获取 ,下列有关说法正确的是
,下列有关说法正确的是
①太阳光催化分解水制氢:
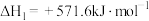
②焦炭与水反应制氢:
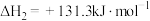
③甲烷与水反应制氢:
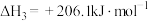
 ,下列有关说法正确的是
,下列有关说法正确的是①太阳光催化分解水制氢:

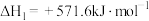
②焦炭与水反应制氢:

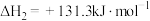
③甲烷与水反应制氢:

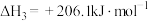
| A.反应①中电能转化为化学能 |
| B.反应②为放热反应 |
C.反应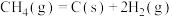 的 的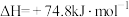 |
D.由上述可知 的燃烧热为 的燃烧热为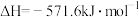 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】煤的液化可以合成甲醇。下列有关说法正确的是
①“气化”: C(s)+2H2O(g)=CO2(g)+2H2(g) ΔH1=+90.1kJ·mol-1;
②催化液化Ⅰ:CO2(g)+3H2(g)= CH3OH(g)+H2O(g) ΔH2= -49.0kJ•mol-1;
③催化液化Ⅱ:CO2(g)+2H2(g)=CH3OH(g)+ O2(g) ΔH3= akJ•mol-1;
O2(g) ΔH3= akJ•mol-1;
①“气化”: C(s)+2H2O(g)=CO2(g)+2H2(g) ΔH1=+90.1kJ·mol-1;
②催化液化Ⅰ:CO2(g)+3H2(g)= CH3OH(g)+H2O(g) ΔH2= -49.0kJ•mol-1;
③催化液化Ⅱ:CO2(g)+2H2(g)=CH3OH(g)+
 O2(g) ΔH3= akJ•mol-1;
O2(g) ΔH3= akJ•mol-1; | A.催化液化Ⅰ中使用催化剂,反应的活化能Ea、ΔH2都减小 |
| B.反应C(s)+H2O(g) +H2(g)=CH3OH(g) ΔH= 41.1 kJ•mol-1 |
| C.ΔH2>ΔH3 |
| D.KOH为电解质溶液的甲醇燃料电池中负极的电极反应为:CH3OH-6e-+6OH-= CO2+5H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列热化学方程式书写正确的是
A.已知:1molH2(g)和1molCl2(g)反应生成2molHCl(g)时放出184.6kJ的热量,则有 H2(g)+ H2(g)+ Cl2(g)=HClg) △H=-92.3kJ/mol Cl2(g)=HClg) △H=-92.3kJ/mol |
| B.2NO2=O2+2NO △H=+116.2kJ/mol |
| C.已知稀溶液中,H+(aq)+OH-(aq)=H2O(1)△H=-57.3kJ/mol,则有Ba(OH)2(aq)+H2SO4(aq)=BaSO4(s)+2H2O(l) △H=-114.6kJ/mol |
| D.2H2(g)+O2(g)=2H2O(l) △H=571.6kJ/mol |
您最近一年使用:0次



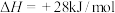


 ,下列判断正确的是
,下列判断正确的是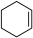 (g)+H2(g)→
(g)+H2(g)→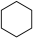 (g)
(g)
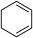 (g)+2H2(g)→
(g)+2H2(g)→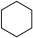 (g)
(g)
 (g)+3H2(g)→
(g)+3H2(g)→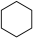 (g)
(g)
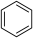 (g)+ H2(g)→
(g)+ H2(g)→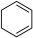 (g)
(g)


