某元素基态原子的价电子排布为ns1,当它跟卤素结合时可形成的化学键是
| A.一定是共价键 |
| B.一定是离子键 |
| C.可能是共价键,也可能是离子键 |
| D.一定是极性共价键 |
更新时间:2023-08-23 21:19:53
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】有A、B、C、D四种元素,其中A、B、C属于同一周期, A原子最外层p能级的电子数等于次外层的电子总数;B原子最外层中有三个未成对的电子; C元素可分别,与A、B、D生成RC2型化合物,其中的DC2与C3互为等电子体。下列叙述中不正确的是
| A.D原子的简化电子排布式为[Ar]3s23p4 |
| B.B、C两元素的第一电离能大小关系为B>C |
C.AD2 的电子式为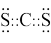 |
| D.由B60分子形成的晶体与A60相似,分子中总键能:B60 >A60 |
您最近一年使用:0次
【推荐2】下列化学用语表述错误的是
A.中子数为10的氧原子: |
B.基态溴原子的电子排布式: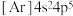 |
C. 的电子式: 的电子式: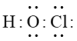 |
D.基态氮原子的价层电子轨道表示式: |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】铁和钛是重要的金属材料,铁及其化合物在生活中常用于净水、制作颜料、食品保鲜等。Ti-Fe合金是优良的储氢合金。一种利用钛铁矿( ,含
,含 杂质)制备钛的工艺流程如下。
杂质)制备钛的工艺流程如下。
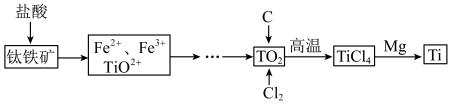
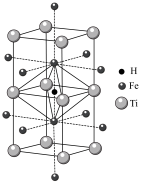
下列关于制取钛的工艺流程及Ti-Fe储氢合金(结构如图)的说法不正确的是
 ,含
,含 杂质)制备钛的工艺流程如下。
杂质)制备钛的工艺流程如下。
下列关于制取钛的工艺流程及Ti-Fe储氢合金(结构如图)的说法不正确的是

A. 的价电子排布为 的价电子排布为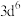 |
| B.Ti-Fe储氢合金中H原子位于金属原子形成的四面体空隙中 |
C. 完全水解生成 完全水解生成 : :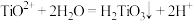 |
D. 与盐酸反应: 与盐酸反应: |
您最近一年使用:0次



