某学习小组将氯气和空气按体积比1∶3混合,通入含水 的碳酸钠中制备
的碳酸钠中制备 ,然后用水吸收
,然后用水吸收 制备次氯酸溶液。
制备次氯酸溶液。
ⅰ. 在饱和食盐水中溶解度很小,能与含水
在饱和食盐水中溶解度很小,能与含水 的碳酸钠反应生成
的碳酸钠反应生成 。
。
ⅱ. 极易溶于水生成
极易溶于水生成 ;
; 的沸点为
的沸点为 ,
, 以上分解为
以上分解为 和
和 。
。
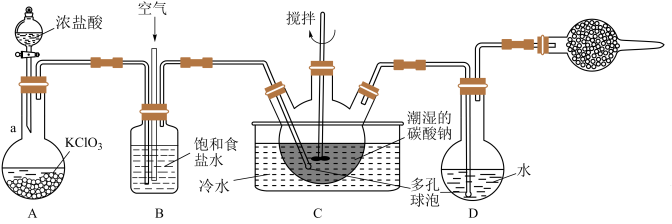
(1)仪器 的名称是
的名称是_________ ,A中发生反应的离子方程式为_________ 。
(2)实验中须控制 与空气(不参与反应)的体积比为
与空气(不参与反应)的体积比为 ,装置
,装置 的作用
的作用__________________ (答出2条即可)
(3)装置 中生成
中生成 ,反应的化学方程式为
,反应的化学方程式为__________________ 。
(4)将制得的 溶液加入滴有酚酞的氢氧化钠溶液中,观察到溶液红色褪去。溶液褪色的原因可能有两个:①
溶液加入滴有酚酞的氢氧化钠溶液中,观察到溶液红色褪去。溶液褪色的原因可能有两个:① 与
与 发生中和反应,②
发生中和反应,②____________ 。设计实验探究溶液红色褪去的原因___________________________ 。
(5)测定装置D中 溶液的物质的量浓度的实验方案:取
溶液的物质的量浓度的实验方案:取 溶液,加入足量
溶液,加入足量 溶液,再加入足量硝酸银溶液,过滤,洗涤,干燥,用电子天平称量沉淀的质量为
溶液,再加入足量硝酸银溶液,过滤,洗涤,干燥,用电子天平称量沉淀的质量为 ,则
,则 溶液的物质的量浓度为
溶液的物质的量浓度为______  (
( 可被
可被 还原成
还原成 )。
)。
 的碳酸钠中制备
的碳酸钠中制备 ,然后用水吸收
,然后用水吸收 制备次氯酸溶液。
制备次氯酸溶液。ⅰ.
 在饱和食盐水中溶解度很小,能与含水
在饱和食盐水中溶解度很小,能与含水 的碳酸钠反应生成
的碳酸钠反应生成 。
。ⅱ.
 极易溶于水生成
极易溶于水生成 ;
; 的沸点为
的沸点为 ,
, 以上分解为
以上分解为 和
和 。
。
(1)仪器
 的名称是
的名称是(2)实验中须控制
 与空气(不参与反应)的体积比为
与空气(不参与反应)的体积比为 ,装置
,装置 的作用
的作用(3)装置
 中生成
中生成 ,反应的化学方程式为
,反应的化学方程式为(4)将制得的
 溶液加入滴有酚酞的氢氧化钠溶液中,观察到溶液红色褪去。溶液褪色的原因可能有两个:①
溶液加入滴有酚酞的氢氧化钠溶液中,观察到溶液红色褪去。溶液褪色的原因可能有两个:① 与
与 发生中和反应,②
发生中和反应,②(5)测定装置D中
 溶液的物质的量浓度的实验方案:取
溶液的物质的量浓度的实验方案:取 溶液,加入足量
溶液,加入足量 溶液,再加入足量硝酸银溶液,过滤,洗涤,干燥,用电子天平称量沉淀的质量为
溶液,再加入足量硝酸银溶液,过滤,洗涤,干燥,用电子天平称量沉淀的质量为 ,则
,则 溶液的物质的量浓度为
溶液的物质的量浓度为 (
( 可被
可被 还原成
还原成 )。
)。
22-23高一上·山东淄博·期末 查看更多[5]
山东省淄博实验中学2022-2023学年高一上学期期末考试化学试题(已下线)专题04 钠、氯及其化合物-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)黑龙江省大庆铁人中学2023-2024学年高一上学期期末考试化学试题海南省白沙学校2023-2024学年高一上学期期末考试化学试题四川省射洪中学校2023-2024学年高一(强基班)上学期第三次月考化学试题
更新时间:2023-08-22 14:33:30
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】已知下表,用化学式或元素符号回答下列问题。
(1)11种元素中,化学性质最不活泼的是_______ ,原子半径最小的是_______ 。
(2)①②③④⑤中,最高价氧化物的水化物,碱性最强的是_______ 。
(3)②③⑤⑨中形成的简单离子半径由大到小的顺序是_______ 。
(4)元素⑦的简单氢化物电子式为_______ ,该氢化物常温下和元素②的单质反应的离子方程式是_______ 。
(5)①和⑤最高价氧化物对应的水化物相互反应的离子方程式为_______ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑥ | ⑦ | ⑧ | |||||
| 3 | ① | ③ | ⑤ | ⑨ | ⑪ | |||
| 4 | ② | ④ | ⑩ |
(2)①②③④⑤中,最高价氧化物的水化物,碱性最强的是
(3)②③⑤⑨中形成的简单离子半径由大到小的顺序是
(4)元素⑦的简单氢化物电子式为
(5)①和⑤最高价氧化物对应的水化物相互反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,取两片质量相等、外形和组成相同表面经过砂纸打磨(完全除掉了氧化物)的铝片,分别加入到盛有体积相同、c(H+)相同的稀硫酸和稀盐酸溶液的两支试管(相同体积)中制取H2。实验现象如下表:
(1)写出以上反应的离子方程式___________ ;
(2)分析上表数据,你得出的结论是:___________ ;
(3)对你以上的结论可能的原因提出假设(写出一个即可):___________ ;
(4)请设计实验对你的假设进行验证:___________ 。
| 时间 酸 | 1min | 2min | 5min | 15min | 20min |
| 实验一:3mol/L盐酸 | 少量气泡 | 较多气泡 | 大量气泡 | 反应剧烈 | 铝片耗尽 |
| 实验二:1.5mol/L硫酸 | 均无明显现象(无气泡) | ||||
(2)分析上表数据,你得出的结论是:
(3)对你以上的结论可能的原因提出假设(写出一个即可):
(4)请设计实验对你的假设进行验证:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】[Co(NH3)6]Cl3(三氯六氨合钴)是一种重要的化工产品,常用于合成其它Co(II)配合物。以下是一种制备三氯六氨合钴的实验方法,回答下列问题:
氯化钴的制备
已知氯化钴(CoCl2)易潮解,可用高熔点金属钴与氯气反应制取氯化钴。实验室提供下列装置进行组合(连接用橡胶管省略):
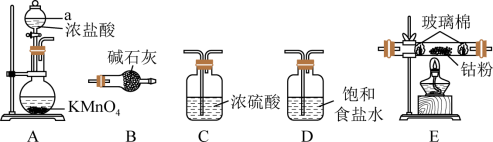
(1)仪器a的名称是______ ,用图中的装置组合制备氯化钴,连接顺序为______ (以上每个装置只能用一次)。
A→______→______→______→______
(2)正确连接好装置,______ ,装药品,先______ ,待后______ ,再点燃E处酒精灯进行实验。
(3)装置E中发生的化学方程式为______ ,装置A中发生的离子方程式为______ 。
(4)用正确的连接装置进行实验,B的作用是______ ;C的作用是______ ;D的作用是______ 。
(5)用正确的连接装置进行实验,此装置的缺点是______ 。
氯化钴的制备
已知氯化钴(CoCl2)易潮解,可用高熔点金属钴与氯气反应制取氯化钴。实验室提供下列装置进行组合(连接用橡胶管省略):

(1)仪器a的名称是
A→______→______→______→______
(2)正确连接好装置,
(3)装置E中发生的化学方程式为
(4)用正确的连接装置进行实验,B的作用是
(5)用正确的连接装置进行实验,此装置的缺点是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】第VA族元素单质及其化合物在生产、生活中有重要的用途。
(1)下列说法正确的是__________ (填序号)。
a.含氧酸的酸性:HNO3>H3PO4>H3AsO4 b.原子半径:S >P>As
c.氢化物的稳定性NH3>PH3> AsH3d.AsH3电子式是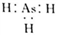
(2)雌黄(As2S3 )和雄黄(As4S4)都是自然界中常见的砷化物,早期都曾用作绘画颜料,因都有抗病毒疗效也用来入药。砷元素有+2、+3两种常见价态。一定条件下,雌黄和雄黄的转化关系如图所示。
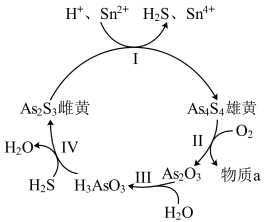
①Ⅱ中若1molAs4S4反应转移28mole-,a物质是__________ 。
②Ⅰ中反应的离子方程式是____________________________________ 。
(3)亚砷酸(H3AsO3)可以用于治疗白血病,其在溶液中存在多种微粒形态,各种微粒物质的量分数与溶液的pH关系如图所示。
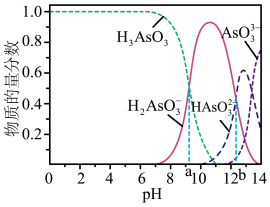
①人体血液的pH在7.35~7.45 之间,用药后人体中含砷元素的主要微粒是___________ 。
②H3AsO3的一级电离常数是6×10-10mol·L-1,n(H3AsO3)∶n(H2AsO3-)=1∶1时,溶液的pH=___________ (列出计算式即可)。
(4)由辉铋矿(主要成分为Bi2S3,含杂质PbO2等)制备Bi2O3的工艺如图所示:
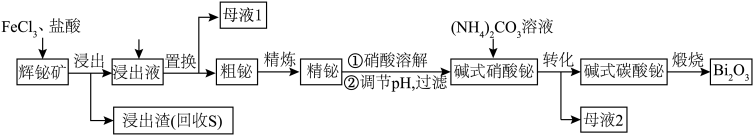
①“浸出”时Bi2S3与FeCl3 溶液反应的离子方程式为________________________________ 。
②“置换”时生成单质铋的离子方程式为____________________________________ 。
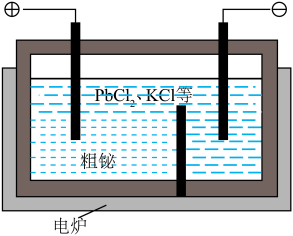
③“粗铋”中含有的杂质主要是Pb,通过熔融盐电解精炼可达到除杂的目的,其装置示意图如所示。电解后阳极底部留下的为精铋。写出阳极电极反应的方程式__________________________ 。
(1)下列说法正确的是
a.含氧酸的酸性:HNO3>H3PO4>H3AsO4 b.原子半径:S >P>As
c.氢化物的稳定性NH3>PH3> AsH3d.AsH3电子式是
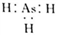
(2)雌黄(As2S3 )和雄黄(As4S4)都是自然界中常见的砷化物,早期都曾用作绘画颜料,因都有抗病毒疗效也用来入药。砷元素有+2、+3两种常见价态。一定条件下,雌黄和雄黄的转化关系如图所示。

①Ⅱ中若1molAs4S4反应转移28mole-,a物质是
②Ⅰ中反应的离子方程式是
(3)亚砷酸(H3AsO3)可以用于治疗白血病,其在溶液中存在多种微粒形态,各种微粒物质的量分数与溶液的pH关系如图所示。

①人体血液的pH在7.35~7.45 之间,用药后人体中含砷元素的主要微粒是
②H3AsO3的一级电离常数是6×10-10mol·L-1,n(H3AsO3)∶n(H2AsO3-)=1∶1时,溶液的pH=
(4)由辉铋矿(主要成分为Bi2S3,含杂质PbO2等)制备Bi2O3的工艺如图所示:

①“浸出”时Bi2S3与FeCl3 溶液反应的离子方程式为
②“置换”时生成单质铋的离子方程式为
③“粗铋”中含有的杂质主要是Pb,通过熔融盐电解精炼可达到除杂的目的,其装置示意图如所示。电解后阳极底部留下的为精铋。写出阳极电极反应的方程式

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】硼、镁及其化合物在工农业生产中应用广泛。已知:硼镁矿主要成分为Mg2B2O5•H2O,硼砂的化学式为Na2B4O7•10H2O.利用硼镁矿制取金属镁及粗硼的工艺流程如下.

回答下列有关问题:
(1)硼砂中B的化合价为_________ ,溶于热水后,常用H2SO4调pH到2~3制取H3BO3,反应的离子方程式为________ 。
(2)X为H3BO3晶体加热脱水的产物,其与Mg反应制取粗硼的化学方程式为________ ,MgCl2•7H2O脱水需要在HCl氛围中加热,其目的是________ 。
(3)硼氢化钠是一种常用的还原剂,它与水反应的离子方程式是BH4-+2H2O=BO2-+4H2↑。硼氢化钠在溶液中能把许多金属离子还原为金属单质,为了抑制它与水的反应,反应应在_______ (填“酸性”“中性”或“碱性”)条件下进行,试完成并配平金离子(Au3+)被硼氢化钠还原的离子方程式:
_____ Au3++____ BH4-+_____ OH-═___ Au↓+______ BO2-+____ ______ 。

回答下列有关问题:
(1)硼砂中B的化合价为
(2)X为H3BO3晶体加热脱水的产物,其与Mg反应制取粗硼的化学方程式为
(3)硼氢化钠是一种常用的还原剂,它与水反应的离子方程式是BH4-+2H2O=BO2-+4H2↑。硼氢化钠在溶液中能把许多金属离子还原为金属单质,为了抑制它与水的反应,反应应在
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】以焙烧黄铁矿(主要成分 FeS2,杂质为 SiO2等)制取 SO2时产生的红渣为原料,制备铵铁蓝 Fe(NH4)[Fe(CN)6]颜料。工艺流程如下:

回答下列问题:
(1)焙烧黄铁矿发生的反应方程式为_____ ,滤渣①的主要成分为_____ (填化学式)。
(2)红渣研细的目的是_____ 。
(3)“还原”时,发生反应的化学方程式为_____ 。
(4)工序①得到绿矾(FeSO4·7H2O)和母液,则工序①的操作名称为_____ 。
(5)用 K3[Fe(CN)6]可检验工序①所得母液中的金属阳离子,检验时发生的离子方程式为_____ ,所得母液循环使用。
(6)沉铁工序产生的白色沉淀 Fe(NH4)2[Fe(CN)6]中Fe 的化合价为_____ ,氧化工序发生反应的离子方程式为_____ 。

回答下列问题:
(1)焙烧黄铁矿发生的反应方程式为
(2)红渣研细的目的是
(3)“还原”时,发生反应的化学方程式为
(4)工序①得到绿矾(FeSO4·7H2O)和母液,则工序①的操作名称为
(5)用 K3[Fe(CN)6]可检验工序①所得母液中的金属阳离子,检验时发生的离子方程式为
(6)沉铁工序产生的白色沉淀 Fe(NH4)2[Fe(CN)6]中Fe 的化合价为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某课外小组利用乙炔与酸性KMnO4溶液反应,测定乙炔的相对分子质量。图为测定装置示意图。
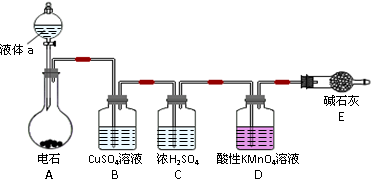
(1)实验室制取乙炔时,分液漏斗中的液体a通常是_______ 。
(2)CuSO4溶液的作用是_______ 。
(3)配平乙炔与酸性KMnO4溶液反应的化学方程式:
C2H2+ KMnO4+ H2SO4= K2SO4+ MnSO4+ CO2↑+ H2O
_____
(4)该小组实验如下:实验前,D装置中KMnO4的物质的量为x mol。实验完毕,D及E装置的总质量共增重y g,此时D中过量的KMnO4恰好能与含z mol FeSO4的溶液完全反应(注:反应中MnO 被还原成Mn2+,Fe2+被氧化成Fe3+)。则所测乙炔的相对分子质量是(请用含字母x、y、z的代数式表示)
被还原成Mn2+,Fe2+被氧化成Fe3+)。则所测乙炔的相对分子质量是(请用含字母x、y、z的代数式表示)_______ 。
(5)若该小组实验原理及所有操作均正确,则下列各因素对所测乙炔的相对分子质量没有影响的是(填选项)_______ 。
A.装置A中产生的气体直接通入酸性KMnO4溶液
B.乙炔通过酸性KMnO4溶液的速率过快,少量乙炔未被氧化而逸出
C.将E装置(盛有碱石灰的干燥管)换成盛有浓硫酸的洗气瓶
(6)另一课外小组认为,该课外小组的实验装置及实验操作存在不足,请用简明文字说明,应采取何种措施或改进?答:_______ 。

(1)实验室制取乙炔时,分液漏斗中的液体a通常是
(2)CuSO4溶液的作用是
(3)配平乙炔与酸性KMnO4溶液反应的化学方程式:
C2H2+ KMnO4+ H2SO4= K2SO4+ MnSO4+ CO2↑+ H2O
(4)该小组实验如下:实验前,D装置中KMnO4的物质的量为x mol。实验完毕,D及E装置的总质量共增重y g,此时D中过量的KMnO4恰好能与含z mol FeSO4的溶液完全反应(注:反应中MnO
 被还原成Mn2+,Fe2+被氧化成Fe3+)。则所测乙炔的相对分子质量是(请用含字母x、y、z的代数式表示)
被还原成Mn2+,Fe2+被氧化成Fe3+)。则所测乙炔的相对分子质量是(请用含字母x、y、z的代数式表示)(5)若该小组实验原理及所有操作均正确,则下列各因素对所测乙炔的相对分子质量没有影响的是(填选项)
A.装置A中产生的气体直接通入酸性KMnO4溶液
B.乙炔通过酸性KMnO4溶液的速率过快,少量乙炔未被氧化而逸出
C.将E装置(盛有碱石灰的干燥管)换成盛有浓硫酸的洗气瓶
(6)另一课外小组认为,该课外小组的实验装置及实验操作存在不足,请用简明文字说明,应采取何种措施或改进?答:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】工业制得的氮化铝(AlN)产品中常含有少量Al4C3、Al2O3、C等杂质。某同学设计如下实验分别测定氮化铝(AlN样品中AlN和Al4C3的质量分数(忽略NH3在强碱性溶液中的溶解)。
(1)实验原理:
①Al4C3与硫酸反应可生成CH4;
②AIN溶于强酸产生铵盐,溶于强碱生成氨气,请写出AlN与NaOH溶液反应的化学方程式:____________ 。
(2)实验装置(如图所示,量气管为碱式滴定管改装)

连好装置后,首先应进行的操作是________ 。
(3)实验过程:称得装置D的初始质量为yg;称取xgAlN样品置于装置B锥形瓶中,各装置中加入相应药品,重新连好装置;读取量气管的初始读数为amL(量气装置左右液面相平)。
①欲首先测量Al4C3质量分数的有关数据,对三个活塞的操作是________ 。
②若无恒压管,对所测气体体积的影响是________ (填“偏大”“偏小”或“无影响”)
③量气管中液面不再发生变化,说明反应已经结束。读取读数之前,应对量气管进行的操作为____ ;若量气管中的液面高于右侧球形容器中的液面,所测气体的体积______ (填“偏大”“偏小”或“无影响”)。
④记录滴定管的读数为bmL(已知:该实验条件下的气体摩尔体积为VmL·mol-1),则Al4C3的质量分数为______ (用含a、b、x、y、Vm的代数式表示)。
⑤测量AlN质量分数的数据:首先关闭活塞__ ,打开活塞___ ,通过分液漏斗加入过量___ ,与装置B瓶内物质充分反应;反应完成后,____ (填入该步应进行的操作),最后称得装置D的质量为zg。
(1)实验原理:
①Al4C3与硫酸反应可生成CH4;
②AIN溶于强酸产生铵盐,溶于强碱生成氨气,请写出AlN与NaOH溶液反应的化学方程式:
(2)实验装置(如图所示,量气管为碱式滴定管改装)

连好装置后,首先应进行的操作是
(3)实验过程:称得装置D的初始质量为yg;称取xgAlN样品置于装置B锥形瓶中,各装置中加入相应药品,重新连好装置;读取量气管的初始读数为amL(量气装置左右液面相平)。
①欲首先测量Al4C3质量分数的有关数据,对三个活塞的操作是
②若无恒压管,对所测气体体积的影响是
③量气管中液面不再发生变化,说明反应已经结束。读取读数之前,应对量气管进行的操作为
④记录滴定管的读数为bmL(已知:该实验条件下的气体摩尔体积为VmL·mol-1),则Al4C3的质量分数为
⑤测量AlN质量分数的数据:首先关闭活塞
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下图为元素周期表的一部,根据元素①~⑧在表中的位置回答下列问题。
(1)元素⑧的最高价氧化物对应水化物的分子式为:___________ ;
(2)元素①与④形成的18电子的化合物的结构式为___________ ;
(3)用电子式表示元素⑤与⑧形成化合物的过程:___________ ;
(4)元素⑥的单质与⑤的最高价氧化物对应水化物反应的化学方程式___________ ;
(5)②是自然界中化合物种类存在最多的元素,其中一种化合物对水果具有催熟作用,能使溴的四氯化碳溶液褪色,该反应的化学方程式是___________ ,反应类型为___________ 。一定条件下,该化合物可以发生自身加聚反应,请写出该反应的化学方程式___________ 。
(6)假设元素⑦的元素符号为X,氧化物XO2是大气中常见污染物,某化学兴趣小组为测定XO2在空气中的含量,以aL/min(标准状况)的流量将空气通入200mL0.100mol/L的酸性高锰酸钾溶液中,发生反应:5XO2+2 +2H2O=5XO
+2H2O=5XO +2Mn2++4H+。bmin钟后,溶液恰好褪色。假定该氧化物能被溶液完全吸收,则空气中该氧化物的含量为
+2Mn2++4H+。bmin钟后,溶液恰好褪色。假定该氧化物能被溶液完全吸收,则空气中该氧化物的含量为___________ g/L。
族 周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |
(2)元素①与④形成的18电子的化合物的结构式为
(3)用电子式表示元素⑤与⑧形成化合物的过程:
(4)元素⑥的单质与⑤的最高价氧化物对应水化物反应的化学方程式
(5)②是自然界中化合物种类存在最多的元素,其中一种化合物对水果具有催熟作用,能使溴的四氯化碳溶液褪色,该反应的化学方程式是
(6)假设元素⑦的元素符号为X,氧化物XO2是大气中常见污染物,某化学兴趣小组为测定XO2在空气中的含量,以aL/min(标准状况)的流量将空气通入200mL0.100mol/L的酸性高锰酸钾溶液中,发生反应:5XO2+2
 +2H2O=5XO
+2H2O=5XO +2Mn2++4H+。bmin钟后,溶液恰好褪色。假定该氧化物能被溶液完全吸收,则空气中该氧化物的含量为
+2Mn2++4H+。bmin钟后,溶液恰好褪色。假定该氧化物能被溶液完全吸收,则空气中该氧化物的含量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
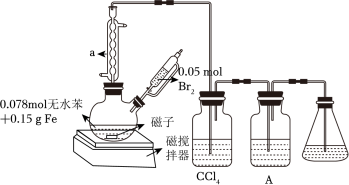
【推荐1】实验室制取溴苯的装置如图所示。
有关数据如下:
回答下列问题:
(1)仪器a的作用是___________ 。
(2)二颈烧瓶中生成有机物发生反应的化学方程式为___________ 。
(3)A装置盛装___________ (填试剂)用于检验诱导期已过,反应开始。当出现 ___________ (填现象)时,证明反应已结束。
(4)取反应后的混合物,经过一系列操作得到纯净的溴苯:
①水洗除去___________ ,分液;
②用NaOH稀溶液洗涤,除去___________ ,分液;
③水洗,分液;
④用干燥剂干燥,过滤;
⑤___________ ,分离溴苯和苯。
(5)经过一系列操作得到纯净的溴苯5ml,产率为___________ (保留三位有效数字)。
有关数据如下:
| 物质 | 苯 | 溴 | 溴苯 |
| 密度(g•cm﹣3) | 0.88 | 3.12 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 在水中的溶解性 | 不溶 | 微溶 | 不溶 |
(1)仪器a的作用是
(2)二颈烧瓶中生成有机物发生反应的化学方程式为
(3)A装置盛装
(4)取反应后的混合物,经过一系列操作得到纯净的溴苯:
①水洗除去
②用NaOH稀溶液洗涤,除去
③水洗,分液;
④用干燥剂干燥,过滤;
⑤
(5)经过一系列操作得到纯净的溴苯5ml,产率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】苯胺是一种重要精细化工原料,在染料、医药等行业中具有广泛的应用。实验室以苯为原料制取苯胺,其原理简示如下:

Ⅰ.制取硝基苯
实验步骤:实验室采用如图所示装置制取硝基苯,恒压滴液漏斗中装有一定量的苯,三颈烧瓶装有一定比例的浓硫酸和浓硝酸混合物。

请回答下列问题:
(1)实验装置中长玻璃管可以用_______ 代替(填仪器名称)。
(2)下列说法中正确的是_______(填序号)。
(3)粗硝基苯用5% NaOH溶液洗涤的目的是_______ 。
Ⅱ.制取苯胺
①组装好实验装置(如下图,夹持仪器已略去),并检查气密性。

②先向三颈烧瓶中加入沸石及硝基苯,再取下恒压滴液漏斗,换上温度计。
③打开活塞K,通入 一段时间。
一段时间。
④利用油浴加热,使反应液温度维持在140℃进行反应。
⑤反应结束后,关闭活塞K,向三颈烧瓶中加入生石灰。
⑤调整好温度计的位置,继续加热,收集182~186℃馏分,得到较纯苯胺。
回答下列问题:
(4)步骤②中温度计水银球的位置位于_______ (填序号,下同),步骤⑥中位于_______ 。
A.烧瓶内反应液中
B.贴近烧瓶内液面处
C.三颈烧瓶出气口(等高线)附近
(5)步骤⑤中,加入生石灰的作用是_______ 。
(6)若实验中硝基苯用量为10mL,最后得到苯胺5.6g,苯胺的产率为_______ (计算结果精确到0.1%)。

| 物质 | 相对分子质量 | 沸点℃ | 密度g/mL | 溶解性 |
| 硝基苯 | 123 | 210.9 | 1.23 | 不溶于水,易溶于乙醇、乙醚 |
| 苯胺 | 93 | 184.4 | 1.02 | 微溶于水,易溶于乙醇、乙醚;还原性强、易被氧化 |
实验步骤:实验室采用如图所示装置制取硝基苯,恒压滴液漏斗中装有一定量的苯,三颈烧瓶装有一定比例的浓硫酸和浓硝酸混合物。

请回答下列问题:
(1)实验装置中长玻璃管可以用
(2)下列说法中正确的是_______(填序号)。
| A.配制混酸时,将浓硝酸沿杯壁缓缓加入浓硫酸中,并不断搅拌、冷却 |
| B.温度控制在50~60℃原因之一是减少副反应的发生 |
| C.制得的粗硝基苯可以先用乙醇萃取,分液后再洗涤 |
| D.浓硫酸可以降低该反应活化能 |
Ⅱ.制取苯胺
①组装好实验装置(如下图,夹持仪器已略去),并检查气密性。

②先向三颈烧瓶中加入沸石及硝基苯,再取下恒压滴液漏斗,换上温度计。
③打开活塞K,通入
 一段时间。
一段时间。④利用油浴加热,使反应液温度维持在140℃进行反应。
⑤反应结束后,关闭活塞K,向三颈烧瓶中加入生石灰。
⑤调整好温度计的位置,继续加热,收集182~186℃馏分,得到较纯苯胺。
回答下列问题:
(4)步骤②中温度计水银球的位置位于
A.烧瓶内反应液中
B.贴近烧瓶内液面处
C.三颈烧瓶出气口(等高线)附近
(5)步骤⑤中,加入生石灰的作用是
(6)若实验中硝基苯用量为10mL,最后得到苯胺5.6g,苯胺的产率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】请回答下列问题
(1)浓硫酸与木炭在加热条件下的化学方程式为___________ 。
(2)试用上述各装置设计一个实验,验证上述反应所产生的各种产物。这些装置的连接顺序(按产物气流从左到右的方向)是(填装置的编号)___________ →___________ →___________ →___________ 。
(3)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色。A瓶溶液的作用是___________ ,C瓶溶液的作用是___________ 。
(4)装置②中所加的固体药品是___________ ,确定装置②在整套装置中位置的理由是___________ 。
(5)装置③中所盛的溶液可验证的产物是___________ 。
| 编号 | ① | ② |
| 装置 | 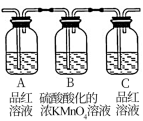 |  |
| 编号 | ③ | ④ |
| 装置 | 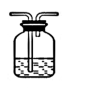 | 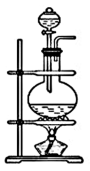 |
(2)试用上述各装置设计一个实验,验证上述反应所产生的各种产物。这些装置的连接顺序(按产物气流从左到右的方向)是(填装置的编号)
(3)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色。A瓶溶液的作用是
(4)装置②中所加的固体药品是
(5)装置③中所盛的溶液可验证的产物是
您最近一年使用:0次



