某兴趣小组设计如图所示装置制取SO2,研究其性质,并进一步探究在适当温度和催化剂的条件下,SO2与O2反应后混合气体的成分。
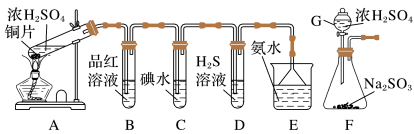
(1)仪器G的名称是___________ 。
(2)写出A中反应的化学方程式___________ 。
(3)装置B、C、D分别用于检验SO2的漂白性、还原性和氧化性。则装置C中反应的离子方程式为___________ 。证明SO2具有氧化性的实验现象是___________ 。
(4)为了实现绿色环保的目标,某同学设计装置F来代替装置A.与装置A相比,装置F的优点是___________ (写出一条即可)。
(5)若选用装置F制取O2可选用的试剂是___________ 。
(6)该小组同学设计如下装置来检验SO2与O2反应后混合气体的成分。
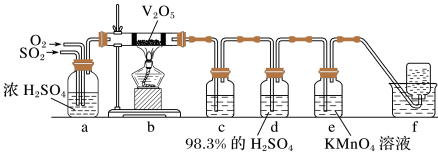
已知:SO3遇水剧烈反应,放出大量的热,产生酸雾。98.3%的H2SO4可以吸收SO3和酸雾。
供选择试剂:蒸馏水、0.5mol·L-1BaCl2溶液、98.3%的H2SO4、2.0mol·L-1NaOH溶液、KMnO4溶液。
①c中应选用的试剂是___________ ,e中试剂的作用是___________ ,f中收集的气体是___________ 。
②甲同学提出用饱和NaHSO3溶液代替98.3%的H2SO4,乙同学提出质疑,认为此方案不可行,请简述乙同学认为不可行的理由:___________ 。

(1)仪器G的名称是
(2)写出A中反应的化学方程式
(3)装置B、C、D分别用于检验SO2的漂白性、还原性和氧化性。则装置C中反应的离子方程式为
(4)为了实现绿色环保的目标,某同学设计装置F来代替装置A.与装置A相比,装置F的优点是
(5)若选用装置F制取O2可选用的试剂是
(6)该小组同学设计如下装置来检验SO2与O2反应后混合气体的成分。

已知:SO3遇水剧烈反应,放出大量的热,产生酸雾。98.3%的H2SO4可以吸收SO3和酸雾。
供选择试剂:蒸馏水、0.5mol·L-1BaCl2溶液、98.3%的H2SO4、2.0mol·L-1NaOH溶液、KMnO4溶液。
①c中应选用的试剂是
②甲同学提出用饱和NaHSO3溶液代替98.3%的H2SO4,乙同学提出质疑,认为此方案不可行,请简述乙同学认为不可行的理由:
更新时间:2023-08-24 22:41:56
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】某研究小组设计如图装置制取 并对其性质进行探究(部分夹持装置略)。
并对其性质进行探究(部分夹持装置略)。
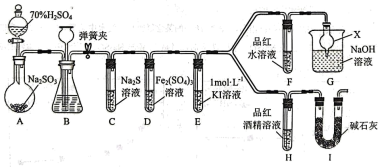
回答下列问题:
(1)仪器 的名称是
的名称是___________ 装置C的作用是验证 具有
具有___________ 性。
(2)装置B的作用除了可以通过观察产生气泡的多少判断反应的快慢外,还有___________ 。B中应选用的试剂为___________ 。
(3)装置D中发生反应的离子方程式为___________ ,小组某同学为验证 与
与 发生反应,设计实验:取适量装置D中溶液,滴加少量溴水,溴水褪色说明发生反应。该方案是否合理并说明理由
发生反应,设计实验:取适量装置D中溶液,滴加少量溴水,溴水褪色说明发生反应。该方案是否合理并说明理由___________ 。
(4)实验开始后,发现装置 中的溶液迅速变黄,继续通入
中的溶液迅速变黄,继续通入 ,一段时间后出现乳黄色浑浊。查阅资料得知:
,一段时间后出现乳黄色浑浊。查阅资料得知: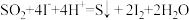 。实验结束取适量装置
。实验结束取适量装置 中浊液,向其中滴加几滴淀粉溶液,振荡,无明显现象,用离子方程式说明加入淀粉溶液无明显现象的原因是
中浊液,向其中滴加几滴淀粉溶液,振荡,无明显现象,用离子方程式说明加入淀粉溶液无明显现象的原因是___________ 。
(5)小组同学观察到装置 中红色褪去,装置
中红色褪去,装置 中无明显现象,据此分析能使品红水溶液褪色的微粒可能是
中无明显现象,据此分析能使品红水溶液褪色的微粒可能是___________ 。
 并对其性质进行探究(部分夹持装置略)。
并对其性质进行探究(部分夹持装置略)。
回答下列问题:
(1)仪器
 的名称是
的名称是 具有
具有(2)装置B的作用除了可以通过观察产生气泡的多少判断反应的快慢外,还有
(3)装置D中发生反应的离子方程式为
 与
与 发生反应,设计实验:取适量装置D中溶液,滴加少量溴水,溴水褪色说明发生反应。该方案是否合理并说明理由
发生反应,设计实验:取适量装置D中溶液,滴加少量溴水,溴水褪色说明发生反应。该方案是否合理并说明理由(4)实验开始后,发现装置
 中的溶液迅速变黄,继续通入
中的溶液迅速变黄,继续通入 ,一段时间后出现乳黄色浑浊。查阅资料得知:
,一段时间后出现乳黄色浑浊。查阅资料得知: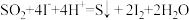 。实验结束取适量装置
。实验结束取适量装置 中浊液,向其中滴加几滴淀粉溶液,振荡,无明显现象,用离子方程式说明加入淀粉溶液无明显现象的原因是
中浊液,向其中滴加几滴淀粉溶液,振荡,无明显现象,用离子方程式说明加入淀粉溶液无明显现象的原因是(5)小组同学观察到装置
 中红色褪去,装置
中红色褪去,装置 中无明显现象,据此分析能使品红水溶液褪色的微粒可能是
中无明显现象,据此分析能使品红水溶液褪色的微粒可能是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】学习小组在实验字研究SO2并进行相关性质的探究。葡萄酒中SO2最大使用量0.25g∙L-1,取300.00mL葡萄酒,通过适当的方法使所含SO2全部逸出并用H2O2将其全部氧化为H2SO4,然后用0.0900mol∙L-1NaOH标准溶液进行滴定。
(1)如图所示,仪器A的名称_______ 。
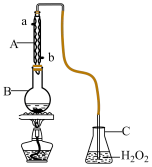
(2)写出 SO2气体与H2O2溶液反应的化学方程式_______ 。
(3)用标准液滴定前排气泡时,应选择图中的_______(填字母)。
(4)上述滴定实验中若滴定终点时溶液的pH=8.8,可选择_______ 为指示剂,选择该指示剂时如何判断反应到达滴定终点_______ 。
(5)滴定前读数时平视凹液面,滴定终点读数时俯视刻度线,则测量结果比实际值_______ (填“偏高”“偏低”或“无影响”)。
(6)滴定至终点时,消耗NaOH溶液20.00mL,则该葡萄酒中SO2的含量是否超标?_______ (填“是”或“否”)
(1)如图所示,仪器A的名称

(2)写出 SO2气体与H2O2溶液反应的化学方程式
(3)用标准液滴定前排气泡时,应选择图中的_______(填字母)。
A.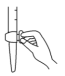 | B.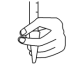 | C. | D. |
(5)滴定前读数时平视凹液面,滴定终点读数时俯视刻度线,则测量结果比实际值
(6)滴定至终点时,消耗NaOH溶液20.00mL,则该葡萄酒中SO2的含量是否超标?
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】硫代硫酸钠(Na2S2O3)可用做分析试剂及鞣革还原剂。实验室制取硫代硫酸钠的装置如图所示。
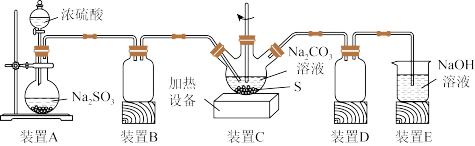
(1)装置B的作用是_______ ,装置E发生作用时反应的离子方程式为_______ 。
(2)装置C用于制取Na2S2O3,反应分两步,第二步反应的化学方程式为S+Na2SO3=Na2S2O3,则第一步反应的化学方程式为_______ 。
(3)若将SO2与Cl2以1∶1的物质的量之比通入品红溶液中,发现品红溶液不褪色,原因是(用化学方程式解释)_______ 。
(4)Na2SO3常因被空气中的氧气氧化而变质,验证本实验所用Na2SO3固体是否变质的方法是:取少量Na2SO3固体于试管中,加入适量的水配成溶液,_______ 。
(5)用已知浓度的硫代硫酸钠溶液可以测定I2溶液的物质的量浓度。
步骤Ⅰ:准确称取7.9g硫代硫酸钠固体,加水溶解后,全部转移到100mL容量瓶中,加水定容至100mL。
步骤Ⅱ:量取含I2溶液20.0mL,向其中加入步骤Ⅰ所配硫代硫酸钠溶液,恰好完全反应时消耗硫代硫酸钠溶液20.0mL。
已知反应为 (未配平),则含I2溶液中I2的物质的量浓度为
(未配平),则含I2溶液中I2的物质的量浓度为_______ 。

(1)装置B的作用是
(2)装置C用于制取Na2S2O3,反应分两步,第二步反应的化学方程式为S+Na2SO3=Na2S2O3,则第一步反应的化学方程式为
(3)若将SO2与Cl2以1∶1的物质的量之比通入品红溶液中,发现品红溶液不褪色,原因是(用化学方程式解释)
(4)Na2SO3常因被空气中的氧气氧化而变质,验证本实验所用Na2SO3固体是否变质的方法是:取少量Na2SO3固体于试管中,加入适量的水配成溶液,
(5)用已知浓度的硫代硫酸钠溶液可以测定I2溶液的物质的量浓度。
步骤Ⅰ:准确称取7.9g硫代硫酸钠固体,加水溶解后,全部转移到100mL容量瓶中,加水定容至100mL。
步骤Ⅱ:量取含I2溶液20.0mL,向其中加入步骤Ⅰ所配硫代硫酸钠溶液,恰好完全反应时消耗硫代硫酸钠溶液20.0mL。
已知反应为
 (未配平),则含I2溶液中I2的物质的量浓度为
(未配平),则含I2溶液中I2的物质的量浓度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如下的实验装置。
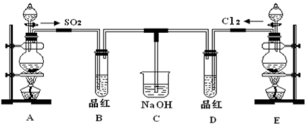
(1)实验室用装置E制备Cl2,其反应的离子方程式为__________________________ ;若有8mol的HCl参加反应,则转移的电子总数为________ 。
(2)该装置中氢氧化钠溶液的作用是___________________ 。
(3)通气后B、D两个试管中的现象______________ 。停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别为B:________ ,D:________ 。
(4)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强。他们将制得的SO2和Cl2按1:1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析该现象的原因(用离子方程式表示)____________________ 。

(1)实验室用装置E制备Cl2,其反应的离子方程式为
(2)该装置中氢氧化钠溶液的作用是
(3)通气后B、D两个试管中的现象
(4)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强。他们将制得的SO2和Cl2按1:1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析该现象的原因(用离子方程式表示)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某小组同学用下图所示装置验证卤素单质氧化性的相对强弱。请回答:
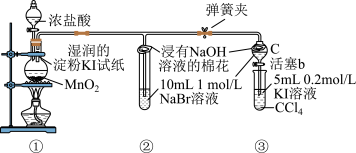
(1)①中产生的是黄绿色气体,其电子式是_______ ,在该反应中浓盐酸表现了_______ 性和_______ 性。
(2)反应一段时间后,①中湿润的淀粉碘化钾试纸可观察到的现象是_______ 。
(3)B中试管口处浸有 NaOH 溶液的棉花的作用是_______ 。
(4)由②、③中的现象说明卤素单质的氧化性由强到弱的顺序是_______ 。
(5)实验室中所用少量氯气也可用下列方法制取:K2Cr2O7+14HCl(浓) =2KCl+2CrCl3+ 3Cl2↑+7H2O,该氧化剂与还原剂的物质的量之比为_______ ;该反应中每有 73gHCl 被氧化,生成标况下 Cl2的体积为_______ L。

(1)①中产生的是黄绿色气体,其电子式是
(2)反应一段时间后,①中湿润的淀粉碘化钾试纸可观察到的现象是
(3)B中试管口处浸有 NaOH 溶液的棉花的作用是
(4)由②、③中的现象说明卤素单质的氧化性由强到弱的顺序是
(5)实验室中所用少量氯气也可用下列方法制取:K2Cr2O7+14HCl(浓) =2KCl+2CrCl3+ 3Cl2↑+7H2O,该氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某学习小组在通过反应Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O研究反应速率的影响因素后,对Na2S2O3产生了兴趣,查资料知Na2S2O3的名称为硫代硫酸钠,可视为一个S原子取代了Na2SO4中的一个O原子。该实验小组运用类比学习的思想预测了Na2S2O3的某些性质,并通过实验探究了自己的预测。
【提出假设】
(1)部分学生认为Na2S2O3与Na2SO4结构相似,化学性质也相似,因此推测室温时Na2S2O3溶液的pH____ 7(填“>”、“=”或“<”)。
(2)部分学生从S元素化合价推测Na2S2O3与Na2SO3性质相似,推测具有较强的______________ 。
【实验探究】取适量Na2S2O3晶体,溶于水中制成Na2S2O3溶液,进行如下探究(填写表中空格)。
【实验结论】
(5)从探究①、②的结论:_________________________________________________________ 。
【问题讨论】
(6)甲同学向“探究②”反应后的溶液中滴加AgNO3溶液,观察到有白色沉淀产生,并据此认为氯水可将Na2S2O3氧化。你认为该方案是否正确并说明理由______________________________ 。
(7)请你重新设计一个实验方案,证明Na2S2O3被氯水氧化,你的方案是______________________________ 。
【提出假设】
(1)部分学生认为Na2S2O3与Na2SO4结构相似,化学性质也相似,因此推测室温时Na2S2O3溶液的pH
(2)部分学生从S元素化合价推测Na2S2O3与Na2SO3性质相似,推测具有较强的
【实验探究】取适量Na2S2O3晶体,溶于水中制成Na2S2O3溶液,进行如下探究(填写表中空格)。
| 实验操作 | 实验现象 | 现象解释(用离子方程式表示) | |
| 探究① | 用玻璃棒蘸取Na2S2O3溶液点在pH试纸中部,将试纸颜色与标准比色卡对照 | 溶液pH=8 | (3) |
| 探究② | 向新制氯水(pH<2)中滴加少量Na2S2O3溶液 | 氯水颜色变浅 | (4) |
(5)从探究①、②的结论:
【问题讨论】
(6)甲同学向“探究②”反应后的溶液中滴加AgNO3溶液,观察到有白色沉淀产生,并据此认为氯水可将Na2S2O3氧化。你认为该方案是否正确并说明理由
(7)请你重新设计一个实验方案,证明Na2S2O3被氯水氧化,你的方案是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】资料显示:锌与浓硫酸共热除生成二氧化硫气体外,还可能产生氢气;在加热的条件下二氧化硫可被CuO氧化。为验证该反应的气体产物及性质,设计了如下图所示的实验装置(设锌与浓硫酸共热时产生的气体为X)。
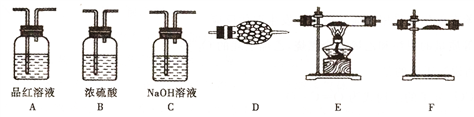
(1)上述装置的连接顺序为:气体X→A→____ →A→ → → →D;
(2)反应开始后,观察到第一个装置A中的品红溶液褪色,实验结束后取适量该溶液于试管中并加热,现象为______________ ;
(3)装置C的作用是____ ,C中的NaOH溶液不能用下列____ 代替;
a.酸性KMnO4溶液 b.CaCl2溶液 c.饱和NaHSO3溶液
装置D的作用是____________ ;
(4)气体X中可能含有H2的原因是____ 。

(1)上述装置的连接顺序为:气体X→A→
(2)反应开始后,观察到第一个装置A中的品红溶液褪色,实验结束后取适量该溶液于试管中并加热,现象为
(3)装置C的作用是
a.酸性KMnO4溶液 b.CaCl2溶液 c.饱和NaHSO3溶液
装置D的作用是
(4)气体X中可能含有H2的原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某小组同学探究物质的溶解度大小与沉淀转化方向之间的关系。已知:
(1)探究BaCO3和BaSO4之间的转化
实验操作: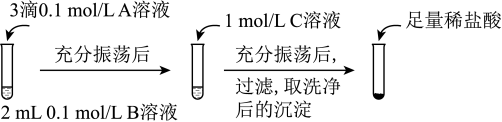
① 实验Ⅰ说明BaCO3全部转化为BaSO4,依据的现象是加入盐酸后,______ 。
② 实验Ⅱ中加入稀盐酸后发生反应的离子方程式是______ 。
③ 实验Ⅱ说明沉淀发生了部分转化,结合BaSO4的沉淀溶解平衡解释原因:______ 。
(2)探究AgCl和AgI之间的转化
实验Ⅲ: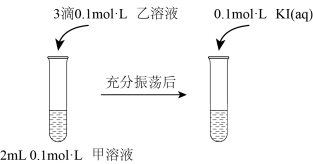
实验Ⅳ:在试管中进行溶液间反应时,同学们无法观察到AgI转化为AgCl,于是又设计了如下实验(电压表读数:a>c>b>0)。
注:其他条件不变时,参与原电池反应的氧化剂(或还原剂)的氧化性(或还原性)越强,原电池的电压越大;离子的氧化性(或还原性)强弱与其浓度有关。
① 实验Ⅲ证明了AgCl转化为AgI,甲溶液可以是______ (填序号)。
a. AgNO3溶液 b. NaCl溶液 c. KI溶液
② 实验Ⅳ的步骤ⅰ中,B中石墨上的电极反应式是______ 。
③ 结合信息,解释实验Ⅳ中b<a的原因:______ 。
④ 实验Ⅳ的现象能说明AgI转化为AgCl,理由是______ 。
(3)综合实验Ⅰ~Ⅳ,可得出结论:______ 。
| 物质 | BaSO4 | BaCO3 | AgI | AgCl | |
| 溶解度/g(20℃) | 2.4×10-4 | 1.4×10-3 | 3.0×10-7 | 1.5×10-4 |
实验操作:

| 试剂A | 试剂B | 试剂C | 加入盐酸后的现象 | |
| 实验Ⅰ | BaCl2 | Na2CO3 | Na2SO4 | …… |
| 实验Ⅱ | Na2SO4 | Na2CO3 | 有少量气泡产生,沉淀部分溶解 |
② 实验Ⅱ中加入稀盐酸后发生反应的离子方程式是
③ 实验Ⅱ说明沉淀发生了部分转化,结合BaSO4的沉淀溶解平衡解释原因:
(2)探究AgCl和AgI之间的转化
实验Ⅲ:
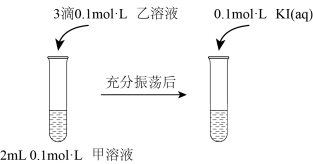
实验Ⅳ:在试管中进行溶液间反应时,同学们无法观察到AgI转化为AgCl,于是又设计了如下实验(电压表读数:a>c>b>0)。
| 装置 | 步骤 | 电压表读数 | |
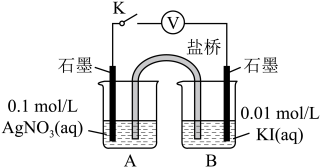 | ⅰ.如图连接装置并加入试剂,闭合K | a | |
| ⅱ.向B中滴入AgNO3(aq),至沉淀完全 | b | ||
| ⅲ.再向B中投入一定量NaCl (s) | c | ||
| ⅳ.重复ⅰ,再向B中加入与ⅲ等量NaCl(s) | a |
① 实验Ⅲ证明了AgCl转化为AgI,甲溶液可以是
a. AgNO3溶液 b. NaCl溶液 c. KI溶液
② 实验Ⅳ的步骤ⅰ中,B中石墨上的电极反应式是
③ 结合信息,解释实验Ⅳ中b<a的原因:
④ 实验Ⅳ的现象能说明AgI转化为AgCl,理由是
(3)综合实验Ⅰ~Ⅳ,可得出结论:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】用图1实验装置(铁架台、酒精灯略) 验证溴乙烷的性质:
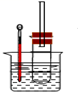
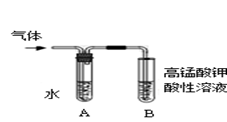
图1 图2
Ⅰ:在试管中加入10mL6mol/L NaOH溶液和2mL 溴乙烷,振荡.
II:将试管如图1固定后,水浴加热.
(1) 写出图1中反应的化学方程式_____________________________________ ;
(2)为证明溴乙烷在NaOH乙醇溶液中发生的是_________ 反应(填反应类型),将生成的气体通入如图2装置。A试管中的水的作用是_____________ ,若无A试管,B试管中的试剂应为_________ 。


图1 图2
Ⅰ:在试管中加入10mL6mol/L NaOH溶液和2mL 溴乙烷,振荡.
II:将试管如图1固定后,水浴加热.
(1) 写出图1中反应的化学方程式
(2)为证明溴乙烷在NaOH乙醇溶液中发生的是
您最近一年使用:0次



