回答下列问题:
(1)某学习小组研究1L某待测液,已知该待测液中除含有0.2mol•L-1的Na+外,还可能含有下列离子中的一种或几种:
现进行如图实验操作(每次实验所加试剂均过量):

①由气体B可确定待测液中含有的离子是_______ 。
②由沉淀D和沉淀E可以判断待测液中一定含有的离子是________ 。
③由白色沉淀B可确定待测液中含有的离子是________ ,请写出溶液A反应生成沉淀B的离子方程式_______ 。
④综合分析,待测液中K+的最小浓度为________ 。
(2)该小组将26.3gNiSO4•nH2O样品在900℃下煅烧,样品受热过程的热重曲线(样品质量随温度变化的曲线)如图所示。

已知:L→N时失掉全部的结晶水。请回答下列问题。
①n的值是______ 。
②固体Q的化学式为_______ 。
(1)某学习小组研究1L某待测液,已知该待测液中除含有0.2mol•L-1的Na+外,还可能含有下列离子中的一种或几种:
| 阳离子 | K+、NH 、Mg2+、Ba2+、Fe3+ 、Mg2+、Ba2+、Fe3+ |
| 阴离子 | Cl-、Br-、CO 、HCO 、HCO 、SO 、SO |

①由气体B可确定待测液中含有的离子是
②由沉淀D和沉淀E可以判断待测液中一定含有的离子是
③由白色沉淀B可确定待测液中含有的离子是
④综合分析,待测液中K+的最小浓度为
(2)该小组将26.3gNiSO4•nH2O样品在900℃下煅烧,样品受热过程的热重曲线(样品质量随温度变化的曲线)如图所示。

已知:L→N时失掉全部的结晶水。请回答下列问题。
①n的值是
②固体Q的化学式为
更新时间:2023-08-29 20:08:42
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】工业上,常用过二硫酸铵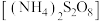 溶液检验废水中的
溶液检验废水中的 (无色)。离子方程式为
(无色)。离子方程式为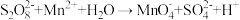 (未配平)。
(未配平)。
(1)已知 分子中S元素为最高价态,则分子中
分子中S元素为最高价态,则分子中 价O与
价O与 价O的个数比为
价O的个数比为___________ 。
(2)上述反应中,还原产物是___________ 。
(3)某实验需要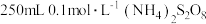 溶液,用
溶液,用 固体配制该溶液时,如果配制过程中,漏掉了“洗涤烧杯和玻璃棒”步骤,配制的浓度将
固体配制该溶液时,如果配制过程中,漏掉了“洗涤烧杯和玻璃棒”步骤,配制的浓度将___________ (填“偏高”、“偏低”或“无影响”)。
(4)测定废水中 的浓度:取
的浓度:取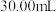 废水于锥形瓶中,滴加
废水于锥形瓶中,滴加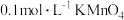 溶液产生黑色
溶液产生黑色 浑浊,至溶液变为浅红色且半分钟内不褪色时,消耗
浑浊,至溶液变为浅红色且半分钟内不褪色时,消耗 溶液
溶液 (假设废水中其他杂质不参与反应)。该废水中
(假设废水中其他杂质不参与反应)。该废水中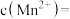
___________  。
。
(5)设计简易实验证明处理后的废水中含有 :
:___________ 。
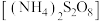 溶液检验废水中的
溶液检验废水中的 (无色)。离子方程式为
(无色)。离子方程式为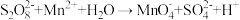 (未配平)。
(未配平)。(1)已知
 分子中S元素为最高价态,则分子中
分子中S元素为最高价态,则分子中 价O与
价O与 价O的个数比为
价O的个数比为(2)上述反应中,还原产物是
(3)某实验需要
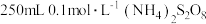 溶液,用
溶液,用 固体配制该溶液时,如果配制过程中,漏掉了“洗涤烧杯和玻璃棒”步骤,配制的浓度将
固体配制该溶液时,如果配制过程中,漏掉了“洗涤烧杯和玻璃棒”步骤,配制的浓度将(4)测定废水中
 的浓度:取
的浓度:取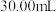 废水于锥形瓶中,滴加
废水于锥形瓶中,滴加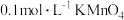 溶液产生黑色
溶液产生黑色 浑浊,至溶液变为浅红色且半分钟内不褪色时,消耗
浑浊,至溶液变为浅红色且半分钟内不褪色时,消耗 溶液
溶液 (假设废水中其他杂质不参与反应)。该废水中
(假设废水中其他杂质不参与反应)。该废水中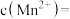
 。
。(5)设计简易实验证明处理后的废水中含有
 :
:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有一瓶NaCl、Na 2 SO 4 混合溶液,如何检验其中的Cl - ___________ ?
您最近一年使用:0次
【推荐3】现有三种可溶性物质A、B、C,其中A、B属于盐,C属于碱,它们溶于水后电离产生的所有离子如下表所示:
请根据下列叙述回答问题:
(1)C的化学式为___ 。
(2)A溶液与B溶液反应可生成气体,则该反应的离子方程式为___ 。
(3)A、B溶液与C溶液反应可分别生成白色沉淀D和E,其中D可溶于稀硝酸。
①B的化学式为___ ,鉴别溶液中B的阴离子的试剂为___ 。
②D溶于稀硝酸的离子方程式为___ 。
③D与E的混合物ag,加入足量盐酸,完全反应生成的气体在标准状况下体积为VL,则E在混合物中的质量分数的表达式为___ 。
| 阳离子 | Na+ H+ Ba2+ |
| 阴离子 | OH- CO32- SO42- |
请根据下列叙述回答问题:
(1)C的化学式为
(2)A溶液与B溶液反应可生成气体,则该反应的离子方程式为
(3)A、B溶液与C溶液反应可分别生成白色沉淀D和E,其中D可溶于稀硝酸。
①B的化学式为
②D溶于稀硝酸的离子方程式为
③D与E的混合物ag,加入足量盐酸,完全反应生成的气体在标准状况下体积为VL,则E在混合物中的质量分数的表达式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】硫酸铁铵[NH4Fe(SO4)2·xH2O]是一种重要铁盐。为充分利用资源,变废为宝,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流程如下:
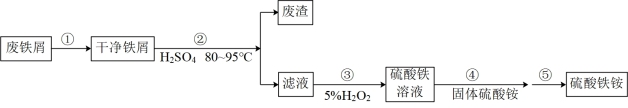
采用热重分析法测定硫酸铁铵晶体样品所含结晶水数,将样品加热到150 ℃时,失掉1.5个结晶水,失重5.6%。硫酸铁铵晶体的化学式为_______ 。

采用热重分析法测定硫酸铁铵晶体样品所含结晶水数,将样品加热到150 ℃时,失掉1.5个结晶水,失重5.6%。硫酸铁铵晶体的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】水是生命之源,它与我们的生活密切相关。
(1)自来水厂常用高铁酸钾(K2FeO4)改善水质。简述高铁酸钾用于杀菌消毒同时又起到净水作用的原理_____________________________________________________________ 。
(2)电镀废水中含有剧毒的NaCN,加入NaClO处理该碱性废水时生成Na2CO3、NaCl和N2。
①写出该反应的离子方程式:__________________________________________ 。
②处理a m3含NaCN bmg·L-1的废水,至少需要NaClO的质量为______________ g。
(3)某工业废水中可能含有Na+、Mg2+、A13+、Fe3+、NH4+、CO32-、SO42-、NO3-中的几种,为确定其成分,设计如下实验:
a.取该废水进行焰色反应实验,火焰为黄色;
b.另取10mL该废水于试管中,加入足量的Ba(NO3)2溶液和稀硝酸,充分反应后过滤得到4.66g白色沉淀;
c.另取10mL该废水于试管中,滴加NaOH溶液,产生沉淀的质量随所加NaOH溶液体积的变化关系如下图所示(不考虑沉淀的溶解和损失)。
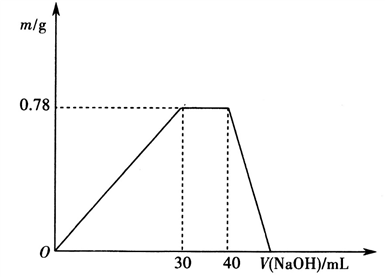
根据上述实验和图表数据回答:
①该工业废水中一定不存在的离子有_________________ (写离子符号)。
②c(NaOH)=_____________________ 。
③NO3-是否存在?_______ (填“存在”、“不存在”或“不确定”),理由是_____________________________________________________
(1)自来水厂常用高铁酸钾(K2FeO4)改善水质。简述高铁酸钾用于杀菌消毒同时又起到净水作用的原理
(2)电镀废水中含有剧毒的NaCN,加入NaClO处理该碱性废水时生成Na2CO3、NaCl和N2。
①写出该反应的离子方程式:
②处理a m3含NaCN bmg·L-1的废水,至少需要NaClO的质量为
(3)某工业废水中可能含有Na+、Mg2+、A13+、Fe3+、NH4+、CO32-、SO42-、NO3-中的几种,为确定其成分,设计如下实验:
a.取该废水进行焰色反应实验,火焰为黄色;
b.另取10mL该废水于试管中,加入足量的Ba(NO3)2溶液和稀硝酸,充分反应后过滤得到4.66g白色沉淀;
c.另取10mL该废水于试管中,滴加NaOH溶液,产生沉淀的质量随所加NaOH溶液体积的变化关系如下图所示(不考虑沉淀的溶解和损失)。

根据上述实验和图表数据回答:
①该工业废水中一定不存在的离子有
②c(NaOH)=
③NO3-是否存在?
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】将铁粉和铝粉的混合物逐渐加入100mL的稀硝酸中,其产生的有关离子浓度与加入铁粉和铝粉的混合物的质量的关系如下图所示:
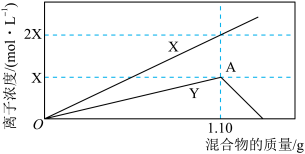
若反应过程中生成的气体为NO,溶液的体积变化忽略不计。请回答下列问题:
(1)X表示的变化离子是_______________ (填离子符号)。
(2)OA段发生反应的离子方程式是___________________________________ 。
(3)稀硝酸溶解1.10g铁粉和铝粉后溶液还能继续溶解混合物的原因是________________
(4)该硝酸的浓度是_____________ mol·L-1。

若反应过程中生成的气体为NO,溶液的体积变化忽略不计。请回答下列问题:
(1)X表示的变化离子是
(2)OA段发生反应的离子方程式是
(3)稀硝酸溶解1.10g铁粉和铝粉后溶液还能继续溶解混合物的原因是
(4)该硝酸的浓度是
您最近一年使用:0次



