小沁老师在检查同学们的笔记时,由于错误过多而火冒三丈,把红笔扔下,请你帮助她找出剩下的笔记中需要更改的内容_______ 。

A.在上图的晶胞中,原子分数坐标参数A为 ,C为
,C为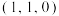 ,B为
,B为 ,则E原子的坐标为
,则E原子的坐标为
B.邻羟基苯乙醛的结构简式(虚线表示氢键):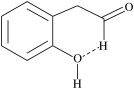
C.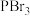 的VSEPR模型:正四面体型
的VSEPR模型:正四面体型
D.标况下 氯乙烷分子数:
氯乙烷分子数:
E.硼烷氨络合物( )的结构式:
)的结构式: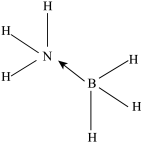

A.在上图的晶胞中,原子分数坐标参数A为
 ,C为
,C为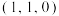 ,B为
,B为 ,则E原子的坐标为
,则E原子的坐标为
B.邻羟基苯乙醛的结构简式(虚线表示氢键):

C.
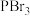 的VSEPR模型:正四面体型
的VSEPR模型:正四面体型D.标况下
 氯乙烷分子数:
氯乙烷分子数:
E.硼烷氨络合物(
 )的结构式:
)的结构式:
22-23高二下·浙江·期中 查看更多[1]
(已下线)【2023】【高二下】【期中复习卷】【学军】【高中化学】【冯杲升收集】
更新时间:2023-09-23 16:45:40
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】物质的结构决定物质的性质,请回答下列涉及物质结构和性质的问题:
(1)第二周期中,元素的第一电离能处于B与N之间的元素有________ 种。
(2)某元素位于第四周期Ⅷ族,其基态原子的未成对电子数与基态碳原子的末成对电子数相同,则其基态原子的价层电子排布式为_________________ 。
(3)乙烯酮(CH2=C=O)是一种重要的有机中间体,可用CH3COOH在(C2H5O)3P=O存在下加热脱H2O得到。乙烯酮分子中碳原子杂化轨道类型是__________________ 。
1mol(C2H5O)3P=O分子中含有的σ键的数目为_________________ 。
(4)已知固态NH3、H2O、HF的氢键键能和结构如下:
由此可知NH3、H2O、HF沸点由高到低的顺序为___________________ 。
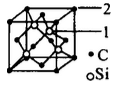
(5)碳化硅的结构与金刚石类似,如下图所示,其硬度仅次于金刚石,具有较强的耐磨性能。碳化硅晶胞结构中每个碳原子周围与其距离最近的硅原子有______ 个,与碳原子等距离最近的碳原子有_____ 个。已知碳化硅晶胞边长为apm,则碳化硅的密度为__________ g/cm3(已知C和Si的相对原子质量分别为12和28,阿伏伽德罗常数用NA表示)。
(1)第二周期中,元素的第一电离能处于B与N之间的元素有
(2)某元素位于第四周期Ⅷ族,其基态原子的未成对电子数与基态碳原子的末成对电子数相同,则其基态原子的价层电子排布式为
(3)乙烯酮(CH2=C=O)是一种重要的有机中间体,可用CH3COOH在(C2H5O)3P=O存在下加热脱H2O得到。乙烯酮分子中碳原子杂化轨道类型是
1mol(C2H5O)3P=O分子中含有的σ键的数目为
(4)已知固态NH3、H2O、HF的氢键键能和结构如下:
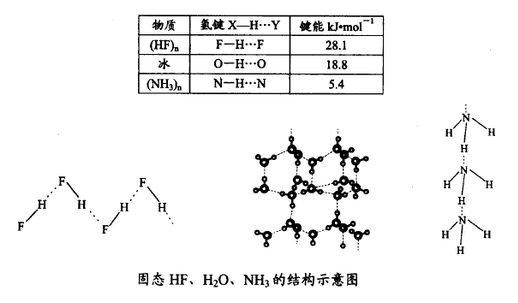
由此可知NH3、H2O、HF沸点由高到低的顺序为
(5)碳化硅的结构与金刚石类似,如下图所示,其硬度仅次于金刚石,具有较强的耐磨性能。碳化硅晶胞结构中每个碳原子周围与其距离最近的硅原子有
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐2】氮是地球上极为丰富的元素
(1)Li3N晶体中氮以N3-的形式存在,基态N3-的电子排布式为_______ ;
(2)X离子中所有电子正好充满K、L、M三个电子层,它与N3-形成的晶体结构如图所示。X的元素符号是_______ ,X离子与N3-形成的化合物化学式为_______ 。

(3)水是生命之源,它与我们的生活密切相关。在化学实验和科学研究中,水也是一种常用的试剂。下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排序)。与冰的晶体类型相同的是_______ (请用相应的编号填写)

(4)在冰晶体中,每个水分子与相邻的4个水分子形成氢键,已知冰的升华热是51 kJ/mol,除氢键外,水分子间还存在范德华力(11 kJ/mol),则冰晶体中氢键的“键能”是_______ kJ/mol;
(1)Li3N晶体中氮以N3-的形式存在,基态N3-的电子排布式为
(2)X离子中所有电子正好充满K、L、M三个电子层,它与N3-形成的晶体结构如图所示。X的元素符号是

(3)水是生命之源,它与我们的生活密切相关。在化学实验和科学研究中,水也是一种常用的试剂。下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排序)。与冰的晶体类型相同的是

(4)在冰晶体中,每个水分子与相邻的4个水分子形成氢键,已知冰的升华热是51 kJ/mol,除氢键外,水分子间还存在范德华力(11 kJ/mol),则冰晶体中氢键的“键能”是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】I.有四种化合物W、X、Y、Z,它们是由短周期元素A、B、C、D、E中的两种元素组成。已知
(1)A、B、C、D、E的原子序数依次增大,且A、D同主族,C、E同主族;B、C 同周期;
(2)W由A、B组成,其分子中原子个数比为A:B=4:1,常温为气态。
(3)X由A、C组成,其分子中原子数比为A:C=1:1
(4)Y是C、D形成的离子化合物,且Y晶体中相应元素的原子个数比为1:1
(5)Z是由D、E形成的离子化合物,其中阳离子比阴离子少一个电子层,阳离子数与阴离子数之比为2:1 则B为__________ ,W为_________ ,X的结构式________ Y的电子式为______________ 。
II.(1).一元素原子的N层上只有1个电子,该元素原子各内层均已充满,写出该原子电子排布式:________________ ,
(2)一元素属于短周期元素,该元素的原子核外所有P轨道全满或者半满,写出该元素原子的价电子轨道排布图__________________ ,
(3)乙烯分子中有__________ 个σ键,___________ π键。
(1)A、B、C、D、E的原子序数依次增大,且A、D同主族,C、E同主族;B、C 同周期;
(2)W由A、B组成,其分子中原子个数比为A:B=4:1,常温为气态。
(3)X由A、C组成,其分子中原子数比为A:C=1:1
(4)Y是C、D形成的离子化合物,且Y晶体中相应元素的原子个数比为1:1
(5)Z是由D、E形成的离子化合物,其中阳离子比阴离子少一个电子层,阳离子数与阴离子数之比为2:1 则B为
II.(1).一元素原子的N层上只有1个电子,该元素原子各内层均已充满,写出该原子电子排布式:
(2)一元素属于短周期元素,该元素的原子核外所有P轨道全满或者半满,写出该元素原子的价电子轨道排布图
(3)乙烯分子中有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】短周期元素A、B、C、D原子序数依次增大,且C元素最高价氧化物对应的水化物在水溶液中能电离出电子数相等的阴、阳离子。A、C位于同一主族,A为非金属元素,B的最外层电子数是次外层电子数的3倍,B、C的最外层电子数之和与D的最外层电子数相等。E单质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏。请回答下列问题:
(1)基态D原子的价电子轨道表示式___________________________ 。
(2)由上述A、B、D三种元素形成的ADB分子中存在的 键分别称为
键分别称为_________ 。
(3)B、D两种元素可形成多种阴离子,如 、
、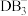 、
、 等,这三种阴离子的空间结构分别为
等,这三种阴离子的空间结构分别为______________________ 。比较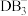 和
和 的键角大小并说明理由:
的键角大小并说明理由:_______________________ 。
(4)E元素原子基态时电子所占据的轨道个数为:_________ ;试分析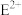 具有较强还原性的原因
具有较强还原性的原因___________________________ 。
(1)基态D原子的价电子轨道表示式
(2)由上述A、B、D三种元素形成的ADB分子中存在的
 键分别称为
键分别称为(3)B、D两种元素可形成多种阴离子,如
 、
、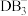 、
、 等,这三种阴离子的空间结构分别为
等,这三种阴离子的空间结构分别为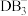 和
和 的键角大小并说明理由:
的键角大小并说明理由:(4)E元素原子基态时电子所占据的轨道个数为:
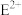 具有较强还原性的原因
具有较强还原性的原因
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】H+可与H2O形成H3O+,H3O+中O原子采用sp3杂化。H3O+中H-O-H键角比H2O中H-O-H键角大,原因___________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)Zn的氯化物与氨水反应可形成配合物 ,1mol该配合物中含有σ键的数目为
,1mol该配合物中含有σ键的数目为______ 。
(2)若 与
与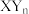 通过B原子与X原子间的配位键结合形成配合物,则该配合物提供孤电子对的原子是
通过B原子与X原子间的配位键结合形成配合物,则该配合物提供孤电子对的原子是______ 。
(3)金属镍在电池、合金、催化剂等方面应用广泛。过渡金属配合物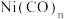 的中心原子价层电子数与配体提供电子总数之和为18,则n=
的中心原子价层电子数与配体提供电子总数之和为18,则n=______ 。
 ,1mol该配合物中含有σ键的数目为
,1mol该配合物中含有σ键的数目为(2)若
 与
与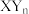 通过B原子与X原子间的配位键结合形成配合物,则该配合物提供孤电子对的原子是
通过B原子与X原子间的配位键结合形成配合物,则该配合物提供孤电子对的原子是(3)金属镍在电池、合金、催化剂等方面应用广泛。过渡金属配合物
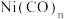 的中心原子价层电子数与配体提供电子总数之和为18,则n=
的中心原子价层电子数与配体提供电子总数之和为18,则n=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】无水硫酸铜为_______ 色固体,把它溶于水后得到_______ 色溶液,原因是溶液形成了[Cu(H2O)4]2+配离子,中心离子是_______ ,配位数为_______ ,配体是_______ 分子。向该溶液中滴入氨水,现象是_______ ,继续滴加氨水至过量,现象是_______ ,请写出所得物质内界结构式_______ ,中心离子与配体之间以_______ 键相结合。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】Ⅰ.铜单质及其化合物在很多领域有重要的用途,如金属铜用来制造电线电缆,五水硫酸铜可用作杀菌剂。
(1)向CuSO4溶液中加入过量NaOH溶液可生成[Cu(OH)4]2−。不考虑空间构型,[Cu(OH)4]2−的结构可用示意图表示为________ 。
(2)胆矾CuSO4·5H2O可写[Cu(H2O)4]SO4·H2O,其结构示意图如下:

下列有关胆矾的说法正确的是________ 。
A.所有氧原子都采取sp3杂化
B.氧原子存在配位键和氢键两种化学键
C.Cu2+的价电子排布式为3d84s1
D.胆矾中的水在不同温度下会分步失去
Ⅱ.经研究表明,Fe(SCN)3是配合物,Fe3+与SCN−不仅能以1∶3的个数比配合,还可以其他个数比配合。请按要求填空:
(1)若所得Fe3+和SCN−的配合物中,主要是Fe3+与SCN−以个数比1∶1配合所得离子显红色。该离子的离子符号是________ 。
(2)若Fe3+与SCN−以个数比1∶5配合,则FeCl3与KSCN在水溶液中发生反应的化学方程式可以表示为________________________________________________ 。
(1)向CuSO4溶液中加入过量NaOH溶液可生成[Cu(OH)4]2−。不考虑空间构型,[Cu(OH)4]2−的结构可用示意图表示为
(2)胆矾CuSO4·5H2O可写[Cu(H2O)4]SO4·H2O,其结构示意图如下:

下列有关胆矾的说法正确的是
A.所有氧原子都采取sp3杂化
B.氧原子存在配位键和氢键两种化学键
C.Cu2+的价电子排布式为3d84s1
D.胆矾中的水在不同温度下会分步失去
Ⅱ.经研究表明,Fe(SCN)3是配合物,Fe3+与SCN−不仅能以1∶3的个数比配合,还可以其他个数比配合。请按要求填空:
(1)若所得Fe3+和SCN−的配合物中,主要是Fe3+与SCN−以个数比1∶1配合所得离子显红色。该离子的离子符号是
(2)若Fe3+与SCN−以个数比1∶5配合,则FeCl3与KSCN在水溶液中发生反应的化学方程式可以表示为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】MgH2晶体属四方晶系,其晶胞结构如图所示,晶胞参数a=b=450pm,c=301pm,原子坐标为A(0,0,0)、B(0.305,0.305,0)、C(1,1,0.67)、D(0.195,0.805,0.5)

(1)Mg2+的半径为72pm,则H-的半径为___________ pm(列出计算式即可)。
(2)用NA表示阿伏加德罗常数的值,MgH2晶体中H-的密度是标准状况下氢气密度的___________ 倍(列出计算式即可,标准状况下氢气的密度为0.089g·L-1)。

(1)Mg2+的半径为72pm,则H-的半径为
(2)用NA表示阿伏加德罗常数的值,MgH2晶体中H-的密度是标准状况下氢气密度的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】向硫酸铜水溶液中逐滴滴加氨水,先生成蓝色沉淀,继续滴加氨水得到深蓝色溶液,再向溶液中加入乙醇,有深蓝色晶体[Cu(NH3)4]SO4·H2O析出。
(1)铜元素位于元素周期表中____ 区,高温超导体钇钡铜氧材料中铜元素有+2和+3两种价态,基态Cu3+的电子排布式为____ 。
(2)非金属元素N、O、S的第一电离能由大到小的顺序是____ (用元素符号表示)。
(3)上述深蓝色晶体中含有的元素的电负性最小的是____ (用元素符号表示)。
(4)H2O的中心原子轨道杂化类型为____ 杂化;SO42-离子的立体构型是____ ,写出与SO42-互为等电子体的一种离子____ 。
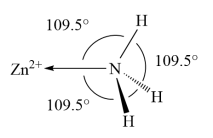
(5)NH3分子在独立存在时H-N-H键角为106.7°。如图为[Zn(NH3)6]2+离子的部分结构以及H-N-H键角的测量值。解释配合物中H-N-H键角变为109.5°的原因____ 。
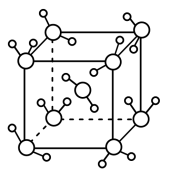
(6)最新研究发现,水能凝结成13种类型的结晶体。除普通冰外,还有-30℃才凝固的低温冰,180℃依然不变的热冰,比水密度大的重冰等。重冰的结构如图所示。已知晶胞参数a=333.7 pm,阿伏加 德罗常数的值取6.02×1023,则重冰的密度为____ g.cm-3(只列式,不计算)。
(1)铜元素位于元素周期表中
(2)非金属元素N、O、S的第一电离能由大到小的顺序是
(3)上述深蓝色晶体中含有的元素的电负性最小的是
(4)H2O的中心原子轨道杂化类型为
(5)NH3分子在独立存在时H-N-H键角为106.7°。如图为[Zn(NH3)6]2+离子的部分结构以及H-N-H键角的测量值。解释配合物中H-N-H键角变为109.5°的原因

(6)最新研究发现,水能凝结成13种类型的结晶体。除普通冰外,还有-30℃才凝固的低温冰,180℃依然不变的热冰,比水密度大的重冰等。重冰的结构如图所示。已知晶胞参数a=333.7 pm,阿伏加 德罗常数的值取6.02×1023,则重冰的密度为

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】硫和钒的相关化合物,在药物化学及催化化学等领域应用广泛。回答下列问题:
(1)基态钒原子的外围电子轨道表达式为___________ ,钒有+2、+3、+4、+5等多种化合价,其中最稳定的化合价是________ ,VO43-的几何构型为________ .
(2)2-巯基烟酸氧钒配合物(图1) 是副作用小的有效调节血糖的新型药物。

①基态S原子中原子核外未成对电子数为_______ ,该药物中S原子的杂化方式是_______ .所含第二周期元素第一电离能按由大到小顺序的排列是___________ .
②2-巯基烟酸(图2) 水溶性优于2-巯基烟酸氧钒配合物的原因是_________ .
(3)多原子分子中各原子若在同一平面,且有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域Π键”,下列物质中存在“离域Π键”的是_____ .
A.SO2 B.SO42- C.H2S D.CS2
(4)某六方硫钒化合物晶体的晶胞如图3所示,该晶胞的化学式为______ 。图4 为该晶胞的俯视图,该晶胞的密度为________ g/cm3 (列出计算式即可)。

(1)基态钒原子的外围电子轨道表达式为
(2)2-巯基烟酸氧钒配合物(图1) 是副作用小的有效调节血糖的新型药物。

①基态S原子中原子核外未成对电子数为
②2-巯基烟酸(图2) 水溶性优于2-巯基烟酸氧钒配合物的原因是
(3)多原子分子中各原子若在同一平面,且有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域Π键”,下列物质中存在“离域Π键”的是
A.SO2 B.SO42- C.H2S D.CS2
(4)某六方硫钒化合物晶体的晶胞如图3所示,该晶胞的化学式为

您最近一年使用:0次



