下列关系错误的是
| A.沸点:CO>N2 | B.第一电离能:Si<P<S |
| C.在水中的溶解度:SO2>CO2 | D.还原性:稀盐酸<浓盐酸 |
更新时间:2023-09-01 07:07:34
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】反应①②分别是从海藻灰和某种矿石中提取碘的主要反应:
①2NaI+MnO2+3H2SO4=2NaHSO4+MnSO4+2H2O+I2;
②2NaIO3+5NaHSO3=2Na2SO4+3NaHSO4+H2O+I2。
下列说法正确的是
①2NaI+MnO2+3H2SO4=2NaHSO4+MnSO4+2H2O+I2;
②2NaIO3+5NaHSO3=2Na2SO4+3NaHSO4+H2O+I2。
下列说法正确的是
| A.两个反应中硫元素均被氧化 |
| B.碘元素在反应①中被氧化,在反应②中被还原 |
C.氧化性:MnO2> > > >I2 >I2 |
| D.反应①②中生成等量的I2时,转移电子数之比为2∶5 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】 和足量的
和足量的 溶液充分反应,再加入足量
溶液充分反应,再加入足量 固体,发生化学反应(忽略溶解过程溶液体积的变化):
固体,发生化学反应(忽略溶解过程溶液体积的变化):
①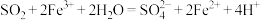
②
下列说法不正确的是
 和足量的
和足量的 溶液充分反应,再加入足量
溶液充分反应,再加入足量 固体,发生化学反应(忽略溶解过程溶液体积的变化):
固体,发生化学反应(忽略溶解过程溶液体积的变化):①
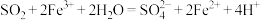
②

下列说法不正确的是
A.氧化性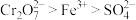 |
B.反应前后, 的浓度不变 的浓度不变 |
C.整体来看, 可以当做总反应的催化剂 可以当做总反应的催化剂 |
D.由上述反应原理推断: 能将 能将 氧化成 氧化成 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】四种短周期主族元素W、X、Y、Z原子序数依次增大,W含量在地壳中最高,X和Z构成的盐是海水中最主要的盐类,且该盐对水的电离没有影响,Y元素的最外层电子数比内层电子总数少4,下列说法正确的是
| A.W元素的第一电离能大于X元素 |
| B.因为酸性H2YO4>HZO,所以Y的非金属性强于Z |
| C.原子半径:X>Z> Y> W |
| D.四种元素中,Z元素的电负性数值最大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】前四周期主族元素 、
、 、
、 、
、 、
、 的原子序数依次增大,
的原子序数依次增大, 、
、 可组成最简单有机物
可组成最简单有机物 ,
, 、
、 可形成一种淡黄色粉末状的氧化物
可形成一种淡黄色粉末状的氧化物 ,
, 和
和 位于同一主族,下列说法正确的是
位于同一主族,下列说法正确的是
 、
、 、
、 、
、 、
、 的原子序数依次增大,
的原子序数依次增大, 、
、 可组成最简单有机物
可组成最简单有机物 ,
, 、
、 可形成一种淡黄色粉末状的氧化物
可形成一种淡黄色粉末状的氧化物 ,
, 和
和 位于同一主族,下列说法正确的是
位于同一主族,下列说法正确的是A.第一电离能: |
B.离子半径: |
C.物质 能与 能与 、 、 组成的一种物质反应,且可作为呼吸面具供氧剂 组成的一种物质反应,且可作为呼吸面具供氧剂 |
D.基态 原子 原子 能级的电子总数比 能级的电子总数比 能级的电子总数少7 能级的电子总数少7 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列关于O、S及其化合物的说法中,错误的是
| A.O的电负性比S的大,可推断H2O分子的极性比H2S的极性大 |
| B.电子云重叠程度O-H比S-H的大,可推断O-H比S-H更稳定 |
| C.H2O的相对分子质量比H2S的小,可推断H2O的沸点比H2S的低 |
| D.H2O的成键电子排斥力大,可推测的H2O键角比H2S的大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列生活中的现象与物质结构关联不正确的是
| A.蔗糖易溶于水与蔗糖和水分子的极性有关 |
| B.干冰易升华与其分子间作用力弱有关 |
| C.电子从激发态跃迁到基态的过程中释放能量产生紫色光—钾盐可用作紫色烟花的原料 |
| D.圆形容器中结出的冰是圆形的,体现了晶体的自范性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列有关科学家及其贡献说法不正确的是
| A.俄国化学家门捷列夫按照相对原子质量的大小编制了第一张元素周期表 |
| B.英国科学家道尔顿提出原子学说,为近代化学的发展奠定了坚实的基础 |
| C.我国化学家侯德榜通过“联合制碱法”制得的“碱”是小苏打 |
| D.荷兰物理学家范德华最早研究分子间作用力,分子间作用力对物质沸点有影响 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
| A.BCl3 和 PCl3 中,每个原子的最外层都具有 8 电子稳定结构 |
| B.所有共价化合物熔化时需克服微粒间的作用力类型都相同 |
| C.NaHSO4 晶体熔融时,离子键被破坏,共价键不受影响 |
| D.NH3 和 CO2 两种分子中,每个原子的最外层都具有 8 电子稳定结构 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】四氯化锗( )是光导纤维的常用掺杂剂,锗与硅同族。下列说法不正确的是
)是光导纤维的常用掺杂剂,锗与硅同族。下列说法不正确的是
 )是光导纤维的常用掺杂剂,锗与硅同族。下列说法不正确的是
)是光导纤维的常用掺杂剂,锗与硅同族。下列说法不正确的是A.基态 原子价层电子排布式为 原子价层电子排布式为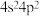 | B. 的熔点比 的熔点比 低 低 |
C. 的空间构型为正四面体 的空间构型为正四面体 | D.第一电离能大小: |
您最近一年使用:0次


 为非极性分子
为非极性分子 常因保存不慎而被氧化,产生剧毒物光气
常因保存不慎而被氧化,产生剧毒物光气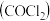 :
: ,下列说法不正确的有
,下列说法不正确的有

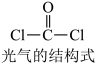
 分子为含极性键的非极性分子
分子为含极性键的非极性分子 分子中含有3个
分子中含有3个 键、一个
键、一个 键,中心C原子采用
键,中心C原子采用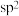 杂化
杂化

