单质钨的化学性质比较稳定,主要用来制造灯丝和高速切削合金钢、超硬模具。工业上利用黑钨矿(主要成分为FeWO4和MnWO4,还含少量Si、As的化合物)生产钨的工艺流程如图所示。已知:常温下钨酸难溶于水。WO3难溶于水,能与水蒸气反应生成一种挥发性极强的水钨化合物WO2(OH)2.回答下列问题:
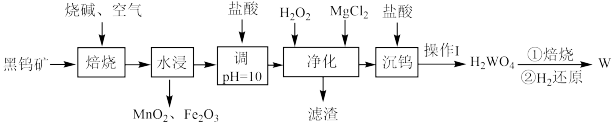
(1)焙烧过程中生成MnO2的化学方程式为___________ ,为加快此过程的反应速率,可采取的措施有___________ (答出两条)。
(2)沉钨时pH过低,可形成多钨酸根离子,其中最重要的是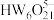 和
和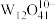 ,写出生成
,写出生成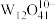 的离子方程式:
的离子方程式:___________ 。
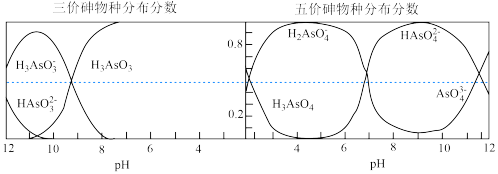
(3)滤渣的成分为___________ (填化学式),常温时H3AsO3、H3AsO4水溶液中含砷的各物种的分布分数如图所示,写出净化时加入H2O2发生的主要反应的离子方程式:___________ 。
(4)还原制备W单质时要适当加快氢气的流速,目的是___________ 。
(5)操作Ⅰ的名称为___________ ,若黑钨矿中钨的质量分数为ω,提炼过程中利用率为m,欲用nkg黑钨矿制得纯度≥99%的金属钨,则产品中杂质含量最大为___________ kg。

(1)焙烧过程中生成MnO2的化学方程式为
(2)沉钨时pH过低,可形成多钨酸根离子,其中最重要的是
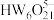 和
和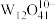 ,写出生成
,写出生成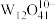 的离子方程式:
的离子方程式:(3)滤渣的成分为

(4)还原制备W单质时要适当加快氢气的流速,目的是
(5)操作Ⅰ的名称为
更新时间:2023-10-02 20:21:23
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】我国是稀土储量大国,氧化铈(CeO2)是一种应用广泛的稀土氧化物。一种用氟碳铈矿(CeFCO3,含BaO、SiO2等杂质)为原料制备CeO2的工艺如下图。

已知:①Ce3+可形成难溶于水的复盐[(Ce2(SO4)3·Na2SO4·nH2O],其氢氧化物也难溶于水。
②硫脲的结构简式为CS(NH2)2,在酸条件下易被氧化为(CSN2H3)2。
请回答:
(1)实验室常用下图所示仪器进行固体物质的粉碎,该仪器的名称是___________ 。
(2)焙烧后加入稀硫酸浸出,Ce元素的浸出率和稀硫酸浓度、温度的关系如图所示,下列说法正确的是_______

(3)步骤④发生的离子方程式为___________ 。
(4)取ag所制CeO2,溶解后配制成250mL溶液。取bmL该溶液用0.01mol·L-1(NH4)2Fe(SO4)2溶液滴定,滴定时发生反应:Fe2++Ce4+=Fe3++Ce3+,达到滴定终点时消耗(NH4)2Fe(SO4)2溶液VmL。
实验室配制250ml0.01mol/L的(NH4)2Fe(SO4)2溶液的过程如下(未排序):
①将已恢复至室温的溶液沿玻璃棒注入250mL容量瓶中;
②盖好容量瓶瓶塞,反复上下颠倒,摇匀;
③用天平称取ng(NH4)2Fe(SO4)2固体并放入烧杯中,加入约30mL蒸馏水充分搅拌、溶解;
④用30mL蒸馏水洗涤烧杯内壁和玻璃棒2~3次,并将每次洗涤液转入容量瓶中,轻轻振荡;
⑤定容:用胶头滴管滴加至凹液面和刻度线相切;
⑥将配置好的溶液倒入试剂瓶中,贴好标签;
实验操作顺序依次为___________ (填序号)。滴定过程中,接近终点时需采用半滴操作,具体操作是___________ 。
(5)该产品的质量分数为___________ (列出表达式)

已知:①Ce3+可形成难溶于水的复盐[(Ce2(SO4)3·Na2SO4·nH2O],其氢氧化物也难溶于水。
②硫脲的结构简式为CS(NH2)2,在酸条件下易被氧化为(CSN2H3)2。
请回答:
(1)实验室常用下图所示仪器进行固体物质的粉碎,该仪器的名称是

(2)焙烧后加入稀硫酸浸出,Ce元素的浸出率和稀硫酸浓度、温度的关系如图所示,下列说法正确的是_______

| A.固体A的成分是SiO2 |
| B.步骤①和步骤②均包含过滤、洗涤操作,洗涤的目的相同 |
C.步骤②加入硫脲的目的将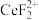 还原为 还原为 |
| D.根据上图,焙烧后加入稀硫酸浸出时,适宜的条件为85℃,c(H2SO4)=2.5mol/L |
(3)步骤④发生的离子方程式为
(4)取ag所制CeO2,溶解后配制成250mL溶液。取bmL该溶液用0.01mol·L-1(NH4)2Fe(SO4)2溶液滴定,滴定时发生反应:Fe2++Ce4+=Fe3++Ce3+,达到滴定终点时消耗(NH4)2Fe(SO4)2溶液VmL。
实验室配制250ml0.01mol/L的(NH4)2Fe(SO4)2溶液的过程如下(未排序):
①将已恢复至室温的溶液沿玻璃棒注入250mL容量瓶中;
②盖好容量瓶瓶塞,反复上下颠倒,摇匀;
③用天平称取ng(NH4)2Fe(SO4)2固体并放入烧杯中,加入约30mL蒸馏水充分搅拌、溶解;
④用30mL蒸馏水洗涤烧杯内壁和玻璃棒2~3次,并将每次洗涤液转入容量瓶中,轻轻振荡;
⑤定容:用胶头滴管滴加至凹液面和刻度线相切;
⑥将配置好的溶液倒入试剂瓶中,贴好标签;
实验操作顺序依次为
(5)该产品的质量分数为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】下表是元素周期表的一部分,列出了九种元素在周期表中的位置:
请用化学用语回答下列问题:
(1)在上述元素中,金属性最强的是_______ ,在③~⑦元素中,原子半径最大的是_______ 。
(2)①~⑨中元素最高价氧化物对应水化物中酸性最强的是_______ (填物质化学式)。写出①和④的最高价氧化物对应水化物反应的离子方程式_______ 。
(3)用电子式表示③和⑨形成的化合物的过程_______ 。
(4)表中元素①和⑦可以形成一种淡黄色物质X,X中阴阳离子的个数比_______ ,0.1molX与水反应转移电子数为_______ 。
(5)表中元素⑥和⑧可形成一种相对分子量为66的化合物Y,Y分子中各原子均达到“8电子稳定结构”,Y的化学式_______ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 3 | ① | ③ | ④ | ⑨ | ||||
| 4 | ② |
(1)在上述元素中,金属性最强的是
(2)①~⑨中元素最高价氧化物对应水化物中酸性最强的是
(3)用电子式表示③和⑨形成的化合物的过程
(4)表中元素①和⑦可以形成一种淡黄色物质X,X中阴阳离子的个数比
(5)表中元素⑥和⑧可形成一种相对分子量为66的化合物Y,Y分子中各原子均达到“8电子稳定结构”,Y的化学式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
真题
解题方法
【推荐3】亚硫酸盐是一种常见食品添加剂。为检验某食品中亚硫酸盐含量(通常1kg样品中含SO2的质量计),某研究小组设计了如下两种实验流程:
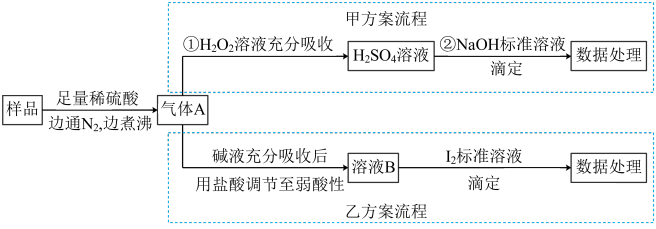
(1)气体A的主要成分是______ ,为防止煮沸时发生暴沸,必须先向烧瓶中加入______ ;通入N2的目的是______ 。
(2)写出甲方案第①步反应的离子方程式:______ 。
(3)甲方案第②步滴定前,滴定管需用NaOH标准溶液润洗,其操作方法是______ 。
(4)若用盐酸代替稀硫酸处理样品,则按乙方案实验测定的结果______ (填“偏高”、“偏低”或“无影响”)
(5)若取样品wg,按乙方案测得消耗0.01000mol·L-1I2溶液VmL,则1kg样品中含SO2的质量是______ g(用含w、V的代数式表示)。

(1)气体A的主要成分是
(2)写出甲方案第①步反应的离子方程式:
(3)甲方案第②步滴定前,滴定管需用NaOH标准溶液润洗,其操作方法是
(4)若用盐酸代替稀硫酸处理样品,则按乙方案实验测定的结果
(5)若取样品wg,按乙方案测得消耗0.01000mol·L-1I2溶液VmL,则1kg样品中含SO2的质量是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】硫酸铁铵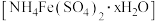 是一种重要铁盐。为充分利用资源,变废为宝,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流程如下:
是一种重要铁盐。为充分利用资源,变废为宝,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流程如下:
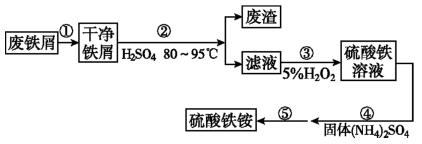
回答下列问题:
(1)步骤①的目的是去除废铁屑表面的油污,方法是_______ 。
(2)步骤②需要加热的目的是_______ ,温度保持80~95℃,采用的合适加热方式是_______ 。铁屑中含有少量硫化物,反应产生的气体需要净化处理,合适的装置为_______ (填标号)。

(3)步骤③中选用足量的 ,理由是
,理由是_______ 。
(4)步骤⑤的具体实验操作有_______ ,经干燥得到硫酸铁铵晶体样品。
(5)采用热重分析法测定硫酸铁铵晶体样品所含结晶水数,将样品加热到150℃时失掉1.5个结晶水,失重5.6%。硫酸铁铵晶体的化学式为_______ 。
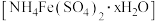 是一种重要铁盐。为充分利用资源,变废为宝,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流程如下:
是一种重要铁盐。为充分利用资源,变废为宝,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流程如下:
回答下列问题:
(1)步骤①的目的是去除废铁屑表面的油污,方法是
(2)步骤②需要加热的目的是

(3)步骤③中选用足量的
 ,理由是
,理由是(4)步骤⑤的具体实验操作有
(5)采用热重分析法测定硫酸铁铵晶体样品所含结晶水数,将样品加热到150℃时失掉1.5个结晶水,失重5.6%。硫酸铁铵晶体的化学式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】工业制备高锰酸钾是锰的重要化合物和常用的氧化剂。以下是工业上用软锰矿制备高锰酸钾的一种工艺流程。

(1)KMnO4稀溶液是一种常用的消毒剂。其消毒原理与下列物质相同的是_______ (填代号)。
a.84消毒液(NaClO溶液) b.双氧水 c.苯酚 d.75%酒精
(2)高锰酸钾保存在棕色试剂瓶,下列试剂保存不需要棕色试剂瓶的是_______ (填代号)。
a.浓硝酸 b.硝酸银 c.氯水 d.烧碱
(3)上述流程中可以循环使用的物质有_______ 。_______ (写化学式)。
(4)若不考虑物质循环与制备过程中的损失,则1 mol MnO2可制得_______ mol KMnO4。
(5)该生产中需要纯净的CO2气体。若实验室要制备纯净的CO2,所需试剂最好选择(选填代号)_______ 。
a.石灰石 b.稀HCl c.稀H2SO4 d.纯碱
(6)操作Ⅰ的名称是_______ ;操作Ⅱ根据KMnO4和K2CO3两物质在_______ (填性质)上的差异,采用_______ (填操作步骤)。趁热过滤得到KMnO4粗晶体。

(1)KMnO4稀溶液是一种常用的消毒剂。其消毒原理与下列物质相同的是
a.84消毒液(NaClO溶液) b.双氧水 c.苯酚 d.75%酒精
(2)高锰酸钾保存在棕色试剂瓶,下列试剂保存不需要棕色试剂瓶的是
a.浓硝酸 b.硝酸银 c.氯水 d.烧碱
(3)上述流程中可以循环使用的物质有
(4)若不考虑物质循环与制备过程中的损失,则1 mol MnO2可制得
(5)该生产中需要纯净的CO2气体。若实验室要制备纯净的CO2,所需试剂最好选择(选填代号)
a.石灰石 b.稀HCl c.稀H2SO4 d.纯碱
(6)操作Ⅰ的名称是
您最近一年使用:0次
【推荐3】锂离子电池正极材料有钴酸锂(LiCoO2)、铝箔和不溶性杂质。现欲利用以下工艺流程回收正极材料中的某些金属资源。
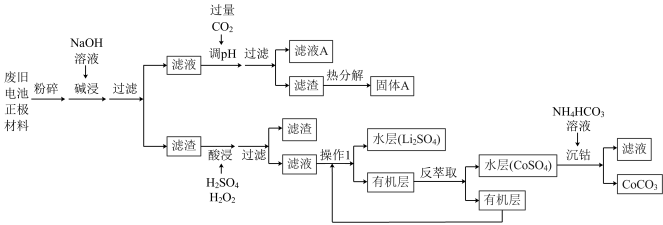
(1)“粉碎”的目的是_____ 。操作1的名称为_____ 。
(2)“碱浸”发生反应的离子方程式为_____ 。
(3)“酸浸”发生反应的化学方程式为_____ 。
(4)“沉钴”反应的离子方程式为_____ 。
(5)滤液A中能回收利用的主要物质是_____ 。若某锂离子电池正极材料中铝箔的质量分数为5.4%,则100kg该正极材料理论上最多能获得固体A_____ kg。

(1)“粉碎”的目的是
(2)“碱浸”发生反应的离子方程式为
(3)“酸浸”发生反应的化学方程式为
(4)“沉钴”反应的离子方程式为
(5)滤液A中能回收利用的主要物质是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题:
I.硝酸钾KNO3用途广泛,用作分析试剂和氧化剂,制造炸药、在食品工业用作发色剂,护色剂,抗做生物剂,防腐剂,如用于腌肉,在午餐肉中起防腐作用。某KNO3溶液I含有少量的Fe3+、 ,现从该溶液中获取纯净的KNO3晶体,进行如下操作。
,现从该溶液中获取纯净的KNO3晶体,进行如下操作。

(1)试剂1是___________
(2)溶液III中主要存在的金属阳离子有___________
(3)步骤4中发生的离子反应方程式为___________ 、
(4)步骤5涉及的操作为___________ 、冷却结晶、过滤。
II. 一份无色透明溶液中可能含有K+、Na+、Fe3+、H+、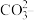 、
、 、
、 离子中的若干种,
离子中的若干种,且离子个数相等 。为了确定定溶液的组成,进行了如下操作:
①取2mL溶液,加足量稀盐酸,产生无色无味气体,该气体能使澄清石灰水变浑浊。
②取2mL溶液,先加足量稀硝酸酸化,有气体产生,再加硝酸银溶液进行检验,有白色沉淀产生。
(5)原溶液中一定不存在的阴离子是___________ 。
(6)原溶液中一定存在的阳离子是___________ 。 该离子的原子结构示意图为
该离子的原子结构示意图为___________ 。
(7)向该透明溶液中加入NaOH溶液,是否有反应发生?若没有,填“否”:若有,请写出有关的离子方程式。___________ 。
I.硝酸钾KNO3用途广泛,用作分析试剂和氧化剂,制造炸药、在食品工业用作发色剂,护色剂,抗做生物剂,防腐剂,如用于腌肉,在午餐肉中起防腐作用。某KNO3溶液I含有少量的Fe3+、
 ,现从该溶液中获取纯净的KNO3晶体,进行如下操作。
,现从该溶液中获取纯净的KNO3晶体,进行如下操作。
(1)试剂1是
(2)溶液III中主要存在的金属阳离子有
(3)步骤4中发生的离子反应方程式为
(4)步骤5涉及的操作为
II. 一份无色透明溶液中可能含有K+、Na+、Fe3+、H+、
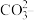 、
、 、
、 离子中的若干种,
离子中的若干种,①取2mL溶液,加足量稀盐酸,产生无色无味气体,该气体能使澄清石灰水变浑浊。
②取2mL溶液,先加足量稀硝酸酸化,有气体产生,再加硝酸银溶液进行检验,有白色沉淀产生。
(5)原溶液中一定不存在的阴离子是
(6)原溶液中一定存在的阳离子是
 该离子的原子结构示意图为
该离子的原子结构示意图为(7)向该透明溶液中加入NaOH溶液,是否有反应发生?若没有,填“否”:若有,请写出有关的离子方程式。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】以铬铁矿[主要成分为Fe(CrO2)2,还含有Al2O3、Fe2O3、SiO2等杂质]为主要原料生产重格酸钠晶体(Na2Cr2O7·2H2O,Na2Cr2O7是一种强氧化剂)的主要工艺流程如下:

(1)亚铬酸亚铁[Fe(CrO2)2]中Cr的化合价是________ 。
(2)煅烧生成Na2CrO4的化学方程式为_________ 。
(3)酸化滤液Na2CrO4时,不选用盐酸的原因是________ ,从平衡角度分析酸化的原理________ 。
(4)该工艺中某种产物可以再利用,该物质的化学式为________ 。
(5)采用石墨电极电解Na2CrO4溶液,可实现Na2CrO4→Na2Cr2O7的转化,其原理如图所示。

①写出I电极的电极反应式:____________ 。
②当Na2CrO4转化为1molNa2Cr2O7时,理论上II电极上转移电子的物质的量为_____ 。
(6)称取2.500g重铬酸钠晶体试样,加入蒸馏水配制成250mL溶液,从中取出25.00mL于碘量瓶中,向其中加入10mL2mol/LH2SO4溶液和足量碘化钾(铬的还原产物为Cr3+),放于暗处5min。然后加入100mL.水,加入3mL淀粉指示剂,用0.120mol/L的Na2S2O3标准溶液进行滴定(发生反应:I2+2 ==2I-+
==2I-+ ),当达到滴定终点时,共用去40.00mLNa2S2O3标准溶液,则所得产品的纯度为
),当达到滴定终点时,共用去40.00mLNa2S2O3标准溶液,则所得产品的纯度为_____ (设整个过程中其他杂质不参加反应)(保留3位有效数字)。

(1)亚铬酸亚铁[Fe(CrO2)2]中Cr的化合价是
(2)煅烧生成Na2CrO4的化学方程式为
(3)酸化滤液Na2CrO4时,不选用盐酸的原因是
(4)该工艺中某种产物可以再利用,该物质的化学式为
(5)采用石墨电极电解Na2CrO4溶液,可实现Na2CrO4→Na2Cr2O7的转化,其原理如图所示。

①写出I电极的电极反应式:
②当Na2CrO4转化为1molNa2Cr2O7时,理论上II电极上转移电子的物质的量为
(6)称取2.500g重铬酸钠晶体试样,加入蒸馏水配制成250mL溶液,从中取出25.00mL于碘量瓶中,向其中加入10mL2mol/LH2SO4溶液和足量碘化钾(铬的还原产物为Cr3+),放于暗处5min。然后加入100mL.水,加入3mL淀粉指示剂,用0.120mol/L的Na2S2O3标准溶液进行滴定(发生反应:I2+2
 ==2I-+
==2I-+ ),当达到滴定终点时,共用去40.00mLNa2S2O3标准溶液,则所得产品的纯度为
),当达到滴定终点时,共用去40.00mLNa2S2O3标准溶液,则所得产品的纯度为
您最近一年使用:0次
【推荐3】由硫铁矿“烧渣”(主要成分:Fe3O4、Fe2O3和FeO)制备绿矾(FeSO4·7H2O))的流程如图:
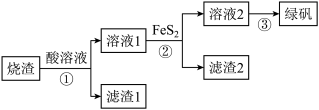
已知:FeS2(S的化合价为-1)难溶于水。
(1)①中加入的酸为___ ,滤渣2的主要成分是___ 。
(2)①中生成Fe3+的离子方程式为Fe3O4+8H+=2Fe3++Fe2++4H2O、___ 。
(3)检验②中Fe3+已经完全转化成Fe2+的实验方法:取适量溶液2,___ 。
(4)通过③得到绿矾晶体的实验操作:加热浓缩、冷却结晶、___ 。

已知:FeS2(S的化合价为-1)难溶于水。
(1)①中加入的酸为
(2)①中生成Fe3+的离子方程式为Fe3O4+8H+=2Fe3++Fe2++4H2O、
(3)检验②中Fe3+已经完全转化成Fe2+的实验方法:取适量溶液2,
(4)通过③得到绿矾晶体的实验操作:加热浓缩、冷却结晶、
您最近一年使用:0次



