某小组设计实验测定某胆矾( )样品的纯度(杂质不反应);称取
)样品的纯度(杂质不反应);称取 g胆矾样品溶于蒸馏水,加入足量KI溶液,充分反应后,过滤把滤液配制成250mL溶液,准确量取配制液25.00mL,于锥形瓶中,滴加2滴溶液X,用c
g胆矾样品溶于蒸馏水,加入足量KI溶液,充分反应后,过滤把滤液配制成250mL溶液,准确量取配制液25.00mL,于锥形瓶中,滴加2滴溶液X,用c 
 溶液滴定至终点,消耗滴定液V mL。已知:
溶液滴定至终点,消耗滴定液V mL。已知: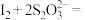
 。下列叙述错误的是
。下列叙述错误的是
 )样品的纯度(杂质不反应);称取
)样品的纯度(杂质不反应);称取 g胆矾样品溶于蒸馏水,加入足量KI溶液,充分反应后,过滤把滤液配制成250mL溶液,准确量取配制液25.00mL,于锥形瓶中,滴加2滴溶液X,用c
g胆矾样品溶于蒸馏水,加入足量KI溶液,充分反应后,过滤把滤液配制成250mL溶液,准确量取配制液25.00mL,于锥形瓶中,滴加2滴溶液X,用c 
 溶液滴定至终点,消耗滴定液V mL。已知:
溶液滴定至终点,消耗滴定液V mL。已知: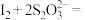
 。下列叙述错误的是
。下列叙述错误的是| A.滴定终点颜色由蓝色变为无色 |
B.加入足量KI溶液反应为 |
C.胆矾纯度为 |
| D.若用待测液润洗锥形瓶,结果会偏低 |
更新时间:2023-09-09 17:35:06
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】NA为阿伏加 德罗常数的值,下列说法正确的是( )
| A.16gO2和O3的混合气体中含有的分子数为0.5NA |
| B.0.3molAgNO3受热完全分解(2AgNO3=2Ag+2NO2↑+O2↑),用排水法收集到气体的分子数为 0.25NA |
| C.0.5NA个氯气分子所占体积约是11.2L |
| D.2.3g金属钠在装有氧气的集气瓶中完全燃烧,转移的电子数为0.1NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】向一定量的Cu、Fe2O3的混合物中加入600mL 2mol/L的盐酸,恰好使混合物完全溶解,所得溶液中不含Fe3+,再加入过量1 mol/L NaOH溶液,将沉淀过滤、洗涤、干燥,称得质量比原混合物增重17.6g,若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量是
| A.4.8 g | B.8.8 g | C.9.6g | D.14.4g |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法正确的有几项
(1)AgCl难溶于水,故属于弱电解质
(2)氨水中存在NH3·H2O分子,故氨水属于弱电解质
(3)稀醋酸加水稀释,各离子浓度减小但是电离程度增大
(4)用广泛pH试纸测定NaClO溶液的pH为12
(5)稀醋酸中加入CH3COONa固体,醋酸的电离程度减小,溶液导电能力增强
(6)对于0.1mol/L醋酸溶液,适当加热,溶液中 的值增大
的值增大
(7)将液面在8.20mL处的25mL碱式滴定管中的NaOH溶液全部放出,其体积为16.80mL
(8)中和滴定实验时,滴定管、锥形瓶均用待装溶液润洗
(9)将氯化钠溶液加热,溶液pH值将变小
(1)AgCl难溶于水,故属于弱电解质
(2)氨水中存在NH3·H2O分子,故氨水属于弱电解质
(3)稀醋酸加水稀释,各离子浓度减小但是电离程度增大
(4)用广泛pH试纸测定NaClO溶液的pH为12
(5)稀醋酸中加入CH3COONa固体,醋酸的电离程度减小,溶液导电能力增强
(6)对于0.1mol/L醋酸溶液,适当加热,溶液中
 的值增大
的值增大(7)将液面在8.20mL处的25mL碱式滴定管中的NaOH溶液全部放出,其体积为16.80mL
(8)中和滴定实验时,滴定管、锥形瓶均用待装溶液润洗
(9)将氯化钠溶液加热,溶液pH值将变小
| A.2 | B.3 | C.4 | D.5 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列有关实验的叙述正确的是( )


| A.将Cl2通入KI淀粉溶液中,溶液先变蓝后褪色,说明Cl2有漂白性 |
| B.图甲用于除去乙烯中的SO2 |
| C.用图乙装置蒸干明矾溶液制KAl(SO4)2·12H2O晶体 |
| D.滴定接近终点时,滴定管的尖嘴可以接触锥形瓶内壁 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】乙二胺(H2NCH2CH2NH2),无色液体,电离类似于氨:NH3+H2O⇌NH4++OH-,25℃时,kb1=10-4.07,kb2=10-7.15;乙二胺溶液中含氮微粒的物质的量浓度分数随溶液pH的变化如图。下列说法不正确的是( )


| A.曲线Ⅱ代表的微粒符号为H2NCH2CH2NH3+ |
| B.曲线Ⅰ与曲线II相交点对应pH=6.85 |
| C.乙二胺在水溶液中第二步电离的方程式H2NCH2CH2NH3++H2O⇌[H3NCH2CH2NH3]2++OH- |
| D.0.1 mol/LH2NCH2CH2NH3Cl溶液中各离子浓度大小关系为:c(Cl-)>c(H2NCH2CH2NH3+)>c(H+)>c(OH-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】 为二元酸,其电离过程为:
为二元酸,其电离过程为: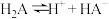 ,
, 。常温时,向20mL0.1mol/L
。常温时,向20mL0.1mol/L 水溶液中逐滴滴加0.1mol/L NaOH溶液,混合溶液中
水溶液中逐滴滴加0.1mol/L NaOH溶液,混合溶液中 、
、 和
和 的物质的量分数(
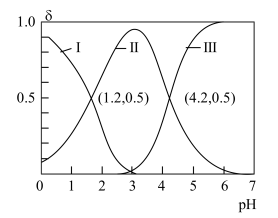
的物质的量分数( )随pH变化的关系如图所示。下列说法正确的是
)随pH变化的关系如图所示。下列说法正确的是
 为二元酸,其电离过程为:
为二元酸,其电离过程为: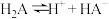 ,
, 。常温时,向20mL0.1mol/L
。常温时,向20mL0.1mol/L 水溶液中逐滴滴加0.1mol/L NaOH溶液,混合溶液中
水溶液中逐滴滴加0.1mol/L NaOH溶液,混合溶液中 、
、 和
和 的物质的量分数(
的物质的量分数( )随pH变化的关系如图所示。下列说法正确的是
)随pH变化的关系如图所示。下列说法正确的是
A. 的 的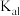 为 为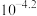 |
B.当溶液中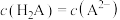 时,pH=2.7 时,pH=2.7 |
C.曲线II表示 |
| D.向pH=4.2的溶液中继续滴加NaOH溶液,水的电离程度持续变大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】测定鸡蛋壳中碳酸钙含量的方法如下:将一定质量鸡蛋壳粉碎后用已知浓度与体积的足量盐酸充分溶解(假设其他成分不反应),直到不再有气泡产生。再加入2滴酚酞试液,用标准NaOH溶液滴定至终点,记录消耗NaOH溶液体积。若某次测定的碳酸钙含量偏高,可能的原因是
| A.所用的盐酸浓度过高,有一定挥发 | B.终点时溶液呈较深的红色 |
| C.滴定管清洗后直接盛装标准NaOH溶液 | D.滴定前未通过加热赶走溶解的CO2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】用0.1000 mol/L的盐酸滴定20.00 mL NaOH溶液,测定其浓度,下列说法正确的是
| A.需用NaOH溶液润洗锥形瓶 |
| B.用量筒量取20.00 mL NaOH溶液 |
| C.使用酚酞做指示剂,滴定终点的现象为溶液浅红色褪去,半分钟不变色 |
| D.滴定前,没有除去酸式滴定管中的气泡,滴定后气泡消失,所测浓度会偏小 |
您最近一年使用:0次


 溶液检验
溶液检验 ,其现象是产生蓝色沉淀
,其现象是产生蓝色沉淀 (橙色)溶液和
(橙色)溶液和 (黄色)溶液的平衡体系中加入浓盐酸,溶液变橙色
(黄色)溶液的平衡体系中加入浓盐酸,溶液变橙色 溶液滴定未知浓度的盐酸时,下列情况会使盐酸的物质的量浓度偏低
溶液滴定未知浓度的盐酸时,下列情况会使盐酸的物质的量浓度偏低

