某科研小组采用如下方案回收一种光盘金属层中的少量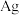 (金属层中其他金属含量过低,对实验的影响可忽略)。
(金属层中其他金属含量过低,对实验的影响可忽略)。
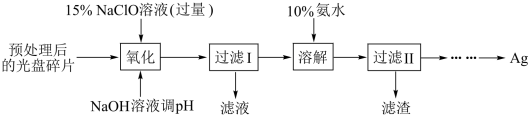
已知:① 溶液在受热或酸性条件下易分解,如:
溶液在受热或酸性条件下易分解,如: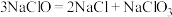
② 可溶于氨水生成
可溶于氨水生成
③常温时 (水合肼)在碱性条件下能还原
(水合肼)在碱性条件下能还原 :
: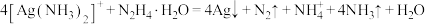 。
。
(1)“氧化”阶段需在 条件下进行,适宜的加热方式为
条件下进行,适宜的加热方式为___________ 。
(2) 溶液与
溶液与 反应的产物为
反应的产物为 、
、 和
和 ,该反应的化学方程式为
,该反应的化学方程式为___________ 。 也能氧化
也能氧化 ,从反应产物的角度分析,以
,从反应产物的角度分析,以 代替
代替 的缺点是
的缺点是___________ 。
(3)为提高 的回收率,需对“过滤Ⅱ”的滤渣进行洗涤,并
的回收率,需对“过滤Ⅱ”的滤渣进行洗涤,并___________ 。
(4)若省略“过滤Ⅰ”,直接向冷却后的反应容器中滴加 氨水,则需要增加氨水的用量,除因过量
氨水,则需要增加氨水的用量,除因过量 与
与 反应外(该条件下
反应外(该条件下 与
与 不反应),还因为
不反应),还因为___________ 。
(5)“溶解”阶段发生反应的离子方程式为___________ 。
(6)请设计从“过滤Ⅱ”后的滤液中获取单质 的实验方案:
的实验方案:___________ (实验中须使用的试剂有: 水合肼溶液,
水合肼溶液,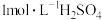 )。
)。
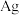 (金属层中其他金属含量过低,对实验的影响可忽略)。
(金属层中其他金属含量过低,对实验的影响可忽略)。
已知:①
 溶液在受热或酸性条件下易分解,如:
溶液在受热或酸性条件下易分解,如: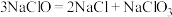
②
 可溶于氨水生成
可溶于氨水生成
③常温时
 (水合肼)在碱性条件下能还原
(水合肼)在碱性条件下能还原 :
: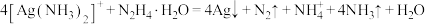 。
。(1)“氧化”阶段需在
 条件下进行,适宜的加热方式为
条件下进行,适宜的加热方式为(2)
 溶液与
溶液与 反应的产物为
反应的产物为 、
、 和
和 ,该反应的化学方程式为
,该反应的化学方程式为 也能氧化
也能氧化 ,从反应产物的角度分析,以
,从反应产物的角度分析,以 代替
代替 的缺点是
的缺点是(3)为提高
 的回收率,需对“过滤Ⅱ”的滤渣进行洗涤,并
的回收率,需对“过滤Ⅱ”的滤渣进行洗涤,并(4)若省略“过滤Ⅰ”,直接向冷却后的反应容器中滴加
 氨水,则需要增加氨水的用量,除因过量
氨水,则需要增加氨水的用量,除因过量 与
与 反应外(该条件下
反应外(该条件下 与
与 不反应),还因为
不反应),还因为(5)“溶解”阶段发生反应的离子方程式为
(6)请设计从“过滤Ⅱ”后的滤液中获取单质
 的实验方案:
的实验方案: 水合肼溶液,
水合肼溶液,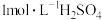 )。
)。
23-24高三上·河北石家庄·阶段练习 查看更多[3]
更新时间:2023-10-27 08:35:17
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
【推荐1】铜及其合金是人类最早使用的金属材料。
(1)铜原子的价电子排布式是___________ 。
(2)如图是金属Ca和Cu所形成的某种合金的晶胞结构示意图,则该合金中Ca和Cu的原子个数比为___________ 。

(3)Cu2+能与NH3、H2O、Cl-等形成配位数为4的配合物。
①[Cu(NH3)4]2+的结构式是为___________ 。
且[Cu(NH3)4]2+中存在的化学键类型有___________ (填序号)。
A、配位键 B、金属键 C、极性共价键 D、非极性共价键 E、离子键
②[Cu(NH3)4]2+具有对称的空间构型,[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为___________ 。
③某种含Cu2+的化合物可催化丙烯醇制备丙醛的反应:HOCH2CH=CH2→CH3CH2CHO,在丙烯醇分子中共有___________ σ键和___________ π键。
(1)铜原子的价电子排布式是
(2)如图是金属Ca和Cu所形成的某种合金的晶胞结构示意图,则该合金中Ca和Cu的原子个数比为

(3)Cu2+能与NH3、H2O、Cl-等形成配位数为4的配合物。
①[Cu(NH3)4]2+的结构式是为
且[Cu(NH3)4]2+中存在的化学键类型有
A、配位键 B、金属键 C、极性共价键 D、非极性共价键 E、离子键
②[Cu(NH3)4]2+具有对称的空间构型,[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为
③某种含Cu2+的化合物可催化丙烯醇制备丙醛的反应:HOCH2CH=CH2→CH3CH2CHO,在丙烯醇分子中共有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】配位化合物广泛应用于物质分离、定量测定、医药、催化等方面。SiC俗称金刚砂,晶体结构与金刚石相似。
(1)已知CuCl2溶液与乙二胺H2N-CH2CH2-NH2作用,可形成配离子(如图所示),该配合物中铜离子的配位数是_______ ,乙二胺分子中N原子成键时采取的杂化类型是_______ 。

(2)利用氧化法可制备某些配位化合物。如2CoCl2+2NH4Cl+8NH3+H2O2=2[Co(NH3)5Cl]Cl2+2H2O提供孤电子对的成键原子是_______ 和_______ ,1mol[Co(NH3)5Cl]Cl2的配离子中σ键的物质的量为_______ mol。
(3)SiC晶体晶胞结构如下图所示:
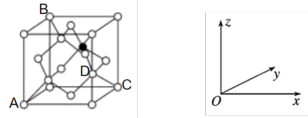
①已用黑球表示了其中一个硅原子,那么在该晶胞图中还需要涂黑的硅原子有_______ 个。
②该晶体类型为_______ ,在SiC晶体中,每个Si原子的配位数为_______ 个,若晶胞的边长为anm(NA代表阿伏加德罗常数的值),则该晶体的密度表达式为_______ g/cm3。
③原子坐标参数表示晶胞内部各原子的相对位置。上图中各原子坐标参数A为(0,0,0);B为(0,1,1);C为(1,1,0);则D原子的坐标参数为_______ 。
(1)已知CuCl2溶液与乙二胺H2N-CH2CH2-NH2作用,可形成配离子(如图所示),该配合物中铜离子的配位数是

(2)利用氧化法可制备某些配位化合物。如2CoCl2+2NH4Cl+8NH3+H2O2=2[Co(NH3)5Cl]Cl2+2H2O提供孤电子对的成键原子是
(3)SiC晶体晶胞结构如下图所示:

①已用黑球表示了其中一个硅原子,那么在该晶胞图中还需要涂黑的硅原子有
②该晶体类型为
③原子坐标参数表示晶胞内部各原子的相对位置。上图中各原子坐标参数A为(0,0,0);B为(0,1,1);C为(1,1,0);则D原子的坐标参数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】某二水合、六配位的锰配合物中各元素分析结果如下:
试回答下列问题:
(1)通过计算写出该配合物的化学式_______ 。
(2)该配合物具有八面体结构,画出该配合物所有可能几何异构体的结构式(用a表示H2O,用b表示Cl,用c表示相对分子质量最大的配位体):_______ ;
(3)实验表明:该配合物晶体属正交面心晶胞,结构具有高度的对称性。试在下侧方框内写出该配合物的结构式(用a表示H2O,用b表示Cl,用c表示相对分子质量最大的配位体)_______ ;

(4)有人认为,最大配位体c可通过如下路线合成(其中X、Y均为六元环状化合物,c中有多个环):CH2=NH→X Y(化学C6H15O3N3)
Y(化学C6H15O3N3) c,写出X、Y、c的结构简式:
c,写出X、Y、c的结构简式:_______ 、_______ 、_______ 。
| 元素 | Mn | Cl | C | N | O | H |
| 质量分数(%) | 12.4 | 16.1 | 32.6 | 25.3 | 7.2 | 6.4 |
试回答下列问题:
(1)通过计算写出该配合物的化学式
(2)该配合物具有八面体结构,画出该配合物所有可能几何异构体的结构式(用a表示H2O,用b表示Cl,用c表示相对分子质量最大的配位体):
(3)实验表明:该配合物晶体属正交面心晶胞,结构具有高度的对称性。试在下侧方框内写出该配合物的结构式(用a表示H2O,用b表示Cl,用c表示相对分子质量最大的配位体)

(4)有人认为,最大配位体c可通过如下路线合成(其中X、Y均为六元环状化合物,c中有多个环):CH2=NH→X
 Y(化学C6H15O3N3)
Y(化学C6H15O3N3) c,写出X、Y、c的结构简式:
c,写出X、Y、c的结构简式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室以 为原料制备
为原料制备 并进行定量分析。
并进行定量分析。
已知:
 。
。
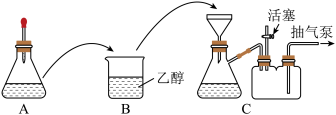
(1)配制溶液。称取一定质量的 晶体,放入锥形瓶中,溶解后滴加氨水,装置如图A所示(胶头滴管中吸有氨水)。
晶体,放入锥形瓶中,溶解后滴加氨水,装置如图A所示(胶头滴管中吸有氨水)。
①与烧杯相比,使用装置A作为反应器的优点是___________ 。
②滴加氨水时,有浅蓝色沉淀 生成;继续滴加氨水,沉淀消失,得到深蓝色
生成;继续滴加氨水,沉淀消失,得到深蓝色 溶液。写出
溶液。写出 与氨水反应的离子方程式:
与氨水反应的离子方程式:___________ 。
(2)制备晶体。将A中溶液转移至B中,析出 晶体:将B中混合物转移至装置C的漏斗中,减压过滤,用乙醇洗涤晶体2~3次;取出晶体,干燥。两次转移均需洗涤原容器,目的是
晶体:将B中混合物转移至装置C的漏斗中,减压过滤,用乙醇洗涤晶体2~3次;取出晶体,干燥。两次转移均需洗涤原容器,目的是___________ 。
(3)废液回收。从含有 、乙醇和氨水的废液中回收乙醇并获得
、乙醇和氨水的废液中回收乙醇并获得 、
、 的混合溶液,应加入的试剂是
的混合溶液,应加入的试剂是___________ (填化学式),回收乙醇的实验方法为___________ 。
(4)测定晶体中 的含量。请补充完整实验方案:取一定质量的
的含量。请补充完整实验方案:取一定质量的 晶体,加适量蒸馏水溶解
晶体,加适量蒸馏水溶解___________ ,干燥,灼烧至恒重。(须使用的试剂:蒸馏水, 溶液,
溶液,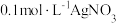 溶液)
溶液)
 为原料制备
为原料制备 并进行定量分析。
并进行定量分析。已知:

 。
。
(1)配制溶液。称取一定质量的
 晶体,放入锥形瓶中,溶解后滴加氨水,装置如图A所示(胶头滴管中吸有氨水)。
晶体,放入锥形瓶中,溶解后滴加氨水,装置如图A所示(胶头滴管中吸有氨水)。①与烧杯相比,使用装置A作为反应器的优点是
②滴加氨水时,有浅蓝色沉淀
 生成;继续滴加氨水,沉淀消失,得到深蓝色
生成;继续滴加氨水,沉淀消失,得到深蓝色 溶液。写出
溶液。写出 与氨水反应的离子方程式:
与氨水反应的离子方程式:(2)制备晶体。将A中溶液转移至B中,析出
 晶体:将B中混合物转移至装置C的漏斗中,减压过滤,用乙醇洗涤晶体2~3次;取出晶体,干燥。两次转移均需洗涤原容器,目的是
晶体:将B中混合物转移至装置C的漏斗中,减压过滤,用乙醇洗涤晶体2~3次;取出晶体,干燥。两次转移均需洗涤原容器,目的是(3)废液回收。从含有
 、乙醇和氨水的废液中回收乙醇并获得
、乙醇和氨水的废液中回收乙醇并获得 、
、 的混合溶液,应加入的试剂是
的混合溶液,应加入的试剂是(4)测定晶体中
 的含量。请补充完整实验方案:取一定质量的
的含量。请补充完整实验方案:取一定质量的 晶体,加适量蒸馏水溶解
晶体,加适量蒸馏水溶解 溶液,
溶液,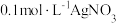 溶液)
溶液)
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】原子序数小于36的X、Y、Z、W四种元素,其中X原子核外电子只有一种运动状态,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W在周期表的位置为第四周期IB族。
回答下列问题:
(1)1molY2X4含有σ键的数目______ NA。
(2)元素X、Y、Z可形成一种一元弱酸分子,其中Y原子的杂化轨道类型为______ 。
(3)向含W2+离子的溶液中逐滴加入氨水,发生反应的现象为______ ,用离子方程式表示:______ ,继续加入氨水,会看到的现象为______ ,用离子方程式表示:______ 。
回答下列问题:
(1)1molY2X4含有σ键的数目
(2)元素X、Y、Z可形成一种一元弱酸分子,其中Y原子的杂化轨道类型为
(3)向含W2+离子的溶液中逐滴加入氨水,发生反应的现象为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】铜及其化合物在化学与生活中应用广泛,某实验兴趣小组对硫酸铜进行实验探究,步骤如下:
①无水CuSO4是一种白色的固体,溶于水所得溶液为天蓝色。
②向盛有硫酸铜溶液的试管中加入氨水,析出蓝色的沉淀。
③向蓝色的沉淀中继续加氨水,沉淀溶解,得到深蓝色透明的溶液。
④向深蓝色透明的溶液中加入极性较小的溶剂乙醇,将析出深蓝色的晶体。回答下列问题
(1)基态铜原子的电子排布式为___________ 。
(2)铜有两种氧化物CuO和Cu2O,二者较稳定的是___________ ,请从结构的角度解释原因是___________
(3)实验步骤①中得到天蓝色溶液是因为产生了___________ (填离子符号),该离子中的化学键类型是___________ ,该离子的空间结构为___________ ,0.1mol该离子中所含σ键数目为___________ 。
(4)步骤②析出蓝色的沉淀的离子方程式为___________ ,步骤③沉淀溶解,得到深蓝色透明的溶液的离子方程式为___________ 。
(5)步骤④中乙醇的作用是___________ 得到的蓝色晶体是___________ (填化学式)
①无水CuSO4是一种白色的固体,溶于水所得溶液为天蓝色。
②向盛有硫酸铜溶液的试管中加入氨水,析出蓝色的沉淀。
③向蓝色的沉淀中继续加氨水,沉淀溶解,得到深蓝色透明的溶液。
④向深蓝色透明的溶液中加入极性较小的溶剂乙醇,将析出深蓝色的晶体。回答下列问题
(1)基态铜原子的电子排布式为
(2)铜有两种氧化物CuO和Cu2O,二者较稳定的是
(3)实验步骤①中得到天蓝色溶液是因为产生了
(4)步骤②析出蓝色的沉淀的离子方程式为
(5)步骤④中乙醇的作用是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】地下卤水含有丰富的化学资源,可用于生产粗盐、粗溴、粗碘等产品。
(1)粗盐一般含有NaCl、 、
、 和
和 等杂质。从粗盐制得精盐的过程如下:
等杂质。从粗盐制得精盐的过程如下:

请回答下列问题:
① 的电离方程式为
的电离方程式为___________ 。
②试剂I是___________ (填化学式)。
③加入试剂III产生气体的离子方程式为___________ 。
④操作c的名称为___________ ,操作b能否省略___________ (填“能”或“否”),其理由为___________ 。
⑤设计实验说明所得溶液B中是否含有 :
:___________ 。
(2)地下卤水经过处理得到“析钠母液”,进一步提纯的工艺流程如下:

已知:①“析钠母液”主要含有 、
、 、
、 、
、 等。
等。
②氧化性: ,
, 为易挥发的红棕色液体,
为易挥发的红棕色液体, 为紫黑色固体
为紫黑色固体
回答下列问题:
①往“析钠母液”中,通入少量氯气时,主要发生反应的离子方程式为___________ 。
②“碱液吸收”中,发生反应: (未配平)。配平上述反应,并用单线桥或双线桥法表示该反应电子转移的方向和数目,
(未配平)。配平上述反应,并用单线桥或双线桥法表示该反应电子转移的方向和数目,___________ 若生成4.8g溴单质时,转移电子数目为___________  。
。
③“氧化析碘”中,氧化产物和还原产物的物质的量之比为___________ 。
(1)粗盐一般含有NaCl、
 、
、 和
和 等杂质。从粗盐制得精盐的过程如下:
等杂质。从粗盐制得精盐的过程如下:
请回答下列问题:
①
 的电离方程式为
的电离方程式为②试剂I是
③加入试剂III产生气体的离子方程式为
④操作c的名称为
⑤设计实验说明所得溶液B中是否含有
 :
:(2)地下卤水经过处理得到“析钠母液”,进一步提纯的工艺流程如下:

已知:①“析钠母液”主要含有
 、
、 、
、 、
、 等。
等。②氧化性:
 ,
, 为易挥发的红棕色液体,
为易挥发的红棕色液体, 为紫黑色固体
为紫黑色固体回答下列问题:
①往“析钠母液”中,通入少量氯气时,主要发生反应的离子方程式为
②“碱液吸收”中,发生反应:
 (未配平)。配平上述反应,并用单线桥或双线桥法表示该反应电子转移的方向和数目,
(未配平)。配平上述反应,并用单线桥或双线桥法表示该反应电子转移的方向和数目, 。
。③“氧化析碘”中,氧化产物和还原产物的物质的量之比为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】以废锌催化剂(主要成分为ZnO 及少量Fe2O3、CuO、MnO、SiO2)为原料制备锌的流程如下:

已知:①“浸取”时,ZnO、CuO转化为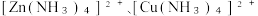 进入溶液;②25℃时, Ksp
进入溶液;②25℃时, Ksp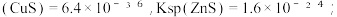 ③深度除杂标准:溶液中
③深度除杂标准:溶液中 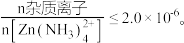
(1)“滤渣1”的主要成分为 Mn(OH)2、SiO2和_______ 。
(2)“深度除锰”是在碱性条件下将残留的Mn2+转化为MnO2,离子方程式为_______ 。
(3)“深度除铜”时,锌的最终回收率、[除铜效果以反应后溶液中铜锌比 表示]与“(NH4)2S 加入量”[以
表示]与“(NH4)2S 加入量”[以 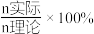 表示]的关系曲线如图所示。
表示]的关系曲线如图所示。
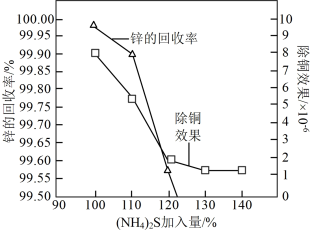
①当(NH4)2S加入量≥100%时,锌的最终回收率下降的原因是_______ (用离子方程式表示),该反应的平衡常数为_______ 。{已知 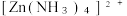 的
的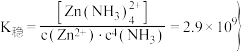
②“深度除铜”时(NH4)2S加入量最好应选_______ (填字母)。
A.100% B.110% C.120% D.130%
(4)ZnO存在多种晶体结构,其中纤锌矿型和闪锌矿型是最常见的晶体结构,如图结构。
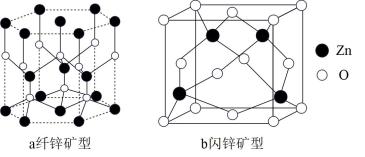
①图a纤锌矿型ZnO晶体中O2-的配位数为_______ 。
②图b闪锌矿型晶胞密度为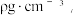 则Zn2+与(O2-的距离为
则Zn2+与(O2-的距离为_______ nm。(设NA为阿伏加德罗常数的值)

已知:①“浸取”时,ZnO、CuO转化为
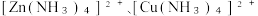 进入溶液;②25℃时, Ksp
进入溶液;②25℃时, Ksp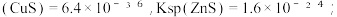 ③深度除杂标准:溶液中
③深度除杂标准:溶液中 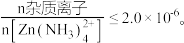
(1)“滤渣1”的主要成分为 Mn(OH)2、SiO2和
(2)“深度除锰”是在碱性条件下将残留的Mn2+转化为MnO2,离子方程式为
(3)“深度除铜”时,锌的最终回收率、[除铜效果以反应后溶液中铜锌比
 表示]与“(NH4)2S 加入量”[以
表示]与“(NH4)2S 加入量”[以 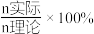 表示]的关系曲线如图所示。
表示]的关系曲线如图所示。
①当(NH4)2S加入量≥100%时,锌的最终回收率下降的原因是
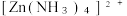 的
的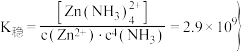
②“深度除铜”时(NH4)2S加入量最好应选
A.100% B.110% C.120% D.130%
(4)ZnO存在多种晶体结构,其中纤锌矿型和闪锌矿型是最常见的晶体结构,如图结构。

①图a纤锌矿型ZnO晶体中O2-的配位数为
②图b闪锌矿型晶胞密度为
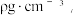 则Zn2+与(O2-的距离为
则Zn2+与(O2-的距离为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】和硅同一主族的锗也是重要的半导体材料,锗广泛用于航空航天测控、光纤通讯等领域。一种纯GeO2粗品(主要含GeO2、As2O3)制备锗工艺如下:
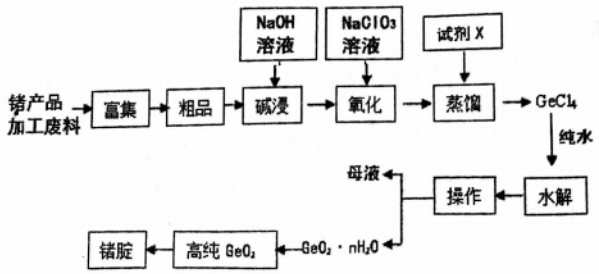
已知:①GeO2和As203都是两性氧化物;
②GeCl4的熔点为-49.5℃,GeCl4和AsC13的沸点分别为84℃、130.2℃。
回答下列问题:
(1)试剂X为:_____________ (填化学式)。
(2)“氧化”的过程是将NaAs02都氧化为Na3As04,其反应的离子方程式为:_______________________________________________ 。
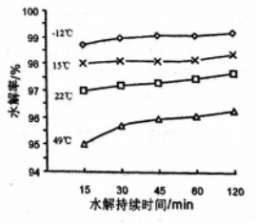
(3)GeCl4的水解率随温度变化曲线如图所示。结合图象和题干分析:“水解”操作时保持较低温度来提高产率的原因(说一条即可):__________________________ 。
(4)GeCl4水解生成Ge02·nH20,此过程用化学方程式可表示为:__________________________ 。
(5)传统的提纯方法是将“粗品”直接加入浓盐酸中蒸馏,其缺点是:__________________________ 。
(6)“操作”包括:__________________________ ;检验Ge02·nH20是否洗涤干净的方法:___________________________________________ 。

已知:①GeO2和As203都是两性氧化物;
②GeCl4的熔点为-49.5℃,GeCl4和AsC13的沸点分别为84℃、130.2℃。
回答下列问题:
(1)试剂X为:
(2)“氧化”的过程是将NaAs02都氧化为Na3As04,其反应的离子方程式为:
(3)GeCl4的水解率随温度变化曲线如图所示。结合图象和题干分析:“水解”操作时保持较低温度来提高产率的原因(说一条即可):

(4)GeCl4水解生成Ge02·nH20,此过程用化学方程式可表示为:
(5)传统的提纯方法是将“粗品”直接加入浓盐酸中蒸馏,其缺点是:
(6)“操作”包括:
您最近一年使用:0次



