Ⅰ.黑火药是由硫磺粉、硝酸钾和木炭按一定比例混合而成的。爆炸时发生的反应为: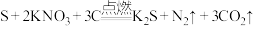 。
。
(1)该反应中,氧化剂是_____ (填化学式,下同),氧化产物是_____ 。在上述反应中若有 硫单质完全反应,被硫单质氧化的单质
硫单质完全反应,被硫单质氧化的单质 的质量是
的质量是_____ g。
Ⅱ.造纸工业是国民经济十大支柱制造业之一,在《天工开物》中记载了比较完善的造纸方法。但造纸过程会消耗大量的资源并产生污水,因此资源的回收利用以及污水的处理非常重要。某造纸厂制浆及废水处理流程如下: 。制浆废水中大部分碱性物质被回收利用,剩余的有机物在细菌池被微生物分解除去。
。制浆废水中大部分碱性物质被回收利用,剩余的有机物在细菌池被微生物分解除去。
(2)“碱液重生”过程分为以下两步反应,请补充反应ii的离子方程式:
ⅰ.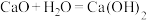 (石灰乳)
(石灰乳)
ⅱ._____ 。
(3)反应 的化学方程式为
的化学方程式为_____ 。
(4)为防止细菌失活,须先调 至中性。下列物质中,可实现该目的的有_____(填选项字母)
至中性。下列物质中,可实现该目的的有_____(填选项字母)
(5)上述过程中,循环使用的物质有_____ (写化学式)。
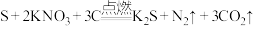 。
。(1)该反应中,氧化剂是
 硫单质完全反应,被硫单质氧化的单质
硫单质完全反应,被硫单质氧化的单质 的质量是
的质量是Ⅱ.造纸工业是国民经济十大支柱制造业之一,在《天工开物》中记载了比较完善的造纸方法。但造纸过程会消耗大量的资源并产生污水,因此资源的回收利用以及污水的处理非常重要。某造纸厂制浆及废水处理流程如下:

 。制浆废水中大部分碱性物质被回收利用,剩余的有机物在细菌池被微生物分解除去。
。制浆废水中大部分碱性物质被回收利用,剩余的有机物在细菌池被微生物分解除去。(2)“碱液重生”过程分为以下两步反应,请补充反应ii的离子方程式:
ⅰ.
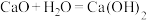 (石灰乳)
(石灰乳)ⅱ.
(3)反应
 的化学方程式为
的化学方程式为(4)为防止细菌失活,须先调
 至中性。下列物质中,可实现该目的的有_____(填选项字母)
至中性。下列物质中,可实现该目的的有_____(填选项字母)A. | B. | C. | D. |
更新时间:2023-10-20 07:17:42
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】以下元素均为短周期元素:
(1)B在周期表中的位置______ ,C离子的结构示意图_______ 。
(2)D的最低价含氧酸的电子式______ 。
(3)M的简单气态氢化物与B的单质形成燃料电池(KOH为电解液),写出其负极反应方程式____ 。(产物中无有毒有害物质)
(4)A在真空高压下能与由D、E组成的分子呈正四面体结构的化合物Y反应生成2种固体物质,其中一种是自然界中硬度最大的物质。该反应的化学方程式:______ 。
(5)仅由A、B、E组成的一种生活中的常用盐,其中A的质量分数为43%,其水溶液与D单质物质的量比为1:1反应的离子方程式为___________ 。
元素代号 | 相关信息 |
M | 非金属元素,其气态氢化物的水溶液呈碱性 |
A | A的单质与冷水剧烈反应,得到强碱性溶液 |
B | B的原子最外层电子数是内层电子数的三倍 |
C | 在第三周期中,C的简单离子半径最小 |
D | A、B、D组成的36电子的化合物X是家用消毒剂的主要成分 |
E | 所有有机物中都含有E元素 |
(1)B在周期表中的位置
(2)D的最低价含氧酸的电子式
(3)M的简单气态氢化物与B的单质形成燃料电池(KOH为电解液),写出其负极反应方程式
(4)A在真空高压下能与由D、E组成的分子呈正四面体结构的化合物Y反应生成2种固体物质,其中一种是自然界中硬度最大的物质。该反应的化学方程式:
(5)仅由A、B、E组成的一种生活中的常用盐,其中A的质量分数为43%,其水溶液与D单质物质的量比为1:1反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】某工厂的工业废水中含有大量的FeSO4和较多的Cu2+。为了减少污染并变废为宝,工厂计划从该废水中回收FeSO4和金属铜。请根据以下流程图,回答下列问题:
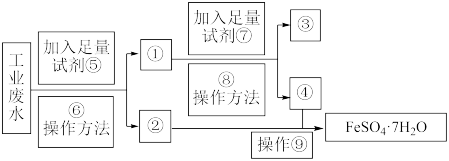
(1)⑥操作方法的名称是_______ ;操作⑨包括:蒸发浓缩、_______ 、过滤、洗涤、低温干燥。
(2)加入试剂⑤发生反应的离子方程式为_______ 。
(3)试剂⑦的化学式为_______ 。
(4)某兴趣小组同学欲鉴别④中的金属阳离子,设计如下实验:
甲同学取2.0 mL ④溶液,滴加氢氧化钠溶液,产生白色沉淀且很快变为灰绿色,最后变为红褐色沉淀,其中涉及氧化还原反应的化学方程式为_______ 。
乙同学取2.0 mL ④溶液,先加入几滴KSCN溶液,无明显现象,再加入几滴氯水,溶液变红,其中涉及氧化还原反应的离子方程式为_______ 。

(1)⑥操作方法的名称是
(2)加入试剂⑤发生反应的离子方程式为
(3)试剂⑦的化学式为
(4)某兴趣小组同学欲鉴别④中的金属阳离子,设计如下实验:
甲同学取2.0 mL ④溶液,滴加氢氧化钠溶液,产生白色沉淀且很快变为灰绿色,最后变为红褐色沉淀,其中涉及氧化还原反应的化学方程式为
乙同学取2.0 mL ④溶液,先加入几滴KSCN溶液,无明显现象,再加入几滴氯水,溶液变红,其中涉及氧化还原反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】现有以下物质:①浓盐酸,②乙醇,③熔融的KNO3,④NaHSO4固体,⑤铜丝,⑥NaHCO3,⑦氨水,⑧NaOH,⑨Cl2,⑩CO2。
请回答:
(1)能导电的是___ ,属于电解质的是___ ,属于非电解质的是___ 。
(2)写出④和⑧在水溶液中的电离方程式:④___ ,⑧___ 。
(3)写出①和⑥反应的离子方程式:___ ,该离子方程式还可表示上述某两种物质间的反应,请写出化学方程式___ 。
(4)工业上用⑧和⑨可制备“84消毒液”,其有效成分为NaClO,加酸可以增强“84消毒液”的消毒效果,但其不能与①混合使用,否则容易生成一种黄绿色的有毒气体,写出该反应的离子方程式___ 。
请回答:
(1)能导电的是
(2)写出④和⑧在水溶液中的电离方程式:④
(3)写出①和⑥反应的离子方程式:
(4)工业上用⑧和⑨可制备“84消毒液”,其有效成分为NaClO,加酸可以增强“84消毒液”的消毒效果,但其不能与①混合使用,否则容易生成一种黄绿色的有毒气体,写出该反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】请回答下面的问题
(1)氧化亚铜(Cu2O)是一种鲜红色粉末状固体,几乎不溶于水,可在酸性溶液中发生反应与硫酸、硝酸的反应如下:
i.Cu2O+H2SO4=CuSO4+Cu+H2O;
ii.3Cu2O+14HNO3(稀)=6Cu(NO3)2+2NO↑+7H2O
①反应i中还原剂为___________ (填化学式,下同),还原产物为___________ 。
②用单线桥标出反应ii中电子转移的方向和数目:___________ 。
③请写出反应ii的离子方程式:___________ 。
(2)高铁酸钠(Na2FeO4)有强氧化性,可以有效杀灭水中的细菌和病毒。已知湿法制备高铁酸钠的反应体系有六种微粒:Fe(OH)3、ClO-、OH-、 、Cl-、H2O。写出并配平湿法制备高铁酸钠的离子方程式:
、Cl-、H2O。写出并配平湿法制备高铁酸钠的离子方程式:___________ 。
(1)氧化亚铜(Cu2O)是一种鲜红色粉末状固体,几乎不溶于水,可在酸性溶液中发生反应与硫酸、硝酸的反应如下:
i.Cu2O+H2SO4=CuSO4+Cu+H2O;
ii.3Cu2O+14HNO3(稀)=6Cu(NO3)2+2NO↑+7H2O
①反应i中还原剂为
②用单线桥标出反应ii中电子转移的方向和数目:
③请写出反应ii的离子方程式:
(2)高铁酸钠(Na2FeO4)有强氧化性,可以有效杀灭水中的细菌和病毒。已知湿法制备高铁酸钠的反应体系有六种微粒:Fe(OH)3、ClO-、OH-、
 、Cl-、H2O。写出并配平湿法制备高铁酸钠的离子方程式:
、Cl-、H2O。写出并配平湿法制备高铁酸钠的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知反应①2F2+2H2O=4HF+O2↑;
②AlCl3+3NaHCO3=Al(OH)3↓+3NaCl+3CO2↑ ;
③2Na+2H2O=2NaOH+H2↑;
④CaO+H2O = Ca(OH)2
⑤SO2+Cl2+2H2O=H2SO4+2HCl;
⑥NaH+H2O=NaOH+H2↑;
⑦CO+H2O CO2+H2;
CO2+H2;
⑧3NO2+H2O = 2HNO3+NO
(1)上述反应中不属于氧化还原反应的有(填序号,下同)_______
(2)H2O被氧化的是_______ ;属于氧化还原反应,但H2O既不被氧化,也不被还原的是_______ 。
(3)用双线桥法表示反应⑧中电子转移的方向和数目_______ 。
(4)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲,也永远会激励着我们去奋发图强。黑火药在发生爆炸时,发生如下的反应:S+2KNO3+3C=K2S+N2↑+3CO2↑。被还原的元素是_______ 。
②AlCl3+3NaHCO3=Al(OH)3↓+3NaCl+3CO2↑ ;
③2Na+2H2O=2NaOH+H2↑;
④CaO+H2O = Ca(OH)2
⑤SO2+Cl2+2H2O=H2SO4+2HCl;
⑥NaH+H2O=NaOH+H2↑;
⑦CO+H2O
 CO2+H2;
CO2+H2;⑧3NO2+H2O = 2HNO3+NO
(1)上述反应中不属于氧化还原反应的有(填序号,下同)
(2)H2O被氧化的是
(3)用双线桥法表示反应⑧中电子转移的方向和数目
(4)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲,也永远会激励着我们去奋发图强。黑火药在发生爆炸时,发生如下的反应:S+2KNO3+3C=K2S+N2↑+3CO2↑。被还原的元素是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】氧化还原反应是一类重要的反应。
(1)已知反应Cu+2Fe3+=Cu2++2Fe2+,氧化性Fe3+____ Cu2+(填“<"或“> ")。
(2)已知钢在常温下能被HNO3溶解,反应方程式为: 3Cu+8HNO3= 3Cu(NO3)2+ 2NO↑+4H2O
①请将上述反应改成离子方程式,并用单线桥法表示电子得失的方向和数目__________
②若生成448mL的NO(标准状况下),则该过程中转移的电子是_______ mol
③被还原的硝酸占参加反应硝酸的比例为____________ 。
(3)在xR2++yH++O2=mR3++nH2O的离子方程式中,对系数m和R2+、R3+判断正确的是______ 。
A m=y,R3+是还原剂 B m=2y,R2+被氧化
C m=2,R3+是氧化剂 D m=4,R2+是还原剂
(4)实验室所用少量氯气是用下列方法制取的4HCl(浓)+MnO2 Cl2↑+MnCl2+2H2O其中氧化剂与还原剂的物质的量之比
Cl2↑+MnCl2+2H2O其中氧化剂与还原剂的物质的量之比_____ ,写出该反应的离子方程式__________
(1)已知反应Cu+2Fe3+=Cu2++2Fe2+,氧化性Fe3+
(2)已知钢在常温下能被HNO3溶解,反应方程式为: 3Cu+8HNO3= 3Cu(NO3)2+ 2NO↑+4H2O
①请将上述反应改成离子方程式,并用单线桥法表示电子得失的方向和数目
②若生成448mL的NO(标准状况下),则该过程中转移的电子是
③被还原的硝酸占参加反应硝酸的比例为
(3)在xR2++yH++O2=mR3++nH2O的离子方程式中,对系数m和R2+、R3+判断正确的是
A m=y,R3+是还原剂 B m=2y,R2+被氧化
C m=2,R3+是氧化剂 D m=4,R2+是还原剂
(4)实验室所用少量氯气是用下列方法制取的4HCl(浓)+MnO2
 Cl2↑+MnCl2+2H2O其中氧化剂与还原剂的物质的量之比
Cl2↑+MnCl2+2H2O其中氧化剂与还原剂的物质的量之比
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】请回答下列问题:
(1)氯酸钾和浓盐酸之间有下列反应: 。
。
该反应中发生还原反应的物质是___________ (填化学式,下同),氧化产物是___________ ;用双线桥标出方程式中的电子的转移情况:___________ 。
(2) 可用于制备一种新型,高效、多功能绿色水处理剂高铁酸钾(
可用于制备一种新型,高效、多功能绿色水处理剂高铁酸钾( ),氧化性比
),氧化性比 、
、 、
、 、
、 更强,主要反应:
更强,主要反应: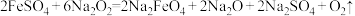 。
。
①上述反应中作还原剂的是___________ (填化学式)。
②简要说明 作为水处理剂时所起的作用
作为水处理剂时所起的作用___________ (写出一点即可)。
③在上述反应过程中可生成一种 白色沉淀,该沉淀极易被空气中的氧气氧化,反应的化学方程式为
白色沉淀,该沉淀极易被空气中的氧气氧化,反应的化学方程式为 (红褐色沉淀),该反应属于四大基本反应中的
(红褐色沉淀),该反应属于四大基本反应中的___________ (填反应类型名称),每当有1分子 参与反应转移
参与反应转移___________ 个电子。
(1)氯酸钾和浓盐酸之间有下列反应:
 。
。该反应中发生还原反应的物质是
(2)
 可用于制备一种新型,高效、多功能绿色水处理剂高铁酸钾(
可用于制备一种新型,高效、多功能绿色水处理剂高铁酸钾( ),氧化性比
),氧化性比 、
、 、
、 、
、 更强,主要反应:
更强,主要反应: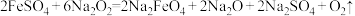 。
。①上述反应中作还原剂的是
②简要说明
 作为水处理剂时所起的作用
作为水处理剂时所起的作用③在上述反应过程中可生成一种
 白色沉淀,该沉淀极易被空气中的氧气氧化,反应的化学方程式为
白色沉淀,该沉淀极易被空气中的氧气氧化,反应的化学方程式为 (红褐色沉淀),该反应属于四大基本反应中的
(红褐色沉淀),该反应属于四大基本反应中的 参与反应转移
参与反应转移
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】CuCl是有机合成的重要催化剂,并用于颜料、防腐等工业。工业上由废铜料(含Fe、Al及其化合物、SiO2杂质),生产CuCl的工艺流程如下:
已知:CuCl溶于NaCl的浓溶液可生成CuCl2-,CuCl2-的溶液用水稀释后可生成CuCl沉淀
煅烧的主要目的是___________
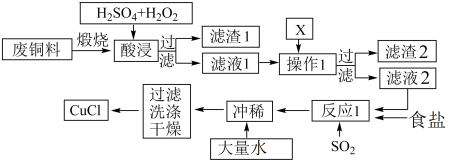
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Cu(OH)2 | 5.6 | 6.7 |
| Al(OH)3 | 3.8 | 4.7 |
煅烧的主要目的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】地球上的溴元素主要以Br﹣形式存在于海水中,某学习小组用提取粗食盐后的母液制备溴单质,实验过程如下:
请回答:

(1)下列说法正确的是_____ 。
A.步骤①试剂X可选氯气,一般在通风橱内进行实验
B.残留液中是否含有溴离子,可通过加CCl4萃取后观察下层溶液颜色来确定
C.溶液A中鼓入热空气是利用溴易挥发的特点分离出溴,也可用水蒸气代替
D.NaOH溶液可用饱和Na2CO3或Na2SO3代替
(2)酸化时用硫酸而不用盐酸的原因可能是_____ 。
请回答:

(1)下列说法正确的是
A.步骤①试剂X可选氯气,一般在通风橱内进行实验
B.残留液中是否含有溴离子,可通过加CCl4萃取后观察下层溶液颜色来确定
C.溶液A中鼓入热空气是利用溴易挥发的特点分离出溴,也可用水蒸气代替
D.NaOH溶液可用饱和Na2CO3或Na2SO3代替
(2)酸化时用硫酸而不用盐酸的原因可能是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】按要求填空。
(1)工业制胆矾时,将粗制CuO粉末(含杂质FeO、Fe2O3)慢慢加入适量的稀H2SO4中完全溶解,除去杂质离子后,再蒸发结晶可得纯净的胆矾晶体。已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;pH在3~4时,Fe3+以Fe(OH)3的形式完全沉淀。回答下列问题:
为除去溶液中的Fe2+,可先加入_______ ,(从下面四个选项选择)将Fe2+氧化为Fe3+,反应的离子方程式为_______________________ ,然后加入适量的__________ (写化学式)调整溶液的pH使Fe3+转化为Fe(OH)3沉淀。
A.KMnO4 B.Cl2 C.浓硫酸 D.H2O2
(2)如图为钠硫高能电池的结构示意图,该电池的工作温度为320 ℃左右,电池反应为2Na+xS=Na2Sx,正极的电极反应式为___________ 。M(由Na2O和Al2O3制得)的两个作用是________________ 。与铅蓄电池相比,当消耗相同质量的负极活性物质时,钠硫电池的理论放电量是铅蓄电池的_______ 倍。

(3)室温时,向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,当溶液pH=7时,溶液中各离子浓度由大到小的排列顺序是_______________ 。
(1)工业制胆矾时,将粗制CuO粉末(含杂质FeO、Fe2O3)慢慢加入适量的稀H2SO4中完全溶解,除去杂质离子后,再蒸发结晶可得纯净的胆矾晶体。已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;pH在3~4时,Fe3+以Fe(OH)3的形式完全沉淀。回答下列问题:
为除去溶液中的Fe2+,可先加入
A.KMnO4 B.Cl2 C.浓硫酸 D.H2O2
(2)如图为钠硫高能电池的结构示意图,该电池的工作温度为320 ℃左右,电池反应为2Na+xS=Na2Sx,正极的电极反应式为

(3)室温时,向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,当溶液pH=7时,溶液中各离子浓度由大到小的排列顺序是
您最近一年使用:0次



