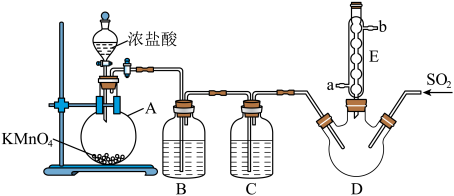
硫酰氯(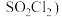 是一种重要的化工试济,氯化法是合成硫酰氯的常用方法。实验室合成硫酰氯的实验装置如下图所示(部分夹持装置未画出):
是一种重要的化工试济,氯化法是合成硫酰氯的常用方法。实验室合成硫酰氯的实验装置如下图所示(部分夹持装置未画出):
已知:① (1)
(1)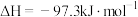 。
。
②常温下硫酰氯为无色液体,熔点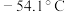 ,沸点
,沸点 ,在潮湿空气中“发烟”。
,在潮湿空气中“发烟”。
③ 以上或长时间存放硫酰氯都易分解,生成
以上或长时间存放硫酰氯都易分解,生成 和
和 。
。
回答下列问题:
(1)硫酰氯在潮湿空气中“发烟”的原因是_______ (用化学方程式表示)。
(2)装置A中发生反应的离子方程式为_______ 。
(3)仪器 的名称为
的名称为_______ ,其作用是_______ 。
(4)整套装置存在一处明显的缺䧄,请你提出改进措施_______ 。
(5)当装置A中生成氯气 (已折算成标准状况)时,则最终得到纯净的硫酰氯5.4g。硫酰氯的产率为
(已折算成标准状况)时,则最终得到纯净的硫酰氯5.4g。硫酰氯的产率为_______ 。
(6)氯磺酸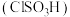 加热分解,也能制得硫酰氯与另外一种物质,该反应的化学方程式为
加热分解,也能制得硫酰氯与另外一种物质,该反应的化学方程式为_______ ,从分解的产物中分离出硫酰氯的操作方法是_______ 。
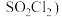 是一种重要的化工试济,氯化法是合成硫酰氯的常用方法。实验室合成硫酰氯的实验装置如下图所示(部分夹持装置未画出):
是一种重要的化工试济,氯化法是合成硫酰氯的常用方法。实验室合成硫酰氯的实验装置如下图所示(部分夹持装置未画出):
已知:①
 (1)
(1)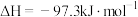 。
。②常温下硫酰氯为无色液体,熔点
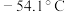 ,沸点
,沸点 ,在潮湿空气中“发烟”。
,在潮湿空气中“发烟”。③
 以上或长时间存放硫酰氯都易分解,生成
以上或长时间存放硫酰氯都易分解,生成 和
和 。
。回答下列问题:
(1)硫酰氯在潮湿空气中“发烟”的原因是
(2)装置A中发生反应的离子方程式为
(3)仪器
 的名称为
的名称为(4)整套装置存在一处明显的缺䧄,请你提出改进措施
(5)当装置A中生成氯气
 (已折算成标准状况)时,则最终得到纯净的硫酰氯5.4g。硫酰氯的产率为
(已折算成标准状况)时,则最终得到纯净的硫酰氯5.4g。硫酰氯的产率为(6)氯磺酸
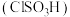 加热分解,也能制得硫酰氯与另外一种物质,该反应的化学方程式为
加热分解,也能制得硫酰氯与另外一种物质,该反应的化学方程式为
更新时间:2023-09-24 09:02:51
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】黄铁矿的主要成分是 ,其中含有一定量的铜、钴等金属。某工厂在传统回收工艺的基础上进一步改进焙烧方式,研究出高效利用硫铁矿资源的工艺如下:
,其中含有一定量的铜、钴等金属。某工厂在传统回收工艺的基础上进一步改进焙烧方式,研究出高效利用硫铁矿资源的工艺如下:

(1)研究表明,随着磨矿细度的增加,铜、钴的浸出率都会相应增加,其主要原因是:___________
(2)黄铁矿的氧化焙烧是制硫酸工艺的重要一步,其产物之一是 ,反应的化学方程式为:
,反应的化学方程式为:___________ ;制硫酸工艺中涉及反应2SO2+O2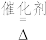 2SO3 ΔH<0,该反应需将温度控制在
2SO3 ΔH<0,该反应需将温度控制在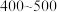 ℃,原因是
℃,原因是___________ 。
(3)氧化还原焙烧渣仍有少量CuS,已知CuS不溶于 ,但当浸出过程含有硫酸铁时,也可氧化浸出,其反应的离子方程式为:
,但当浸出过程含有硫酸铁时,也可氧化浸出,其反应的离子方程式为:___________ 。
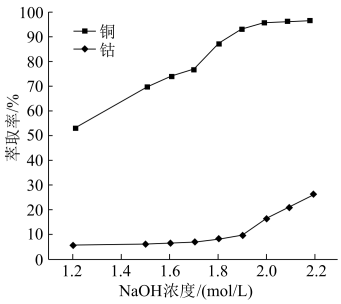
(4)浸液通过加入萃取剂可实现铜和钴的分离,在萃取前加入NaOH溶液乳化可提高分离效率,不同浓度的溶液对萃取率的影响如图,则NaOH溶液最佳的浓度为___________ 。
用硫酸浸取后的浸渣能用磁选法分离,则该氧化物为___________ (填化学式)
已知黄铁矿氧化焙烧前后主要元素质量分数如图:
为测定铜的浸出率,取50g焙烧后的烧渣,经处理后测得 物质的量为
物质的量为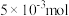 ,则铜离子的浸出率为
,则铜离子的浸出率为___________ (结果保留三位有效数字)。
 ,其中含有一定量的铜、钴等金属。某工厂在传统回收工艺的基础上进一步改进焙烧方式,研究出高效利用硫铁矿资源的工艺如下:
,其中含有一定量的铜、钴等金属。某工厂在传统回收工艺的基础上进一步改进焙烧方式,研究出高效利用硫铁矿资源的工艺如下:
(1)研究表明,随着磨矿细度的增加,铜、钴的浸出率都会相应增加,其主要原因是:
(2)黄铁矿的氧化焙烧是制硫酸工艺的重要一步,其产物之一是
 ,反应的化学方程式为:
,反应的化学方程式为: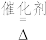 2SO3 ΔH<0,该反应需将温度控制在
2SO3 ΔH<0,该反应需将温度控制在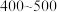 ℃,原因是
℃,原因是(3)氧化还原焙烧渣仍有少量CuS,已知CuS不溶于
 ,但当浸出过程含有硫酸铁时,也可氧化浸出,其反应的离子方程式为:
,但当浸出过程含有硫酸铁时,也可氧化浸出,其反应的离子方程式为:(4)浸液通过加入萃取剂可实现铜和钴的分离,在萃取前加入NaOH溶液乳化可提高分离效率,不同浓度的溶液对萃取率的影响如图,则NaOH溶液最佳的浓度为

用硫酸浸取后的浸渣能用磁选法分离,则该氧化物为
已知黄铁矿氧化焙烧前后主要元素质量分数如图:
| 项目 | Fe | S | Cu | Co |
| 焙烧前(%) | 40.28 | 42.55 | 0.53 | 0.022 |
| 焙烧后(%) | 53.08 | 0.96 | 0.76 | 0.047 |
 物质的量为
物质的量为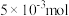 ,则铜离子的浸出率为
,则铜离子的浸出率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】利用铁元素价类二维图可以多角度研究含铁物质的性质及转化关系;请完成下列问题。
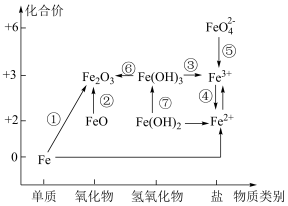
(1)下列说法正确的是______。
(2)检验溶液中是否存在 的试剂是
的试剂是______ 。写出对应的离子方程式_____________________________ 。
(3) 常用作杀菌消毒剂,生产
常用作杀菌消毒剂,生产 的反应原理是:
的反应原理是:
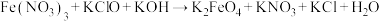 (未配平),则该反应中氧化剂与还原剂的物质的量之比为
(未配平),则该反应中氧化剂与还原剂的物质的量之比为______ 。
(4)电子工业需用30%的 溶液腐蚀敷在绝缘板上的铜制造印刷电路板。写出
溶液腐蚀敷在绝缘板上的铜制造印刷电路板。写出 溶液腐蚀铜的化学反应方程式:
溶液腐蚀铜的化学反应方程式:_________________________________ 。
(5)某中学实验小组设计如下实验探究亚铁盐的性质。
①实验Ⅰ中由白色沉淀生成红褐色沉淀的化学方程式______ 。
②对实验Ⅱ所得白色沉淀展开研究:查阅资料:在溶液中不存在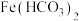
ⅰ取Ⅱ中少量白色沉淀,充分洗涤,向其中加入稀硫酸,沉淀完全溶解,产生无色气泡;
ⅱ向ⅰ所得溶液中滴入 试剂,溶液几乎不变红;
试剂,溶液几乎不变红;
ⅲ向ⅱ溶液中再滴入少量氯水,溶液立即变为红色。
根据以上现象,实验Ⅱ中生成的白色沉淀的化学式为______ 。
(6)测定补铁剂中铁元素的含量。
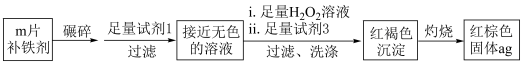
计算每片该补铁剂含铁元素的质量为______ g。

(1)下列说法正确的是______。
A. 是碱性氧化物 是碱性氧化物 |
B. 是一种黑色粉末,不稳定,在空气中受热,能被迅速氧化发生转化② 是一种黑色粉末,不稳定,在空气中受热,能被迅速氧化发生转化② |
C. 不稳定,在加热情况下可实现转化⑥ 不稳定,在加热情况下可实现转化⑥ |
D.硫酸亚铁片和维生素 (具有还原性)同时服用能增强治疗缺铁性贫血的效果 (具有还原性)同时服用能增强治疗缺铁性贫血的效果 |
(2)检验溶液中是否存在
 的试剂是
的试剂是(3)
 常用作杀菌消毒剂,生产
常用作杀菌消毒剂,生产 的反应原理是:
的反应原理是: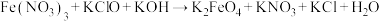 (未配平),则该反应中氧化剂与还原剂的物质的量之比为
(未配平),则该反应中氧化剂与还原剂的物质的量之比为(4)电子工业需用30%的
 溶液腐蚀敷在绝缘板上的铜制造印刷电路板。写出
溶液腐蚀敷在绝缘板上的铜制造印刷电路板。写出 溶液腐蚀铜的化学反应方程式:
溶液腐蚀铜的化学反应方程式:(5)某中学实验小组设计如下实验探究亚铁盐的性质。
实验方案 | 现象 | |
Ⅰ | 1.0mL 0.1mol/L 溶液中滴加1.0mL 0.5mol/L 溶液中滴加1.0mL 0.5mol/L 溶液 溶液 | 生成白色沉淀,后沉淀基本变为红褐色 |
Ⅱ | 1.0mL 0.1mol/L 溶液中滴加1.0mL 0.5mol/L 溶液中滴加1.0mL 0.5mol/L 溶液 溶液 | 生成白色沉淀,后沉淀颜色几乎不变 |
②对实验Ⅱ所得白色沉淀展开研究:查阅资料:在溶液中不存在
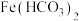
ⅰ取Ⅱ中少量白色沉淀,充分洗涤,向其中加入稀硫酸,沉淀完全溶解,产生无色气泡;
ⅱ向ⅰ所得溶液中滴入
 试剂,溶液几乎不变红;
试剂,溶液几乎不变红;ⅲ向ⅱ溶液中再滴入少量氯水,溶液立即变为红色。
根据以上现象,实验Ⅱ中生成的白色沉淀的化学式为
(6)测定补铁剂中铁元素的含量。

计算每片该补铁剂含铁元素的质量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】海带中含有丰富的碘,某校化学兴趣小组的同学们设计联合氯碱工业,以海带灰为原料提碘的工艺流程如图:
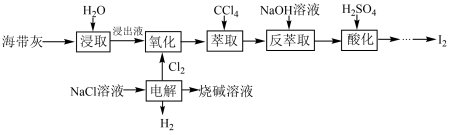
回答下列问题:
(1)“浸取”操作需要进行2~3次,将所得浸取液合并后进入下一流程,其目的是_____ ;请你设计实验证明“浸取”已经进行完全:_____ (需要用到的实验药品有:淀粉溶液、硫酸酸化的H2O2溶液,写出具体实验操作和现象)。
(2)“电解”反应的化学方程式为_____ 。
(3)“萃取”时,CCl4层的颜色为______ 色;“反萃取”时生成NaI和NaIO3,写出该反应的离子方程式:______ 。
(4)“酸化”后生成含I2的悬浊液,需要经过_____ (填操作名称)操作得到I2。
(5)该工艺流程实际操作中,碘的损失率为23.8%。若以2.5t海带灰为原料,最终制得I2物质的量为3×103mol,则该原料中含碘量为______ %
(6)该工艺流程中,除了H2O和NaCl以外,可以循环利用的物质有_____ (填化学式)。

回答下列问题:
(1)“浸取”操作需要进行2~3次,将所得浸取液合并后进入下一流程,其目的是
(2)“电解”反应的化学方程式为
(3)“萃取”时,CCl4层的颜色为
(4)“酸化”后生成含I2的悬浊液,需要经过
(5)该工艺流程实际操作中,碘的损失率为23.8%。若以2.5t海带灰为原料,最终制得I2物质的量为3×103mol,则该原料中含碘量为
(6)该工艺流程中,除了H2O和NaCl以外,可以循环利用的物质有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】次氯酸溶液是常用的消毒剂和漂白剂。某学习小组根据需要欲制备浓度不小于0.8mol/L的次氯酸溶液。
资料1:常温常压下,Cl2O为棕黄色气体,沸点为3.8℃,42 ℃以上会分解生成Cl2和O2,Cl2O易溶于水并与水立即反应生成 HClO。
资料2:将氯气和空气(不参与反应)按体积比1∶3混合通入潮湿的碳酸钠中发生反应2Cl2+2Na2CO3+H2O=Cl2O+2NaCl+2NaHCO3,用水吸收Cl2O(不含Cl2)制得次氯酸溶液。
(装置及实验)用以下装置制备次氯酸溶液。
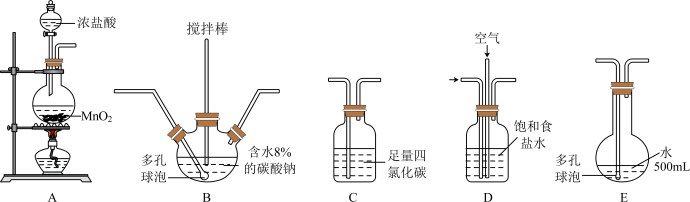
回答下列问题:
(1)各装置的连接顺序为_____ →_____ →_____ →____ →E。
(2)装置A中反应的离子方程式是__________________________ 。
(3)实验中控制氯气与空气体积比的方法是_____________________ 。
(4)反应过程中,装置B需放在冷水中,其目的是_________________________ 。
(5)装置E采用棕色圆底烧瓶是因为______________________ 。
(6)若装置B中生成的Cl2O气体有20%滞留在E前各装置中,其余均溶于装置E的水中,装置E所得500mL次氯酸溶液浓度为0.8mol/L,则至少需要含水8%的碳酸钠的质量为_________ g。
(7)已知次氯酸可被H2O2、FeCl2等物质还原成Cl-。测定E中次氯酸溶液的物质的量浓度的实验方案为:用________________ 准确量取20.00 mL次氯酸溶液,加入足量的________ 溶液,再加入足量的________ 溶液,过滤,洗涤,真空干燥,称量沉淀的质量。(可选用的试剂:H2O2溶液、FeCl2溶液、AgNO3溶液。)
资料1:常温常压下,Cl2O为棕黄色气体,沸点为3.8℃,42 ℃以上会分解生成Cl2和O2,Cl2O易溶于水并与水立即反应生成 HClO。
资料2:将氯气和空气(不参与反应)按体积比1∶3混合通入潮湿的碳酸钠中发生反应2Cl2+2Na2CO3+H2O=Cl2O+2NaCl+2NaHCO3,用水吸收Cl2O(不含Cl2)制得次氯酸溶液。
(装置及实验)用以下装置制备次氯酸溶液。

回答下列问题:
(1)各装置的连接顺序为
(2)装置A中反应的离子方程式是
(3)实验中控制氯气与空气体积比的方法是
(4)反应过程中,装置B需放在冷水中,其目的是
(5)装置E采用棕色圆底烧瓶是因为
(6)若装置B中生成的Cl2O气体有20%滞留在E前各装置中,其余均溶于装置E的水中,装置E所得500mL次氯酸溶液浓度为0.8mol/L,则至少需要含水8%的碳酸钠的质量为
(7)已知次氯酸可被H2O2、FeCl2等物质还原成Cl-。测定E中次氯酸溶液的物质的量浓度的实验方案为:用
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】实验室里用如图所示仪器和药品来制取纯净的无水氯化铝(2Al+3Cl2 2AlCl3)。图中A、B、C、D、E、F表示玻璃管接口,接口的弯曲和伸长等部分未画出。(氯化铝易吸水)
2AlCl3)。图中A、B、C、D、E、F表示玻璃管接口,接口的弯曲和伸长等部分未画出。(氯化铝易吸水)
(1)如果所制气体从左向右流向时,上述各仪器装置的正确连接顺序是(填各装置的序号)_______ ,其中②与④装置相连时,玻璃管接口(用装置中字母表示)应是_______ 接_______ 。
(2)装置②的作用是_______ ;装置④的作用是_______ 。
(3)实验开始时,应首先检验装置的_______ ,实验结束时,应先熄灭_______ 处的酒精灯。
(4)在装置⑤的烧瓶中,发生反应的化学方程式为_______
(5)装置⑥中发生的离子反应方程式为_______ 。
 2AlCl3)。图中A、B、C、D、E、F表示玻璃管接口,接口的弯曲和伸长等部分未画出。(氯化铝易吸水)
2AlCl3)。图中A、B、C、D、E、F表示玻璃管接口,接口的弯曲和伸长等部分未画出。(氯化铝易吸水)| 序号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 仪器及装置图 | 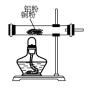 |  |  | 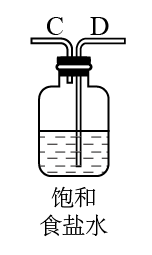 |  | 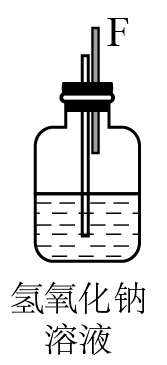 |
(2)装置②的作用是
(3)实验开始时,应首先检验装置的
(4)在装置⑤的烧瓶中,发生反应的化学方程式为
(5)装置⑥中发生的离子反应方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】疫情防控期间,含氯消毒剂功不可没。
(1)实验室用 和浓盐酸制取
和浓盐酸制取 的离子方程式为
的离子方程式为_______ 。
(2) 是新型的自来水消毒剂,某研究小组用如图装置制备少量
是新型的自来水消毒剂,某研究小组用如图装置制备少量 (夹持装置已略去)。
(夹持装置已略去)。

已知:常温下 极不稳定,为易溶于水但不与水反应的易挥发、易爆气体,沸点11℃。
极不稳定,为易溶于水但不与水反应的易挥发、易爆气体,沸点11℃。
①产物 中
中 的化合价是
的化合价是_______ 。
②以 和
和 为原料,制得
为原料,制得 和
和 ,反应的化学方程式为
,反应的化学方程式为_______ 。
③盛放 仪器的名称为
仪器的名称为_______ ,冰水浴的作用是_______ 。
④产物气被集气瓶B中盛放的稳定剂(某混合盐溶液)吸收,稳定剂的作用是_______ 。
⑤烧杯中混合液的作用是吸收尾气,试配平离子方程式:_______ 。
______ ______
______ _____
_____ _____
_____ _____
_____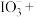 ______
______
(3)有效氯可用于衡量含氯消毒剂的消毒能力, 的有效氯=有效系数×含氯量
的有效氯=有效系数×含氯量 ,其中2是有效系数即
,其中2是有效系数即 夺取电子数,含氯量为氯的相对原子量与消毒剂分子量的比值。已知理论上
夺取电子数,含氯量为氯的相对原子量与消毒剂分子量的比值。已知理论上 杀菌消毒的最终产物为
杀菌消毒的最终产物为 ,则
,则 的有效系数为
的有效系数为_______ ,其有效氯为_______ (保留1位小数)。
(4) 在杀菌消毒过程中会产生副产物亚氯酸盐
在杀菌消毒过程中会产生副产物亚氯酸盐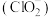 ,需将其转化为
,需将其转化为 除去。下列试剂中,可将
除去。下列试剂中,可将 转化为
转化为 的是
的是_______ (填字母序号)。
A. B.
B. C.
C.
(1)实验室用
 和浓盐酸制取
和浓盐酸制取 的离子方程式为
的离子方程式为(2)
 是新型的自来水消毒剂,某研究小组用如图装置制备少量
是新型的自来水消毒剂,某研究小组用如图装置制备少量 (夹持装置已略去)。
(夹持装置已略去)。
已知:常温下
 极不稳定,为易溶于水但不与水反应的易挥发、易爆气体,沸点11℃。
极不稳定,为易溶于水但不与水反应的易挥发、易爆气体,沸点11℃。①产物
 中
中 的化合价是
的化合价是②以
 和
和 为原料,制得
为原料,制得 和
和 ,反应的化学方程式为
,反应的化学方程式为③盛放
 仪器的名称为
仪器的名称为④产物气被集气瓶B中盛放的稳定剂(某混合盐溶液)吸收,稳定剂的作用是
⑤烧杯中混合液的作用是吸收尾气,试配平离子方程式:
______
 ______
______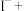 _____
_____ _____
_____ _____
_____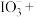 ______
______
(3)有效氯可用于衡量含氯消毒剂的消毒能力,
 的有效氯=有效系数×含氯量
的有效氯=有效系数×含氯量 ,其中2是有效系数即
,其中2是有效系数即 夺取电子数,含氯量为氯的相对原子量与消毒剂分子量的比值。已知理论上
夺取电子数,含氯量为氯的相对原子量与消毒剂分子量的比值。已知理论上 杀菌消毒的最终产物为
杀菌消毒的最终产物为 ,则
,则 的有效系数为
的有效系数为(4)
 在杀菌消毒过程中会产生副产物亚氯酸盐
在杀菌消毒过程中会产生副产物亚氯酸盐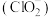 ,需将其转化为
,需将其转化为 除去。下列试剂中,可将
除去。下列试剂中,可将 转化为
转化为 的是
的是A.
 B.
B. C.
C.
您最近一年使用:0次



