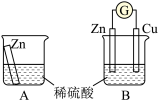
I.某兴趣小组为探究原电池工作原理,利用金属Zn与稀H2SO4反应,通过如图所示装置A、B进行实验,实验过程中装置A内溶液的温度升高,装置B的电流计指针发生偏转。
根据所学知识,完成下列各题:
(1)装置B为原电池,则Cu作_______ (填“正”或“负”)极,Zn电极上的电极反应式为_______ 。
(2)一般把金属导线称为“电子导体”,把电解质溶液称为“离子导体”。装置B中电池工作时“电子导体”中电子的流动方向可描述为_______ ;“离子导体”中H+离子的移动方向可描述为_______ 。
(3)从反应速率的角度上看,可以观察到A中反应比B中_______ (填“快”或“慢”)
(4)装置B中稀H2SO4用足量CuSO4溶液代替,起始时Zn电极和Cu电极的质量相等,当导线中有0.2mol电子转移时,Zn电极和Cu电极的质量差为_______ 。
II.某温度时,在一个2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。根据图中数据填空:
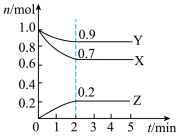
(5)该反应的化学方程式为_______ ;
(6)反应开始至2min末,以气体X表示的平均反应速率为_______ ;
(7)恒温恒容条件下,能说明该反应达到化学平衡状态的标志是_______ 。
①混合气体的压强不再变化 ②混合气体的密度不再变化 ③X的百分含量不再变化 ④混合气体的平均相对分子质量不再变化 ⑤v(X):v(Y)=3:1

根据所学知识,完成下列各题:
(1)装置B为原电池,则Cu作
(2)一般把金属导线称为“电子导体”,把电解质溶液称为“离子导体”。装置B中电池工作时“电子导体”中电子的流动方向可描述为
(3)从反应速率的角度上看,可以观察到A中反应比B中
(4)装置B中稀H2SO4用足量CuSO4溶液代替,起始时Zn电极和Cu电极的质量相等,当导线中有0.2mol电子转移时,Zn电极和Cu电极的质量差为
II.某温度时,在一个2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。根据图中数据填空:

(5)该反应的化学方程式为
(6)反应开始至2min末,以气体X表示的平均反应速率为
(7)恒温恒容条件下,能说明该反应达到化学平衡状态的标志是
①混合气体的压强不再变化 ②混合气体的密度不再变化 ③X的百分含量不再变化 ④混合气体的平均相对分子质量不再变化 ⑤v(X):v(Y)=3:1
| A.①②⑤ | B.①③④ | C.②③④ | D.③④⑤ |
更新时间:2023-09-25 09:38:12
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】请回答:
(1)写出乙烯的结构式:_______ ;写出CaC2的电子式:______ 。
(2)取50mL过氧化氢水溶液,在少量I-存在下分解:2H2O2=2H2O+O2↑。
在一定温度下,测得O2的放出量(已折合成标况)如表:
20~40min,消耗H2O2的平均速率为______ mol•L-1•min-1。
(3)如图是实验室研究海水对铁闸不同部位腐蚀情况的剖面示意图。
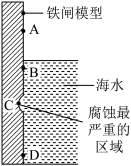
①该电化腐蚀称为______ (填“吸氧腐蚀”或“析氢腐蚀”)。
②图中A、B、C、D四个区域,生成铁锈最多的是______ (填字母)。
(1)写出乙烯的结构式:
(2)取50mL过氧化氢水溶液,在少量I-存在下分解:2H2O2=2H2O+O2↑。
在一定温度下,测得O2的放出量(已折合成标况)如表:
| t/min | 0 | 20 | 40 |
| V(O2)/L | 0 | 0.448 | 0.672 |
(3)如图是实验室研究海水对铁闸不同部位腐蚀情况的剖面示意图。

①该电化腐蚀称为
②图中A、B、C、D四个区域,生成铁锈最多的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】在2L密闭容器内,800℃时反应:2NO(g)+O2(g) 2NO2(g)体系中,c(NO)随时间的变化如表:
2NO2(g)体系中,c(NO)随时间的变化如表:
(1)分析上表,该反应达到平衡状态所需时间是_________ 。
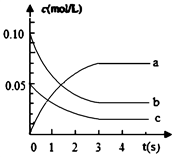
(2)上图中表示NO2的浓度变化曲线是_______________ 。
(3)用NO表示从0~2s内该反应的平均速率v=________ 。
(4)v(NO):v(O2) =______________ 。
(5)达到平衡状态时O2的转化率为________ 。
 2NO2(g)体系中,c(NO)随时间的变化如表:
2NO2(g)体系中,c(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)(mol/L) | 0.10 | 0.05 | 0.04 | 0.03 | 0.03 | 0.03 |
(1)分析上表,该反应达到平衡状态所需时间是

(2)上图中表示NO2的浓度变化曲线是
(3)用NO表示从0~2s内该反应的平均速率v=
(4)v(NO):v(O2) =
(5)达到平衡状态时O2的转化率为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】向某密闭容器中充入等物质的量的气体M和N,一定条件下发生反应,达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间的变化如图1、图2所示。
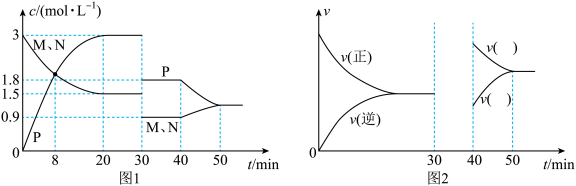
回答下列问题:
(1)该反应的化学方程式为_______ ,其
_______ (填“>”、“<”或“=”)0。
(2)30min时改变的条件是____ ,40min时改变的条件是____ ,请在图2中画出30min~40min的正逆反应速率变化曲线以及标出40min~50min内 、
、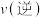 对应的曲线
对应的曲线_____ 。
(3)0~8min内,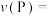
_______ ;50min后,M的转化率为_______ (保留三位有效数字)。
(4)20min~30min内,反应平衡时的平衡常数K=_______ 。

回答下列问题:
(1)该反应的化学方程式为

(2)30min时改变的条件是
 、
、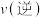 对应的曲线
对应的曲线(3)0~8min内,
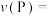
(4)20min~30min内,反应平衡时的平衡常数K=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】正确认识和使用电池有利于我们每一个人的日常生活。
I.电化学法处理SO2是目前研究的热点。利用双氧水氧化吸收SO2可消除SO2污染,设计装置如图所示(已知石墨只起导电作用,质子交换膜只允许H+通过)。

(1)石墨2为_____ (填“正极”或“负极”),负极的电极反应式为________ 。
(2)反应的总方程式为______________ 。
(3)放电时H+迁移向______ 。(填“正极”或“负极”)
(4)某同学关于原电池的笔记中,不合理的有_____ 。
①原电池两电极材料可以相同
②原电池负极材料参与反应,正极材料都不参与反应
③Fe-浓硝酸-Cu原电池,Fe是负极
④原电池是将化学能转变为电能的装置
Ⅱ.航天技术中使用的氢氧燃料电池具有高能、轻便和不污染环境等优点。
(1)某碱式氢氧燃料电池的电解质溶液是KOH溶液,则其负极反应为_______ 。
(2)氢氧燃料电池用于航天飞船,电极反应产生的水,经过冷凝后可用作航天员的饮用水,当得到1.8g饮用水时,转移的电子的物质的量为_____________ 。
I.电化学法处理SO2是目前研究的热点。利用双氧水氧化吸收SO2可消除SO2污染,设计装置如图所示(已知石墨只起导电作用,质子交换膜只允许H+通过)。

(1)石墨2为
(2)反应的总方程式为
(3)放电时H+迁移向
(4)某同学关于原电池的笔记中,不合理的有
①原电池两电极材料可以相同
②原电池负极材料参与反应,正极材料都不参与反应
③Fe-浓硝酸-Cu原电池,Fe是负极
④原电池是将化学能转变为电能的装置
Ⅱ.航天技术中使用的氢氧燃料电池具有高能、轻便和不污染环境等优点。
(1)某碱式氢氧燃料电池的电解质溶液是KOH溶液,则其负极反应为
(2)氢氧燃料电池用于航天飞船,电极反应产生的水,经过冷凝后可用作航天员的饮用水,当得到1.8g饮用水时,转移的电子的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有如下两个反应:(A)NaOH+HCl=NaCl+H2O
(B)2FeCl3+Cu=2FeCl2+CuCl2
(1)根据两反应本质,判断能否设计成原电池(填“能”或“不能”)
(A)___________________ (B)___________________
(2)如果(A或B)不能,说明其原因__________________________
(3)如果(A或B)可以,指出正、负极的电极材料,并写出电极反应式
负极:材料:_____ ;电极反应式:______________________________
正极:材料_______ ;电极反应式_______________________________ 。
(B)2FeCl3+Cu=2FeCl2+CuCl2
(1)根据两反应本质,判断能否设计成原电池(填“能”或“不能”)
(A)
(2)如果(A或B)不能,说明其原因
(3)如果(A或B)可以,指出正、负极的电极材料,并写出电极反应式
负极:材料:
正极:材料
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某小组研究化学反应中的能量变化,进行了如下实验。
(1)实验 I:将Zn片和Cu片分别插入盛有50mL 2mol•L-1稀硫酸的烧杯中。

观察到Zn片表面产生气泡,溶液温度由T1℃升到T2℃;Cu片表面无明显变化。
①Zn片与稀硫酸反应的离子方程式为_______ 。
②Zn片与稀硫酸反应的能量变化关系符合如图_______ (填“A”或“B”)。

(2)实验Ⅱ:用导线将电流表、小灯泡与Zn片、Cu片相连接,插入盛有50mL2mol•L-1稀硫酸的烧杯中。

①观察到电流表指针发生偏转,Cu片表面产生气泡,溶液温度由T1℃升到T3℃。
②结合电子的移动方向,解释Cu片表面产生气泡的原因_______ 。
(3)实验I和Ⅱ产生等量气体时,测得T2>T3.结合能量的转化形式,分析两溶液温度变化幅度不同的原因_______ 。
(4)将Zn片和Cu片换成Fe片和石墨棒,重复实验Ⅱ,判断电流表指针是否发生偏转。若不偏转,说明理由;若偏转,写出Fe片表面发生的电极反应式,理由或电极反应式是_______ 。
(1)实验 I:将Zn片和Cu片分别插入盛有50mL 2mol•L-1稀硫酸的烧杯中。

观察到Zn片表面产生气泡,溶液温度由T1℃升到T2℃;Cu片表面无明显变化。
①Zn片与稀硫酸反应的离子方程式为
②Zn片与稀硫酸反应的能量变化关系符合如图

(2)实验Ⅱ:用导线将电流表、小灯泡与Zn片、Cu片相连接,插入盛有50mL2mol•L-1稀硫酸的烧杯中。

①观察到电流表指针发生偏转,Cu片表面产生气泡,溶液温度由T1℃升到T3℃。
②结合电子的移动方向,解释Cu片表面产生气泡的原因
(3)实验I和Ⅱ产生等量气体时,测得T2>T3.结合能量的转化形式,分析两溶液温度变化幅度不同的原因
(4)将Zn片和Cu片换成Fe片和石墨棒,重复实验Ⅱ,判断电流表指针是否发生偏转。若不偏转,说明理由;若偏转,写出Fe片表面发生的电极反应式,理由或电极反应式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】化学电源在生产生活中有着广泛的应用,请回答下列问题:
(1)根据构成原电池的本质判断,下列化学(或离子)方程式正确且能设计成原电池的是_______(填字母,下同)。
(2)为了探究化学反应中的能量变化,某同学设计了如下两个实验(如图)。有关反应一段时间后的实验现象,下列说法正确的是_______。
(3)请利用反应“Cu+2Ag+=Cu2++2Ag”设计一个化学电池(正极材料用碳棒),该电池的负极材料是_______ ,发生的电极反应是_______ ,电解质溶液是_______ 。
(4)正极上出现的现象是_______ 。
(5)若导线上转移电子1 mol,则生成银_______  。
。
(1)根据构成原电池的本质判断,下列化学(或离子)方程式正确且能设计成原电池的是_______(填字母,下同)。
A.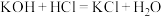 | B. |
C.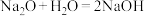 | D. |
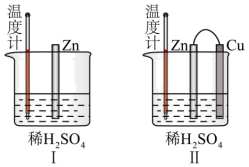
| A.图Ⅰ中温度计的示数高于图Ⅱ的示数 |
| B.图Ⅰ和图Ⅱ中温度计的示数相等,且均高于室温 |
| C.图Ⅰ和图Ⅱ的气泡均产生于锌棒表面 |
| D.图Ⅱ中产生气体的速率比Ⅰ慢 |
(4)正极上出现的现象是
(5)若导线上转移电子1 mol,则生成银
 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】根据下式所示的氧化还原反应设计一个原电池:Cu+2Ag+=Cu2++2Ag
(1)装置可采用烧杯和盐桥,画出此原电池的装置简图;
(2)注明原电池的正极和负极,以及外电路中电子流向;
(3)写出两个电极上的电极反应式。
(1)装置可采用烧杯和盐桥,画出此原电池的装置简图;
(2)注明原电池的正极和负极,以及外电路中电子流向;
(3)写出两个电极上的电极反应式。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】由碳棒、铁片和200mL稀H2SO4组成的原电池中,当在碳棒上共放出3.36L(标准状况)气体时,求消耗铁多少克?有多少个电子通过了电线?____________ 、_______________________________
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】化学能与电能之间可以相互转化。
(1)直接提供电能的反应一般是放热反应,下列反应能设计成原电池的是_____
A.Ba(OH)2·8H2O与NH4Cl反应
B.氢氧化钠与稀盐酸反应
C.灼热的炭与 CO2反应
D.H2与 Cl2燃烧反应
(2)氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀了一层细小的铂粉,铂吸附气体的能力强,性质稳定。请回答:
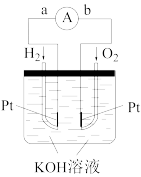
①电池的负极反应式为:_____ 。
②电池工作时 OH-向_____ 移动(填“正极”或“负极”)。
③正极上消耗标况下 4.48L 气体时, 转移电子的数目为_____ 。
(1)直接提供电能的反应一般是放热反应,下列反应能设计成原电池的是
A.Ba(OH)2·8H2O与NH4Cl反应
B.氢氧化钠与稀盐酸反应
C.灼热的炭与 CO2反应
D.H2与 Cl2燃烧反应
(2)氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀了一层细小的铂粉,铂吸附气体的能力强,性质稳定。请回答:

①电池的负极反应式为:
②电池工作时 OH-向
③正极上消耗标况下 4.48L 气体时, 转移电子的数目为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】人们利用原电池原理制作了多种电池,以满足日常生活、生产和科学技术等方面的需要。请根据题中提供的信息,回答下列问题。
(1)铅蓄电池在放电时的总反应为 ,则其正极反应为
,则其正极反应为___ 。
(2)FeCl3溶液腐蚀印刷电路铜板时发生反应: ,若将此反应设计成原电池,则负极所用的电极材料为
,若将此反应设计成原电池,则负极所用的电极材料为___ ,电极反应式:___ 。
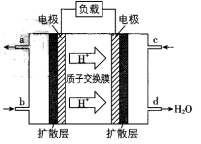
(3)已知甲醇燃料电池的工作原理如图所示,该电池工作时,b口通入的物质为___ (填化学式),该电池正极上的电极反应式为___ ;当6.4g甲醇(CH3OH)完全反应生成CO2时,有___ mol电子发生转移。若将电池的电解质溶液换为KOH溶液,则负极反应式为____ 。
(1)铅蓄电池在放电时的总反应为
 ,则其正极反应为
,则其正极反应为(2)FeCl3溶液腐蚀印刷电路铜板时发生反应:
 ,若将此反应设计成原电池,则负极所用的电极材料为
,若将此反应设计成原电池,则负极所用的电极材料为(3)已知甲醇燃料电池的工作原理如图所示,该电池工作时,b口通入的物质为

您最近一年使用:0次




