己二酸(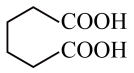 )是一种重要的化工原料和合成中间体。某实验小组以钨磷酸为催化剂,开展己二酸的合成及性质探究实验。
)是一种重要的化工原料和合成中间体。某实验小组以钨磷酸为催化剂,开展己二酸的合成及性质探究实验。
Ⅰ.催化剂钨磷酸晶体(H3PW12O40)的制备
实验流程如图:

(1)操作Ⅰ所需的玻璃仪器除烧杯外还有___________ ,乙醚的作用为 ___________ 。
(2)水层中的物质有大量NaCl和少量HCl,步骤①中发生反应的化学方程式是___________ 。
Ⅱ.己二酸的合成
向三颈烧瓶中加入0.10g钨磷酸催化剂和30mL30%双氧水,在室温下搅拌5min,然后加入5.0mL试剂X,得到溶液A。
(3)环己烯、环己醇、环己酮均可被双氧水氧化成己二酸。仅从所需双氧水理论用量的角度看,试剂X的最佳选择是________ (填序号)。
A.环己烯(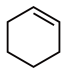 ) B.环己醇(
) B.环己醇(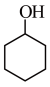 ) C.环己酮(
) C.环己酮(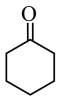 )
)
(4)如图是己二酸的浓度与温度关系曲线图。介稳区表示己二酸溶液处于饱和状态,稳定区表示己二酸溶液处于不饱和状态。实验室常根据直线EHI从溶液A获取己二酸晶体,对应的实验操作为___________ ,过滤。

Ⅲ.己二酸的性质探究
以己二酸和乙醇为原料,用如图所示装置制备己二酸二乙酯。
步骤1:向如图所示的装置A中加入30mL乙醇、10mL己二酸、0.6mL浓硫酸、10mL苯和2~3片碎瓷片。组装好仪器,并预先在分水器内加入一定量水,开始缓慢加热A(沸点65℃),加热回流1h,直至反应基本完成。
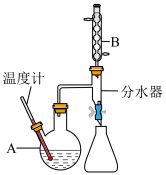
步骤 2:待反应液冷却至室温后倒入分液漏斗中,洗涤干燥后蒸馏,收集相应馏分,得到己二酸 二乙酯 9.6 g。
(5)装置中分水器的作用是________ ,判断反应已经完成的标志是 ___________ 。
(6)本次实验的产率为(某种生成物的实际产量与理论产量的百分比)___________ 。(结果保留两位有效数字)
 )是一种重要的化工原料和合成中间体。某实验小组以钨磷酸为催化剂,开展己二酸的合成及性质探究实验。
)是一种重要的化工原料和合成中间体。某实验小组以钨磷酸为催化剂,开展己二酸的合成及性质探究实验。Ⅰ.催化剂钨磷酸晶体(H3PW12O40)的制备
实验流程如图:

(1)操作Ⅰ所需的玻璃仪器除烧杯外还有
(2)水层中的物质有大量NaCl和少量HCl,步骤①中发生反应的化学方程式是
Ⅱ.己二酸的合成
向三颈烧瓶中加入0.10g钨磷酸催化剂和30mL30%双氧水,在室温下搅拌5min,然后加入5.0mL试剂X,得到溶液A。
(3)环己烯、环己醇、环己酮均可被双氧水氧化成己二酸。仅从所需双氧水理论用量的角度看,试剂X的最佳选择是
A.环己烯(
 ) B.环己醇(
) B.环己醇( ) C.环己酮(
) C.环己酮( )
)(4)如图是己二酸的浓度与温度关系曲线图。介稳区表示己二酸溶液处于饱和状态,稳定区表示己二酸溶液处于不饱和状态。实验室常根据直线EHI从溶液A获取己二酸晶体,对应的实验操作为

Ⅲ.己二酸的性质探究
以己二酸和乙醇为原料,用如图所示装置制备己二酸二乙酯。
步骤1:向如图所示的装置A中加入30mL乙醇、10mL己二酸、0.6mL浓硫酸、10mL苯和2~3片碎瓷片。组装好仪器,并预先在分水器内加入一定量水,开始缓慢加热A(沸点65℃),加热回流1h,直至反应基本完成。

步骤 2:待反应液冷却至室温后倒入分液漏斗中,洗涤干燥后蒸馏,收集相应馏分,得到己二酸 二乙酯 9.6 g。
| 有机物名称 | 相对分子质量 | 密度(g/cm3) | 沸点(℃) | 溶解性 |
| 己二酸 | 146 | 1.36 | 330 | 微溶于水,易溶于乙醇 |
| 乙醇 | 46 | 0.79 | 78.5 | 易溶于水 |
| 己二酸二乙酯 | 202 | 1.00 | 247 | 难溶于水、易溶于乙醇 |
| 苯 | 78 | 0.88 | 80.1 | 难溶于水 |
(5)装置中分水器的作用是
(6)本次实验的产率为(某种生成物的实际产量与理论产量的百分比)
更新时间:2023-09-27 09:46:18
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】牙膏中的固体摩擦剂主要由碳酸钙、氢氧化铝和少量不与 溶液、
溶液、 反应的成分组成,兴趣小组对摩擦剂的主要成分及含量进行探究。
反应的成分组成,兴趣小组对摩擦剂的主要成分及含量进行探究。
Ⅰ.摩擦剂中氢氧化铝的定性检验。取适量摩擦挤样品,加水充分溶解后,过滤,向滤渣中加入过理 溶液,再次过滤,向滤液中通入过理
溶液,再次过滤,向滤液中通入过理 ,有白色沉淀生成,则证明摩擦剂含有
,有白色沉淀生成,则证明摩擦剂含有 。已知:
。已知:
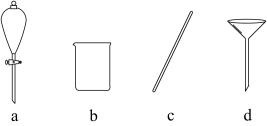
(1)在过滤操作中,不需要用到的玻璃仪器有_______ (选填编号)
(2)氢氧化铝与 溶液反应的离子方程式是
溶液反应的离子方程式是_______
(3)某同学认为向再次过滤的滤液中通 后有白色沉淀生成,不能证明摩擦剂中一定含有
后有白色沉淀生成,不能证明摩擦剂中一定含有 ,若要确认其含有
,若要确认其含有 ,则取该白色沉淀少许,洗涤后滴入过量盐酸,若出现
,则取该白色沉淀少许,洗涤后滴入过量盐酸,若出现_______ (填写实验现象),证明白色沉淀是 ,即摩擦剂中含有
,即摩擦剂中含有 。
。
Ⅱ.摩擦剂中碳酸钙含量的测定。如图所示进行实验,滴入盐酸克分反应后,打开 ,持续通入一段时间空气后,取下C装置,过滤、洗涤沉淀、干燥、冷却、称重
,持续通入一段时间空气后,取下C装置,过滤、洗涤沉淀、干燥、冷却、称重 质量,计算样品中碳酸钙的质量分数。
质量,计算样品中碳酸钙的质量分数。
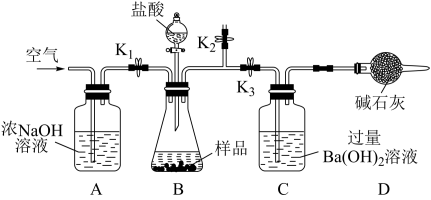
完成下列填空:
(4)检查装置气密性后,如图加入试剂,关闭 ,打开
,打开 和
和 ,持续鼓入空气一段时间后,关闭
,持续鼓入空气一段时间后,关闭 和
和 ,打开
,打开 ,再向锥形瓶中滴入盐酸。以上操作的目的是
,再向锥形瓶中滴入盐酸。以上操作的目的是_______ 。
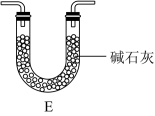
(5)有小组认为,过滤,称量 质量,操作繁杂且易产生实验误差,故将图中C装置调换成E装置(如图),你认为是否合适?并简述原因
质量,操作繁杂且易产生实验误差,故将图中C装置调换成E装置(如图),你认为是否合适?并简述原因_______ 。
(6)实验中称取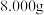 样品,若测得
样品,若测得 平均质量为
平均质量为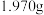 。则摩擦剂样品中碳酸钙的质量分数是
。则摩擦剂样品中碳酸钙的质量分数是_______ (小数点后保留三位数字)。
 溶液、
溶液、 反应的成分组成,兴趣小组对摩擦剂的主要成分及含量进行探究。
反应的成分组成,兴趣小组对摩擦剂的主要成分及含量进行探究。Ⅰ.摩擦剂中氢氧化铝的定性检验。取适量摩擦挤样品,加水充分溶解后,过滤,向滤渣中加入过理
 溶液,再次过滤,向滤液中通入过理
溶液,再次过滤,向滤液中通入过理 ,有白色沉淀生成,则证明摩擦剂含有
,有白色沉淀生成,则证明摩擦剂含有 。已知:
。已知:
(1)在过滤操作中,不需要用到的玻璃仪器有

(2)氢氧化铝与
 溶液反应的离子方程式是
溶液反应的离子方程式是(3)某同学认为向再次过滤的滤液中通
 后有白色沉淀生成,不能证明摩擦剂中一定含有
后有白色沉淀生成,不能证明摩擦剂中一定含有 ,若要确认其含有
,若要确认其含有 ,则取该白色沉淀少许,洗涤后滴入过量盐酸,若出现
,则取该白色沉淀少许,洗涤后滴入过量盐酸,若出现 ,即摩擦剂中含有
,即摩擦剂中含有 。
。Ⅱ.摩擦剂中碳酸钙含量的测定。如图所示进行实验,滴入盐酸克分反应后,打开
 ,持续通入一段时间空气后,取下C装置,过滤、洗涤沉淀、干燥、冷却、称重
,持续通入一段时间空气后,取下C装置,过滤、洗涤沉淀、干燥、冷却、称重 质量,计算样品中碳酸钙的质量分数。
质量,计算样品中碳酸钙的质量分数。
完成下列填空:
(4)检查装置气密性后,如图加入试剂,关闭
 ,打开
,打开 和
和 ,持续鼓入空气一段时间后,关闭
,持续鼓入空气一段时间后,关闭 和
和 ,打开
,打开 ,再向锥形瓶中滴入盐酸。以上操作的目的是
,再向锥形瓶中滴入盐酸。以上操作的目的是(5)有小组认为,过滤,称量
 质量,操作繁杂且易产生实验误差,故将图中C装置调换成E装置(如图),你认为是否合适?并简述原因
质量,操作繁杂且易产生实验误差,故将图中C装置调换成E装置(如图),你认为是否合适?并简述原因(6)实验中称取
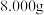 样品,若测得
样品,若测得 平均质量为
平均质量为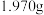 。则摩擦剂样品中碳酸钙的质量分数是
。则摩擦剂样品中碳酸钙的质量分数是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】过氧乙酸(CH3COOOH)是一种常用的消毒剂,易溶于水、易挥发、见光或受热易分解。其制备原理为: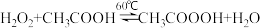 △H<0,同时利用乙酸丁酯与水形成共沸物(沸点90.7℃)及时分离出水,以提高产率。实验装置如图。
△H<0,同时利用乙酸丁酯与水形成共沸物(沸点90.7℃)及时分离出水,以提高产率。实验装置如图。

(1)过氧乙酸保存时应注意______________ (填标号)。
A.避光B.低温C.密闭D.隔绝空气
(2)仪器a的名称为______________ ,其中盛放的试剂为______________ (填“乙酸”或“双氧水”)。
(3)为减少反应瓶中乙酸丁酯的损耗,反应开始前,在油水分离器中应进行的操作是______________ 。
(4)反应体系采用减压的目的是____ 。
(5)过氧乙酸(含有少量H2O2杂质)的含量测定流程如图。

①判断H2O2恰好除尽的实验现象是______________ 。
②过氧乙酸被Fe2+还原,还原产物之一为乙酸,其离子方程式为______________
③若样品体积为VomL,加入c1mol·L-1FeSO4溶液V1mL,消耗c2mol·L-1K2Cr2O7溶液V2mL。则过氧乙酸含量为______________ g.L-l。
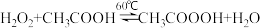 △H<0,同时利用乙酸丁酯与水形成共沸物(沸点90.7℃)及时分离出水,以提高产率。实验装置如图。
△H<0,同时利用乙酸丁酯与水形成共沸物(沸点90.7℃)及时分离出水,以提高产率。实验装置如图。
(1)过氧乙酸保存时应注意
A.避光B.低温C.密闭D.隔绝空气
(2)仪器a的名称为
(3)为减少反应瓶中乙酸丁酯的损耗,反应开始前,在油水分离器中应进行的操作是
(4)反应体系采用减压的目的是
(5)过氧乙酸(含有少量H2O2杂质)的含量测定流程如图。

①判断H2O2恰好除尽的实验现象是
②过氧乙酸被Fe2+还原,还原产物之一为乙酸,其离子方程式为
③若样品体积为VomL,加入c1mol·L-1FeSO4溶液V1mL,消耗c2mol·L-1K2Cr2O7溶液V2mL。则过氧乙酸含量为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】镍的单质及氧化物常用作催化剂。以含镍废渣(主要含Ni,还含少量NiO、 和
和 )为原料可通过如下过程制取高纯度NiO。
)为原料可通过如下过程制取高纯度NiO。

已知①常温时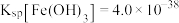 ,
,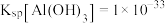 ,
,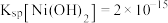 ,溶液中离子的浓度小于
,溶液中离子的浓度小于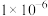 可认为已除尽。
可认为已除尽。
② 难溶于水。
难溶于水。
(1)“浸取”时,当加料完成后,提高镍元素浸出速率的方法有___________ 、___________ 。
(2)“浸取”后,测得溶液中 、
、 和
和 的物质的量浓度分别为
的物质的量浓度分别为 、
、 和
和 ,则“除铝铁”时应控制溶液的
,则“除铝铁”时应控制溶液的 范围为
范围为___________ (设加入氨水时溶液体积不发生变化) 。
(3)“沉镍”后所得 中可能吸附含有少量
中可能吸附含有少量 ,若“沉镍”时使用
,若“沉镍”时使用 溶液,则所得
溶液,则所得 中可能吸附含有少量
中可能吸附含有少量 ,实际生产流程中用
,实际生产流程中用 而不用
而不用 的原因是
的原因是___________ 。
(4)雷尼镍是一种多孔的单质镍,可用作催化剂,工业上可由镍铝合金制得。选择合适的试剂,补充完整制取雷尼镍的方法:取粉碎后的镍铝合金,___________ ,真空干燥得到雷尼镍。(实验中可选用的试剂:10%的稀硫酸、20%的 溶液)
溶液)
(5)为测定某 产品的纯度,现进行如下实验:准确取
产品的纯度,现进行如下实验:准确取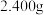 样品,用足量硫酸溶解后,加水稀释到
样品,用足量硫酸溶解后,加水稀释到 ,取
,取 所配溶液于锥形瓶中,加入
所配溶液于锥形瓶中,加入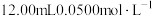 标准
标准 溶液,振荡使其充分反应;向反应后的溶液滴加
溶液,振荡使其充分反应;向反应后的溶液滴加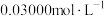 的
的 标准溶液与过量的
标准溶液与过量的 反应,恰好完全反应时消耗
反应,恰好完全反应时消耗 标准溶液体积为
标准溶液体积为 ,计算
,计算 产品的纯度
产品的纯度___________ (写出计算过程,杂质不参与反应),实验过程中反应如下: (未配平);
(未配平);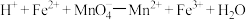 (未配平)。
(未配平)。
 和
和 )为原料可通过如下过程制取高纯度NiO。
)为原料可通过如下过程制取高纯度NiO。
已知①常温时
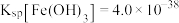 ,
,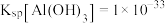 ,
,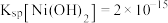 ,溶液中离子的浓度小于
,溶液中离子的浓度小于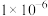 可认为已除尽。
可认为已除尽。②
 难溶于水。
难溶于水。(1)“浸取”时,当加料完成后,提高镍元素浸出速率的方法有
(2)“浸取”后,测得溶液中
 、
、 和
和 的物质的量浓度分别为
的物质的量浓度分别为 、
、 和
和 ,则“除铝铁”时应控制溶液的
,则“除铝铁”时应控制溶液的 范围为
范围为(3)“沉镍”后所得
 中可能吸附含有少量
中可能吸附含有少量 ,若“沉镍”时使用
,若“沉镍”时使用 溶液,则所得
溶液,则所得 中可能吸附含有少量
中可能吸附含有少量 ,实际生产流程中用
,实际生产流程中用 而不用
而不用 的原因是
的原因是(4)雷尼镍是一种多孔的单质镍,可用作催化剂,工业上可由镍铝合金制得。选择合适的试剂,补充完整制取雷尼镍的方法:取粉碎后的镍铝合金,
 溶液)
溶液)(5)为测定某
 产品的纯度,现进行如下实验:准确取
产品的纯度,现进行如下实验:准确取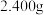 样品,用足量硫酸溶解后,加水稀释到
样品,用足量硫酸溶解后,加水稀释到 ,取
,取 所配溶液于锥形瓶中,加入
所配溶液于锥形瓶中,加入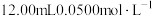 标准
标准 溶液,振荡使其充分反应;向反应后的溶液滴加
溶液,振荡使其充分反应;向反应后的溶液滴加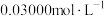 的
的 标准溶液与过量的
标准溶液与过量的 反应,恰好完全反应时消耗
反应,恰好完全反应时消耗 标准溶液体积为
标准溶液体积为 ,计算
,计算 产品的纯度
产品的纯度 (未配平);
(未配平);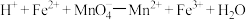 (未配平)。
(未配平)。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】电解金属锰阳极渣(主要成分MnO2,杂质为PbCO3、Fe2O3、CuO)和黄铁矿(FeS2)为原料可制备Mn3O4,其流程如图所示:
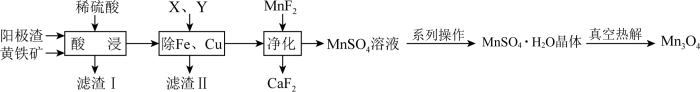
已知:部分阳离子以氢氧化物形式完全沉淀时的pH如下:Fe3+ 3.7,Fe2+ 9.7,Cu2+ 7.4,Mn2+ 9.8
回答下列问题:
(1)“酸浸”过程中,滤渣Ⅰ的主要成分为S、______ (填化学式)。
(2)“酸浸”过程中Fe2+、Fe3+的质量浓度、Mn浸出率与时间的关系如图1所示。
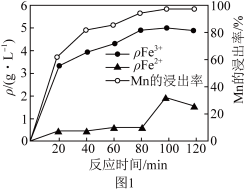
20~80min,浸出Mn元素的主要离子方程式为______ 。80~100min时,Fe2+浓度上升的原因可能是______ 。
(3)“除Fe、Cu”过程中依次加入的试剂X、Y为______ (填序号)。
A.NH3•H2O、H2O2 B.H2O2、CaCO3 C.SO2、MnCO3
(4)硫酸锰晶体的溶解度曲线如图2,由MnSO4溶液获得MnSO4•H2O晶体的系列操作为______ 、洗涤、干燥。
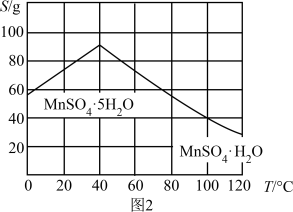
(5)“真空热解”过程中,测得固体的质量随温度变化如图3所示。需控制的温度为______ 。
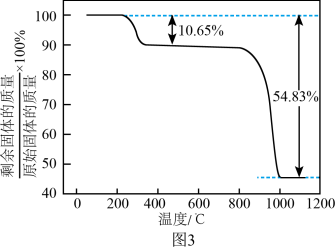
(6)由MnSO4溶液制取Mn3O4的另一种方案是:向MnSO4溶液中加入氨水,产生Mn(OH)2沉淀和少量Mn2(OH)2SO4,滤出,洗净,加水打成浆,浆液边加热边持续通空气,制得Mn3O4。沉淀加热通空气过程中,7小时之前,溶液的pH=6,7小时之后迅速下降,原因是______ 。

已知:部分阳离子以氢氧化物形式完全沉淀时的pH如下:Fe3+ 3.7,Fe2+ 9.7,Cu2+ 7.4,Mn2+ 9.8
回答下列问题:
(1)“酸浸”过程中,滤渣Ⅰ的主要成分为S、
(2)“酸浸”过程中Fe2+、Fe3+的质量浓度、Mn浸出率与时间的关系如图1所示。

20~80min,浸出Mn元素的主要离子方程式为
(3)“除Fe、Cu”过程中依次加入的试剂X、Y为
A.NH3•H2O、H2O2 B.H2O2、CaCO3 C.SO2、MnCO3
(4)硫酸锰晶体的溶解度曲线如图2,由MnSO4溶液获得MnSO4•H2O晶体的系列操作为

(5)“真空热解”过程中,测得固体的质量随温度变化如图3所示。需控制的温度为

(6)由MnSO4溶液制取Mn3O4的另一种方案是:向MnSO4溶液中加入氨水,产生Mn(OH)2沉淀和少量Mn2(OH)2SO4,滤出,洗净,加水打成浆,浆液边加热边持续通空气,制得Mn3O4。沉淀加热通空气过程中,7小时之前,溶液的pH=6,7小时之后迅速下降,原因是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】某含钒废渣饼主要含V2O3、Fe(II)V2O4、VOSO4、Fe(II)Cr2O4,常采用酸浸还原后直接萃取的方法回收钒,或者采用碱浸氧化后直接离子交换法同时回收钒和铬,从而达到变废为宝的目的。
(1)酸浸还原后直接萃取的方法回收钒:
①已知萃取剂P204在实验条件下对 具有高选择性,对
具有高选择性,对 也有一定萃取能力但不萃取
也有一定萃取能力但不萃取 ,则酸浸还原时选用还原剂
,则酸浸还原时选用还原剂 的目的是将+6价Cr还原得到
的目的是将+6价Cr还原得到 、
、___________ 。
②已知实际生产中酸浸还原后仍会存在少量的 ,萃取时发生的反应为:
,萃取时发生的反应为: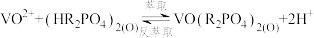 ,沉淀絮凝物对
,沉淀絮凝物对 有一定的吸附能力,待萃液初始pH对
有一定的吸附能力,待萃液初始pH对 萃取率的影响如图,则最佳pH条件为
萃取率的影响如图,则最佳pH条件为___________ (填序号):
A.1.0B.1.5C.2.2D.2.5

萃取率出现如图所示趋势的原因为___________ 。
(2)碱浸氧化后直接离子交换法同时回收钒和铬:
① 为两性氧化物,偏酸性,在强碱性介质溶液中易溶解生成钒酸盐(
为两性氧化物,偏酸性,在强碱性介质溶液中易溶解生成钒酸盐( ),该反应的离子方程式为
),该反应的离子方程式为___________
②碱浸氧化时选用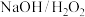 ,
,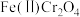 ,被氧化得到的氧化产物为
,被氧化得到的氧化产物为 和
和 ,写出该反应的化学方程式为
,写出该反应的化学方程式为___________
③“碱浸氧化”过程在通电条件下进行,更有利于 中V(IV)的浸出和V(IV)的氧化,电碱浸氧化机理如图
中V(IV)的浸出和V(IV)的氧化,电碱浸氧化机理如图

则 中V(IV)的浸出和V(IV)被氧化成
中V(IV)的浸出和V(IV)被氧化成 的过程为:一是
的过程为:一是 生成了
生成了 ,有利于使V(IV)从废渣饼中浸出;二是
,有利于使V(IV)从废渣饼中浸出;二是___________ 。
(1)酸浸还原后直接萃取的方法回收钒:
①已知萃取剂P204在实验条件下对
 具有高选择性,对
具有高选择性,对 也有一定萃取能力但不萃取
也有一定萃取能力但不萃取 ,则酸浸还原时选用还原剂
,则酸浸还原时选用还原剂 的目的是将+6价Cr还原得到
的目的是将+6价Cr还原得到 、
、②已知实际生产中酸浸还原后仍会存在少量的
 ,萃取时发生的反应为:
,萃取时发生的反应为: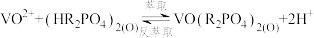 ,沉淀絮凝物对
,沉淀絮凝物对 有一定的吸附能力,待萃液初始pH对
有一定的吸附能力,待萃液初始pH对 萃取率的影响如图,则最佳pH条件为
萃取率的影响如图,则最佳pH条件为A.1.0B.1.5C.2.2D.2.5

萃取率出现如图所示趋势的原因为
(2)碱浸氧化后直接离子交换法同时回收钒和铬:
①
 为两性氧化物,偏酸性,在强碱性介质溶液中易溶解生成钒酸盐(
为两性氧化物,偏酸性,在强碱性介质溶液中易溶解生成钒酸盐( ),该反应的离子方程式为
),该反应的离子方程式为②碱浸氧化时选用
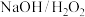 ,
,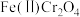 ,被氧化得到的氧化产物为
,被氧化得到的氧化产物为 和
和 ,写出该反应的化学方程式为
,写出该反应的化学方程式为③“碱浸氧化”过程在通电条件下进行,更有利于
 中V(IV)的浸出和V(IV)的氧化,电碱浸氧化机理如图
中V(IV)的浸出和V(IV)的氧化,电碱浸氧化机理如图
则
 中V(IV)的浸出和V(IV)被氧化成
中V(IV)的浸出和V(IV)被氧化成 的过程为:一是
的过程为:一是 生成了
生成了 ,有利于使V(IV)从废渣饼中浸出;二是
,有利于使V(IV)从废渣饼中浸出;二是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】某研究小组制备配合物顺式-二甘氨酸合铜[(H2NCH2COO)2Cu],结构简式为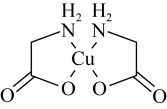 并测定所得产品中铜的含量。回答下列问题:
并测定所得产品中铜的含量。回答下列问题:
如图所示,向装有CuSO4溶液的三颈烧瓶中滴加氨水,先出现蓝色沉淀,后蓝色沉淀消失,溶液变为深蓝色。再加入过量的NaOH溶液,过滤,洗涤,干燥。
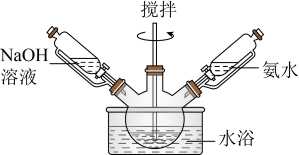
(2)写出少量的氨水和硫酸铜溶液反应的离子方程式:
Ⅱ.制备顺式-二甘氨酸合铜[(H2NCH2COO)2Cu]
将制得的Cu(OH)2固体置于烧杯中,加入甘氨酸,水浴加热至65~70℃,搅拌,充分反应后趁热过滤,往滤液中加入10mL95%的乙醇溶液,冷却结晶,过滤、洗涤、干燥,得产品。
(3)写出Cu(OH)2与甘氨酸反应的化学方程式
(4)下列说法中正确的是
a.实验Ⅰ中不用CuSO4溶液直接与NaOH反应的原因可能是防止生成碱式硫酸铜沉淀
b.实验Ⅱ中,趁热过滤的目的是除去Cu(OH)2的同时减少产物的析出
c.加入95%的乙醇溶液能增大顺式-二甘氨酸合铜的溶解度
Ⅲ.产品中Cu元素含量的测定,实验流程如下:
A.用分析天平称量产品xg,用水溶解,再加入适量硫酸,配制成100mL样品溶液;
B.用移液管移取20.00mL溶液到碘量瓶中,加入过量KI固体,在暗处静置5分钟,用标准Na2S2O3溶液滴定至溶液呈浅黄色,加入适量NH4SCN溶液,剧烈振荡碘量瓶,加入淀粉溶液,用标准Na2S2O3溶液滴定至终点:再取20.00mL溶液进行一次平行实验。
已知:
ⅰ.2Cu2++4I-=2CuI↓+I2,2
 +I2=2I-+
+I2=2I-+ ;
;ⅱ.CuI固体能吸附溶液中的少量碘单质;
ⅲ.Ksp(CuSCN)<Ksp(CuI)。
(5)①配制100mL样品溶液时,需要的玻璃仪器有烧杯、玻璃棒、
②溶解时加入硫酸的作用是
③加入适量NH4SCN溶液,剧烈振荡碘量瓶的目的是
④滴定终点的现象是
⑤若两次平行实验,平均消耗0.1000mol/L Na2S2O3溶液20.00mL,则xg产品中含Cu的质量为
您最近一年使用:0次



